Procedimiento de fabricación de partículas de un conjugado antitrombótico.
Un procedimiento de fabricación de una pluralidad de partículas que utilizan un conjugado antitrombóticopolimérico como vehículo para un agente terapéutico que comprende las etapas de:
disolver un agente terapéutico y un conjugado antitrombótico polimérico en al menos un disolvente para formaruna primera disolución,
mezclar la primera disolución con una segunda disolución acuosa que comprende agua y al menos untensioactivo para formar una emulsión, y
eliminar el disolvente de la emulsión para formar una pluralidad de partículas,
en el que el conjugado antitrombótico polimérico es un conjugado de (a) un copolímero biocompatible ybioabsorbible tipo peine que comprende poli(alcohol vinílico) y un poliéster biodegradable, y (b) una heparinaque extiende las cadenas laterales del copolímero tipo peine, y en el que el agente terapéutico es hidrófobo.
Tipo: Patente Europea. Resumen de patente/invención. Número de Solicitud: E10187104.
Solicitante: CORDIS CORPORATION.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 14201 N.W. 60th Avenue Miami Lakes, FL 33104 ESTADOS UNIDOS DE AMERICA.
Inventor/es: ZHAO,JONATHON.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61F2/06 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61F FILTROS IMPLANTABLES EN LOS VASOS SANGUINEOS; PROTESIS; DISPOSITIVOS QUE MANTIENEN LA LUZ O QUE EVITAN EL COLAPSO DE ESTRUCTURAS TUBULARES, p. ej. STENTS; DISPOSITIVOS DE ORTOPEDIA, CURA O PARA LA CONTRACEPCION; FOMENTACION; TRATAMIENTO O PROTECCION DE OJOS Y OIDOS; VENDAJES, APOSITOS O COMPRESAS ABSORBENTES; BOTIQUINES DE PRIMEROS AUXILIOS (prótesis dentales A61C). › A61F 2/00 Filtros implantables en los vasos sanguíneos; Prótesis, es decir, elementos de sustitución o de reemplazo para partes del cuerpo; Dispositivos para unirlas al cuerpo; Dispositivos para proporcionar permeabilidad o para evitar que colapsen las estructuras tubulares del cuerpo, p. ej. stents (como artículos cosméticos, ver las subclases apropiadas, p. ej. pelucas o postizos, A41G 3/00, A41G 5/00, uñas artificiales A45D 31/00; prótesis dentales A61C 13/00; materiales para prótesis A61L 27/00; riñones artificiales A61M 1/14; corazones artificiales A61M 60/00). › Vasos sanguíneos.
- A61L31/10 A61 […] › A61L PROCEDIMIENTOS O APARATOS PARA ESTERILIZAR MATERIALES U OBJECTOS EN GENERAL; DESINFECCION, ESTERILIZACION O DESODORIZACION DEL AIRE; ASPECTOS QUIMICOS DE VENDAS, APOSITOS, COMPRESAS ABSORBENTES O ARTICULOS QUIRURGICOS; MATERIALES PARA VENDAS, APOSITOS, COMPRESAS ABSORBENTES O ARTICULOS QUIRURGICOS (conservación de cuerpos o desinfección caracterizada por los agentes empleados A01N; conservación, p. ej. esterilización de alimentos o productos alimenticios A23; preparaciones de uso medico, dental o para el aseo A61K). › A61L 31/00 Materiales para otros artículos quirúrgicos. › Materiales macromoleculares.
- A61L31/16 A61L 31/00 […] › Materiales biológicamente activos, p. ej. sustancias terapéuticas.
- A61L33/00 A61L […] › Tratamiento antitrombogénico de artículos quirúrgicos, p. ej. de suturas, catéteres, prótesis o de artículos para la manipulación o el acondicionamiento de la sangre; Materiales para llevar a cabo dicho tratamiento.
PDF original: ES-2399186_T3.pdf
Fragmento de la descripción:
Procedimiento de fabricación de partículas de un conjugado antitrombótico La presente invención se refiere a un material para la aplicación a al menos una parte de la superficie de un artículo o para implantación dentro de un artículo. En particular, la presente invención se refiere a un polímero bioabsorbible tipo peine que tiene una composición antitrombótica conjugada con el mismo en el que un agente antirreestenóico u otro agente terapéutico está contenido dentro de la matriz polimérica del polímero bioabsorbible. La presente invención también se refiere a un dispositivo que tiene el conjugado recubierto en su superficie o contenido dentro del dispositivo.
La estenosis en el estrechamiento o constricción de un vaso resultante de la formación de grasas, colesterol y otras sustancias con el tiempo. En casos graves, la estenosis puede ocluir completamente un vaso. Se han empleado procedimientos de intervención para abrir vasos estenosados. Un ejemplo de un procedimiento de intervención es la angioplastia coronaria transluminal percutánea (ACTP) o angioplastia coronaria con balón. En este procedimiento, un catéter de balón se inserta y se expande en la porción constreñida del vaso para limpiar un bloqueo. Aproximadamente un tercio de los pacientes que se someten a ACTP padecen reestenosis, en la que el vaso se bloquea de nuevo, en el plazo de aproximadamente seis meses desde el procedimiento. Por tanto, las arterias reestenosadas pueden tener que volver a someterse a otra angioplastia. Con el fin de evitar ACTP adicional, dispositivos médicos implantables tales como prótesis endovasculares se han dispuesto dentro del vaso tras ACTP o en vez de ACTP. Sin embargo, la reestenosis puede todavía producirse incluso con la implantación de una prótesis endovascular.
La reestenosis puede inhibirse por un procedimiento común que consiste en insertar una prótesis endovascular en la región afectada de la arteria en lugar de, o junto con, angioplastia. Una prótesis endovascular es un tubo hecho de metal o plástico que puede tener tanto paredes sólidas como paredes de malla. La mayoría de las prótesis endovasculares en uso son metálicas y son tanto auto-expandibles como expandibles por balón. La decisión de someter al procedimiento de inserción de prótesis endovascular depende de ciertas características de la estenosis arterial. Esto incluye el tamaño de la arteria y la localización de la estenosis. La función de la prótesis endovascular es reforzar la arteria que se ha ensanchado recientemente usando angioplastia, o, si no se usó angioplastia, la prótesis endovascular se usa para prevenir el retroceso elástico de la arteria. Las prótesis endovasculares normalmente se implantan mediante un catéter. En el caso de una prótesis endovascular expandible por balón, la prótesis endovascular es colapsada a un pequeño diámetro y se desliza sobre un catéter de balón. Entonces, el catéter es maniobrado por la vasculatura del paciente al sitio de la lesión o el área que se amplió recientemente. Una vez en posición, la prótesis endovascular se expande y se asegura en su sitio. La prótesis endovascular permanece en la arteria permanentemente, la mantiene abierta, mejora la circulación sanguínea a través de la arteria y alivia síntomas (normalmente dolor torácico) .
Las prótesis endovasculares no son completamente eficaces en prevenir la reestenosis en el sitio del implante. La reestenosis puede producirse sobre la longitud de la prótesis endovascular y/o pasados los extremos de la prótesis endovascular. Los médicos han empleado recientemente nuevos tipos de prótesis endovasculares que están recubiertas con una delgada película de polímero cargada con un fármaco que inhibe la proliferación de células lisas. El recubrimiento se aplica a la prótesis endovascular antes de la inserción en la arteria usando procedimientos muy conocidos en la técnica, tales como una técnica de evaporación de disolvente. La técnica de evaporación de disolvente implica mezclar el polímero y fármaco en un disolvente. La disolución que comprende polímero, fármaco y disolvente puede entonces aplicarse a la superficie de la prótesis endovascular tanto sumergiendo como pulverizando. Entonces, la prótesis endovascular se somete a un procedimiento de secado, durante el cual el disolvente se evapora, y el material polimérico, con el fármaco dispersado en su interior, forma una delgada capa de película sobre la prótesis endovascular.
El mecanismo de liberación del fármaco de los materiales poliméricos depende de la naturaleza del material polimérico y del fármaco a incorporar. El fármaco se difunde a través del polímero a la interfase polímero-fluido y luego al fluido. La liberación también puede producirse mediante degradación del material polimérico. La degradación del material polimérico puede producirse mediante hidrólisis o un procedimiento de digestión enzimática, conduciendo a la liberación del fármaco incorporado hacia el tejido circundante.
Una consideración importante en el uso de prótesis endovasculares recubiertas es la velocidad de liberación del fármaco del recubrimiento. Se desea que una cantidad terapéutica eficaz del fármaco sea liberada de la prótesis endovascular durante un periodo de tiempo razonablemente prolongado para cubrir la duración de los siguientes procesos biológicos y un procedimiento de angioplastia o la implantación de una prótesis endovascular. La liberación rápida, una alta velocidad de liberación inmediatamente tras la implantación, es no deseable y un problema persistente. Aunque normalmente no es perjudicial para el paciente, una liberación rápida “desperdicia” el suministro limitado del fármaco liberando varios veces la cantidad eficaz requerida y acorta la duración del periodo de liberación. Se han desarrollado varias técnicas en un intento de reducir la liberación rápida. Por ejemplo, el documento US-6258121 desvela un procedimiento de alterar la velocidad de liberación mezclando dos polímeros con diferentes velocidades de liberación e incorporándolos en una única capa.
Un posible inconveniente asociado a la implantación de una prótesis endovascular liberadora de fármaco (DES) es que la trombosis puede producirse en diferentes momentos tras la implantación o despliegue. La trombosis es la formación de coágulos de sangre sobre o cerca de un dispositivo implantado en el vaso sanguíneo. El coágulo se forma normalmente por una agregación de factores de sangre, principalmente plaquetas y fibrina, con atrapamiento de elementos celulares. La trombosis, como la estenosis, frecuentemente produce obstrucción vascular en el momento de su formación. Tanto la reestenosis como la trombosis son dos afecciones graves y potencialmente mortales que requieren intervención médica. Una formación de trombo sobre la superficie de una prótesis endovascular es frecuentemente letal, conduciendo a una alta tasa de mortalidad de entre el 20 y el 40% en los pacientes que padecen una trombosis en un vaso.
Aunque son eficaces en reducir la reestenosis, algunos de los componentes de los recubrimientos utilizados para prevenir la reestenosis pueden aumentar el riesgo de trombosis. Las prótesis endovascular liberadoras de fármaco no están normalmente asociadas a un aumento de trombosis aguda y subaguda (SAT) , o una trombosis a medio plazo (30 días después de la implantación de la prótesis endovascular) tras una implantación de prótesis endovascular. Sin embargo, estudios de seguimiento clínico a largo plazo sugieren que estos dispositivos pueden participar con elevadas tasas incidentes de trombosis a plazo muy largo (LST) . Aunque se ha encontrado que el aumento de LST es inferior al 1%, una alta tasa de mortalidad normalmente se asocia a LST. Una forma para prevenir esto es incluir un recubrimiento de un anticoagulante, tal como heparina, sobre el dispositivo.
Una forma de tratar la formación de trombosis por prótesis endovascular es mediante el uso de un anticoagulante tal como una heparina. La heparina es una sustancia que es muy conocida por su capacidad de anticoagulación. Se conoce en la técnica aplicar un delgado recubrimiento de polímero cargado con heparina sobre la superficie de una prótesis endovascular usando la técnica de evaporación de disolvente. Por ejemplo, el documento US-5837313 describe un procedimiento de preparación de una composición de recubrimiento de heparina. Sin embargo, un inconveniente del uso de heparina es que no co-existe bien con agentes que previenen la reestenosis. Por ejemplo, si la heparina se mezcla con un agente antitrombótico dentro de un recubrimiento de polímero, la naturaleza hidrófila de la heparina interferirá con el perfil de liberación deseado para el agente... [Seguir leyendo]
Reivindicaciones:
1. Un procedimiento de fabricación de una pluralidad de partículas que utilizan un conjugado antitrombótico polimérico como vehículo para un agente terapéutico que comprende las etapas de:
disolver un agente terapéutico y un conjugado antitrombótico polimérico en al menos un disolvente para formar
una primera disolución, mezclar la primera disolución con una segunda disolución acuosa que comprende agua y al menos un tensioactivo para formar una emulsión, y eliminar el disolvente de la emulsión para formar una pluralidad de partículas, en el que el conjugado antitrombótico polimérico es un conjugado de (a) un copolímero biocompatible y
bioabsorbible tipo peine que comprende poli (alcohol vinílico) y un poliéster biodegradable, y (b) una heparina que extiende las cadenas laterales del copolímero tipo peine, y en el que el agente terapéutico es hidrófobo.
2. El procedimiento de la reivindicación 1, en el que la heparina es una heparina desulfatada.
3. El procedimiento de la reivindicación 1, en el que el peso molecular del poli (alcohol vinílico) es igual a o inferior a
50.000 dalton.
4. El procedimiento de la reivindicación 1, en el que el poliéster biodegradable está seleccionado de un grupo que consiste en policaprolactona (PCL) , ácido poli-D, L-láctico (DL-PLA) , ácido poli-L-láctico (L-PLA) , poli (ácido glicólico) (PGA) , poli (ácido láctico-co-ácido glicólico) (PLGA) .
5. El procedimiento de la reivindicación 1, en el que el copolímero biocompatible tipo peine comprende copolímero de PVA-PLA y el agente antitrombótico comprende una molécula de heparina, teniendo el conjugado la siguiente 20 estructura:
en la que n es un número entero de 2-1000; y m es un número entero de 100 a 5000; LA es unidad de repetición de ácido láctico; SA es ácido succínico; Hp es heparina.
6. El procedimiento de la reivindicación 1, en el que el copolímero biocompatible tipo peine comprende PVA y un terpolímero de 1, 1-polilactida, glicolida y caprolactona y el agente antitrombótico comprende una molécula de heparina.
7. El procedimiento de la reivindicación 1, en el que el copolímero biocompatible tipo peine comprende PVA y un terpolímero de d, l-polilactida, glicolida y caprolactona y el agente antitrombótico comprende una molécula de heparina.
8. El procedimiento de la reivindicación 1, en el que la pluralidad de partículas comprende micro-partículas.
9. El procedimiento de la reivindicación 1, en el que la pluralidad de partículas comprende nano-partículas.
Patentes similares o relacionadas:
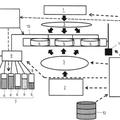 Procedimiento y dispositivo para producir un objeto multicelular tridimensional, del 29 de Julio de 2020, de TECHNISCHE UNIVERSITAT BERLIN: Procedimiento para producir un objeto multicelular tridimensional, con los pasos siguientes:
a) introducción de un primer líquido fotopolimerizable […]
Procedimiento y dispositivo para producir un objeto multicelular tridimensional, del 29 de Julio de 2020, de TECHNISCHE UNIVERSITAT BERLIN: Procedimiento para producir un objeto multicelular tridimensional, con los pasos siguientes:
a) introducción de un primer líquido fotopolimerizable […]
Tapón de catéter extraíble y aplicaciones del mismo, del 3 de Junio de 2020, de Pristine Access Technologies Ltd: Tapón de catéter extraíble , que comprende: un cuerpo de tapón configurado para […]
Dispositivos de cierre automático, del 29 de Abril de 2020, de Solinas Medical Inc: Un puerto de acceso que se puede unir a una superficie dentro del cuerpo de un paciente, que comprende: un cuerpo del puerto que comprende un material […]
Dispositivo para el tratamiento del aneurisma de aorta, del 21 de Abril de 2020, de SERVICIO ANDALUZ DE SALUD: Dispositivo para el tratamiento del aneurisma de aorta. La invención describe un dispositivo para el tratamiento del aneurisma de aorta que comprende: un estent exterior […]
Endoprótesis y dispositivo de colocación para implantar tal endoprótesis, del 15 de Abril de 2020, de Kardiozis: Stent vascular o stent cardiaco que comprende al menos una parte de cuerpo, en el que están dispuestos elementos trombogénicos al menos […]
Dispositivos para tratar la vasculatura de la extremidad inferior, del 12 de Febrero de 2020, de LimFlow GmbH: Un sistema de prótesis implantable para tratar una oclusión en un primer vaso, el sistema de prótesis comprende: un estent (100, 134, 140, 150, 160, 200, 220, […]
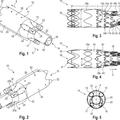 Prótesis vascular autoexpandible, del 29 de Enero de 2020, de JOTEC GMBH: Prótesis vascular autoexpandible para la implantación en un vaso sanguíneo de un paciente, con un cuerpo de base cilíndrico hueco , así […]
Prótesis vascular autoexpandible, del 29 de Enero de 2020, de JOTEC GMBH: Prótesis vascular autoexpandible para la implantación en un vaso sanguíneo de un paciente, con un cuerpo de base cilíndrico hueco , así […]
Dispositivo de protección de microválvula, del 22 de Enero de 2020, de Surefire Medical, Inc: Un dispositivo endovascular para reducir el reflujo de un agente de embolización en un vaso durante un procedimiento de terapia de embolización, comprendiendo […]