COMPOSICIONES DE MEDICAMENTOS A BASE DE SALES DE TIOTROPIO Y EPINASTINA PARA LA TERAPIA DE ENFERMEDADES DE LAS VIAS RESPIRATORIAS.
Medicamento, caracterizado por un contenido en sales de tiotropio (1) en combinación con uno o varios antihistamínicos (2),
eventualmente en forma de sus enantiómeros, mezclas de los enantiómeros o en forma de los racematos, eventualmente en forma de los solvatos o hidratos así como, eventualmente, junto con un coadyuvante farmacéuticamente compatible, en que en el caso del antihistamínico (2) se trata de epinastina, eventualmente en forma de sus sales por adición de ácidos fisiológicamente compatibles
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP01/12510.
Solicitante: BOEHRINGER INGELHEIM PHARMA KG.
Nacionalidad solicitante: Alemania.
Dirección: BINGERSTRASSE 172,55216 INGELHEIM AM RHEIN.
Inventor/es: SCHMELZER, CHRISTEL, MEADE, CHRISTOPHER, JOHN, MONTAGUE, PAIRET, MICHEL, PIEPER, MICHAEL, PAUL.
Fecha de Publicación: .
Fecha Concesión Europea: 23 de Diciembre de 2009.
Clasificación Internacional de Patentes:
- A61K31/46 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › Aza-8-biciclo[3.2.1]octano; Sus derivados, p. ej. atropina, cocaína.
- A61K31/4745 A61K 31/00 […] › condensados con sistemas cíclicos teniendo el nitrógeno como heteroátomo de un ciclo, p. ej. fenantrolinas (derivados de la yohimbina, vinblastina A61K 31/475; derivados de la ergolina A61K 31/48).
- A61K31/496 A61K 31/00 […] › Piperazinas no condensadas conteniendo otros heterociclos, p. ej. rifampicina, tiotixeno.
- A61K31/55 A61K 31/00 […] › que tienen ciclos con siete eslabones, p. ej. azelastina, pentilentetrazol.
- A61K31/56 A61K 31/00 […] › Compuestos que contienen el sistema cíclico del ciclopenta[a]hidrofenantreno; Sus derivados, p. ej. esteroides.
- A61K31/57 A61K 31/00 […] › sustituidos en posición 17 beta por una cadena con dos átomos de carbono, p. ej. pregnano, progesterona.
- A61K31/58 A61K 31/00 […] › que contienen heterociclos, p. ej. aldosterona, danazol, estanozolol, pancuronium, digitogenina (digitoxina A61K 31/704).
- A61K45/06 A61K […] › A61K 45/00 Preparaciones medicinales que contienen ingredientes activos no previstos en los grupos A61K 31/00 - A61K 41/00. › Mezclas de ingredientes activos sin caracterización química, p. ej. compuestos antiflojísticos y para el corazón.
- A61K9/00M20B
Clasificación PCT:
- A61K31/46 A61K 31/00 […] › Aza-8-biciclo[3.2.1]octano; Sus derivados, p. ej. atropina, cocaína.
- A61K31/55 A61K 31/00 […] › que tienen ciclos con siete eslabones, p. ej. azelastina, pentilentetrazol.
- A61P11/00 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › Medicamentos para el tratamiento de trastornos del aparato respiratorio.
- A61P11/02 A61P […] › A61P 11/00 Medicamentos para el tratamiento de trastornos del aparato respiratorio. › Agentes nasales, p. ej. descongestivos.
Clasificación antigua:
- A61K45/00 A61K […] › Preparaciones medicinales que contienen ingredientes activos no previstos en los grupos A61K 31/00 - A61K 41/00.
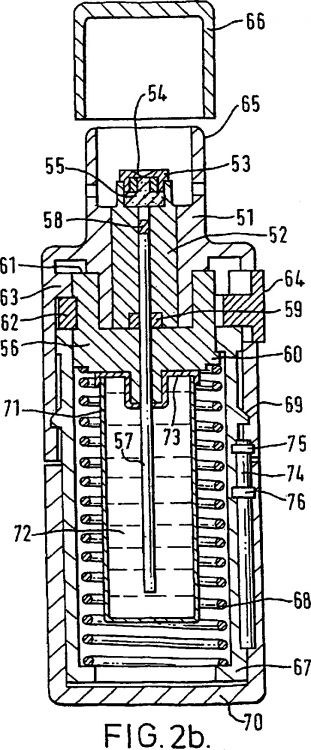
Fragmento de la descripción:
Composiciones de medicamentos a base de sales de tiotropio y epinastina para la terapia de enfermedades de las vías respiratorias.
La presente invención se refiere a nuevas composiciones de medicamentos a base de sales de tiotropio y el antihistamínico epinastina, a procedimientos para su preparación, así como a su utilización en la terapia de enfermedades de las vías respiratorias.
Descripción de la invención
La presente invención se refiere a nuevas composiciones de medicamentos a base de sales de tiotropio y el antihistamínico epinastina, a procedimientos para su preparación, así como a su utilización en la terapia de enfermedades de las vías respiratorias.
Tanto los anticolinérgicos como los antihistamínicos se pueden emplear, de manera conocida, en la terapia de enfermedades de las vías respiratorias. Así, por ejemplo, Naclerio (Clinical and Experimental Allergy, vol. 28, supl. 6, 1998, 54-59) o también Simons (Drugs, vol. 38, nº 2, 1989, 313-331) dan a conocer posibles terapias de, por ejemplo, rinitis mediante bromuro de ipratropio y antagonistas del receptor H1, eventualmente en combinación con corticosteroides. No obstante, no se dan a conocer tandas terapéuticas con, por ejemplo, bromuro de tiotropio.
Sorprendentemente, se puede observar, además, un efecto terapéutico inesperadamente ventajoso, en particular un efecto sinérgico en el tratamiento de enfermedades de las vías respiratorias superiores e inferiores, en particular en el tratamiento de rinitis alérgica o no alérgica, cuando pasa a emplearse uno o varios, preferiblemente una sal de tiotropio junto con el antihistamínico epinastina.
Los efectos precedentemente mencionados se observan tanto en la aplicación simultánea dentro de una única formulación de principios activos, como también en el caso de la aplicación sucesiva de los dos principios activos en formulaciones separadas. De acuerdo con la invención, se prefiere la aplicación simultánea de los dos componentes de principios activos en una única formulación.
En el marco de la presente invención se entienden por sales de tiotropio 1 sales que contienen como catión tiotropio, el componente farmacológicamente activo. En el marco de la presente solicitud de patente, una referencia al catión precedente se ha de considerar mediante la utilización de la designación 1'. Una referencia a compuestos 1 abarca, por naturaleza, una referencia al componente 1' (tiotropio).
Por las sales 1 empleables en el marco de la presente invención se han de entender los compuestos que, junto a tiotropio como ion conjugado (anión) contienen cloruro, bromuro, yoduro, metanosulfonato, para-toluenosulfonato o metilsulfato. En el marco de la presente invención se prefieren de todas las sales 1 el metanosulfonato, cloruro, bromuro o yoduro, otorgándose una particular importancia al metanosulfonato o al bromuro. De extraordinaria importancia de acuerdo con la invención como sal 1 es el bromuro de tiotropio.
En el marco de la presente invención, se entienden por antihistamínico (en lo que sigue 2) epinastina.
Una referencia a epinastina 2 abarca, en el marco de la presente invención, una referencia a sus sales por adición de ácidos farmacológicamente compatibles, eventualmente existentes.
Por las sales por adición de ácidos fisiológicamente compatibles que pueden ser formadas por 2 se entienden, de acuerdo con la invención, sales farmacéuticamente compatibles que se eligen de las sales del ácido clorhídrico, ácido bromhídrico, ácido sulfúrico, ácido fosfórico, ácido metanosulfónico, ácido acético, ácido fumárico, ácido succínico, ácido láctico, ácido cítrico, ácido tartárico o ácido maleico. De acuerdo con la invención se prefieren las sales de los compuestos 2 que se eligen del grupo consistente en acetato, hidrocloruro, hidrobromuro, sulfato, fosfato y metanosulfonato. Particularmente preferidos a este respecto son hidrocloruros e hidrobromuros. De acuerdo con la invención se le otorga una extraordinaria importancia al hidrocloruro de epinastina.
La aplicación de las combinaciones de medicamentos a base de 1 y 2 de acuerdo con la invención se efectúa preferiblemente por vía inhalativa o como administración nasal. En este caso, pueden pasar a emplearse polvos de inhalación adecuados que, envasados en cápsulas adecuadas (inhaletas), son aplicados mediante correspondientes inhaladores de polvo. Alternativamente a ello, una aplicación por inhalación puede efectuarse también por aplicación de aerosoles de inhalación adecuados. A ellos pertenecen también aerosoles de inhalación que, por ejemplo, contienen HFA134a (también denominado TG134a), HFA227 (también denominado TG227) o su mezcla como gas propulsor. La aplicación por inhalación puede efectuarse, además, mediante soluciones adecuadas de la combinación de medicamentos consistente en 1 y 2.
Si la aplicación de la combinación de medicamentos consistente en 1 y 2 se efectúa por vía nasal, pueden pasar a emplearse soluciones adecuadas que son aplicadas mediante correspondientes bombas. Alternativamente a ello, una aplicación nasal puede efectuarse también por aplicación de polvos adecuados.
Un aspecto de la presente invención se refiere, de manera correspondiente, a un medicamento que contiene una combinación a base de 1 y 2.
Otro aspecto de la presente invención se refiere a un medicamento que contiene una o varias sales 1 y uno o varios compuestos 2, eventualmente en forma de sus solvatos o hidratos. También en este caso, los principios activos pueden estar contenidos conjuntamente en una única forma de administración o en dos formas de administración separadas. De acuerdo con la invención se prefieren medicamentos que contienen los principios activos 1 y 2 en una única forma de administración.
Otro aspecto de la presente invención se refiere a un medicamento que, junto a cantidades terapéuticamente eficaces de 1 y 2, contiene una sustancia de soporte farmacéuticamente compatible. Otro aspecto de la presente invención se refiere a un medicamento que, junto a cantidades terapéuticamente eficaces de 1 y 2, no contiene ninguna sustancia de soporte farmacéuticamente compatible.
La presente invención se refiere, además, a la utilización de 1 y 2 para la preparación de un medicamento que contiene cantidades terapéuticamente eficaces de 1 y 2 para el tratamiento de enfermedades de las vías respiratorias superiores e inferiores, en particular para el tratamiento de la rinitis alérgica o no alérgica.
La presente invención se dirige, además, a la utilización, simultánea o sucesiva de dosis terapéuticamente eficaces de la combinación de los medicamentos 1 y 2 precedentes para el tratamiento de enfermedades de las vías respiratorias superiores e inferiores, en particular para el tratamiento de rinitis alérgica o no alérgica.
En las combinaciones de principios activos de acuerdo con la invención a base de 1 y 2, los componentes 1 y 2 pueden estar contenidos en forma de sus enantiómeros, mezclas de los enantiómeros o en forma de los racematos.
Las relaciones en las que se pueden emplear los principios activos 1 y 2 en las combinaciones de principios activos de acuerdo con la invención, son variables. Los principios activos 1 y 2 pueden presentarse, eventualmente, en forma de sus solvatos o hidratos. En función de la elección de los compuestos 1 ó 2, las relaciones en peso empleables en el marco de la presente invención varían en virtud del diferente peso molecular de las distintos compuestos, así como en virtud de su diferente poder de acción. Por norma general, las combinaciones de medicamentos de acuerdo con la invención contienen los compuestos 1 y 2 en relaciones en peso que se encuentran en un intervalo de 1:300 a 50:1, preferiblemente de 1:250 a 40:1. En el caso de las combinaciones de principios activos particularmente preferidas que contienen sal de tiotropio como compuesto 1, las relaciones en peso de 1 a 2 se encuentran preferiblemente en un intervalo en el que tiotropio 1' y 2 están contenidos en relaciones de 1:150 a 30:1, además preferiblemente de 1:50 a 20:1.
A título de ejemplo y sin con ello limitar el alcance de la invención, combinaciones...
Reivindicaciones:
1. Medicamento, caracterizado por un contenido en sales de tiotropio (1) en combinación con uno o varios antihistamínicos (2), eventualmente en forma de sus enantiómeros, mezclas de los enantiómeros o en forma de los racematos, eventualmente en forma de los solvatos o hidratos así como, eventualmente, junto con un coadyuvante farmacéuticamente compatible, en que en el caso del antihistamínico (2) se trata de epinastina, eventualmente en forma de sus sales por adición de ácidos fisiológicamente compatibles.
2. Medicamento según la reivindicación 1, caracterizado porque 1 está contenido en forma del cloruro, bromuro, yoduro, metanosulfonato, para-toluenosulfonato o metilsulfato, preferiblemente en forma del bromuro.
3. Medicamento según una de las reivindicaciones 1 ó 2, caracterizado porque 2 pasa a emplearse en forma de una de sus sales por adición de ácidos fisiológicamente compatibles, que se eligen del grupo consistente en las sales del ácido clorhídrico, ácido bromhídrico, ácido sulfúrico, ácido fosfórico, ácido metanosulfónico, ácido acético, ácido fumárico, ácido succínico, ácido láctico, ácido cítrico, ácido tartárico y ácido maleico.
4. Medicamento según la reivindicación 3, caracterizado porque 2 pasa a emplearse en forma del hidrocloruro de epinastina.
5. Medicamento según una de las reivindicaciones 1 a 4, caracterizado porque las relaciones en peso de 1 a 2 se encuentran en un intervalo de 1:300 a 50:1, preferiblemente de 1:250 a 40:1.
6. Medicamento según una de las reivindicaciones 1 a 5, caracterizado porque una aplicación única corresponde a una dosificación de la combinación de principios activos 1 y 2 de 0,01 a 10000 µg, preferiblemente de 0,1 a 2000 µg.
7. Medicamento según una de las reivindicaciones 1 a 6, caracterizado porque se presenta en forma de una forma de administración adecuada para la inhalación o la aplicación nasal.
8. Medicamento según la reivindicación 7, caracterizado porque se trata de una forma de administración elegida del grupo de polvos de inhalación, aerosoles de dosificación con contenido en gas propulsor y soluciones o suspensiones de inhalación exentas de gas propulsor.
9. Medicamento según la reivindicación 8, caracterizado porque es un polvo de inhalación que contiene 1 y 2 en mezcla con coadyuvantes fisiológicamente inocuos adecuados, elegidos del grupo consistente en monosacáridos, disacáridos, oligosacáridos y polisacáridos, polialcoholes, sales o mezclas de estos coadyuvantes entre sí.
10. Polvos de inhalación según la reivindicación 9, caracterizados porque el coadyuvante presenta un tamaño de partícula medio máximo de hasta 250 µm, preferiblemente entre 10 y 150 µm.
11. Cápsulas, caracterizadas por un contenido en polvos de inhalación según la reivindicación 9 ó 10.
12. Medicamento según la reivindicación 8, caracterizado porque se trata de un aerosol de inhalación con contenido en gas propulsor que contiene 1 y 2 en forma disuelta o dispersada.
13. Aerosol de inhalación con contenido en gas propulsor según la reivindicación 12, caracterizado porque como gas propulsor contiene hidrocarburos tales como n-propano, n-butano o isobutano o hidrocarburos halogenados tales como derivados clorados y/o fluorados del metano, etano, propano, butano, ciclopropano o ciclobutano.
14. Aerosol de inhalación con contenido en gas propulsor según la reivindicación 13, caracterizado porque el gas propulsor representa TG134a, TG227 o una mezcla de los mismos.
15. Aerosol de inhalación con contenido en gas propulsor según la reivindicación 12, 13 ó 14, caracterizado porque eventualmente contiene uno o varios otros componentes elegidos del grupo consistente en co-disolventes, estabilizadores, agentes tensioactivos (surfactantes), antioxidantes, lubricantes y agentes para el ajuste del valor del pH.
16. Aerosol de inhalación con contenido en gas propulsor según una de las reivindicaciones 12 a 15, caracterizado porque puede contener hasta 5% en peso de principio activo 1 y/ó 2.
17. Medicamento según la reivindicación 8, caracterizado porque se trata de una solución o suspensión de inhalación exenta de gas propulsor que como disolvente contiene agua, etanol o una mezcla a base de agua y etanol.
18. Solución o suspensión de inhalación según la reivindicación 17, caracterizada porque el pH asciende a 2-7, preferiblemente 2-5.
19. Solución o suspensión de inhalación según la reivindicación 18, caracterizada porque el pH se ajusta mediante un ácido elegido del grupo consistente en ácido clorhídrico, ácido bromhídrico, ácido nítrico, ácido sulfúrico, ácido ascórbico, ácido cítrico, ácido málico, ácido tartárico, ácido maleico, ácido succínico, ácido fumárico, ácido acético, ácido fórmico, ácido propiónico o mezclas de los mismos.
20. Solución o suspensión de inhalación según una de las reivindicaciones 17 a 19, caracterizada porque contiene eventualmente otros co-disolventes y/o coadyuvantes.
21. Solución o suspensión de inhalación según la reivindicación 20, caracterizada porque como co-disolventes contiene componentes que contienen grupos hidroxilo u otros grupos polares, por ejemplo alcoholes - en particular alcohol isopropílico, glicoles - en particular propilenglicol, polietilenglicol, polipropilenglicol, glicoléter, glicerol, alcoholes polioxietilénicos y ésteres de ácidos grasos de polioxietileno.
22. Solución o suspensión de inhalación según una de las reivindicaciones 20 ó 21, caracterizada porque como coadyuvantes contiene sustancias tensioactivas, estabilizadores, formadores de complejos, antioxidantes y/o sustancias conservantes, saboreantes, sales farmacológicamente inocuas y/o vitaminas.
23. Solución o suspensión de inhalación según la reivindicación 22, caracterizada porque como formadores de complejos contiene ácido edítico o una sal del ácido edítico, preferiblemente edetato de sodio.
24. Solución o suspensión de inhalación según la reivindicación 22 ó 23, caracterizada porque como antioxidantes contiene compuestos elegidos del grupo consistente en ácido ascórbico, vitamina A, vitamina E y tocoferoles.
25. Solución o suspensión de inhalación según la reivindicación 22, 23 ó 24, caracterizada porque como agentes conservantes contiene compuestos elegidos de cloruro de cetilpiridinio, cloruro de benzalconio, ácido benzoico y benzoatos.
26. Solución o suspensión de inhalación según una de las reivindicaciones 20 a 25, caracterizada porque junto a los principios activos 1 y 2 y el disolvente contiene ya sólo cloruro de benzalconio y edetato sódico.
27. Solución o suspensión de inhalación según una de las reivindicaciones 20 a 25, caracterizada porque junto a los principios activos 1 y 2 y el disolvente contiene ya sólo cloruro de benzalconio.
28. Solución o suspensión de inhalación según una de las reivindicaciones 17 a 27, caracterizada porque se trata de un concentrado o de una solución o suspensión de inhalación estéril lista para el uso.
29. Uso de una composición según una de las reivindicaciones 1 a 28, para la preparación de un medicamento para el tratamiento de rinitis alérgica o no alérgica.
Patentes similares o relacionadas:
 Formulaciones de finasterida para la liberación de fármacos en el cabello y el cuero cabelludo, del 29 de Julio de 2020, de POLICHEM SA: Una composición que contiene:
(a) hidroxipropil-quitosano o una sal fisiológicamente aceptable de este en una cantidad de un 0,25 a un 2,0 % […]
Formulaciones de finasterida para la liberación de fármacos en el cabello y el cuero cabelludo, del 29 de Julio de 2020, de POLICHEM SA: Una composición que contiene:
(a) hidroxipropil-quitosano o una sal fisiológicamente aceptable de este en una cantidad de un 0,25 a un 2,0 % […]
Derivados de ácidos biliares como agonistas FXR/TGR5, del 1 de Julio de 2020, de ENANTA PHARMACEUTICALS, INC: Un compuesto representado por la Formula I, o una sal o ester aceptable farmaceuticamente de este: **(Ver fórmula)** en donde: Ra es hidrogeno o -C1-C8 alquilo […]
Yoduro de povidona, un conservante alternativo novelo para composiciones oftálmicas, del 3 de Junio de 2020, de TAKEDA PHARMACEUTICAL COMPANY LIMITED: Una composición oftálmica estable adecuada para administración tópica en el ojo, que comprende una mezcla de: a. yoduro de povidona (PVP-I) a una concentración entre 0,01% […]
Composiciones y métodos para suprimir las proliferaciones endometriales, del 13 de Mayo de 2020, de Allergan Pharmaceuticals International Limited: Antagonista de progesterona seleccionado de 21-metoxi-17a-acetoxi-11b-(4-N,N-dimetilaminofenil)-19- norpregna-4,9-dieno-3,20-diona (CDB-4124) o 17α-acetoxi-11β-(4-N,N-dimetilaminofenil)-19-norpregna-4,9- […]
Composiciones oftálmicas que comprenden povidona yodada, del 29 de Abril de 2020, de CLS PHARMACEUTICALS, INC: Una composición adecuada para la administración tópica a un ojo, eficaz para el tratamiento y/o la profilaxis de una infección por microorganismos […]
Suministro transdérmico, del 8 de Abril de 2020, de AGILE THERAPEUTICS, INC: Un método anticonceptivo, que comprende: (A) aplicar de manera consecutiva múltiples dispositivos de tratamiento de suministro de hormonas transdérmico a la piel […]
Uso de desoxicolato de sodio para la eliminación no quirúrgica de grasa, del 8 de Abril de 2020, de Lundquist Institute for Biomedical Innovation at Harbor-UCLA Medical Center: Uso de desoxicolato de sodio para la eliminación no terapéutica y no quirúrgica de acumulación de grasa localizada.
Composición de suspensión oftálmica, del 1 de Abril de 2020, de BAUSCH & LOMB INCORPORATED: Una suspension oftalmica que comprende un ingrediente activo oftalmico suspendido en un vehiculo de la formulacion, en donde el ingrediente activo oftalmico es loteprednol […]