VECTORES DE EXPRESION QUE COMPRENDEN EL PROMOTOR DEL GEN PKLR HUMANO Y SU USO PARA LA ELABORACION DE COMPOSICIONES FARMACEUTICAS DESTINADAS A TERAPIA GENICA SOMATICA CON EXPRESION ESPECIFICA EN CELULAS ERITROIDES.
Vectores de expresión que comprenden el promotor del gen PKLR humano y su uso para la elaboración de composiciones farmacéuticas destinadas a terapia génica somática con expresión específica en células eritroides.
La presente invención se refiere al uso de secuencias reguladoras del promotor del gen PKLR en la producción de vectores, con la excepción de vectores que comprendan virus adeno-asociados, para ser utilizados en la elaboración de composiciones farmacéuticas destinadas a terapia génica somática en tejido eritroide
Tipo: Patente de Invención. Resumen de patente/invención. Número de Solicitud: P200701024.
Solicitante: CENTRO DE INVESTIGACIONES ENERGETICAS, MEDIOAMBIENTALES Y TECNOLOGICAS (CIEMAT).
Nacionalidad solicitante: España.
Provincia: MADRID.
Inventor/es: GUENECHEA AMURRIO, GUILLERMO, SEGOVIA SANZ,JOSE CARLOS, MEZA,NESTOR W, BUEREN,JUAN ANTONIO, ALMARZA NOVOA,ELENA, ALONSO FERRERO,MARIA EUGENIA.
Fecha de Solicitud: 17 de Abril de 2007.
Fecha de Publicación: .
Fecha de Concesión: 2 de Junio de 2010.
Clasificación Internacional de Patentes:
- A61K48/00D2
- C12N15/86 QUIMICA; METALURGIA. › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 15/00 Técnicas de mutación o de ingeniería genética; ADN o ARN relacionado con la ingeniería genética, vectores, p. ej. plásmidos, o su aislamiento, su preparación o su purificación; Utilización de huéspedes para ello (mutantes o microorganismos modificados por ingeniería genética C12N 1/00, C12N 5/00, C12N 7/00; nuevas plantas en sí A01H; reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00; nuevas razas animales en sí A01K 67/00; utilización de preparaciones medicinales que contienen material genético que es introducido en células del cuerpo humano para tratar enfermedades genéticas, terapia génica A61K 48/00; péptidos en general C07K). › Vectores virales.
Clasificación PCT:
- A61K48/00 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › Preparaciones medicinales que contienen material genético que se introduce en las células del cuerpo vivo para tratar enfermedades genéticas; Terapia génica.
- C12N15/54 C12N 15/00 […] › Transferasas (2).
- C12N15/86 C12N 15/00 […] › Vectores virales.
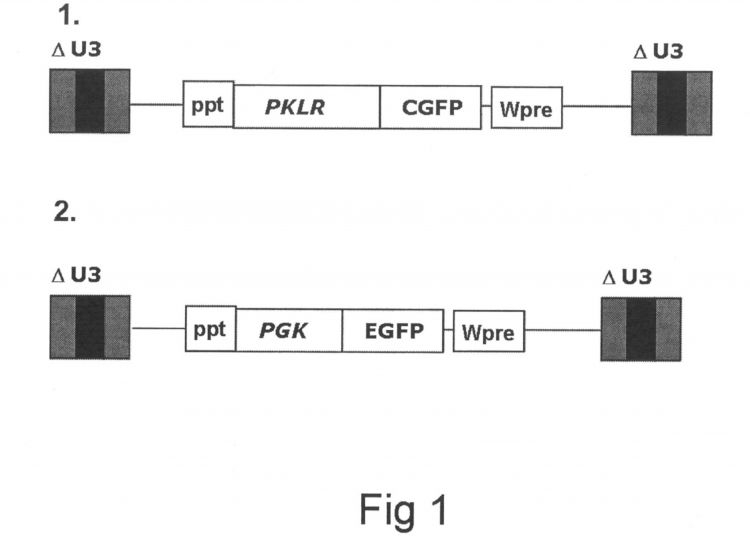
Fragmento de la descripción:
Vectores de expresión que comprenden el promotor del gen PKLR humano y su uso para la elaboración de composiciones farmacéuticas destinadas a terapia génica somática con expresión específica en células eritroides.
Campo de la invención
La presente invención se engloba dentro del campo de la ingeniería genética. Concretamente, la invención se refiere al uso del promotor del gen humano que regula la expresión de la forma R de la piruvato quinasa (hRPK) en la producción de vectores, para ser utilizados en la elaboración de composiciones farmacéuticas destinadas a terapia génica somática. Mediante el uso del promotor del gen PKLR se ha conseguido la generación de vectores en los que el transgén se expresa específicamente y de forma moderada en células de la línea de diferenciación eritroide y más concretamente, en los estadios finales de la diferenciación hacia el eritrocito.
Antecedentes de la invención
El desarrollo de la terapia génica como procedimiento generalizado para el tratamiento de enfermedades dependerá del equilibrio positivo entre el beneficio clínico y el riesgo asociado a esta nueva intervención terapéutica. Aunque ya es evidente la eficacia de la terapia génica para producir una mejoría clínica en pacientes con trastornos hereditarios (1-6), recientemente han surgido reservas relativas a la seguridad de dicha terapia. Los estudios experimentales han demostrado la generación de leucemias en ratones asociadas con la activación de oncogenes endógenos por provirus integrados (7,8). Además, se han observado resultados similares en pacientes humanos, cuyas células madre hematopoyéticas (CMHs) fueron transducidas con vectores gamma-retrovirales que contenían promotores virales (9,10).
La Piruvato Kinasa eritrocitaria (RPK) humana es una enzima glicolítica que se expresa solo en células de linaje eritroide. Durante la diferenciación eritroide, la expresión de la RPK aumenta gradualmente mediante un mecanismo dependiente de la activación de su promotor por factores transcripcionales específicos del tejido eritroide (11). La expresión de la RPK es mayor en eritroblastos basófilos y policromatófilos (11-13).
La RPK humana está codificada por el gen PKLR, con una extensión aproximada de 12 kb. Presenta un total de 12 exones y 11 intrones que codifican la isoforma RPK, y la isoforma LPK producida en el parénquima hepático. Los dos exones iniciales son específicos para cada isoforma, el 1(R) para la RPK y el 1(L) para la LPK, de expresión específica en hígado. El control transcripcional depende de la actividad específica de los promotores que flanquean cada exón 1 (el R y el L), permitiendo su expresión diferencial en tejido eritroide (RPK) y hepático (LPK) respectivamente. La región 5' que flanquea al primer exón (1R) presenta dos cajas CAC, cuatro motivos GATA y un nuevo elemento regulador de trascripción denominado PKR-RE1 con el motivo (CTGTC) ubicados entre los 250 pares de bases corriente arriba del inicio de transcripción, que en conjunto producen una actividad promotora específica en células eritroides (14-30). Por tanto, la expresión de la isoenzima RPK ocurre con una elevada especificidad temporal y absoluta especificidad de tejido, sólo en tejido eritroide, como consecuencia de las características descritas para sus regiones promotoras y reguladoras.
La utilización de promotores específicos de tejido para expresar la proteína de interés en células comprometidas a la diferenciación de un particular linaje evitaría efectos adversos asociados a la expresión ectópica de la proteína en células no deseadas, lo cual ha sido uno de los objetivos desde el comienzo de la terapia génica. Además, en el caso de promotores ubicuos, tales como los virales, se ha comprobado su capacidad para transactivar genes endógenos, incluyendo oncogenes, tras su inserción estable en el genoma de las célula madre. El interés de limitar la influencia del promotor presente en el vector sobre la expresión de genes próximos a su sitio de integración se ha visto reforzada por observaciones recientes que indican que, tanto los vectores gamma-retrovirales, como los vectores lentivirales, tienen una alta probabilidad de inserción en regiones de ADN próximas o dentro de los genes (31-34). La expresión moderada y específica de trangenes con promotores que no se expresen en las células madre limitaría las posibilidades de generar leucemias como consecuencia de la transactivación de oncogenes en células madre. Una de las principales dificultades para generar vectores con especificidad de expresión ha sido el tamaño de las secuencias reguladoras, en términos de número de pares de bases necesario para tener todas las regiones reguladoras necesarias para conferir la especificidad requerida. Cuanto mayor sea el tamaño del promotor menor especificidad tendrá.
Se ha de mencionar cierta documentación perteneciente al estado de la técnica que tiene relación con la presente invención. En primer lugar, citar el sitio de Internet http://egp.gs.washington.edu (ver selección Finished Genes Table) donde se localiza información relativa al gen PKLR humano localizado en la banda q21 del cromosoma 1.
Entre dicha información destacan varios artículos científicos de interés. Así el artículo Biochemical and Biophysical Research Communications 188(2):516-523 (1992), se relaciona con un análisis estructural del gen PKLR y la identificación de la actividad promotora específica en células eritroides.
Asimismo, en el artículo con referencia bibliográfica Nucleic Acids Research 20(21):5669-5676 (1992), se ofrece el resultado de la investigación sobre los mecanismos responsables de la especificidad en células eritroides de dicho promotor.
Finalmente, en los artículos con referencia Blood 101(4):1596-1602 (2003) y Blood Cells, Molecules and Diseases 34:186-190 (2005), se proporciona información concerniente a un elemento regulador del promotor específico eritroide del gen PKLR.
Por otro lado, dentro de la documentación de patentes, se han de mencionar dos documentos. El documento WO 02/29103, se refiere a un sistema para el diagnóstico y evaluación de la progresión de cáncer hepático, carcinoma hepatocelular o metástasis, de un tumor hepático, en un paciente por medio de la detección del nivel de expresión de dos o más genes (uno de ellos sería el gen PKLR humano) en una muestra de tejido de hígado. Igualmente, el documento WO 02/28999, se relaciona con un método de detección de la activación de granulocitos mediante la detección de la expresión diferencial de los genes asociados (uno de ellos sería el promotor específico eritroide del gen PKLR humano) con dicha activación en una micromatriz de ADN (biochip). Dicho método permite el seguimiento de los diversos estados de diferentes enfermedades, así como evaluar la farmacotoxicidad.
Por otro lado, se ha de citar el documento europeo de patente EP 1 193 272, correspondiente a un vector de un virus adeno-asociado de utilidad en terapia génica. Dicho vector contiene un promotor inducible que es el promotor del gen de la piruvato quinasa. Sin embargo, dicho promotor es el promotor específico de hígado del gen PKLR, cuya secuencia es diferente del promotor específico de tejido eritroide aquí propuesto. El promotor específico de hígado no regularía la expresión del gen PKLR en líneas celulares eritroides.
También se ha de mencionar el documento WO 89/02469, concerniente a un elemento intensificador (enhancer) de la transcripción, específico de eritroides humanos. Dicho elemento proporciona una mejora en construcciones genéticas para transfección de células de linaje eritroide. Tales construcciones serán de utilidad en terapia génica de desórdenes en células eritroides, tales como la talasemia o las hemoglobinopatías. Sin embargo en esta patente la secuencia empleada es de un tamaño mayor (800 pb) que la de la presente invención, por consiguiente, es menos específica. Además la secuencia descrita en dicha patente regula la expresión de un gen diferente al gen PKLR. Se trata del gen de la ß-globina, cuya homología con el gen PKLR es nula.
La presente invención va dirigida al uso del promotor específico de eritrocitos (RPK) en la construcción de vectores, con la excepción de vectores que comprendan virus adeno-asociados, para ser utilizados en la elaboración de composiciones farmacéuticas destinadas a terapia génica somática en tejido eritroide. Por lo tanto, la presente invención se diferencia del estado de la técnica porque no está focalizada en el promotor "per se", ni está asociado a vectores adeno-asociados...
Reivindicaciones:
1. Uso de secuencias reguladoras que comprendan el promotor del gen PKLR en la producción de vectores, con la excepción de vectores que comprendan virus adeno-asociados, para ser utilizados en la elaboración de composiciones farmacéuticas destinadas a terapia génica somática en tejido eritroide.
2. Uso de secuencias reguladoras que comprendan el promotor del gen PKLR en la producción de vectores, con la excepción de vectores que comprendan virus adeno-asociados, para ser utilizados en la elaboración de composiciones farmacéuticas destinadas a terapia génica somática en tejido eritroide, según la reivindicación 1, donde la secuencia reguladora es la SEQ ID NO:1.
3. Uso, según cualquiera de las reivindicaciones 1 a 2, caracterizado porque el vector producido comprende un virus integrativo.
4. Uso, según la reivindicación 3, caracterizado porque el vector producido comprende un virus Lentivirus.
5. Vector, con la excepción de vectores que comprendan virus adeno-asociados, caracterizado por que comprende al menos una secuencia reguladora que, a su vez, comprende el promotor del gen PKLR, para ser utilizado en la elaboración de composiciones farmacéuticas destinadas a terapia génica somática en tejido eritroide.
6. Vector, según la reivindicación 5, caracterizado por comprender un virus integrativo.
7. Vector, según cualquiera de las reivindicaciones 5 y 6, caracterizado por comprender un virus Lentivirus.
8. Células transducidas por vectores de las reivindicaciones 5 a 7.
9. Uso de los vectores de las reivindicaciones 5 a 7 para la elaboración de composiciones farmacéuticas destinadas a ser utilizadas en terapia génica somática.
10. Uso de las células de la reivindicación 8, para la elaboración de composiciones farmacéuticas destinadas a ser utilizadas en terapia génica somática.
11. Composiciones farmacéuticas que comprenden vectores de las reivindicaciones 5 a 7 y vehículos farmacéuticamente aceptables.
12. Composiciones farmacéuticas que comprenden las células de la reivindicación 8, y vehículos farmacéuticamente aceptables.
Patentes similares o relacionadas:
Método y medios para purificar vectores retrovíricos, del 29 de Julio de 2020, de Autolus Limited: Una célula productora de retrovirus que expresa una proteína de marcaje en la superficie celular, de tal manera que los vectores retrovíricos producidos por la célula se […]
 CD52 soluble para su uso en el tratamiento o la prevención de la esclerosis múltiple o de la artritis reumatoide, del 29 de Julio de 2020, de THE WALTER AND ELIZA HALL INSTITUTE OF MEDICAL RESEARCH: Uno cualquiera o más de:
i) glucoproteína CD52 soluble, ii) una proteína de fusión que comprende la glucoproteína CD52 soluble como una primera proteína, y una segunda proteína;
[…]
CD52 soluble para su uso en el tratamiento o la prevención de la esclerosis múltiple o de la artritis reumatoide, del 29 de Julio de 2020, de THE WALTER AND ELIZA HALL INSTITUTE OF MEDICAL RESEARCH: Uno cualquiera o más de:
i) glucoproteína CD52 soluble, ii) una proteína de fusión que comprende la glucoproteína CD52 soluble como una primera proteína, y una segunda proteína;
[…]
Arenavirus trisegmentados como vectores de vacunas, del 22 de Julio de 2020, de UNIVERSITE DE GENEVE: Una partícula de arenavirus trisegmentada infecciosa y competente para la replicación que comprende un segmento L y dos segmentos S, en donde uno de los dos segmentos […]
Promotor híbrido y usos del mismo, del 15 de Julio de 2020, de Just Biotherapeutics, Inc: Un promotor híbrido, que comprende: (i) una secuencia potenciadora de citomegalovirus murino (mCMV), que comprende un elemento potenciador de mCMV (mCMV-E) y una […]
Señal para el empaquetamiento de vectores del virus de la gripe, del 24 de Junio de 2020, de WISCONSIN ALUMNI RESEARCH FOUNDATION: Un vector del virus de la gripe para la expresión y empaquetamiento de ARNv recombinante, en el que el vector comprende: secuencias correspondientes […]
Métodos y composiciones para la producción de virus vaccina, del 10 de Junio de 2020, de SillaJen Biotherapeutics, Inc: Un metodo para producir un virus vaccinia de la cepa Wyeth o Western Reserve que comprende: (a) infectar las celulas HeLa adheridas a una superficie […]
Vectores de AAV dirigidos a oligodendrocitos, del 10 de Junio de 2020, de THE UNIVERSITY OF NORTH CAROLINA AT CHAPEL HILL: Un ácido nucleico que codifica una cápside de AAV, comprendiendo el ácido nucleico una secuencia codificante de la cápside de AAV que es al menos el 96 % idéntica […]
Terapia génica basada en VAA para la esclerosis múltiple, del 3 de Junio de 2020, de UNIVERSITY OF FLORIDA RESEARCH FOUNDATION, INC.: Un vector de ácido nucleico vírico adenoasociado recombinante (VAAr) con el serotipo VAA8 que comprende: un polinucleótido que incluye un segmento de ácido […]