VACUNACION CON CELULAS INMUNOAISLADAS Y PRODUCTORAS DE UN INMUNOMODULADOR.
Un producto terapéutico específico para un paciente, caracterizado por dos componentes:
(a) un primer componente que comprende una macrocápsula recuperable que comprende células humanas alogénicas inmunoaisladas, que segregan un agente inmunoestimulador a razón de entre 500 y 1000 ng/24 horas, en donde el agente inmunoestimulador es GM-CSF; y
(b) un segundo componente específico para un paciente, que comprende células tumorales irradiadas del paciente,
para su uso en la terapia del cáncer de dicho paciente
Tipo: Resumen de patente/invención. Número de Solicitud: W0307140EP.
Solicitante: MAXIVAX SA.
Nacionalidad solicitante: Suiza.
Dirección: RUE MASSOT 7,1206 GENEVE.
Inventor/es: MACH,NICOLAS.
Fecha de Publicación: .
Fecha Concesión Europea: 11 de Noviembre de 2009.
Clasificación Internacional de Patentes:
- A61K38/19 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 38/00 Preparaciones medicinales que contienen péptidos (péptidos que contienen ciclos beta-lactama A61K 31/00; dipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina 2,5-dionas, A61K 31/00; péptidos basados en la ergolina A61K 31/48; que contienen compuestos macromoleculares que tienen unidades aminoácido repartidas estadísticamente A61K 31/74; preparaciones medicinales que contienen antígenos o anticuerpos A61K 39/00; preparaciones medicinales caracterizadas por los ingredientes no activos, p. ej. péptidos como soportes de fármacos, A61K 47/00). › Citoquinas; Linfoquinas; Interferones.
- A61K38/19B
- A61K39/00D6
- A61K39/39 A61K […] › A61K 39/00 Preparaciones medicinales que contienen antígenos o anticuerpos (materiales para ensayos inmunológicos G01N 33/53). › caracterizados por los aditivos inmunoestimulantes, p. ej. por los adyuvantes químicos.
Clasificación PCT:
- A61K39/00 A61K […] › Preparaciones medicinales que contienen antígenos o anticuerpos (materiales para ensayos inmunológicos G01N 33/53).
- A61K39/39 A61K 39/00 […] › caracterizados por los aditivos inmunoestimulantes, p. ej. por los adyuvantes químicos.
- A61P31/00 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › Antiinfecciosos, es decir antibióticos, antisépticos, quimioterápicos.
- A61P35/00 A61P […] › Agentes antineoplásicos.
Clasificación antigua:
- A61K39/00 A61K […] › Preparaciones medicinales que contienen antígenos o anticuerpos (materiales para ensayos inmunológicos G01N 33/53).
- A61K39/39 A61K 39/00 […] › caracterizados por los aditivos inmunoestimulantes, p. ej. por los adyuvantes químicos.
- A61P31/00 A61P […] › Antiinfecciosos, es decir antibióticos, antisépticos, quimioterápicos.
- A61P35/00 A61P […] › Agentes antineoplásicos.
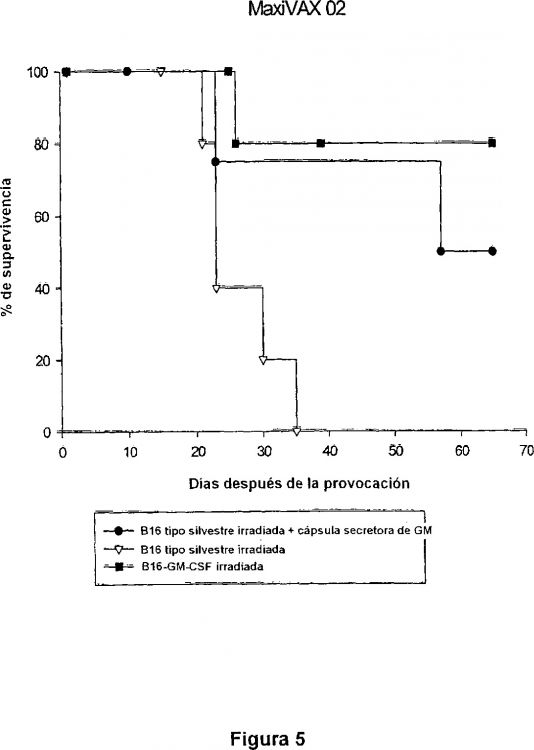
Fragmento de la descripción:
Vacunación con células inmunoaisladas y productoras de un inmunomodulador.
La presente invención se refiere a un nuevo método para proporcionar un coadyuvante activo o inmunomodulador, por ejemplo en el contexto de la inmunización en personas o en animales. De acuerdo con este método, un inmunomodulador, por ejemplo el GM-CSF (factor estimulador de colonias de granulocitos-macrófagos), es liberado de células encapsuladas inmunoprotegidas que producen esta proteína. Este sistema está particularmente bien adaptado a la vacunación por cuanto proporciona el inmunomodulador en una forma activa, de una manera continuada no inmunogénica, en la vecindad inmediata del antígeno o de los antígenos de la vacuna. La estrategia de la invención está perfectamente adaptada tanto para la terapia del cáncer como para la vacunación contra agentes infecciosos.
Fundamento de la invención
En el campo de la vacunación, las vacunas de primera generación comprendían tan solo el antígeno contra el que se deseaba una respuesta inmunitaria. Sin embargo, como en la mayor parte de los casos la presencia de un solo antígeno no es más que débilmente eficaz, se desarrolló una segunda generación de vacunas en la que la composición de vacunación incluye uno o más coadyuvantes como inmunomoduladores para potenciar esta respuesta inmunitaria.
Se han publicado varias técnicas diferentes para proporcionar el coadyuvante en el sitio de vacunación, dependiendo del contexto de la inmunización.
En el contexto de las vacunas basadas en un antígeno (al contrario que en las vacunas basadas en células), una técnica ampliamente aplicable usada para proporcionar el coadyuvante necesario es simplemente combinar el antígeno con el coadyuvante en la composición de vacunación. La composición resultante es administrada directamente al sujeto, suministrando así el antígeno y el coadyuvante de una manera simultánea y co-localizada.
Sin embargo, este sencillo método no puede ser usado en todas las versiones de vacunación. Por ejemplo, en la mayor parte de los cánceres, los antígenos útiles son frecuentemente desconocidos. Este es el caso para la mayoría de los cánceres comunes en las personas, tales como el cáncer de pulmón, colon, estómago, linfoma o cerebro. Por consiguiente, se necesitan nuevas estrategias de inmunización tales como el método basado en células. La estrategia de inmunización que implica a vacunas basadas en células, en las que el antígeno o los antígenos contra los cuales ser requiere una respuesta inmunitaria es producido por células completas implantadas en un sujeto, necesita el uso de técnicas más elaboradas para asegurar el suministro eficiente del coadyuvante.
Una solución en este tipo de contexto es inyectar directamente el inmunomodulador en el sitio de la vacunación. El inmunomodulador puede ser "desnudo" o alternativamente puede ser administrado en una formulación de liberación lenta usando microesferas liposómicas pegiladas (solicitud de patente internacional WO 98/33520, presentada por Bynstryn). Esta estrategia está sin embargo limitada por dificultades técnicas y bioquímicas, así como por cierto grado de liberación sistémica que induce toxicidades potenciales.
Un método alternativo que ha sido propuesto para salvar los problemas que surgen de la técnica de inyección directa es el uso de "células by-stander" (células circundantes o espectadoras) para producir localmente los inmunomoduladores. De acuerdo con este método, se implantas células que producen el coadyuvante en las proximidades de la fuente de antígeno, proporcionando así una eficaz liberación local de coadyuvante en el sitio de la vacuna. La eficacia de este método ha sido demostrada en ratones en los que la vacuna es una mezcla de fibroblastos secretores de GM-CSF y células tumorales irradiadas (Aruga et al., Cancer Research, 57, 1997, 3230-3237).
Sin embargo, ni siquiera este método está totalmente libre de inconvenientes. En realidad, para la inmunización humana, es sabido que se requieren inmunizaciones múltiples. Como las células by-stander singénicas no son fácilmente disponibles, se usan células alogénicas en la inmensa mayoría de los casos. En consecuencia, después de la primera inyección, las "células by-stander" son reconocidas por el sistema inmunitario del hospedador (alorreconocimiento) y son rechazadas, impidiendo así la posterior producción de inmunomodulador. Además, el alorreconocimiento de las "células by-stander" pone en peligro la respuesta inmunitaria deseada contra la sustancia antigénica de la vacuna.
Con el fin de evitar este alorreconocimiento, el trabajo de Borrello et al. (Human Gene Therapy, 1999) ha descrito una estrategia en la que las células suministradoras del GM-CSF son una línea celular, la K-562, que no logra expresar antígenos HLA clase I o II, disminuyendo potencialmente la magnitud de las alorrespuestas generadas en inmunizaciones repetidas. Las células K-562, modificadas para segregar GM-CSF, no expresan moléculas del MHC en su superficie. Son HLA negativas. Sin embargo estas células son células cancerosas humanas y son altamente sensibles a potentes mecanismos de rechazo que ocurren sin la intervención de las proteínas HLA de clase I o II. Se sabe que al menos dos subtipos de linfocitos conocidos como células T ?d o linfocitos asesinos naturales (NK: Natural Killer) atacan y destruyen a las células extrañas por mecanismos independientes del HLA de clase I o II. En relación con la línea de células K-562, se sabe que es muy sensible a las células NK y también a las células T ?d (J. Immunotherapy 2000 23: 536-548 Schilbach K. et al.) y por tanto se usan como control o testigo positivo para la actividad de las células NK.
Es por tanto probable que las células by-stander K-562 inyectadas en el sitio de la vacuna sean destruidas eficaz y rápidamente por mecanismos citotóxicos no dependientes del MHC. Esto puede muy bien reducir de forma significativa la liberación del inmunomodulador.
Además de ser muy sensibles a la destrucción rápida por las células NK, las células K-562 pueden expresar MHC de clase I al exponerlas a interferón ?. Es posible que tal citocina pudiera estar presente o ser liberada en el sitio de vacunación durante la primera inmunización o después de inmunizaciones repetidas. Tal regulación por exceso del MHC de clase I conducirá también a una rápida destrucción de la célula a través de la inmunidad celular clásica.
Por estas razones, el uso de células tales como las K-562 en la vacunación trae consigo numerosos inconvenientes.
Otra solución, ampliamente usada en el contexto de las vacunas basadas en células, por ejemplo en la terapia del cáncer, es acoplar la producción de antígeno y la liberación de inmunomodulador, modificando por ingeniería genética la célula que es la fuente del antígeno, para que suministre también el inmunomodulador. Por ejemplo, en las vacunas del cáncer, la fuente de antígeno es normalmente una célula tumoral entera. Esta célula puede modificarse por ingeniería genética, por ejemplo mediante transfección, para que produzca al mismo tiempo el coadyuvante necesario. Se han publicados respuestas inmunitarias antitumorales potentes, específicas y prolongadas en el modelo de ratones usando esta técnica, que se apoya en vectores retrovirales como método de transferencia de genes para construir células tumorales que suministren GM-CSF.
En vista de los favorables resultados obtenidos en el modelo con ratones, los primeros experimentos con personas utilizaron la misma estrategia (Simons JW. et al. 1997 Cancer Research, 43 (11); Soiffer R. et al. 1998, Proc. Natl. Acad. Sci. USA, 95, 13141; Simons et al. 1999, Cancer Research, 59 (20)). Sin embargo, la técnica demostró ser muy laboriosa y requerir mucho tiempo, porque las células del paciente, recolectadas quirúrgicamente, necesitan ser expandidas in vitro para la infección retroviral, impidiendo un uso amplio del método.
Por tanto se ha propuesto el uso de otro vector viral para infectar las células tumorales para soslayar estas dificultades. Virus construidos por ingeniería genética como los adenovirus pueden infectar las células tumorales muy eficazmente y con procedimientos mucho más simples. Dado que los adenovirus pueden infectar células no en división, las células tumorales recolectadas pueden ser infectadas inmediatamente, evitando la larga y tediosa etapa de cultivo primario que se requiere cuando se usan...
Reivindicaciones:
1. Un producto terapéutico específico para un paciente, caracterizado por dos componentes:
(a) un primer componente que comprende una macrocápsula recuperable que comprende células humanas alogénicas inmunoaisladas, que segregan un agente inmunoestimulador a razón de entre 500 y 1000 ng/24 horas, en donde el agente inmunoestimulador es GM-CSF; y
(b) un segundo componente específico para un paciente, que comprende células tumorales irradiadas del paciente,
para su uso en la terapia del cáncer de dicho paciente.
2. El producto terapéutico según la reivindicación 1ª, en el que las células de la macrocápsula son irradiadas antes de la implantación.
3. El producto terapéutico según la reivindicación 1ª, en el que las células inmunoaisladas producen además otro agente inmunoestimulador.
4. El producto terapéutico según la reivindicación 3ª, en el que el otro agente inmunoestimulador se elige entre el grupo que consiste en IL-12, IL-15, IL-4, interferón gamma, quimiocinas y factores de crecimiento dendrítico.
5. El producto terapéutico según la reivindicación 1ª, en el que dicha macrocápsula es permeable selectivamente.
6. El producto terapéutico según la reivindicación 5ª, en el que dicha macrocápsula es permeable selectivamente a moléculas con un peso molecular inferior a 280 kDa.
7. El producto terapéutico según una cualquiera de las reivindicaciones 1ª a 6ª, en el que dichas células inmunoaisladas son modificadas por ingeniería genética para que segreguen moléculas inmunoestimuladoras.
8. El producto terapéutico según la reivindicación 7ª, en el que la modificación genética se consigue mediante transfección por un plásmido o infección por un virus.
9. El producto terapéutico según una cualquiera de las reivindicaciones 1ª a 8ª, en el que dichas células inmunoaisladas son una línea de células de fibroblasto o epiteliales humanas.
10. El producto terapéutico según una cualquiera de las reivindicaciones 1ª a 9ª, en el que dichas células inmunoaisladas son células inmortales o inmortalizadas.
11. El producto terapéutico según una cualquiera de las reivindicaciones 1ª a 10ª, en el que dichas células inmunoaisladas son no tumorales.
12. Una composición farmacéutica que comprende un producto terapéutico según una cualquiera de las reivindicaciones 1ª a 11ª y un vehículo aceptable fisiológicamente para su uso en la terapia del cáncer de dicho paciente.
13. Un kit que comprende un producto terapéutico según una cualquiera de las reivindicaciones 1ª a 11ª, para su uso en la terapia del cáncer de dicho paciente.
14. Un producto terapéutico según una cualquiera de las reivindicaciones 1ª a 11ª, en el que, en la terapia del cáncer, la macrocápsula recuperable es retirada de cinco a siete días después de la implantación.
Patentes similares o relacionadas:
Composición de vacuna que contiene un adyuvante sintético, del 22 de Julio de 2020, de INFECTIOUS DISEASE RESEARCH INSTITUTE: Una composición farmacéutica que comprende: un adyuvante lípido de glucopiranosilo (GLA), que tiene la fórmula: **(Ver fórmula)** en la que: […]
Métodos mejorados para la preparación de escualeno, del 15 de Julio de 2020, de NOVARTIS AG: Un procedimiento para la preparación de escualeno a partir de una composición que comprende escualeno a partir de una fuente animal, dicho procedimiento comprendiendo […]
Respuesta inmune mejorada en especies aviares, del 1 de Julio de 2020, de Bayer Intellectual Property GmbH: Una composición de inmunomodulador, en que la composición del inmunomodulador comprende: a. un vehículo catiónico de administración de liposomas; y […]
Composición farmacéutica que comprende un complejo de carga portador polimérico y al menos un antígeno proteínico o peptídico, del 1 de Julio de 2020, de CureVac AG: Composición farmacéutica que incluye: (A) un complejo de carga portador polimérico, que comprende: a) un portador polimérico que comprende componentes catiónicos reticulados […]
Formulaciones de inulina y de acetato de inulina, del 5 de Junio de 2020, de SOUTH DAKOTA STATE UNIVERSITY (100.0%): Una composición que comprende micropartículas o nanopartículas de acetato de inulina (InAc) y una molécula de carga, en la que la molécula de carga está encapsulada […]
Métodos para proporcionar virosomas con adyuvante y virosomas con adyuvante obtenibles de esta manera, del 3 de Junio de 2020, de BESTEWIL HOLDING B.V: Un método para preparar los virosomas con adyuvante, que comprende las etapas de: (i) proporcionar una composición acuosa de los virosomas sin adyuvante que comprende […]
Inmunomodulación mediante inhibidores de IAP, del 6 de Mayo de 2020, de NOVARTIS AG: Una vacuna que comprende una cantidad inmunogénica de un antígeno procedente de tumor o antígeno tumoral y un adyuvante que comprende un inhibidor de IAP […]
Composición de medio para preparar toxina botulínica, del 6 de Mayo de 2020, de Daewoong Co., Ltd: Una composición de medio libre de EET para su uso en el cultivo de Clostridium botulinum, la composición de medio comprende: peptonas de origen […]