VACUNA PARA EL TRATAMIENTO DE LA CELIAQUÍA Y MÉTODO PARA LA PRODUCCIÓN DE LA VACUNA, USO DE UNA SECUENCIA PEPTÍDICA CONJUGADA CON UNA TOXINA BACTERIANA PARA LA ACTIVACIÓN DEL SISTEMA INMUNE CONTRA PROLAMINAS ASÍ COMO PÉPTIDO DE DISEÑO.
Vacuna para la aplicación en el tratamiento de celiaquía, que contiene como componente eficaz al menos una secuencia peptídica tóxica no ramificada conjugada con una parte de una toxina bacteriana de una gliadina,
siendo la secuencia peptídica tóxica no ramificada Pro Gly Glu Glu Glu Pro Phe Pro Pro Glu Glu Pro Tyr Pro Glu Pro Glu Pro Phe Pro de la α-gliadina y siendo la toxina bacteriana el pentámero B de la toxina del cólera
Tipo: Patente Europea. Resumen de patente/invención. Número de Solicitud: E08016498.
Solicitante: Zimmer, Klaus-Peter, Prof.Dr.med.
Nacionalidad solicitante: Alemania.
Dirección: Löberstrasse 12 35390 Giessen.
Inventor/es: Zimmer,Klaus-Peter,Prof.Dr.med.
Fecha de Publicación: .
Fecha Solicitud PCT: 18 de Septiembre de 2008.
Clasificación Internacional de Patentes:
- A61K38/16B
- A61K38/16C
- A61K39/00D4
Clasificación PCT:
- A61K38/04 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 38/00 Preparaciones medicinales que contienen péptidos (péptidos que contienen ciclos beta-lactama A61K 31/00; dipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina 2,5-dionas, A61K 31/00; péptidos basados en la ergolina A61K 31/48; que contienen compuestos macromoleculares que tienen unidades aminoácido repartidas estadísticamente A61K 31/74; preparaciones medicinales que contienen antígenos o anticuerpos A61K 39/00; preparaciones medicinales caracterizadas por los ingredientes no activos, p. ej. péptidos como soportes de fármacos, A61K 47/00). › Péptidos que tienen hasta 20 aminoácidos en una secuencia totalmente determinada; Sus derivados (gastrinas A61K 38/16, somatostatinas A61K 38/31, melanotropinas A61K 38/34).
- A61K39/35 A61K […] › A61K 39/00 Preparaciones medicinales que contienen antígenos o anticuerpos (materiales para ensayos inmunológicos G01N 33/53). › Alergenos.
- C07K14/415 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 14/00 Péptidos con más de 20 aminoácidos; Gastrinas; Somatostatinas; Melanotropinas; Sus derivados. › de vegetales.
- C07K7/08 C07K […] › C07K 7/00 Péptidos con 5 a 20 aminoácidos en una secuencia totalmente determinada; Sus derivados. › con 12 a 20 aminoácidos.
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Eslovenia, Finlandia, Rumania, Chipre, Lituania, Letonia, Ex República Yugoslava de Macedonia, Albania.
PDF original: ES-2358179_T3.pdf
Fragmento de la descripción:
La invención se refiere a una vacuna de acuerdo con la reivindicación 1 y a un método para la producción de esta vacuna para el tratamiento de la celiaquía de acuerdo con la reivindicación 4 y al uso de acuerdo con la reivindicación 6. Por lo demás, la presente invención se refiere a un péptido de diseño, compuesto de la secuenciade aminoácidos Pro Gly Glu Glu Glu Pro Phe Pro Pro Glu Glu Pro Tyr Pro: Glu Pro Glu Pro Phe Pro de la -gliadina, que está conjugada con el pentámero B de la toxina del cólera.
La celiaquía es una enfermedad autoinmune crónica de la mucosa del intestino delgado, que aparece en individuos genéticamente predispuestos (HLA-DQ2/DQ8) debido a una autodestrucción mediada inmunológicamente de enterocitos con hipersensibilidad a la proteína gluten, que también se conoce como proteína del gluten. Laenfermedad, es decir, la hipersensibilidad al gluten sigue existiendo a lo largo de toda la vida y en parte estádeterminada genéticamente y actualmente no se puede tratar. Solamente se puede recomendar actualmente unadieta sin gluten de por vida como la única posibilidad asegurada para el tratamiento de la celiaquía, por la que vuelve a curarse el intestino y también disminuyen los riesgos de las consecuencias a largo plazo, tales como, por ejemplo,en el peor de los casos, la aparición de un linfoma no Hodgkin o de cáncer de intestino. Sin embargo, también lossíntomas que se presentan después de la inflamación y destrucción prolongada de las células epiteliales intestinales, tales como pérdida de peso, diarrea, vómitos, pérdida de apetito y carencia vitamínica conducen por unlado a una alteración del desarrollo en la edad infantil y por otro lado tienen como consecuencia que la calidad de vida de los pacientes sensibles al gluten está extremadamente disminuida. Por tanto, actualmente, tal como ya se hadescrito anteriormente, sólo una dieta sin gluten puede conducir a que los pacientes afectados queden libres desíntomas. A este respecto es problemático que el gluten aparece en muchas variedades de cereales, tales comotrigo, cebada, centeno y avena, al igual que en sus especies ancestrales botánicamente relacionadas espelta,escanda secada en verde, trigo kamut, escaña cultivada y farro, utilizándose particularmente las variedades de cereales habituales de forma aumentada en la industria alimentaria. Por tanto, se tiene que tener en cuenta de formaextrema cómo están compuestos determinados alimentos, ya que incluso pequeñas cantidades de gluten desencadenan el proceso inmunológico de la autodestrucción de los enterocitos en individuos sensibles al gluten. Yaque la prevalencia, es decir, la frecuencia de los casos sintomáticos en el promedio mundial se encuentra enaproximadamente 1:270 individuos, la industria alimentaria se ha adaptado entre tanto al grupo de los pacientes que padecen celiaquía, de tal forma que entre tanto existen productos alimentarios sin gluten y también etiquetadoscomo tales en el mercado. Sin embargo, estos productos están disponibles solamente como surtido limitado y pueden sólo contribuir a que los pacientes hipersensibles al gluten vivan libres de síntomas, sin embargo,actualmente mediante estas medidas no se puede conseguir una curación.
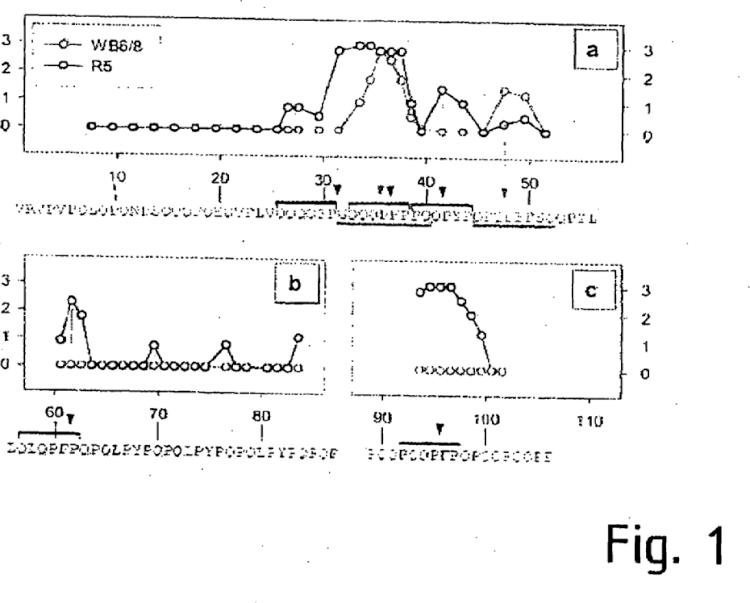
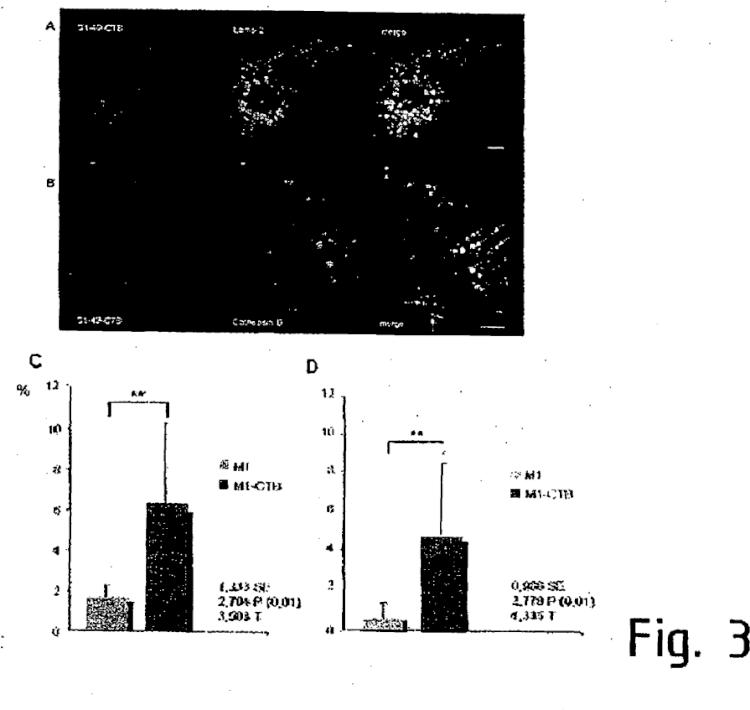
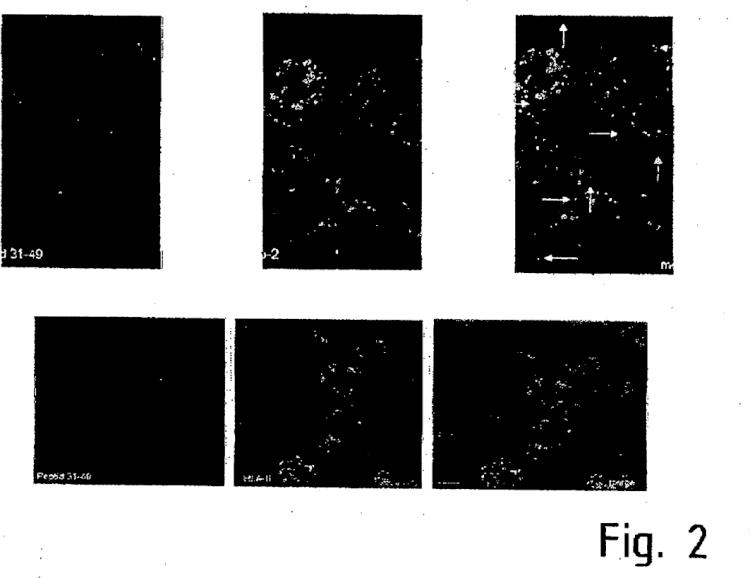
La causa de la hipersensibilidad al gluten son secuencias peptídicas tóxicas, es decir, secciones del gluten que pertenecen a la fracción soluble en alcohol (prolaminas) y que se denominan gliadina, que está compuesta de una secuencia de aminoácidos que presenta una gran cantidad de prolina y glutamina. Particularmente el alto contenidode prolina hace que estos péptidos del gluten o gliadina sean resistentes a la degradación habitual en la digestión,ya que estos péptidos debido a sus restos de prolina sólo se pueden degradar insuficientemente mediante lasenzimas digestivas habituales. Esto conduce en individuos predispuestos correspondientemente con una hipersensibilidad al gluten a la inflamación que se ha indicado anteriormente de la mucosa intestinal, que se debe auna reacción patógena compleja del sistema inmune. Debido a la hidrólisis incompleta de las proteínas ricas enprolina y glutamina se forman epítopos antigénicos que se transportan mediante transcitosis inespecífica desde ellumen intestinal a la mucosa situada por debajo del epitelio intestinal. Determinadas secciones tóxicas, por ejemplo,las secuencias de aminoácidos 31-49 y 57-72 de la -gliadina, se unen a glucoproteínas ancladas en la membrana celular de los enterocitos, que pertenecen a las inmunoglobulinas y que se denominan complejos mayores dehistocompatibilidad (HLA). Esta unión se sigue reforzando debido a que a partir del aminoácido presente en lasecuencia peptídica glutamina se forma por mediación de la enzima transglutaminasa tisular ácido glutámico, por lo que el péptido de gliadina-gluten tóxico se ajusta al bolsillo configurado por el complejo mayor de histocompatibilidad. Esto desencadena una producción aumentada de semioquímicos que desencadenan inflamación, tales como interferón-, TNF-, interleucina-6 e interleucina-2, que terminan en la apoptosis de losenterocitos, es decir, la muerte del tejido, por ejemplo, tiene como consecuencia una atrofia de las vellosidades.Actualmente todavía no se comprende por qué se produce esta producción aumentada de semioquímicos quedesencadenan la inflamación. Normalmente, los antígenos de bacterias o del alimento conducen a una inflamaciónfisiológica controlada que termina finalmente en una tolerancia al antígeno. Sin embargo, los procesos inflamatorios que se presentan en la celiaquía se desarrollan de forma incontrolada, lo que, como ya se ha mencionado anteriormente, finalmente no está comprendido.
Las investigaciones para el tratamiento de la celiaquía se concentran actualmente en la función principalpresentadora de antígenos de las células dendríticas positivas a DQ2/DQ8 de la lámina propia, mientras que a losprocesos que desencadenan inflamación que se desarrollan en los enterocitos no se les otorga mayor importancia para el desarrollo de productos terapéuticos contra la celiaquía, por no hablar de la consideración del desarrollo de una vacuna contra la celiaquía.
El documento WO 99/54452 A1 describe métodos y sustancias para la prevención y tratamiento de una enfermedadautoinmune, proporcionándose una proteína de fusión de la subunidad B de la toxina del cólera no tóxica y unautoantígeno.
Senger S. et al. describen la identificación de un epítopo inmunodominante de -gliadina en ratones transgénicosHLA-DQ8 después de la inmunización oral (J. Immunol. 2005, páginas 8087 a 8095).
Por tanto, es objetivo de la presente invención proporcionar una vacuna contra la celiaquía y un método para la producción de dicha vacuna, que con administración a individuos positivos a DQ2/DQ8 predispuestos genéticamente
Un objetivo adicional de la presente invención es el uso de un antígeno que después de la administración apacientes que están enfermos de celiaquía o que poseen la predisposición a lo mismo provoque una respuestainmune controlada, de tal forma que los pacientes desarrollan una tolerancia a prolaminas, particularmente a gluten Finalmente es objetivo de la presente invención proporcionar una sustancia que se pueda utilizar para el tratamientode celiaquía. De acuerdo con la invención, el anterior objetivo se resuelve mediante una vacuna para la aplicación en el tratamiento de celiaquía con las características de la reivindicación 1. Por lo demás, el anterior objetivo se resuelve en vista a la producción de una vacuna contra la celiaquía por mediode un método con las características de la reivindicación 4. El objetivo adicional, concretamente el uso de un antígeno que después de la administración a pacientes que estánenfermos de celiaquía o que están predispuestos hereditariamente a ello provoque una respuesta inmune controlada, se resuelve mediante el uso de acuerdo con la reivindicación 6. Finalmente el objetivo, concretamente proporcionar una sustancia que se pueda utilizar para el tratamiento de laceliaquía, se resuelve mediante un péptido de diseño con las características de la reivindicación 7. De forma adecuada se ha observado que, a diferencia del proceder... [Seguir leyendo]o a individuos sensibles al gluten posibilite reprimir las inflamaciones que se producen con la ingesta de gluten de lamucosa o captar las secuencias peptídicas (antígenos) tóxicas inmunológicamente, es decir, ajustar el sistemainmune de los pacientes celiacos a los antígenos (secuencias peptídicas tóxicas).
Reivindicaciones:
1. Vacuna para la aplicación en el tratamiento de celiaquía, que contiene como componente eficaz al menosuna secuencia peptídica tóxica no ramificada conjugada con una parte de una toxina bacteriana de una gliadina,siendo la secuencia peptídica tóxica no ramificada Pro Gly Glu Glu Glu Pro Phe Pro Pro Glu Glu Pro Tyr Pro Glu ProGlu Pro Phe Pro de la -gliadina y siendo la toxina bacteriana el pentámero B de la toxina del cólera.
3. Vacuna para el tratamiento de la celiaquía de acuerdo con una de las reivindicaciones 1 a 2, caracterizada por que el tratamiento es una vacunación activa. 5. Método para la producción de una vacuna para el tratamiento de celiaquía de acuerdo con la reivindicación 4, caracterizado por que una subunidad de la toxina bacteriana, que presenta un efecto tolerogénico de antígenos sin la fracción tóxica de la toxina bacteriana se conjuga con la secuencia peptídica. 6. Uso al menos de la secuencia peptídica tóxica no ramificada Pro Gly Glu Glu Glu Pro Phe Pro Pro Glu GluPro Tyr Pro Glu Pro Glu Pro Phe Pro conjugada con el pentámero B de la toxina del cólera para la producción deuna vacuna para la activación específica del sistema inmune contra prolaminas. 7. Péptido de diseño que está compuesto de la secuencia de aminoácidos Pro Gly Glu Glu Glu Pro Phe Pro Pro Glu Glu Pro Tyr Pro Glu Pro Glu Pro Phe Pro de la -gliadina, que está conjugada con el pentámero B de la toxina del cólera. 8. Péptido de diseño de acuerdo con la reivindicación 7 para la producción de un producto terapéutico ovacuna que se puede utilizar para el tratamiento de la celiaquía. 5 2. Vacuna para el tratamiento de la celiaquía de acuerdo con la reivindicación 1, caracterizada por que la toxina bacteriana sirve como adyuvante para la presentación de antígenos de la secuencia peptídica tóxica en losendosomas tardíos de los enterocitos del epitelio intestinal.
10 4. Método para la producción de una vacuna para el tratamiento de la celiaquía de acuerdo con las reivindicaciones 1 a 3, caracterizado por que la secuencia peptídica tóxica no ramificada Pro Gly Glu Glu Pro PhePro Pro Glu Glu Pro Tyr Pro Glu Pro Glu Pro Phe Pro se asocia con al menos una parte de una toxina bacteriana, siendo la toxina bacteriana el pentámero B de la toxina del cólera.
Patentes similares o relacionadas:
 USO DE INHIBIDORES DE LA TRANSACTIVACIÓN DE EGFR EN CÁNCER HUMANO, del 18 de Mayo de 2011, de MAX-PLANCK-GESELLSCHAFT ZUR FORDERUNG DER WISSENSCHAFTEN E.V.: Uso de un compuesto que es capaz de inhibir la activación de un receptor del factor de crecimiento de la familia EGFR para la fabricación de un agente para […]
USO DE INHIBIDORES DE LA TRANSACTIVACIÓN DE EGFR EN CÁNCER HUMANO, del 18 de Mayo de 2011, de MAX-PLANCK-GESELLSCHAFT ZUR FORDERUNG DER WISSENSCHAFTEN E.V.: Uso de un compuesto que es capaz de inhibir la activación de un receptor del factor de crecimiento de la familia EGFR para la fabricación de un agente para […]
INMUNOTOXINAS ANTI-CD64-ETA¿RECOMBINANTES, del 4 de Mayo de 2011, de FRAUNHOFER-GESELLSCHAFT ZUR FORDERUNG DER ANGEWANDTEN FORSCHUNG E.V.: Un complejo recombinante que tiene al menos un componente A, al menos un componente B, comprendiendo el componente A dos o más dominios de unión para el receptor […]
TOXINA DE ADENILATO CICLASA RECOMBINANTE DE BORDETELLA QUE INDUCE LAS RESPUESTAS DE LA CELULA T CONTRA LOS ANTIGENOS TUMORALES, del 28 de Abril de 2010, de INSTITUT PASTEUR I.N.S.E.R.M. INSTITUT NATIONAL DE LA SANTE ET DE LA RECHERCHE MEDICALE LUDWIG INSTITUTE FOR CANCER RESEARCH CENTRE NATIONAL DE LA RECHERCHE SCIENTIFIQUE: Una composición inmunogénica que comprende una proteína recombinante, en donde la proteína recombinante comprende una CyaA de Bordetella o un fragmento de esta, y un péptido […]
 EMPLEO DE UN POLIPEPTIDO QUE COMPRENDE EL DOMINIO C-TERMINAL DE LA CADENA PESADA DE LA TOXINA TETANICA EN EL TRATAMIENTO DEL PARKINSONISMO, del 16 de Octubre de 2008, de UNIVERSIDAD AUTONOMA DE BARCELONA: Se describe el uso de un polipéptido que comprende el dominio C-terminal de la cadena pesada de la toxina tetánica, o un fragmento funcional del mismo, o una […]
EMPLEO DE UN POLIPEPTIDO QUE COMPRENDE EL DOMINIO C-TERMINAL DE LA CADENA PESADA DE LA TOXINA TETANICA EN EL TRATAMIENTO DEL PARKINSONISMO, del 16 de Octubre de 2008, de UNIVERSIDAD AUTONOMA DE BARCELONA: Se describe el uso de un polipéptido que comprende el dominio C-terminal de la cadena pesada de la toxina tetánica, o un fragmento funcional del mismo, o una […]
OBTENCIÓN DE CÉLULAS TR1 ESPECÍFICAS DE ANTÍGENOS DE LOS ALIMENTOS O DE AUTOANTÍGENOS A PARTIR DE UNA POBLACIÓN DE LEUCOCITOS O PBMC, del 14 de Noviembre de 2011, de TXCELL S.A. INSTITUT NATIONAL DE LA SANTÉ ET DE LA RECHERCHE MÉDICALE (INSERM): Un método in vitro para la obtención de una población de células Tr1 específicas de antígenos de alimentos o autoantígenos proveniente de una población de leucocitos o de […]
USO DE VEGF MUTADO PARA LA TERAPIA ANTIANGIOGENICA, del 29 de Septiembre de 2011, de CENTRO DE INGENIERIA GENETICA Y BIOTECNOLOGIA (CIGB): Aplicacion de secuencias oligonucleotídicas y polipeptídicas de moléculas pertenecientes a la familia del factor de permeabilidad vascular (VPF), sus receptores […]
COMPOSICIÓN FARMACÉUTICA O ALIMENTARIA PARA EL TRATAMIENTO DE PATOLOGÍAS ASOCIADAS A UN RECHAZO DE INJERTO, del 21 de Marzo de 2011, de BIOTECH TOOLS S.A: Composición farmacéutica y/o alimentaria que contiene con un vehículo farmacéutico y/o alimentario adecuado, una proteína de estrés y al menos un epítopo conformacional […]
COMPOSICIONES Y METODOS PARA PREVENIR Y TRATAR TRASTORNOS INFLAMATORIOS DE MEDIACION INMUNE, del 10 de Diciembre de 2010, de LOMA LINDA UNIVERSITY: Una composición para prevenir, retardar la aparición de o tratar diabetes en un organismo que es susceptible de desarrollar diabetes, que está […]