USO DE PEPTIDOS DERIVADOS DE LA CADENA B BETA DE FIBRINOGENO HUMANO PARA EL TRATAMIENTO DEL CHOQUE.
Uso de un péptido con la fórmula general II ** ver fórmula** en donde R 1 y R 2,
iguales o diferentes, representan hidrógeno, un grupo hidrocarburo saturado o insaturado de 1 a 10, especialmente de 1 a 3 átomos de carbono, Z1 representa un residuo de histidina, Arg representa un residuo de arginina, Z3 representa un residuo de prolina o valina, Z 4 representa un residuo de leucina o valina, Z5 es un residuo peptídico derivado de la cadena Bbeta de la fibrina, péptido que posee la propiedad biológica de ajustarse al motivo de unión de la VE-cadherina inducible en la cadena BBeta (es decir, BBeta 15-42) de la fibrina humana, para la producción de un composición farmacéutica para el tratamiento de choque
Tipo: Resumen de patente/invención. Número de Solicitud: W05000228AT.
Solicitante: FIBREX MEDICAL RESEARCH & DEVELOPMENT GMBH.
Nacionalidad solicitante: Austria.
Dirección: RABENSTEIG 8/3A,1010 WIEN.
Inventor/es: PETZELBAUER, PETER, ZACHAROWSKI,KAI.
Fecha de Publicación: .
Fecha Concesión Europea: 19 de Agosto de 2009.
Clasificación Internacional de Patentes:
- A61K38/36A
Clasificación PCT:
- A61K38/36 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 38/00 Preparaciones medicinales que contienen péptidos (péptidos que contienen ciclos beta-lactama A61K 31/00; dipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina 2,5-dionas, A61K 31/00; péptidos basados en la ergolina A61K 31/48; que contienen compuestos macromoleculares que tienen unidades aminoácido repartidas estadísticamente A61K 31/74; preparaciones medicinales que contienen antígenos o anticuerpos A61K 39/00; preparaciones medicinales caracterizadas por los ingredientes no activos, p. ej. péptidos como soportes de fármacos, A61K 47/00). › Factores de coagulación sanguínea o de fibrinolisis.
- A61P7/00 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › Medicamentos para el tratamiento de trastornos de la sangre o del fluido extracelular.
- A61P9/00 A61P […] › Medicamentos para el tratamiento de trastornos en el aparato cardiovascular.
Clasificación antigua:
Fragmento de la descripción:
Uso de péptidos derivados de la cadena Bß de fibrinógeno humano para el tratamiento del choque.
Antecedentes de la invención
La presente invención se refiere a una composición farmacéutica para el tratamiento del choque.
Un choque es una complicación aguda de muchos estados patológicos diferentes, que se caracteriza por la incapacidad del sistema cardiovascular de mantener una presión de perfusión suficiente. Los agentes infecciosos pueden causar de forma directa o indirecta una insuficiencia del sistema cardiovascular. Bacterias, toxinas bacterianas, virus y no en último lugar una reacción celular o humoral insuficiente del huésped, acompañados de inflamación y coagulación, pueden producir una pérdida del tono vascular, una pérdida de la función barrera vascular, una pérdida de la potencia de contracción del miocardio y una pérdida de la función de órganos, lo que solo o en combinación puede producir choque y por último la muerte del paciente. El tratamiento de una infección bacteriana se basa en un tratamiento antibiótico que mata las bacterias, sin embargo no trata la toxemia ni corrige la reacción celular o humoral insuficiente. En las bacterias gram negativas el lipopolisacárido (LPS o endotoxina) es responsable de la activación de un choque gram negativo. Las bacterias gram positivas pueden causar una insuficiencia múltiple de órganos y choque séptico sin endotoxemia, la pared celular de las bacterias gram positivas contiene asimismo toxinas como el ácido lipotecoico (LTA) y peptidoglicano (PepG). LTA y PepG actúan en sinergia para liberar citoquinas, como por ejemplo, el factor de necrosis tumoral (TNF)a e interferón (IFN)?, y para inducir iNOS por último producir choque e insuficiencia de órganos.
La endotoxemia, septicemia y choque séptico están relacionados con la generación de grandes cantidades de óxido nítrico (NO). La vasodilatación excesiva y la hiporreactividad vascular frente a agentes hipertensores, que van acompañados de un choque circulatorio, se pueden anular con inhibidores de la isoforma inducible de NO-sintasa (iNOS) (Southan y Szabo, Biochem Pharmacol. 1996; 51:383-94, Thiemermann Gen Pharmacol 1997; 29:159-66); sin embargo, los inhibidores de la iNOS no reducen el daño en órganos producido por las toxinas (Wray et al. Shock 1998; 9:329-335).
El tratamiento del choque causado por una infección vírica es un reto aún mayor, ya que para la mayoría de las infecciones no hay agentes antivirales disponibles. Los tratamientos que solo pretenden la eliminación del agente infeccioso, no son suficientes para los pacientes con choque debido a un agente infeccioso, puesto que los procesos secundarios producidos por el agente infeccioso, que están acompañados por una reacción de inflamación y cambios en el sistema de coagulación, posiblemente sean independientes y produzcan la muerte del paciente, a pesar de la cuestión de si el agente infeccioso causal se neutraliza o no. No hay un tratamiento específico disponible y por lo tanto los procedimientos actuales tienen como fin aliviar los síntomas, lo que incluye ventilación mecánica, reemplazo de líquidos, el uso de medicamentos cardioactivos, el control riguroso de la saturación de oxígeno, la hemoglobina, la glucosa y la función renal. El control exclusivo de la reacción de inflamación, por ejemplo mediante altas dosis de esteroides, o la inhibición de la coagulación con antitrombina no produce mejora de la tasa de supervivencia. La única molécula que hasta ahora ha mostrado que posee una notable eficacia respecto a la disminución de la mortalidad es la "proteína C activada", que interacciona con la coagulación/fibrinólisis y los procesos de inflamación.
Un choque durante el curso de una infección está relacionado en la mayoría de los casos con cambios aparentes o no aparentes en el fibrinógeno plasmático, acompañado de la formación de fibrina y un aumento de los fragmentos de fibrina. Esta activación de la coagulación y vías fibrinolíticas puede producir una coagulación intravascular diseminada (DIC) evidente o no evidente, que tiene como consecuencia el cierre de los vasos y daño a órganos, y un uso de los factores de coagulación que tiene como consecuencia hemorragias. La causa más frecuente de una DIC es una septicemia. Es importante que fibrinógeno, fibrina y fragmentos de fibrina no solo desempeñan un papel en la coagulación de la sangre, sino que muestran varios sitios de unión para células y proteínas de matriz, lo que facilita su interacción con glóbulos blancos, plaquetas, células endoteliales y estructuras de la matriz. Esto produce activación celular, migración celular, liberación de citoquinas y por último una reacción de inflamación. El papel desempeñado por el fibrinógeno o la fibrina en la inflamación, está ampliamente documentado (tratado por Altieri Thromb Haemost 82:781-786; Herrick et al. Int J Biochem Cell Biol 31:741-46). La región D de la molécula contiene numerosos sitios de unión para moléculas de la matriz, células endoteliales, plaquetas y células inflamatorias. La región E de la fibrina se une a CD11c (Loike et al. Proc Natl Acad Sci USA 88:1044-48).
Recientemente se ha descrito un nuevo papel para la secuencia Bbeta15-42 de la fibrina en la inflamación (WO 02/48180). Esta secuencia también está localizada en la región E de la fibrina y solo se activa cuando se procesa fibrinopéptido. Los fragmentos de fibrina, que contienen esta secuencia en el extremo N-terminal libre de la cadena beta, se unen al endotelio y causan una inflamación, y un péptido que se ajusta a los aminoácidos 15-42 de la cadena Bbeta de la fibrina, bloquea la unión de fragmentos de fibrina a la superficie del endotelio y bloquea la inflamación in vitro (WO 02/48180). In vivo este péptido impide una inflamación del miocardio y disminuye la extensión de un infarto de miocardio en situaciones de isquemia/reperfusión (WO 02/48180).
Los fragmentos de fibrina aparecen en cualquier situación con formación de fibrina dañada y fibrinólisis dañada. Especialmente en situaciones de choque debido a un agente infeccioso esta formación de fibrina alterada y esta fibrinólisis alterada representan un gran problema. En muchas enfermedades se ha documentado una reciprocidad directa entre el resultado y el deterioro de la formación de fibrina/fibrinólisis. Por ejemplo el dengue (van Gorp et al. J Med Virol 2002, 67:549-54, Mairuhu et al. Lancet Inf Dis 2003; 3:33-41). En el documento WO 99/02565 se divulga el uso de un ligando de fibrinógeno y/o fibrina para la producción de un agente para el tratamiento y/o profilaxis de trastornos de microcirculación y/o para la influencia en la reología de un mamífero. El síndrome de dificultad respiratoria en adultos (ARDS) es una forma de lesión pulmonar aguda que se caracteriza mediante un almacenamiento extravascular rojizo de fibrina (Idell Am J Respir Med. 2002; 1:383-91). También se observa trombosis en los vasos pulmonares y coagulación intravascular diseminada en relación con ARDS.
Las razones para la persistencia/aparición mundial de fiebre del dengue (DF) y fiebre hemorrágica del dengue (DHF) como gran problema de la sanidad pública son complejas, las medidas de control de los vectores no tuvieron éxito en eliminar DF/DHF. Actualmente, el punto principal de los medios de financiación en el sector público para la investigación del dengue (en el año 2001 se estimó en 15 millones de dólares) está en la epidemiología molecular, la inmunopatofisiología, la investigación para el descubrimiento de vacunas de segunda generación y en enfoques nuevos o mejorados para el control de los vectores.
La mayoría de las vacunas candidatas se encuentran en los Estados Unidos y en Tailandia en fase experimental clínica, sin embargo en el mercado no hay todavía fármacos para el tratamiento de los pacientes infectados y, lo que es aún peor, actualmente no parece estar en marcha ningún tipo de actividad comercial para la investigación y el desarrollo de una quimioterapia. La Organización Mundial de la Salud publicó directrices estratégicas para la lucha de DF/DHF que, como metas de mayor prioridad, comprenden el desarrollo de agente antivíricos, dirigidos a proteasas u otras enzimas apenas estudiadas; el desarrollo de antimediadores, que se dirigen a las causas de la permeabilidad vascular aumentada o la hemostasia modificada.
Compendio de la invención
La invención se refiere al uso de un péptido con la fórmula general II:

Reivindicaciones:
1. Uso de un péptido con la fórmula general II
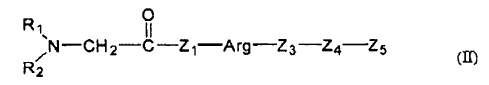
en donde
R1 y R2, iguales o diferentes, representan hidrógeno, un grupo hidrocarburo saturado o insaturado de 1 a 10, especialmente de 1 a 3 átomos de carbono,
Z1 representa un residuo de histidina,
Arg representa un residuo de arginina,
Z3 representa un residuo de prolina o valina,
Z4 representa un residuo de leucina o valina,
Z5 es un residuo peptídico derivado de la cadena Bbeta de la fibrina,
péptido que posee la propiedad biológica de ajustarse al motivo de unión de la VE-cadherina inducible en la cadena Bß (es decir, Bß15-42) de la fibrina humana, para la producción de un composición farmacéutica para el tratamiento de choque.
2. Uso según la reivindicación 1, en donde el grupo hidrocarburo saturado o insaturado en el significado de R1 y R2 comprende de 1 a 3 átomos de carbono.
3. Uso según cualquiera de las reivindicaciones 1 ó 2, caracterizado en que Z5 es un residuo peptídico con la secuencia de aminoácidos

Z1 es un residuo de histidina,
Arg es un residuo de arginina,
Z3 es un residuo de prolina y
Z4 es un residuo de leucina.
4. Uso de un péptido que muestra la secuencia N-terminal

péptido que tiene la propiedad biológica de ajustarse al motivo de unión de VE-cadherina inducible en la cadena Bß (es decir, Bß15-42) de la fibrina humana, para la producción de una composición farmacéutica para el tratamiento de choque.
5. Uso según la reivindicación 4, caracterizado en que el péptido es
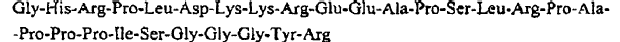
6. Uso según cualquiera de las reivindicaciones 1 a 5, en donde el choque está relacionado con uno o más del grupo que comprende toxinas bacterianas, coagulapatía intravascular diseminada, fascitis necrotizante, choque hemorrágico debido a infección vírica, en particular producida por filovirus, Arenaviridae, Bunyaviridae, flavivirus, dengue, insuficiencia respiratoria hemorrágica aguda, causada por agentes infecciosos o enfermedades autoinmunes, insuficiencia de órganos después de una lesión de órganos, en particular por infarto de miocardio, una operación vascular, un pinzamiento de órganos, un choque hemorrágico, infarto pulmonar, infarto hepático, infarto intestinal, intervenciones quirúrgicas, apoplejía, y el mal funcionamiento de órganos en órganos trasplantados.
Patentes similares o relacionadas:
COMPOSICIÓN PARA LA CREACIÓN, REGENERACIÓN Y REPARACIÓN TISULAR MEDIANTE UN IMPLANTE BIOLÓGICO QUE PORTA CÉLULAS ENRIQUECIDO CON CONCENTRADO DE PLAQUETAS Y COMPLEMENTOS, del 12 de Diciembre de 2011, de GORROCHATEGUI BARRUETA, ALBERTO: La composición incorpora, junto al concentrado de plaquetas que aporta fibrinógeno y concentraciones de factores de crecimiento plaquetarios (PDGFs), otras concentraciones […]
COMPOSICIONES DE OSTEOBLASTOS DE FIBRINA MEZCLADA SEMI-SOLIDIFICADA PARA AGLUTINACIÓN DE FRACTURA ÓSEA Y SU PROCEDIMIENTO DE FABRICACIÓN, del 5 de Julio de 2011, de SEWON CELLONTECH CO., LTD: Una composición de osteoblastos semisólida que contiene fibrina para curar una fractura ósea en la que la composición se prepara mediante un procedimiento que comprende: […]
PROCEDIMIENTO SENCILLO PARA TRASPLANTAR CONDROCITOS INYECTABLES PARA TRASPLANTE DE CONDROCITOS AUTOLOGOS, del 16 de Junio de 2011, de SEWON CELLONTECH CO., LTD: Una composición terapéutica de cartílago para su uso en un procedimiento para trasplantar un condrocito inyectable para trasplante de condrocitos autólogos, obtenible: […]
 ESTRUCTURA QUE CONTIENE MATERIAL DE TRATAMIENTO DE HERIDAS, del 30 de Marzo de 2010, de TYCO HEALTHCARE GROUP LP: Un conjunto de yunque para un aparato grapador circular , comprendiendo el conjunto de yunque: una cabeza de yunque configurada para […]
ESTRUCTURA QUE CONTIENE MATERIAL DE TRATAMIENTO DE HERIDAS, del 30 de Marzo de 2010, de TYCO HEALTHCARE GROUP LP: Un conjunto de yunque para un aparato grapador circular , comprendiendo el conjunto de yunque: una cabeza de yunque configurada para […]
Usos de composiciones de caseína, del 17 de Junio de 2020, de FONTERRA CO-OPERATIVE GROUP LIMITED: Uso de una composicion de caseina para aumentar la concentracion de leucina libre en suero sanguineo en un sujeto, en donde la composicion de caseina comprende o la caseina […]
Forma D1 cristalina altamente estable de la sal de monoetanolamina de eltrombopag, del 17 de Junio de 2020, de F.I.S. FABBRICA ITALIANA SINTETICI S.P.A: Forma D1 de sal de monoetanolamina de eltrombopag cristalina de Fórmula (I): **(Ver fórmula)** que tiene uno de los siguientes picos característicos […]
Procedimiento de preparación de compuestos de diaminofenotiazinio, del 3 de Junio de 2020, de Provepharm Life Solutions: Procedimiento de preparación de un compuesto que responde a la fórmula (I) siguiente: **(Ver fórmula)** en la que cada uno de R1, R2, R3, R4, R5, R6, […]
Inhibidor de alquinil piridina prolil hidroxilasa, y método de preparación y uso médico del mismo, del 22 de Abril de 2020, de Jiangsu Hengrui Medicine Co., Ltd: Un compuesto de fórmula (I) o una sal farmacéuticamente aceptable del mismo: en la que X representa NH, NCH3 o CH2; Y representa hidrógeno, hidroxi, metoxi o etoxi; […]