USO DE LA QUIMOSINA RECOMBINANTE ACTIVA.
Uso de la quimosina recombinante activa.Uso del cuajo, sin activación previa,
obtenido a partir de una célula hospedadora que contiene un vector de expresión que comprende cualquiera de las secuencias que codifican para las proteínas de búfalo seleccionadas del grupo: preproquimosina, proquimosina o quimosina, para la coagulación de la leche
Tipo: Patente de Invención. Resumen de patente/invención. Número de Solicitud: P200702111.
Solicitante: UNIVERSIDAD DE SANTIAGO DE COMPOSTELA.
Nacionalidad solicitante: España.
Provincia: A CORUÑA.
Inventor/es: GONZALEZ VILLA,TOMAS, AGEITOS MARTINEZ,JOSE MANUEL, VALLEJO VIDAL,JUAN ANDRES, POZA DOMINGUEZ,MARGARITA.
Fecha de Solicitud: 27 de Julio de 2007.
Fecha de Publicación: .
Fecha de Concesión: 28 de Abril de 2011.
Clasificación Internacional de Patentes:
- C12N15/67 QUIMICA; METALURGIA. › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 15/00 Técnicas de mutación o de ingeniería genética; ADN o ARN relacionado con la ingeniería genética, vectores, p. ej. plásmidos, o su aislamiento, su preparación o su purificación; Utilización de huéspedes para ello (mutantes o microorganismos modificados por ingeniería genética C12N 1/00, C12N 5/00, C12N 7/00; nuevas plantas en sí A01H; reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00; nuevas razas animales en sí A01K 67/00; utilización de preparaciones medicinales que contienen material genético que es introducido en células del cuerpo humano para tratar enfermedades genéticas, terapia génica A61K 48/00; péptidos en general C07K). › Métodos generales para favorecer la expresión.
- C12N15/81A
Clasificación PCT:
- C12N9/64 C12N […] › C12N 9/00 Enzimas, p. ej. ligasas (6.); Proenzimas; Composiciones que las contienen (preparaciones para la limpieza de los dientes que contienen enzimas A61K 8/66, A61Q 11/00; preparaciones de uso médico que contienen enzimas A61K 38/43; composiciones detergentes que contienen enzimas C11D ); Procesos para preparar, activar, inhibir, separar o purificar enzimas. › que provienen de tejido animal, p. ej. renina.
PDF original: ES-2336171_B1.pdf


Fragmento de la descripción:
Uso de la quimosina recombinante activa.
La presente invención se refiere al uso de quimosina recombinante de búfalo para la elaboración de queso. Esta quimosina se produce en su forma activa por ser directamente secretada por el microorganismo hospedador, sin necesidad de un proceso de activación auto-catalítico intermedio mediado por pH.
Estado de la técnica anterior
Los cuajos empleados en la industria quesera están compuestos básicamente por proteasas aspárticas (cfr. Ustunol & Hicks., 1990, Journal of Dairy Science, vol. 73(1), pp. 8-16). Las proteasas aspárticas poseen dos residuos de ácido aspártico esenciales para su funcionamiento; Asp32 y Asp215. Esta característica, junto con su conformación tridimensional bilobulada, donde el centro activo, rico en ácido aspártico, se sitúa entre ambos lóbulos, les confiere la capacidad de actuar sobre el enlace peptídico Phe105-Met106 existente en la κ-caseína de la leche, originando para-κ-caseína insoluble (cfr. McMahon et al., 1984, Journal of Dairy Science, vol. 67(5), pp. 919-29). Esto conduce a la coagulación de la leche, lo que explica que estas proteasas se hayan estado empleando para la elaboración tradicional de masas queseras como paso previo a la fabricación de distintos tipos de quesos.
La quimosina es la proteasa aspártica más valorada en la industria quesera como fuente de cuajo por su eficiencia a la hora de elaborar masas queseras (cfr. Rao et al., 1998, Microbiology and Molecular Biology Reviews, vol. 62(3), pp. 597-635). Otras proteasas aspárticas empleadas en la industria quesera originan digestiones inespecíficas de las caseínas de la leche y pueden dar lugar a productos que dan sabor amargo a las masas queseras y a pérdidas del contenido proteico durante el desuerado, lo cual provoca una disminución importante del rendimiento en el proceso de elaboración de queso (cfr. Beppu., 1983, Trends in Biotechnology, vol. 1(3), pp. 85-9).
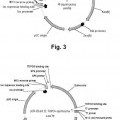
La quimosina se sintetiza in vivo en forma de preproquimosina que contiene un péptido señal de 16 aminoácidos, que es eliminado para originar proquimosina. La proquimosina, a su vez, es procesada a quimosina activa al ser sometida a las condiciones de pH ácido existentes en el estómago que ocasionan la eliminación de un propéptido de 42 aminoácidos ubicado en el extremo aminoterminal (cfr. V B Pedersen et al., 1979, European Journal of Biochemistry, vol. 94(2), pp. 573-80).
En la actualidad existen cuatro fuentes de producción de cuajo de distinto origen para la industria quesera: las animales, las vegetales, las microbianas y las recombinantes. El cuajo de origen animal (quimosina) se ha estado obteniendo tradicionalmente a partir del prensado directo de cuajares de terneros lechales. Este cuajo de origen animal es incapaz de cubrir la demanda actual del mercado. Y, además, con su uso existe el riesgo de aparición de impurezas debido al método de extracción, y también un riesgo de incorporación agentes infecciosos (por ej. Creutzfeld-Jacob).
Por su parte, los cuajos de origen vegetal se han estado obteniendo a partir de infusiones de flores tales como Cynara cardunculus (cfr. Cordeiro et al., 1994, Plant Molecular Biology, vol. 24(5), pp. 733-41) o Gallum verum. Estos cuajos son incapaces de competir industrialmente por lo que se han quedado relegados a la obtención de quesos tradicionales y su uso ha sido reducido a áreas geográficas determinadas.
Los cuajos microbianos se obtienen fundamentalmente a partir de los sobrenadantes de cultivos de microorganismos como Endothia (cfr. Droehse, Helle B et al., Biochimica et Biophysica Acta, Protein Structure and Molecular Enzymology, vol. 995(3), pp 221-4) o Rhizomucor (cfr. Sternberg, 1972, Biochimica et Biophysica Acta. Protein Structure. vol. 285(2), pp. 383-92). Estos cuajos contienen proteasas poco específicas que provocan sabores amargos y una disminución en el rendimiento durante el proceso de elaboración de masas queseras.
Por último, los cuajos recombinantes comercializados se han obtenido, hasta el momento, a partir de microorganismos recombinantes que contienen el gen de la quimosina de Bos taurus (cfr. Emtage et al., 1983, Proceedings of the National Academy of Sciences of the United States of America, vol. 80(12), pp. 3671-5; Mellor et al., 1983, Gene, vol. 24(1), pp 1-14; Cullen et al., 1987, Bio/Technology. vol 5(4), pp. 369-76). Esta quimosina recombinante se comporta de la misma manera que la obtenida a partir del prensado directo de cuajares con la ventaja de que su uso evita ahora la aparición de impurezas o de agentes infecciosos.
Este tipo de quimosinas recombinantes deben ser activadas mediante un proceso de autocatálisis mediado por una simulación del pH ácido del estómago del animal. Solo entonces podrían ser empleadas para la elaboración de queso (cfr. V B Pedersen et al., 1979, European journal of biochemistry. vol. 94(2), pp. 573-80).
Explicación de la invención
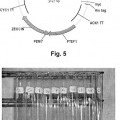
La presente invención se refiere a la obtención de quimosina de búfalo recombinante activa capaz de coagular leche de distinta procedencia para elaborar masas queseras. Esta quimosina de búfalo, una vez clonada en la levadura Pichia pastoris, es secretada por dicho microorganismo al medio extracelular y en su forma activa. Es decir, sin necesidad de ser activada posteriormente mediante simulación del pH de estómago, lo cual supone una optimización en el procedimiento de elaboración de quesos, con un ahorro de tiempo y dinero a la hora de obtener el producto, aumentando considerablemente el rendimiento en su producción.
Por lo tanto, el uso de esta quimosina recombinante de búfalo, que no es sometida al proceso de activación por pH, supone una ventaja adicional frente al estado de la técnica, al evitar un proceso intermedio de activación para la elaboración de masas queseras.
La quimosina de búfalo muestra características fisicoquímicas más estables que la de Bos taurus (cfr. Mohanty et al; 2003, Journal of Dairy Research, vol. 70(1), pp 37-43; Shindo & Arima; 1979, Rakuno Kagaku, Shokuhin no Kenkyu, vol. 28(5), A177-A182) y se ha comprobado que en la elaboración de masas queseras empleando leche de búfala se obtiene un mejor rendimiento si se emplea quimosina de búfalo. Esto resulta interesante para la producción de quesos y, en particular, de queso mozarella, queso característico originado a partir de leche de búfala.
Otro factor a tener en cuenta es que en la secuencia del gen de la quimosina de Bos taurus existe una diana de EcoRI que no existe en la secuencia de Bubalus arnee bubalis. Esta diferencia puede utilizarse para, por ejemplo, diferenciar una cepa recombinante productora de quimosina de Bos taurus de otra productora de quimosina de Bubalus arnee bubalis.
Así, un aspecto de la presente invención se refiere al uso del cuajo obtenido directamente a partir de una célula hospedadora en la cual se ha clonado un gen en un vector de expresión, para la coagulación de la leche. En este vector se han clonado las tres formas del gen, que codifican para las proteínas de búfalo seleccionadas de las secuencias de la preproquimosina, la proquimosina y la quimosina. El cuajo así obtenido no requiere una activación previa para llevar a cabo la coagulación de la leche.
Por "leche" entendemos, en la presente invención, el producto obtenido a partir de las hembras de los mamíferos, en particular de los mamíferos domésticos como la vaca, cabra, oveja, yegua, camella, dromedaria, búfala, etc.....La coagulación se puede lleva a cabo en los tipos de leche aquí descritos o en cualquiera de sus mezclas.
Entendemos por "cuajo" al producto obtenido por la extracción de los cuajares de rumiantes, en la presente invención de cuajo de búfalo, que sirve para coagular la leche. Este cuajo es el sobrenadante obtenido al clonar la quimosina de búfalo en un microorganismo y secretado al medio extracelular, y comprende un enzima, quimosina recombinante activa de búfalo.
El término "quimosina recombinante activa" significa en esta descripción quimosina recombinante secretada por el organismo hospedador directamente en su forma activa, es decir, sin necesidad de llevar a cabo un proceso intermedio auto-catalítico, mediado por el pH, antes de su uso en la elaboración de queso.... [Seguir leyendo]
Reivindicaciones:
1. Uso del cuajo obtenido a partir de una célula hospedadora que contiene un vector de expresión que comprende cualquiera de las secuencias que codifican para las proteínas de búfalo seleccionadas del grupo:
para la coagulación de la leche, donde dicho cuajo no requiere una activación previa.
2. Uso del cuajo según la reivindicación 1, donde el organismo hospedador es Pichia Pastoris.
3. Uso del cuajo según cualquiera de las reivindicaciones 1 a 2, para la elaboración de queso.
4. Uso del cuajo según la reivindicación 3, para la elaboración de queso mozarella.
Patentes similares o relacionadas:
Expresión de proteína biotecnológica mejorada que usa un activador CHEF1 híbrido, del 17 de Junio de 2020, de AGC Biologics, Inc: Un vector de expresión que comprende ADN regulador de la transcripción del factor 1α de elongación de hámster chino (CHEF1) 5' y un activador de citomegalovirus (CMV) que […]
Ácido nucleico que comprende o codifica para un tallo-bucle de histona y una secuencia poli(A) o una señal de poliadenilación para aumentar la expresión de un antígeno patogénico codificado, del 3 de Junio de 2020, de CureVac AG: Secuencia de ácido nucleico que comprende o codifica en la dirección 5' → 3' para: i) • una región codificante, que codifica para al menos […]
Procedimientos para la administración terapéutica de medicamentos de ácido ribonucleico mensajero, del 13 de Mayo de 2020, de Modernatx, Inc: Un ARN mensajero (ARNm) que codifica un polipéptido de interés, donde el ARNm comprende: (i) al menos un sitio de unión de microARN de miR-142-3p; (ii) al […]
Ácidos ribonucleicos con nucleótidos modificados con 4-tio y procedimientos relacionados, del 15 de Abril de 2020, de Translate Bio, Inc: Una molécula de ARNm que tiene una región codificante y opcionalmente, una o más regiones no codificantes, en donde al menos el 25% de los residuos de nucleótidos del […]
Sistema de expresión bacteriano cistrónico doble, del 25 de Marzo de 2020, de LUPIN LIMITED: Un procedimiento para la producción de un anticuerpo o un fragmento del mismo que comprende las etapas de: (i) transformar una célula hospedadora bacteriana […]
Moléculas de ácido nucleico artificiales para una expresión proteica mejorada, del 19 de Febrero de 2020, de CureVac AG: Molécula de ácido nucleico artificial que comprende a) al menos un marco de lectura abierto (ORF); y b) al menos una región 3'-no traducida (3'-UTR) […]
Ácido nucleico que comprende o codifica para un tallo-bucle de histona y una secuencia poli(A) o una señal de poliadenilación para incrementar la expresión de un antígeno tumoral codificado, del 12 de Febrero de 2020, de CureVac AG: Secuencia de ácido nucleico que comprende o codifica para, en la dirección 5' a 3': i) - una región codificante que codifica al menos un péptido […]
Constructo y secuencia para la expresión genética mejorada, del 15 de Enero de 2020, de ProteoNic Biotechnology IP B.V: Metodo para la transcripcion y/o expresion y, opcionalmente, la purificacion del transcrito y/o proteina o polipeptido de interes producidos que […]