Sal de calcio y de sodio de mio-inositol 1,6:2,3:4,5 tripirofosfato para el tratamiento del cáncer.
Una composición farmacéutica que comprende la mezcla de la sal de sodio y de calcio de mio-inositol tripirofosfato y un adyuvante,
diluyente, vehículo, o excipiente farmacéuticamente aceptable de éste, para uso en el tratamiento del cáncer
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2006/009682.
Solicitante: NormOxys, Inc.
Inventor/es: LEHN, JEAN-MARIE, GREFERATH,Ruth Dr, NICOLAU,CLAUDE, FYLAKTAKIDOU,KONSTANTINA C.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K31/66 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › Compuestos del fósforo.
PDF original: ES-2532591_T3.pdf
Fragmento de la descripción:
Sal de calcio y de sodio de mio-inositol 1, 6:2, 3:4, 5 tripirofosfato para el tratamiento del cáncer Esta solicitud reivindica el beneficio bajo 35 USC 119 (e) a la Solicitud Provisional US 60/663.491 presentada el 18 de marzo, 2005.
Campo de la invención La presente invención está dirigida a composiciones para usar la sal de calcio de inositol-tripirofosfato (ITPP-Ca) para aumentar la administración de oxígeno por la sangre roja. ITPP-Ca es un efector alostérico de la hemoglobina que tiene la capacidad de cruzar la membrana plasmática de los glóbulos rojos y disminuir la afinidad por el oxígeno de la hemoglobina de los glóbulos rojos. La presente invención está dirigida además al uso de ITPP-Ca para inhibir la angiogénesis y aumentar la sensibilidad a la radiación de tumores hipóxicos. La presente invención está dirigida además al uso de ITPP-Ca para aumentar PO2 en tumores hipóxicos.
Antecedentes de la invención En el sistema vascular de un ser humano adulto, la sangre tiene un volumen de aproximadamente 5 a 6 litros. Aproximadamente una mitad de este volumen está ocupada por células, incluyendo los glóbulos rojos (eritrocitos) , glóbulos blancos (leucocitos) , y plaquetas de la sangre. Los glóbulos rojos comprenden la mayoría de los componentes celulares de la sangre. El plasma, la parte líquida de la sangre, es aproximadamente 90 por ciento agua y 10 por ciento varios solutos. Estos solutos incluyen proteínas plasmáticas, metabolitos orgánicos y productos de desecho, y compuestos inorgánicos.
La función principal de los glóbulos rojos es transportar oxígeno desde los pulmones a los tejidos del cuerpo, y transportar dióxido de carbono desde los tejidos a los pulmones para su eliminación. Muy poco oxígeno es transportado por el plasma sanguíneo porque el oxígeno sólo es débilmente soluble en disoluciones acuosas. La mayor parte del oxígeno que lleva la sangre es transportado por la hemoglobina de los eritrocitos. Los eritrocitos en los mamíferos no contienen núcleo, mitocondria o cualesquiera otros orgánulos intracelulares, y no usan el oxígeno en su propio metabolismo. Los glóbulos rojos contienen aproximadamente 35 por ciento en peso de hemoglobina, que es responsable de unir y transportar el oxígeno.
La hemoglobina es una proteína que tiene un peso molecular de aproximadamente 64.500 daltons. Contiene cuatro cadenas polipeptídicas y cuatro grupos prostéticos hemo a los que se unen los átomos de hierro en el estado ferroso. La globina normal, la parte proteica de la molécula de hemoglobina, consiste en dos cadenas alfa y dos cadenas beta. Cada una de las cuatro cadenas tiene una estructura terciaria característica en la que la cadena está plegada. Las cuatro cadenas polipeptídicas se ajustan conjuntamente en una organización aproximadamente tetraédrica, para constituir la estructura cuaternaria característica de la hemoglobina. Hay un grupo hemo unido a cada cadena polipeptídica que puede unir reversiblemente una molécula de oxígeno molecular. Cuando la hemoglobina se combina con oxígeno, se forma oxihemoglobina. Cuando el oxígeno se libera, la oxihemoglobina se reduce a desoxihemoglobina.
La administración de oxígeno a los tejidos, incluyendo tumores, depende de varios factores incluyendo, pero no limitado a, el volumen del flujo de sangre, el número de glóbulos rojos, la concentración de hemoglobina en los glóbulos rojos, la afinidad por oxígeno de la hemoglobina y, en determinadas especies, la proporción molar de hemoglobinas intraeritrocíticas con alta y baja afinidad por el oxígeno. La afinidad por el oxígeno de la hemoglobina también depende de cuatro factores, concretamente: (1) la presión parcial de oxígeno; (2) el pH; (3) la concentración de 2, 3-difosfoglicerato (DPG) en la hemoglobina; y (4) la concentración de dióxido de carbono. En los pulmones, a una presión parcial de oxígeno de 100 mm Hg, aproximadamente el 98% de la hemoglobina circulante está saturada con oxígeno. Esto representa la capacidad total de transporte de oxígeno de la sangre. Cuando está completamente oxigenada, 100 ml de sangre completa de mamífero puede transportar aproximadamente 21 ml de oxígeno gaseoso.
El efecto de la presión parcial de oxígeno y el pH en la capacidad de la hemoglobina para unirse al oxígeno se ilustra mejor por el examen de la curva de saturación de oxígeno de la hemoglobina. Una curva de saturación de oxígeno representa el porcentaje de sitios totales de unión a oxígeno de una molécula de hemoglobina que están ocupados por moléculas de oxígeno cuando las disoluciones de la molécula de hemoglobina están en equilibrio con diferentes presiones parciales de oxígeno en la fase de gas.
La curva de saturación de oxígeno para la hemoglobina es sigmoidal. Así, la unión de la primera molécula de oxígeno incrementa la afinidad de la hemoglobina restante para unir moléculas de oxígeno adicionales. Al incrementarse la presión parcial de oxígeno, se alcanza un plató en el que cada una de las moléculas de hemoglobina está saturada y contiene el límite superior de cuatro moléculas de oxígeno.
La unión reversible de oxígeno por la hemoglobina está acompañada por la liberación de protones, según la ecuación:
** (Ver fórmula) **
Así, un incremento en el pH empujará el equilibrio hacia la derecha y causa que la hemoglobina se una a más oxígeno a una presión parcial dada. Una disminución en el pH disminuirá la cantidad de oxigeno unida.
En los pulmones, la presión parcial de oxígeno en los espacios de aire es aproximadamente 90 100 mm Hg y el pH también es alto respecto al pH normal de la sangre (hasta 7, 6) . Por lo tanto, la hemoglobina tenderá a volverse casi máximamente saturada con oxígeno en los pulmones. A esa presión y pH, la hemoglobina está aproximadamente 98 por ciento saturada con oxígeno. Por otra parte, en los capilares en el interior de los tejidos periféricos, la presión parcial de oxígeno es sólo aproximadamente 25 a 40 mm Hg y el pH también es casi neutro (aproximadamente 7, 2 a 7, 3) . Como las células musculares usan oxígeno en una proporción alta, disminuyendo de esta manera la concentración local de oxígeno, se favorece la liberación de parte del oxígeno unido al tejido. Al pasar la sangre a través de los capilares en los músculos, el oxígeno se liberará desde la hemoglobina casi saturada en los glóbulos rojos al plasma sanguíneo y después a las células musculares. La hemoglobina liberará aproximadamente un cuarto de su oxígeno unido al pasar a través de los capilares musculares, de manera que cuando deja el músculo, sólo estará aproximadamente 75 por ciento saturada. En general, la hemoglobina en la sangre venosa que deja el tejido varía entre aproximadamente 65 y 97 por ciento de saturación con oxígeno en sus circuitos repetidos entre los pulmones y los tejidos periféricos. Así, la presión parcial de oxígeno y el pH trabajan conjuntamente para conseguir la liberación de oxígeno por la hemoglobina.
Un tercer factor importante en la regulación del grado de oxigenación de la hemoglobina es el efecto alostérico 2, 3difosfoglicerato (DPG) . DPG es el efector fisiológico normal de la hemoglobina en los eritrocitos de mamíferos. DPG regula la afinidad de unión al oxígeno de la hemoglobina en los glóbulos rojos en relación con la presión parcial de oxígeno en los pulmones. A mayor concentración de DPG en la célula, menor es la afinidad de la hemoglobina por el oxígeno.
Cuando la administración de oxígeno a los tejidos se reduce crónicamente, la concentración de DPG en los eritrocitos es mayor que en individuos normales. Por ejemplo, a altas altitudes la presión parcial de oxígeno es significativamente menor. Correspondientemente, la presión parcial de oxígeno en los tejidos es menor. En unas pocas horas después de que un sujeto humano normal se mueve a una mayor altitud, el nivel de DPG en los glóbulos rojos se incrementa, causando que haya más DPG unido y que la afinidad por el oxígeno de la hemoglobina disminuya. Los incrementos en el nivel de DPG de los glóbulos rojos también ocurren en pacientes que padecen hipoxia. Este ajuste permite que la hemoglobina libere su oxígeno unido más fácilmente en los tejidos para compensar la oxigenación disminuida de la hemoglobina en los pulmones. El cambio inverso ocurre cuando la gente está aclimatada a altas altitudes y desciende a altitudes menores.
Tal y como se aísla normalmente de la sangre, la hemoglobina contiene una cantidad considerable de DPG. Cuando la hemoglobina está "desprovista" de su DPG, muestra una afinidad mucho mayor por el oxígeno. Cuando el DPG se incrementa, la afinidad de unión para el oxígeno de la hemoglobina disminuye.... [Seguir leyendo]
Reivindicaciones:
1. Una composición farmacéutica que comprende la mezcla de la sal de sodio y de calcio de mio-inositol tripirofosfato y un adyuvante, diluyente, vehículo, o excipiente farmacéuticamente aceptable de éste, para uso en el tratamiento del cáncer.
2. La composición para uso de la reivindicación 1, en la que el mio-inositol tripirofosfato es mio-inositol 1, 6:2, 3:4, 5 tripirofosfato.
3. La composición para uso de la reivindicación 1 o reivindicación 2, en la que el cáncer se selecciona del grupo que consiste en rabdomiosarcomas, retinoblastoma, sarcoma de Ewing, neuroblastoma, y osteosarcoma.
4. La composición para uso de la reivindicación 1 o reivindicación 2, en la que el cáncer se selecciona de uno o más
del grupo que consiste en cáncer de mama, cáncer de próstata, cáncer de células renales, cáncer de cerebro, cáncer de ovario, cáncer de colon, cáncer de vejiga, cáncer pancreático, cáncer de estómago, cáncer de esófago, melanoma cutáneo, cáncer de hígado, cáncer de pulmón, cáncer testicular, cáncer de riñón, cáncer de vejiga, cáncer de cuello uterino, linfoma, cáncer de paratiroides, cáncer de pene, cáncer rectal, cáncer del intestino delgado, cáncer de tiroides, cáncer uterino, linfoma de Hodgkin, cáncer de labios y oral, cáncer de piel, leucemia, y mieloma múltiple.
5. La composición para uso de la reivindicación 2, en la que la dosificación de mio-inositol 1, 6:2, 3:4, 5 tripirofosfato es 0, 5 a 1, 5 g/kg.
6. La composición farmacéutica para uso de una cualquiera de las reivindicaciones 1 a 5, en la que la composición se formula para administración intravenosa.
7. La composición para uso de una cualquiera de las reivindicaciones 1 a 6, en la que la mezcla de la sal de sodio y de calcio de mio-inositol tripirofosfato se obtiene mezclando la sal de sodio de mio-inositol tripirofosfato con CaCl2.
Patentes similares o relacionadas:
Proteínas de unión a antígeno para proproteína convertasa subtilisina kexina tipo 9 (PCSK9), del 6 de Mayo de 2020, de AMGEN INC.: Una proteína de unión a antígeno, donde dicha proteína de unión a antígeno (i) comprende (a) un dominio variable de cadena ligera que comprende una secuencia […]
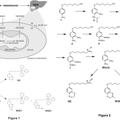 Compuestos secuestrantes de dicarbonilo dirigidos a mitocondrias, del 29 de Abril de 2020, de United Kingdom Research and Innovation: Un compuesto de fórmula 1:
A-L-B
Fórmula 1
o una sal farmacéuticamente aceptable del mismo, en la que:
A es un resto secuestrante de […]
Compuestos secuestrantes de dicarbonilo dirigidos a mitocondrias, del 29 de Abril de 2020, de United Kingdom Research and Innovation: Un compuesto de fórmula 1:
A-L-B
Fórmula 1
o una sal farmacéuticamente aceptable del mismo, en la que:
A es un resto secuestrante de […]
Composición de líquido de diálisis que comprende sustancias inhibidoras de la cristalización, del 12 de Febrero de 2020, de UNIVERSITAT DE LES ILLES BALEARS: Una formulación intravenosa que comprende inositol-fosfato y/o cualquiera de sus sales para su uso en el mantenimiento o aumento de los niveles de inositol-fosfato […]
Formulaciones y formas de dosificación de fosfolípidos oxidados, del 11 de Diciembre de 2019, de VASCULAR BIOGENICS LTD: Una composición farmacéutica que comprende un fosfolípido oxidado que tiene una estructura según la fórmula (I):**Fórmula** en donde R1 […]
Osmolitos para la reducción de los efectos secundarios de esteroides o antihistamínicos, del 8 de Noviembre de 2019, de BITOP AG: Medicamento que contiene como principio activo al menos un soluto compatible para su administración para el tratamiento de reacciones inflamatorias agudas […]
Formulaciones terapéuticas sostenidas inhalables, del 2 de Julio de 2019, de Civitas Therapeutics, Inc. (100.0%): Partículas no poliméricas para la administración pulmonar de un agente terapéutico, profiláctico o diagnóstico, comprendiendo las partículas: (a) un agente terapéutico, […]
Nuevas fenoxiacetamidas anilladas, del 5 de Junio de 2019, de BOEHRINGER INGELHEIM INTERNATIONAL GMBH: Un compuesto de fórmula (I),**Fórmula** en la que R1 y R2 se seleccionan independientemente entre etilo, 2-hidroxietilo, 2-tetrahidrofuranilmetilo y […]
Óxido de arilfósforo y sulfuro de arilfósforo espirocíclicos, del 29 de Mayo de 2019, de Qilu Pharmaceutical Co., Ltd: Un compuesto representado por la fórmula (I) o la fórmula (II) o una sal farmacéuticamente aceptable del mismo,**Fórmula** en las que, T1 se selecciona […]