Método para recuperación de hierro.
Un método para la recuperación de hierro en la forma de un óxido de hierro como producto útil,
tal como hematita, a partir de una solución de deslavado obtenida del deslavado de un mineral de laterita de níquel, que comprende oxidación e hidrólisis de una solución de mezcla de sulfato férrico y urea del deslavado de minerales de laterita de níquel a una temperatura de 60-100°C.
Tipo: Patente Europea. Resumen de patente/invención. Número de Solicitud: E12182923.
Solicitante: Canbekte, Hüsnü Sinan.
Nacionalidad solicitante: Turquía.
Dirección: Hüsrev Gerede Caddesi Gul Apt. No: 30 Kat 4 Daire 12 Nisantasi 34357 Istanbul TURQUIA.
Inventor/es: CANBEKTE,ZEKERIYA.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C22B23/00 QUIMICA; METALURGIA. › C22 METALURGIA; ALEACIONES FERROSAS O NO FERROSAS; TRATAMIENTO DE ALEACIONES O METALES NO FERROSOS. › C22B PRODUCCION O AFINADO DE METALES (fabricación de polvos metálicos o sus suspensiones B22F 9/00; producción de metales por electrólisis o electroforesis C25 ); PRETRATAMIENTO DE MATERIAS PRIMAS. › Obtención del níquel o del cobalto.
PDF original: ES-2550489_T3.pdf
Fragmento de la descripción:
Método para recuperación de hierro Campo técnico de la invención La presente invención se relaciona con un proceso para la precipitación de hierro como hematita a partir de una solución de mezcla Fe2 (SO4) 3/urea que contiene sulfatos de níquel y cobalto.
Antecedentes de la Invención El deslavado de minerales de laterita de níquel con ácido sulfúrico es un proceso ampliamente aplicado. Algunas investigaciones recientes indican que cuando se agrega urea a la solución de deslavado en cantidades suficientes, las velocidades de disolución del metal y las recuperaciones de metal hacia la solución se incrementan marcadamente. Como tales, las caídas de tiempo de deslavado a una hora y las recuperaciones de metal se elevan por encima del 95%.
Estas mejoras son debidas al efecto de la urea sobre la disolución del hierro contenido en el material que contiene el metal. Cuando el hierro es atacado y forzado a disolverse, otros metales que están enlazados con el hierro en alguna clase de enlace se hacen también objetivos fáciles para el ácido sulfúrico y así su velocidad de disolución se incrementa marcadamente.
La remoción del hierro de la solución de deslavado es importante para la recuperación de otros metales y para la economía del proceso. El hierro normalmente es eliminado de la solución en forma de jarosita, goetita o hematita pero en ninguna de ellas da como resultado un producto de hierro utilizable. La jarosita y la goetita producidas como tales se descartan como residuos sin valor económico. Para la producción de hematita, la precipitación de hierro debería llevarse a cabo en un autoclave a temperaturas por encima de 200°C y presión de oxígeno de 18 bars o más. El hierro también puede ser precipitado desde la solución como hidróxido producido por la precipitación con caliza para ser descartado como residuo.
Se ha llevado a cabo un importante volumen de investigación con respecto a la precipitación del hierro como hematita que puede ser utilizada en la industria. La patente de los Estados Unidos 7.294.319 describe un método para precipitar hierro a partir de una solución de sulfato de zinc como hematita bajo condiciones atmosféricas. De la misma manera, la WO 2007/079532 describe un método hidrometalúrgico para precipitar hierro en forma de hematita a partir de soluciones de deslavado que contiene níquel, cobalto y hierro.
El artículo Uniform Particles with a large surface area formed by hydrolysis of Fe2 (S04) 3 with Urea publicado en 1999 en Materials Reserch Bulletin Vol 34 No 6 pp 905-919 describe la hidrólisis de óxido de hierro a partir de una solución de mezcla Fe2 (SO4) 3/Urea bajo diversas condiciones. El artículo indica que una hidrólisis lenta de soluciones acuosas de Fe2 (S04) 3 con Urea en el rango de temperatura de 60-900°C lleva a una forma característica de óxidos hidrosos de hierro (III) y sulfatos básicos. La deshidratación térmica de estos óxidos hidrosos de hierro (III) produce Fe2O3 amorfo.
Resumen de la invención El objetivo de la invención es proveer un método para la recuperación eficiente de hierro como producto de óxido de hierro utilizable, tal como hematita, sin perder urea a partir de una solución de mezcla de Fe2 (SO4) 3/urea que contiene sulfatos de níquel y cobalto, resultante del deslavado de mineral de lateritas de níquel con una mezcla de ácido sulfúrico y urea.
Este objetivo es alcanzado por medio de un método que comprende las características de la reivindicación 1 de la patente. En las sub-reivindicaciones se definen realizaciones adicionales preferidas del método.
Durante el trabajo que llevó a la presente invención se encontró posible recuperar hierro bajo condiciones atmosféricas a partir de una solución de Fe2 (SO4) 3/urea que contiene sulfatos de níquel y cobalto.
El níquel y el cobalto pueden ser recuperados de la solución antes de la recuperación del hierro mediante resinas o mediante cualquier otro método disponible, después de la recuperación del hierro.
Una ventaja con el método de acuerdo con la invención es que el método puede ser ejecutado -en realizaciones preferidas del mismo- a presión atmosférica y una temperaturas de 60°C hasta 100°C, que no se emiten gases y que, debido al tiempo de residencia corto, puede utilizarse un equipo simple y no costoso para llevar a cabo el método. Adicionalmente, el hierro puede ser recuperado como un producto utilizable y una parte importante del 2 5
ácido y casi toda la urea pueden ser reciclados para ser utilizados en el deslavado de minerales de laterita de níquel frescos o materiales que contienen níquel, lo que da como resultado un consumo de ácido reducido en el deslavado.
Así, la presente invención se relaciona con un proceso que involucra la recuperación de hierro disuelto como óxido de hierro y el reciclaje de la mezcla de deslavado.
Ventajosamente, el ácido sulfúrico asociado con la disolución de hierro es recuperado sustancialmente sin pérdida.
Adicionalmente, la urea que es importante en la reducción del tiempo de deslavado de materiales que contienen níquel y en el incremento de las recuperaciones del deslavado del níquel y cobalto es recuperada virtualmente sin pérdida alguna.
Características adicionales del método de acuerdo con la invención serán evidentes a partir de la siguiente descripción y de las reivindicaciones anexas.
Descripción detallada de la invención El término "metal" utilizado aquí y en las reivindicaciones anexas puede abarcar níquel, cobalto y cualquier otro metal que sea normalmente soluble en ácido sulfúrico.
No todas las etapas de a) a i) tal como se detalla más adelante deben ser realizadas en un método de acuerdo con la invención pero pueden ser combinadas libremente en una realización particular del mismo.
a) Para la recuperación de hierro como hematita u óxido de hierro utilizable, el pH de la solución de deslavado a partir del deslavado del material que contiene níquel es ajustado a un pH de 2.5 - 3.0 tratando la solución con mineral de laterita de níquel o material que contiene níquel. No se utiliza caliza ni cal para el ajuste del pH con el fin de prevenir la pérdida de ácido sulfúrico a través de la formación de yeso.
b) Después de la separación sólido-líquido, el residuo obtenido después del ajuste del pH es enviado a un sistema de deslavado separado, mientras que la solución con pH 2.5-3.0 es agitada a una temperatura de alrededor de 90°C centígrados.
c) El níquel y el cobalto disueltos en la solución de deslavado pueden ser recuperados antes de la recuperación de hierro mediante resinas o, alternativamente, pueden ser recuperados después de la recuperación de hierro por cualquier método conocido tal como extracción con solventes y/o electrólisis.
d) Mientras se agita la solución, se agrega un agente oxidante tal como peróxido de hidrógeno y/o oxígeno/aire.
e) La adición de sulfato ferroso en una cantidad estequiométrica ayuda con la conversión de la goetita a hematita.
f) Después de 20-30 minutos de agitación, se agregan partículas de hematita como partículas de semilla. Cuando se detiene la agitación, comienzan a formarse flóculos de partículas de óxido de hierro y a sedimentarse rápidamente.
g) La suspensión es filtrada entonces fácilmente para separar los óxidos de hierro de la solución.
h) La solución, la cual está ahora libre de hierro pero contiene níquel y/o cobalto, si aquellos no han sido recuperados previamente, tendrá un pH de alrededor de 1.0-1.5, la cual, si las concentraciones de níquel y cobalto no son suficientemente altas, puede ser enviada a un sistema de deslavado.
i) Si la concentración de níquel y cobalto en la solución es suficientemente alta, dicha solución puede ser tratada adicionalmente para recuperar los metales. Si se requiere cualquier ajuste del pH de la solución para este propósito, esto puede lograrse tratando la solución con material que contiene níquel. Cualquier residuo de este deslavado con ajuste de pH será enviado a un sistema de deslavado.
En la práctica, el método se lleva a cabo ventajosamente en recipientes hechos de aceros inoxidables o aceros medios o tanques de concreto que pueden ser recubiertos con un recubrimiento protector apropiado.
La invención será explicada ahora adicionalmente en el siguiente ejemplo. Este ejemplo solamente pretende ilustrar la invención y no debería considerarse de manera alguna como limitante del alcance de la invención.
Ejemplo para la precipitación del hierro 3
Se usó una solución de deslavado obtenida del deslavado de un mineral de laterita de níquel. El pH... [Seguir leyendo]
Reivindicaciones:
1. Un método para la recuperación de hierro en la forma de un óxido de hierro como producto útil, tal como hematita, a partir de una solución de deslavado obtenida del deslavado de un mineral de laterita de níquel, que comprende oxidación e hidrólisis de una solución de mezcla de sulfato férrico y urea del deslavado de minerales de laterita de níquel a una temperatura d.
6. 100°C.
2. El método de acuerdo con la reivindicación 1, en donde el pH de la solución que contiene hierro es ajustado a 2.5
3.0 con mineral de laterita de níquel antes de la recuperación de hierro.
3. El método de acuerdo con la reivindicación 1 ó 2, en donde el método es llevado a cabo a presión atmosférica.
4. El método de acuerdo con una cualquiera de las reivindicaciones 1 a 3, en donde se utiliza peróxido de hidrógeno 10 y/o aire y/o gas oxígeno como oxidante.
5. El método de acuerdo con una cualquiera de las reivindicaciones 1 a 4, en donde se usan semillas de hematita para iniciar la formación de óxido de hierro.
6. El método de acuerdo con una cualquiera de la reivindicaciones 1 a 5, en donde, si después de la conversión de
hierro a óxido de hierro el pH de la solución cae a 1.0-1.5, la solución es reutilizada para deslavado de material que 15 contiene níquel fresco.
7. El método de acuerdo con una cualquiera de la reivindicaciones 1 a 6, en donde el ácido sulfúrico asociado con la disolución del hierro es recuperado sustancialmente sin pérdida.
8. El método de acuerdo con una cualquiera de la reivindicaciones 1 a 7, en donde se recupera la urea virtualmente sin pérdida.
Patentes similares o relacionadas:
SISTEMA Y MÉTODO PARA SOLUBILIZAR EN UN MEDIO ACUOSO ELEMENTOS CONTENIDOS EN UN CONCENTRADO MINERAL DEL TIPO SULFURO., del 5 de Marzo de 2020, de PLATINUM GROUP CHILE SPA: La presente invención se refiere a un sistema para otorgar solubilidad en un medio acuoso a los elementos químicos contenidos en un concentrado […]
Método para fabricar un acero inoxidable austenítico a partir de un mineral de laterita de níquel y un mineral de cromita, del 17 de Abril de 2019, de YIEH UNITED STEEL CORP.: Un método para fabricar un acero inoxidable austenítico a partir de un mineral de laterita de níquel y un mineral de cromita, caracterizándose dicho método por las […]
Método para la tostación parcial de concentrados que llevan cobre y/u oro, del 6 de Marzo de 2019, de Outotec (Finland) Oy: Procedimiento para eliminar sulfuros de arsénico y/o antimonio de partículas de mineral que contienen cobre, níquel y/u oro, en donde las partículas de […]
Procedimiento para la extracción de níquel, cobalto y otros metales base a partir de menas de laterita mediante lixiviado en pila y productos que contienen níquel, cobalto y otros metales procedentes de menas de laterita, del 26 de Febrero de 2014, de VALE S.A: Procedimiento para la extracción de níquel, cobalto y otros metales a partir de menas de laterita mediante lixiviado en pila, caracterizado por que […]
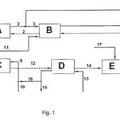 Método para la separación de zinc, hierro, calcio, cobre y manganeso a partir de soluciones acuosas de cobalto y/o níquel, del 9 de Diciembre de 2013, de NORILSK NICKEL HARJAVALTA OY: Un método para separar los metales que forman la impureza de zinc, hierro, cobre, calcio y / o de manganeso dela solución acuosa de los metales del producto cobalto y […]
Método para la separación de zinc, hierro, calcio, cobre y manganeso a partir de soluciones acuosas de cobalto y/o níquel, del 9 de Diciembre de 2013, de NORILSK NICKEL HARJAVALTA OY: Un método para separar los metales que forman la impureza de zinc, hierro, cobre, calcio y / o de manganeso dela solución acuosa de los metales del producto cobalto y […]
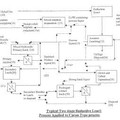 Lixiviación amoniacal reductora de materiales que contienen níquel y cobalto, del 10 de Junio de 2013, de BHP BILLITON SSM DEVELOPMENT PTY LTD: Procedimiento para la recuperación de níquel y/o cobalto de un material impuro de níquel, cobalto oníquel/cobalto mixto, que incluye las etapas […]
Lixiviación amoniacal reductora de materiales que contienen níquel y cobalto, del 10 de Junio de 2013, de BHP BILLITON SSM DEVELOPMENT PTY LTD: Procedimiento para la recuperación de níquel y/o cobalto de un material impuro de níquel, cobalto oníquel/cobalto mixto, que incluye las etapas […]
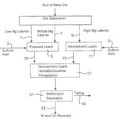 Procedimiento para la lixiviación ácida mejorada de minerales de laterita, del 6 de Febrero de 2013, de BHP BILLITON SSM DEVELOPMENT PTY LTD: Procedimiento para la recuperación de níquel y cobalto a partir de un mineral de laterita niquelífera que incluye lasetapas siguientes:
a) proporcionar […]
Procedimiento para la lixiviación ácida mejorada de minerales de laterita, del 6 de Febrero de 2013, de BHP BILLITON SSM DEVELOPMENT PTY LTD: Procedimiento para la recuperación de níquel y cobalto a partir de un mineral de laterita niquelífera que incluye lasetapas siguientes:
a) proporcionar […]
UN PROCEDIMIENTO PARA LA EXTRACCIÓN DE NÍQUEL A PARTIR DE MINERAL POBRE DE CROMITA, del 22 de Febrero de 2012, de COUNCIL OF SCIENTIFIC AND INDUSTRIAL RESEARCH NATIONAL ALUMINIUM COMPANY LIMITED NATIONAL MINERAL DEVELOPMENT CORPORATION LIMITED: Un procedimiento para la extracción de níquel de mineral pobre de cromita que contiene de 0,6 a 0,9% de níquel, procedimiento que comprende las etapas de: (a) […]