Métodos y reactivos para una transferencia génica eficaz y dirigida a células del linaje de monocitos macrófagos.
Método in vitro para suministrar un compuesto de interés a células CD14+ derivadas de monoblastos que comprende poner en contacto dichas células con un nanotransportador que porta dicho compuesto de interés,
en el que el nanotransportador comprende, como mínimo, el dominio knob de la proteína de fibra corta del adenovirus Ad40 o Ad41, en el que el nanotransportador se selecciona del grupo de un virus o una partícula de tipo viral y en el que dicho virus o partícula de tipo viral no es un subgrupo F de adenovirus del mismo tipo que la proteína de fibra corta.
Tipo: Patente Europea. Resumen de patente/invención. Número de Solicitud: E13191475.
Solicitante: UNIVERSITAT AUTONOMA DE BARCELONA.
Nacionalidad solicitante: España.
Inventor/es: CHILLON RODRIGUEZ,MIGUEL, FERNÁNDEZ GIMENO,Ester, GASSULL DURO,MIQUEL ÁNGEL, RÍO FERNÁNDEZ,ADOLFO.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C12N15/861 QUIMICA; METALURGIA. › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 15/00 Técnicas de mutación o de ingeniería genética; ADN o ARN relacionado con la ingeniería genética, vectores, p. ej. plásmidos, o su aislamiento, su preparación o su purificación; Utilización de huéspedes para ello (mutantes o microorganismos modificados por ingeniería genética C12N 1/00, C12N 5/00, C12N 7/00; nuevas plantas en sí A01H; reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00; nuevas razas animales en sí A01K 67/00; utilización de preparaciones medicinales que contienen material genético que es introducido en células del cuerpo humano para tratar enfermedades genéticas, terapia génica A61K 48/00; péptidos en general C07K). › Vectores adenovirales.
PDF original: ES-2550834_T3.pdf




Fragmento de la descripción:
Métodos y reactivos para una transferencia génica eficaz y dirigida a células del linaje de monocitos-macrófagos SECTOR DE LA INVENCIÓN
La presente invención se refiere a la capacidad del adenovirus 5 humano quimérico que porta la fibra corta de Ad40 entérico para transferir material genético a monocitos y macrófagos en un procedimiento eficaz y selectivo, y a la optimización de la respuesta a la dosis y el perfil de bioseguridad en células transducidas.
ANTECEDENTES DE LA INVENCIÓN
Las células mononucleares se han definido como un linaje de células hematopoyéticas derivadas de células progenitoras en la médula ósea. Las células progenitoras mieloides comprometidas se diferencian formando monocitos sanguíneos, que circulan en la sangre y, a continuación, entran en los tejidos convirtiéndose en macrófagos residentes. Durante muchos años se ha conocido y estudiado la existencia de subconjuntos de monocitos en seres humanos. Se identificaron monocitos humanos mediante la expresión de CD14. Pueden clasificarse además basándose en la expresión de CD16 (el receptor de Fc de alta afinidad) . Las células CD16-se denominan monocitos clásicos dado que son habitualmente aproximadamente el 90% de los monocitos totales en individuos sanos. Las células CD16+ parecen expandirse en muchas enfermedades inflamatorias y presentan una migración preferente a través de las capas endoteliales en respuesta a quimiocinas. Por tanto, se denominan habitualmente monocitos no clásicos o proinflamatorios. Se ha demostrado que este subconjunto de monocitos puede diferenciarse en células dendríticas (CD) . Se ha descrito un aumento considerable en el número de monocitos CD14+CD16+ para una variedad de infecciones sistémicas y localizadas.
Mientras que los monocitos son células ampliamente reclutables, la mayor parte de la capacidad migratoria de macrófagos derivados de monocitos y CD se suprime en el proceso de maduración debido a una pérdida progresiva de receptores de quimiocinas inflamatorias. A la inversa, la regulación por incremento de CCR7 durante el proceso de maduración de CD aumenta su respuesta migratoria hacia los vasos linfáticos y ganglios linfáticos de drenaje. (Eur. J. Immunol 1998. 28:2760-2769; J. Neuroimmunol 2008 197:21-28) .
Por tanto, la manipulación genética de los monocitos sanguíneos es sumamente atractiva dado que puede permitir la manipulación de la respuesta inmunitaria en una ubicación particular en la que tiene lugar un proceso inflamatorio y a la que migrarán preferentemente los monocitos bajo la influencia de factores quimiotácticos liberados por células dañadas en sitios inflamados.
Los monocitos se encuentran en la sangre humana en cantidades variables, oscilando desde el 5-10% de los leucocitos de sangre periférica totales en individuos sanos, aunque este número puede superarse enormemente siempre que esté presente un estado inflamatorio. Varían en tamaño y tienen diferentes grados de granularidad y una morfología nuclear variada. De hecho, los monocitos se reclutan preferentemente en zonas inflamadas, en las que adquieren nuevos papeles y realizan funciones fagocíticas y de presentación de antígenos. En ciertas condiciones, pueden evolucionar a células dendríticas, que son células presentadoras de antígenos sumamente eficaces y que organizan la respuesta inmunitaria provocada frente a un ataque particular y dirigen la función de los linfocitos.
Los macrófagos son relativamente resistentes a la transfección, aunque hay varios informes que reivindican que pueden utilizarse finalmente vectores adenovirales como vectores para transfectar macrófagos derivados de monocitos, células dendríticas o incluso monocitos (Eur. J. Immunol. 1999, 29: 964-972; Blood 1998 91: 392-398; Acta Pharmacol. Sin. 2006, 27: 609-616; Biochem. Biophys. Res. Com. 1993, 195: 1174-1183; Gene Ther. 2000, 7: 263-270, Cytotherapy, 2006 8: 36-46; Mol. Ther. 2007, 16: 210-217 y J. Immunol. 2008, 181: 8018-8026) . Sin embargo, estos informes no utilizan monocitos no diferenciados y no estimulados dado que cultivan células en presencia de diferentes combinaciones de citocinas y factores, tales como factor estimulante de colonias de macrófagos (M-CSF) , también conocido como factor 1 estimulante de colonias (CSF-1) , factor estimulante de colonias de granulocitos y macrófagos (GM-CSF) y otros. En contacto con los monocitos, M-CSF potencia la expresión de antígenos de diferenciación, aumenta las actividades quimiotácticas y fagocíticas y estimula la producción de varias citocinas (Ross J. A. y Auger M. J. en The Macrophage, segunda edición; Oxford University Press, 2002; Pathol. Int. 2008, 58: 143-155) . Además, se ha demostrado que pueden generarse CD humanas a partir de monocitos en presencia de GM-CSF solo (Immunobiology 2008, 213: 859-870) . En cambio, los monocitos se consideran esencialmente como células no transfectables (Gene Ther. 1997, 4: 524-532; J. Immunol. Methods 2008, 330: 86-95) . De ese modo, los intentos hasta la fecha de transfectar selectivamente monocitos no diferenciados y no estimulados de sangre periférica utilizando o bien electroporación o bien métodos virales y no virales no han tenido éxito (Gastroenterology 2006 131:1799-181) . Notablemente, la utilización reciente de vectores de Ad5 quimérico que portan fibras de Ad35 y Ad11 ha permitido la infección de diferentes células sanguíneas primarias incluyendo células T, células B y monocitos (Virology 2006, 25: 349 (1) : 96-111) . Además, Herold y otros, (Langenbacks Archives of Surger y , 2006, 391:72-82) han notificado también la utilización de adenovirus para
transfectar monocitos, Gerstzen y otros., (J. Biol. Chem. 2001, 276: 26846-26851) y Kaan-Shanzer y otros, 2001, Hum. Gene Therapy, 12:1989-2005) han notificado que los adenovirus pueden utilizarse para transducir monocitos de sangre del cordón umbilical. Mayne y otros (J. Immunol. Methods, 2003, 278: 45-56) han descrito que la eficacia de la transfección de células CD14+ con adenovirus puede mejorarse si la células se centrifugan en presencia de adenovirus antes de la etapa de transducción.
La solicitud de patente internacional WO9850053 describe métodos para transducir monocitos utilizando vectores adenovirales quiméricos que utilizan adenovirus Ad5 recombinante que comprende la proteína de fibra de Ad3. Este método permite una eficacia de transducción del 80% (a 100 partículas infectivas/célula) o del 100% (a 1000 100 partículas infectivas/célula) .
Sin embargo, ninguno de estos vectores es particularmente eficaz para su utilización in vivo dado que pueden transducir otros tipos de células dando como resultado por tanto efectos secundarios debidos a la infección de células no diana. Por tanto, se necesitan en la técnica métodos y reactivos que permitan la transducción selectiva y eficaz de monocitos de sangre periférica no comprometidos, no estimulados y no diferenciados.
CARACTERÍSTICAS DE LA INVENCIÓN
La presente invención se refiere a métodos in vitro y a nanotransportadores para su utilización en medicina, tal como se define en las reivindicaciones.
Además, en la presente memoria descriptiva se da a conocer a un nanotransportador que comprende un producto de interés y, como mínimo, una parte de la proteína de fibra corta de un adenovirus del subgrupo F o una variante funcionalmente equivalente del mismo con la condición de que el nanotransportador no sea una partícula viral.
Además se da a conocer un método in vitro para suministrar un compuesto de interés a una célula del linaje de monocitos-macrófagos que comprende poner en contacto dicha célula con un nanotransportador que porta dicho compuesto de interés y en el que el transportador contiene, como mínimo, una parte de la proteína de fibra corta de un adenovirus del grupo F o una variante funcionalmente equivalente del mismo.
Adicionalmente se da a conocer un nanotransportador que comprende un producto de interés y, como mínimo, una parte de la proteína de fibra corta de un adenovirus del subgrupo F o una variante funcionalmente equivalente del mismo para su utilización en medicina.
Adicionalmente se da a conocer un nanotransportador que comprende un producto de interés y, como mínimo, una parte de la proteína de fibra corta de un adenovirus del subgrupo F o una variante funcionalmente equivalente del mismo para su utilización en el tratamiento de una enfermedad asociada a células del linaje de monocitos-macrófagos.
DESCRIPCIÓN BREVE DE LAS FIGURAS
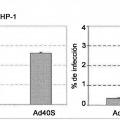
La figura 1 muestra el porcentaje de infección de vectores de adenovirus 5 humano y adenovirus 5/40 quimérico en la línea celular de monocitos murinos RAW 264.7.
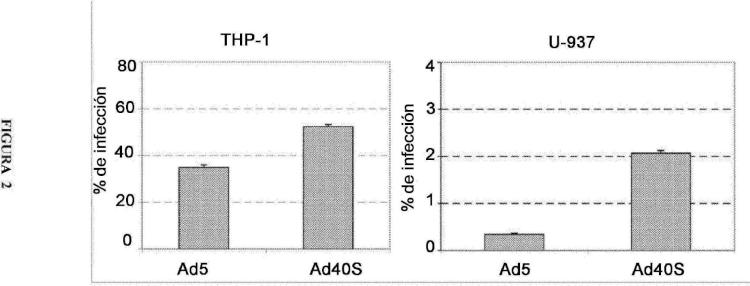
La figura 2 muestra el porcentaje de... [Seguir leyendo]
Reivindicaciones:
1. Método in vitro para suministrar un compuesto de interés a células CD14+ derivadas de monoblastos que comprende poner en contacto dichas células con un nanotransportador que porta dicho compuesto de interés, en el que el nanotransportador comprende, como mínimo, el dominio knob de la proteína de fibra corta del adenovirus Ad40 o Ad41, en el que el nanotransportador se selecciona del grupo de un virus o una partícula de tipo viral y en el que dicho virus o partícula de tipo viral no es un subgrupo F de adenovirus del mismo tipo que la proteína de fibra corta.
2. Método, según la reivindicación 1, en el que el nanotransportador es una partícula adenoviral, preferentemente un Ad5.
3. Método, según la reivindicación 1 ó 2, en el que el compuesto de interés se suministra a una célula del linaje de monocitos-macrófagos seleccionada de una célula sanguínea mononuclear primaria o una célula dendrítica derivada de monocito.
4. Método, según cualquiera de las reivindicaciones anteriores, en el que el producto de interés se selecciona del grupo que comprende agentes terapéuticos, agentes para el diagnóstico, agentes profilácticos, y/o agentes nutracéuticos.
5. Método, según la reivindicación 4, en el que el producto de interés a ser suministrado es una molécula pequeña, un ácido nucleico, tal como agentes de ADNc, ARNip, ARNi, y microARN o ARNhc, ribozimas, plásmidos de ADN, aptámeros, oligonucleótidos antisentido, oligonucleótidos aleatorizados naturales o no naturales; una proteína, un péptido, un lípido, un hidrato de carbono, una hormona, un metal, un elemento radiactivo y un compuesto, un fármaco, una vacuna, un agente inmunológico y/o combinaciones de los mismos.
6. Nanotransportador que comprende un producto de interés y, como mínimo, una parte del dominio knob de la proteína de fibra corta del adenovirus Ad40 o Ad41 para inducir una respuesta inmunitaria mediante el suministro de un antígeno, en el que el nanotransportador se selecciona del grupo de un virus o partícula de tipo viral y en el que dicho virus o partícula de tipo viral no es un subgrupo F de adenovirus del mismo tipo que la proteína de fibra corta.
7. Nanotransportador que comprende un producto de interés y, como mínimo, parte del dominio knob de la proteína de fibra corta del adenovirus Ad40 o Ad41 para reducir una respuesta inmune aumentada mediante el suministro de compuestos citotóxicos, en el que el nanotransportador se selecciona del grupo de un virus o partícula de tipo viral y en el que dicho virus o partícula de tipo viral no es un subgrupo F de adenovirus del mismo tipo que la proteína de fibra corta.
8. Nanotransportador que comprende un producto de interés y, como mínimo, parte del dominio knob de la proteína de fibra corta del adenovirus Ad40 o Ad41 para reducir la inflamación mediante el suministro de un componente antiinflamatorio, en el que el nanotransportador se selecciona del grupo de un virus o una partícula de tipo viral y en el que dicho virus o partícula de tipo viral no es un subgrupo F de adenovirus del mismo tipo que la proteína de fibra corta.
Patentes similares o relacionadas:
Composiciones útiles en el tratamiento de la deficiencia de ornitina transcarbamilasa (OTC), del 8 de Julio de 2020, de THE TRUSTEES OF THE UNIVERSITY OF PENNSYLVANIA: Un vector vírico recombinante que comprende una secuencia de ácido nucleico que codifica la proteína ornitina transcarbamilasa humana (hOTC) y secuencias […]
Composiciones y métodos para la expresión de ARNs de guía de CRISPR utilizando el promotor de H1, del 29 de Enero de 2020, de THE JOHNS HOPKINS UNIVERSITY: Un sistema CRISPR-Cas no natural que comprende un vector que comprende un promotor H1 bidireccional, en donde el promotor de H1 bidireccional comprende: a) elementos […]
Métodos y composiciones para tratar depósitos amiloides, del 22 de Enero de 2020, de UNIVERSITY OF IOWA RESEARCH FOUNDATION: Una partícula de rAAV2 que comprende una proteína de la cápside de AAV2 y un vector que comprende un ácido nucleico que codifica para una […]
 Células dendríticas alogénicas mejoradas para uso en el tratamiento de cáncer, del 30 de Octubre de 2019, de IMMUNICUM AB: Un método para proporcionar células dendríticas proinflamatorias, teniendo dichas células dendríticas proinflamatorias una capacidad mejorada para activar células T alogénicas […]
Células dendríticas alogénicas mejoradas para uso en el tratamiento de cáncer, del 30 de Octubre de 2019, de IMMUNICUM AB: Un método para proporcionar células dendríticas proinflamatorias, teniendo dichas células dendríticas proinflamatorias una capacidad mejorada para activar células T alogénicas […]
Adenovirus que expresan antígenos oncógenos heterólogos, del 4 de Septiembre de 2019, de BOARD OF REGENTS THE UNIVERSITY OF TEXAS SYSTEM: Un adenovirus oncolítico recombinante que tiene un genoma que comprende una o más secuencias de ácido nucleico heterólogas que codifican un antígeno oncógeno, […]
Vector de virus adenoasociado, del 28 de Agosto de 2019, de KING'S COLLEGE LONDON: Un vector de virus adenoasociado (AAV) recombinante que comprende: (a) una proteína de la cápside del AAV2 variante, en el que la proteína de la cápside del AAV2 variante […]
Mutantes de E1A y E1B de adenovirus selectivos de tumor, del 10 de Julio de 2019, de THE REGENTS OF THE UNIVERSITY OF CALIFORNIA: Un adenovirus recombinante que comprende una secuencia de ADN que se inserta en un sitio de inserción de E1b- 19K, en el que dicho sitio de inserción […]
Composiciones de SYN3 y métodos, del 12 de Junio de 2019, de MERCK SHARP & DOHME CORP: Una composicion farmaceutica liofilizada que comprende N-(3-colamidopropil)-N-(3(actobionamidopropil))-colamida (SYN3), hidroxipropil-beta-ciclodextrina (HPßCD) y un sistema […]