Reacción de adición de amida.
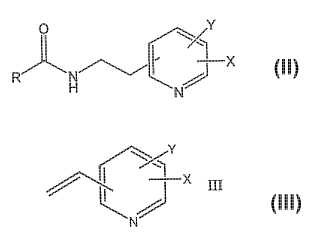
Procedimiento de preparación de un compuesto de fórmula II
que comprende la reacción de un compuesto de fórmula RCONH2 con un compuesto de fórmula III
en el que X e Y se seleccionan independientemente de entre el grupo que comprende H,
metilo, etilo, OMe, OEt ymezclas de los mismos, y en el que R es un resto de fórmula IV
en el que R1, R2 y R3 comprenden conjuntamente, como mínimo, 6 átomos de carbono, y en el que R1, R2 y R3 seseleccionan de tal manera que
(i) R1 se selecciona de entre el grupo que comprende H, Me, Et, isopropilo, alquilo C4-C5ramificado y mezclas de los mismos; y
(ii) R2 y R3 se seleccionan independientemente de entre el grupo que comprende Me, Et,isopropilo, alquilo C4 ramificado y mezclas de los mismos; o
(b) dos cualesquiera de entre R1, R2 y R3, o todos ellos, forman conjuntamente un radical monocíclico,bicíclico o tricíclico que tiene hasta 10 átomos de carbono,
llevándose a cabo la reacción en un disolvente en presencia de una base.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/CH2008/000325.
Solicitante: GIVAUDAN SA.
Nacionalidad solicitante: Suiza.
Dirección: CHEMIN DE LA PARFUMERIE 5 1214 VERNIER SUIZA.
Inventor/es: FURRER,STEFAN,MICHAEL, BOM,DAVID C, DASTRUP,DAVID MAX, UNGUREANU,IOANA MARIA.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C07D213/127 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07D COMPUESTOS HETEROCICLICOS (Compuestos macromoleculares C08). › C07D 213/00 Compuestos heterocíclicos que contienen ciclos de seis miembros, no condensados con otros ciclos, con un átomo de nitrógeno como el único heteroátomo del ciclo y tres o más enlaces dobles entre miembros cíclicos o entre miembros cíclicos y miembros no cíclicos. › Preparación a partir de compuestos que contienen ciclos piridínicos.
PDF original: ES-2420604_T3.pdf
Fragmento de la descripción:
Reacción de adición de amida La presente descripción se refiere a la adición de carboxamidas a vinilpiridinas.
Las p-mentano-carboxamidas N-sustituidas son bien conocidas en la técnica como compuestos que proporcionan una sensación refrescante a la piel o a las membranas mucosas del cuerpo. Se describen ejemplos típicos de este tipo de compuestos, por ejemplo, en la patente británica GB 1.421.744.
En la solicitud de patente internacional publicada WO 2007/or 9719 se dan a conocer compuestos de fórmula general I
en los que X, Y, Z, R1, R2, R3 y m son tal como se definen en dicho documento. En algunos ejemplos particulares, como mínimo dos de entre R1, R2 y R3 forman conjuntamente un radical cíclico.
Habitualmente, estos compuestos se han preparado por reacción de un cloruro de ácido carboxílico de mentano con 20 una monoamina adecuada. Un ejemplo de esto es la siguiente reacción:
Aunque esta reacción es eficaz, implica la utilización de materiales costosos.
Actualmente se ha puesto de manifiesto que es posible preparar estos compuestos por un procedimiento simple y económico. Por consiguiente, se da a conocer un procedimiento para preparar un compuesto de fórmula II
que comprende la reacción de un compuesto de fórmula RCONH2 con un compuesto de fórmula III
en el que X e Y se seleccionan independientemente de entre el grupo que comprende H, metilo (Me) , etilo (Et) , OMe, OEt y mezclas de los mismos, y en el que R es un resto de fórmula IV
en el que R1, R2 y R3 comprenden conjuntamente, como mínimo, 6 átomos de carbono, y se seleccionan de tal manera que
(a)
(i) R1 se selecciona entre el grupo que comprende H, Me, Et, isopropilo y alquilo C4-C5 ramificado;
y 5
(ii) R2 y R3 se seleccionan independientemente de entre el grupo que comprende Me, Et, isopropilo y alquilo C4 ramificado; o
(b) dos cualesquiera de entre R1, R2 y R3, o todos ellos, forman conjuntamente un radical monocíclico, 10 bicíclico o tricíclico que tiene hasta 10 átomos de carbono,
llevándose a cabo la reacción en un disolvente en presencia de una base.
También se describe un compuesto de fórmula II, tal como se ha definido anteriormente, que se puede preparar por 15 un procedimiento, tal como se ha definido anteriormente.
Los compuestos de fórmula III son vinilpiridinas, opcionalmente sustituidas. Se pueden utilizar la 2-vinilpiridina, o la 4-vinilpiridina, o derivados de las mismas.
El disolvente puede ser cualquier disolvente adecuado. El mismo puede ser capaz de disolver todos los reactivos y el producto de reacción. Entre los disolventes útiles se incluyen disolventes no reactivos que contienen oxígeno y nitrógeno, e hidrocarburos aromáticos. Entre los ejemplos no limitativos de disolventes se incluyen xileno, tolueno, dimetilformamida y tetrahidrofurano (THF) .
La cantidad de disolvente presente es cualquier cantidad adecuada.
La base que se puede utilizar en el presente procedimiento puede ser cualquier base adecuada. Entre los ejemplos típicos de bases adecuadas se incluyen metóxido de sodio, terc-butóxido de potasio, diisopropilamina de litio, hidruro de sodio, hidróxido de sodio e hidróxido de potasio. Un intervalo aceptable de concentración está comprendido entre aproximadamente 0, 01 y aproximadamente 0, 5 equivalentes.
Entre los ejemplos particulares de bases se incluyen hidróxido de sodio, hidróxido de potasio y terc-butóxido de potasio. Estos se pueden utilizar en intervalos de concentración comprendidos entre aproximadamente 0, 05 y aproximadamente 0, 25 equivalentes.
En realizaciones particulares, que comprenden la utilización de bases de sodio o potasio, la mezcla puede comprender un agente quelante. Esto permite obtener mayores rendimientos y tiempos de reacción menores. Entre los ejemplos de agentes quelantes adecuados se incluyen éteres de corona, tales como 18-corona-6, particularmente combinados con bases, tales como hidróxido de potasio y terc-butóxido de potasio.
Alternativamente, el propio disolvente se puede seleccionar de modo que tenga propiedades quelantes. Si se utilizan estos disolventes, el agente quelante se puede incluir en una cantidad reducida o incluso prescindir por completo de él. Entre los disolventes útiles a este respecto se incluyen la dimetilformamida (DMF) y la N-metilpirrolidona (NMP) . Se pueden utilizar combinaciones de todos o cualquiera de estos disolventes en cualquier proporción.
En una realización particular, la reacción se calienta o se lleva a cabo a presión, por ejemplo, en una bomba o en un recipiente de microondas cerrado herméticamente. Aunque, por lo general, tomar estas medidas no es esencial, hacerlo puede comportar mayores rendimientos y tiempos de reacción menores. Un intervalo de temperatura particular para el calentamiento es, como mínimo, de aproximadamente 50ºC, más particularmente de entre 50 aproximadamente 100ºC y aproximadamente 200ºC. Naturalmente, la utilización de temperaturas más elevadas afectará a la selección del disolvente, pero el experto en la materia será capaz de seleccionar disolventes adecuados para cada caso.
Son realizaciones particulares del compuesto aquellas en las que R se selecciona de acuerdo con la descripción que 55 se expone a continuación.
En realizaciones particulares, R es un resto seleccionado entre el grupo que comprende 2, 4-dimetilpent-3-ilo, 2, 3, 4dimetilpent-3-ilo, adamantilo, 2-isopropil-5-metilciclohexil-1-ilo y mezclas de los mismos.
Un ejemplo particular de la fórmula IV es el 2-isopropil-5-metil-ciclohexil-2-ilo (en una realización particular, la variante (1R, 2S, 5R) ) .
A continuación, se describe el presente procedimiento haciendo referencia a los siguientes ejemplos no limitativos. 5
Ejemplo 1
Preparación de N- (2-piridin-2-il-etil) -p-mentano-carboxamida [ (1R, 2S, 5R) -2-isopropil-5-metil-N- (2- (piridin-2il) etil) ciclohexanocarboxamida]:
En un matraz de fondo redondo de 153 ml, equipado con agitador magnético y condensador de reflujo, se introdujeron 0, 368 g de p-mentano-carboxamida, 4 ml de tolueno, 0, 32 ml de 2-vinilpiridina, 0, 027 g de 18-corona-6 y 0, 12 ml de terc-butóxido de potasio (20% en THF) . La mezcla se calentó a 110ºC durante 3 horas, obteniéndose un 97% de conversión determinada por cromatografía de gases (CG) .
Ejemplo 2
Preparación de N- (2-piridin-2-il-etil) -p-mentano-carboxamida [ (1R, 2S, 5R) -2-isopropil-5-metil-N- (2- (piridin-2il) etil) ciclohexanocarboxamida]:
En un vial de microondas Biotage de 53 ml, equipado con agitador magnético, se introdujeron 0, 1 g de p-mentanocarboxamida, 0, 55 ml de tolueno, 0, 45 ml de NMP, 0, 086 g de 2-vinilpiridina y 3, 1 mg de KOH. El vial se cerró herméticamente y se calentó en el equipo de microondas Biotage a 150ºC durante 10 minutos, obteniéndose un 90, 9% de conversión determinada por CG.
Ejemplo 3
Preparación de N- (2-piridin-2-il-etil) -p-mentano-carboxamida [ (1R, 2S, 5R) -2-isopropil-5-metil-N- (2- (piridin-2il) etil) ciclohexanocarboxamida]:
En un vial de microondas Biotage de 5 ml, equipado con agitador magnético, se introdujeron 0, 1 g de p-mentanocarboxamida, 1, 0 ml de THF, 0, 086 g de 2-vinilpiridina y 0, 1 equivalentes de terc-butóxido de potasio (KOtBu) (20% en THF) . El vial se cerró herméticamente y se calentó en el equipo de microondas Biotage a 160ºC durante 20 minutos, obteniéndose un 88% de conversión determinada por CG.
Ejemplo 4
Preparación de N- (2-piridin-2-il-etil) -p-mentano-carboxamida [ (1R, 2S, 5R) -2-isopropil-5-metil-N- (2- (piridin-2il) etil) ciclohexanocarboxamida]:
En un vial de microondas Biotage de 5 ml, equipado con agitador magnético, se introdujeron 0, 1 g de p-mentanocarboxamida, 1, 0 ml de NMP, 0, 086 g de 2-vinilpiridina y 0, 1 equivalentes de KOtBu (20% en THF) . El vial se cerró herméticamente y se calentó en el equipo de microondas Biotage a 150ºC durante 10 minutos, obteniéndose un 95, 3% de conversión determinada por CG.
Ejemplo 5
Preparación de N- (2-piridin-2-il-etil) -p-mentano-carboxamida [ (1R, 2S, 5R) -2-isopropil-5-metil-N- (2- (piridin-2il) etil) ciclohexanocarboxamida]:
En un vial de microondas Biotage de 5 ml, equipado con agitador magnético, se introdujeron 0, 1 g de p-mentanocarboxamida, 1, 0 ml de NMP, 0, 086 g de 2-vinilpiridina y 2, 2 mg de NaOH. El vial se cerró herméticamente y se calentó en el equipo de microondas Biotage a 150ºC durante 10 minutos, obteniéndose un 85, 7% de conversión determinada por CG.
Ejemplo 6
Preparación de N- (2-piridin-2-il-etil) -p-mentano-carboxamida [ (1R, 2S, 5R)... [Seguir leyendo]
Reivindicaciones:
1. Procedimiento de preparación de un compuesto de fórmula II
que comprende la reacción de un compuesto de fórmula RCONH2 con un compuesto de fórmula III
en el que X e Y se seleccionan independientemente de entre el grupo que comprende H, metilo, etilo, OMe, OEt y mezclas de los mismos, y en el que R es un resto de fórmula IV
en el que R1, R2 y R3 comprenden conjuntamente, como mínimo, 6 átomos de carbono, y en el que R1, R2 y R3 se seleccionan de tal manera que
(a) 20
(i) R1 se selecciona de entre el grupo que comprende H, Me, Et, isopropilo, alquilo C4-C5 ramificado y mezclas de los mismos; y
(ii) R2 y R3 se seleccionan independientemente de entre el grupo que comprende Me, Et, 25 isopropilo, alquilo C4 ramificado y mezclas de los mismos; o (b) dos cualesquiera de entre R1, R2 y R3, o todos ellos, forman conjuntamente un radical monocíclico, bicíclico o tricíclico que tiene hasta 10 átomos de carbono,
llevándose a cabo la reacción en un disolvente en presencia de una base.
2. Procedimiento, según la reivindicación 1, en el que R es un resto seleccionado de entre el grupo que comprende 2, 4-dimetilpent-3-ilo, 2, 3, 4-dimetilpent-3-ilo, adamantilo, 2-isopropil-5-metil-ciclohexil-1-ilo y mezclas de los mismos.
3. Procedimiento, según la reivindicación 2, en el que R es 2-isopropil-5-metil-ciclohexil-1-ilo en la forma (1R, 2S, 5R) .
4. Procedimiento, según la reivindicación 1, en el que la base se selecciona entre el grupo que comprende hidróxido de sodio, hidróxido de potasio, terc-butóxido de potasio y mezclas de los mismos. 40
5. Procedimiento, según la reivindicación 1, en el que la base se selecciona entre el grupo que comprende bases que contienen sodio y potasio, y el disolvente comprende, como mínimo, un agente quelante.
6. Procedimiento, según la reivindicación 5, en el que el agente quelante se selecciona entre el grupo que
comprende disolventes con propiedades quelantes y agentes quelantes añadidos independientemente, y que es preferentemente un éter de corona.
7. Procedimiento, según la reivindicación 1, en el que la reacción se lleva a cabo en condiciones seleccionadas,
como mínimo, entre una de entre una temperatura elevada y una presión elevada, siendo la temperatura, 50 preferentemente, de como mínimo 50ºC, y estando comprendida, más preferentemente, entre 100ºC y 200ºC.
Patentes similares o relacionadas:
Proceso de fabricación para derivados de triazina, pirimidina y piridina, del 9 de Enero de 2019, de Universität Basel: Un método para fabricar un compuesto de fórmula (I)**Fórmula** o un estereómero, tautómero o una sal del mismo, en la que, U es CRU o N, […]
Procedimiento para la desoxigenación de N-óxidos de piridina, quinolina e isoquinolina., del 20 de Julio de 2017, de UNIVERSIDAD DE BURGOS: La presente invención se refiere a un procedimiento para la desoxigenación catalítica de N-óxidos de piridina, quinolina e isoquinolina a los correspondientes compuestos […]
Procedimiento para la preparación de compuestos fluoro-, cloro- y fluorocloro-alquilados mediante catálisis heterogénea, del 8 de Febrero de 2017, de LONZA LTD.: Procedimiento para la preparación de un compuesto fluoro-, cloro- o fluorocloro-alquilado mediante una reacción de un compuesto COMPSUBST con […]
Procedimiento mejorado para preparar 1-(6-metilpiridin-3-il)-2-[4-(metilsulfonil)fenil]etanona, un compuesto intermedio de etoricoxib, del 30 de Septiembre de 2013, de F.I.S. FABBRICA ITALIANA SINTETICI S.P.A: Procedimiento para preparar 1-(6-metilpiridin-3-il)-2-[4-(metilsulfonil)fenil]etanona de fórmula (I) o una sal de lamisma: **Fórmula** que comprende […]
METODO DE PRODUCCION Y METODO DE SEPARACION DE DERIVADOS DE 2,4'-DIPIRIDILO Y METODOS DE PRODUCCION DE DERIVADOS DE BENZOXAZEPINA Y SUS SALES., del 1 de Marzo de 2006, de SUNTORY LIMITED: UN PROCEDIMIENTO DE PRODUCCION DE DERIVADOS DE 2,4' - DIPIRIDILO MEDIANTE UNA REACCION DE ACOPLAMIENTO CRUZADO DE UN DERIVADO DE 2 - HALOPIRIDINA Y UNA […]
NUEVAS PIRIDILCICLOALQUILETILAMINAS PURAS EN CUANTO A LOS ENANTIOMEROS Y SUS SALES, ASI COMO PROCEDIMIENTO PARA SU PREPARACION., del 16 de Junio de 2001, de BOEHRINGER INGELHEIM PHARMA KG: LA PRESENTE INVENCION SE REFIERE A NUEVAS AMINAS PIRIDILO CICLOALQUILOETILO ENANTIOMERAS PURAS DE LA FORMULA GENERAL 1A Y 1B A SUS SALES, ASI COMO PROCESO PARA […]
PROCEDIMIENTO PARA LA PREPARACION DE ESTERES INSATURADOS DE ACIDOS 4-(3', 5'-DIHALOGENPIRIDIL-2'-OXI)-0(-FENOXI-PROPION Y -PROPIONTIO-LICOS., del 16 de Octubre de 1979, de CIBA-GEIGY AG: Procedimientos para la preparación de esteres insaturados de ácidos 4-(3,5-dihalogenpiridil-2-oxi)-alfa-fenoxi-propión- y propiontiólicos, […]
PROCEDIMIENTO PARA LA PRODUCCIÓN DE ALQUENIL-PIRIDINAS, del 16 de Marzo de 1960, de SICEDISON, S. P. A: Procedimiento para la producción de alquenil-piridinas, caracterizado por una o varias de las operaciones siguiente: a) paso de vapores de alkil-piridina […]