Métodos para producir microfolículos pilosos y papilas de novo y su uso para ensayos in vitro e implantaciones in vivo.
Papila de novo que comprende un agregado celular de fibroblastos de papila pilosa dérmica (DPF) de mamífero,
exhibiendo el agregado celular la forma y el tamaño de una papila dérmica (DP) fisiológica de un folículo piloso tras su aislamiento y después de su recubrimiento con proteínas de matriz extracelular, preferiblemente colágeno IV, fibronectina y/o laminina, donde la papila de novo se produce mediante un método que comprende las etapas de:
(a) proporcionar al menos una papila dérmica (DP) de al menos un folículo piloso de mamífero,
(b) aislar fibroblastos de papila pilosa dérmica (las DPF) de la DP por fijación de manera mecánica de dicha DP en la superficie de un recipiente de cultivo celular, según lo cual la lámina basal se perfora para permitir que migren dichas DPF,
(c) extender las DPF aisladas en cultivo monocapa sin recubrimiento de colágeno, en el que dichas DPF se hacen pasar al menos una vez,
(d) condensar las DPF extendidas en un agregado celular que presentan el tamaño y la forma de la DP fisiológica, en los que dichas DPF se diferencian en recipientes de cultivo no adhesivo en una concentración de células por superficie del recipiente de 1.000 a 100.000 DPF/cm2, y
(e) recubrir la papila de novo con proteínas de matriz extracelular, preferiblemente colágeno IV, fibronectina y/o laminina.
Tipo: Patente Europea. Resumen de patente/invención. Número de Solicitud: E12150985.
Solicitante: TECHNISCHE UNIVERSITAT BERLIN.
Nacionalidad solicitante: Alemania.
Dirección: Strasse des 17. Juni 135 10623 Berlin ALEMANIA.
Inventor/es: LINDNER,Gerd, LAUSTER,Roland.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61L27/36 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61L PROCEDIMIENTOS O APARATOS PARA ESTERILIZAR MATERIALES U OBJECTOS EN GENERAL; DESINFECCION, ESTERILIZACION O DESODORIZACION DEL AIRE; ASPECTOS QUIMICOS DE VENDAS, APOSITOS, COMPRESAS ABSORBENTES O ARTICULOS QUIRURGICOS; MATERIALES PARA VENDAS, APOSITOS, COMPRESAS ABSORBENTES O ARTICULOS QUIRURGICOS (conservación de cuerpos o desinfección caracterizada por los agentes empleados A01N; conservación, p. ej. esterilización de alimentos o productos alimenticios A23; preparaciones de uso medico, dental o para el aseo A61K). › A61L 27/00 Materiales para prótesis o para revestimiento de prótesis (prótesis dentales A61C 13/00; forma o estructura de las prótesis A61F 2/00; empleo de preparaciones para la fabricación de dientes artificiales A61K 6/80; riñones artificiales A61M 1/14). › que contienen ingredientes de composición indeterminada o sus productos de reacción.
- A61L27/38 A61L 27/00 […] › Células animales (para utilizar en piel artificial A61L 27/60).
- A61L27/60 A61L 27/00 […] › Materiales utilizables en piel artificial.
- C12N5/071 QUIMICA; METALURGIA. › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 5/00 Células no diferenciadas humanas, animales o vegetales, p. ej. líneas celulares; Tejidos; Su cultivo o conservación; Medios de cultivo para este fin (reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00). › Células o tejidos de vertebrados, p.ej. células o tejidos humanos.
PDF original: ES-2549055_T3.pdf
Fragmento de la descripción:
Métodos para producir microfolículos pilosos y papilas de novo y su uso para ensayos in vitro e implantaciones in vivo 5
La presente invención se refiere a un método para producir microfolículos pilosos por co-cultivo de las papilas de novo con otra población celular del folículo piloso en los recipientes para cultivo de adhesión ultra-baja. La invención también se refiere a un método para producir papilas de novo utilizables en un método para producir microfolículo piloso. Son objeto de la invención también los microfolículos pilosos y las papilas de novo producidas por los métodos mencionados. Los microfolículos pilosos y/o las papilas de novo se pueden usar como implantes para tratar 10 condiciones de cabello reducidas y para el ensayo in vitro de los efectos moduladores del cabello o los efectos tóxicos de sustancias.
Debido a la función crítica que desempeña el cabello en la comunicación humana no verbal, un individuo afectado demanda invariablemente ayuda cuando disminuye el crecimiento del cabello. El último tratamiento es, por supuesto, 15 restablecer o regenerar folículos pilosos cíclicos, sanos, nuevos. Hasta muy recientemente, la medicina no podía ofrecer tratamientos válidos a estos pacientes. A finales del siglo veinte, se comercializaron diversos fármacos que, sin embargo modestamente e inconsecuentemente, estimulaban el crecimiento del cabello. Son ejemplos minoxidil, finasteride y latanoprost. La compleja sincronización y los cambios de expresión de los genes de myriad requeridos para la orquestación del desarrollo y la ciclación de folículo piloso es probable que impidan una solución 20 farmacéutica simple al tratamiento de la alopecia avanzada. Por consiguiente, sus efectos quedan muy lejos del objetivo último de generar nuevos folículos pilosos en el cuero cabelludo calvo. Aprovechando los tipos de células que se conoce cómo forman un folículo piloso, los tratamientos con base celular llegarán a la clínica más pronto que la solución puramente molecular.
Una solución al tratamiento con base celular de folículo piloso implicaría eliminar un pequeño número de folículos pilosos, aislar células competentes y/o inductivas de los mismos y extender después esas células ex vivo al tiempo que mantener su especial capacidad para generar nuevos folículos pilosos. Claramente, las condiciones del cultivo celular que mantienen la capacidad inductiva de las células dérmicas del folículo y la competencia de las células epiteliales del folículo piloso son necesarias antes de que se pueda desarrollar cualquier tipo de tratamiento con 30 base celular para la alopecia. Como estudios recientes demostraron que la propiedad inductiva de las células dérmicas disminuye con el tiempo in vitro, la investigación se ha centrado en mantener las propiedades tricogénicas de las células de folículo piloso en el cultivo. La mayor parte del progreso reciente ha resultado de avances en la metodología de cultivo para folículos pilosos intactos y sus componentes celulares. Las células de folículo piloso humanas desarrolladas en cultivo incluyen fibroblastos de papila folicular, queratinocitos de envoltura externa de la 35 raíz (ORS, por sus siglas en inglés) y células epidérmicas germinativas de la matriz del cabello (Tobin et al., J. Invest. Dermatology 104 (1) , 86-88, 1.995) .
El objetivo de los esfuerzos de la bioingeniería actual es generar o reconstituir sistemas de órganos completamente organizados y funcionales partiendo de células disociadas que se han propagado en condiciones de cultivo de tejido 40 definidas. Desde hace tiempo se ha reconocido que el folículo piloso presenta una profunda capacidad regenerativa, porque se cicla por la duración de la vida del individuo y reproduce su medio ciclo inferior después del ciclo. Los fibroblastos de las papilas pilosas dérmicas y la envoltura de tejido conjuntivo son de tipo hemocitoblasto en naturaleza y presentan propiedades de inducción del crecimiento del cabello específicas. El folículo piloso se vuelve a formar mediante interacciones entre hemocitoblastos epiteliales competentes y células dérmicas poderosamente 45 inductivas durante su ciclo de crecimiento. Es posible reconstituir un folículo piloso completo de hemocitoblastos epiteliales y mesenquimales de folículos pilosos.
Las principales estimulaciones que se requiere estudiar con cualquier tipo de tratamiento basado en células para la alopecia incluyen la eficacia de la formación de folículo piloso y la elección del tipo de célula, que se resume por 50 Stenn & Cotsarelis, Curr. Opinion Biotech. 16, 493-497, 2.005. Para la bioingeniería del folículo piloso, se podía empezar con elementos dérmicos de folículos disociados con o sin células competentes del folículo u otras fuentes epiteliales. El número de células disociadas se extendería en el cultivo y después las células dérmicas solas, o junto con células epiteliales competentes, se volverían a introducir en el cuero cabelludo alopécico. Los estudios previos han demostrado que partir de células dérmicas inductoras colocadas correctamente dará como resultado la 55 formación de nuevo folículo. Por otra parte, partir de una combinación de células epiteliales y dérmicas tricogénicas, disociadas o agregadas, también ha demostrado ser una manera eficaz de producir nuevos folículos pilosos.
Los primeros intentos en las soluciones basadas en células para tratar la alopecia son probablemente usar tejido autólogo para bioingeniería de folículos pilosos para evitar el rechazo inmunológico de las células donadoras. Sin 60 embargo, existe la interesante posibilidad de que se pueda desarrollar tejido de folículo piloso heterólogo (alogénico) para trasplante de tejido, basado en el concepto de que el folículo piloso es un sitio inmuno-privilegiado que no expresa antígenos de clase I MHC (complejo principal de histocompatibilidad, por sus siglas en inglés) . Sin embargo, el ensayo de seguridad y los obstáculos reguladores para este tipo de solución requerirían enormes recursos financieros. 65
Otra posible solución para los folículos pilosos de bioingeniería implica formar en realidad folículos pilosos como miniórganos in vitro y trasplantar después los folículos recién generados de nuevo en el cuero cabelludo alopécico. Se conoce a partir de la patente alemana DE 101 62 814 B4 que se puede producir un equivalente de piel y cabello proporcionando una pseudodermis o una preparación de pseudodermis, así como pseudopapilas que comprenden células de papilas dérmicas cultivadas sobre un portador adecuado o en una matriz adecuada o precursores de 5 pseudopapilas que comprenden células de papilas dérmicas cultivadas en un medio formador de matriz adecuado, capaz de formar una matriz in situ e introducir las pseudopapilas o el precursor de las pseudopapilas en la pseudodermis o preparación de pseudodermis. Esta clase de solución requeriría un sistema de cultivo de células mucho más complicado implicando matrices tridimensionales, quizá embebidas con factores de crecimiento apropiados, para permitir que células tanto dérmicas como epidérmicas se diferencien hacia la estructura 10 tridimensional de un folículo piloso normal. En particular, la estructura de la papila sólo se obtiene formando cavidades, tal como por punzonado o pinchazo, en dicha pseudodermis y poniendo dichas pseudopapilas en las mismas, que están conformadas para que sus dimensiones correspondan a las cavidades formadas en los PD. La solución carece de disposición voluntaria de las células en la estructura de papila fisiológica aproximada, así como contactos directos con las células. 15
Se ha mostrado recientemente otro método para producir una población de hemocitoblastos multipotentes o progenie de los mismos, que proceden de un folículo piloso o una porción que contiene papilas dérmicas del mismo. El método de la patente internacional WO 2005/071063 A1 comprende el cultivo de dicho folículo piloso o porción que contiene papilas dérmicas en condiciones bajo las cuales crecen hemocitoblastos multipotentes y proliferan sin 20 adherirse. No se obtienen papilas dérmicas por este procedimiento, sino los hemocitoblastos multipotentes aislados usados directamente para inducir el crecimiento del cabello o la regeneración de piel en un mamífero. Sin embargo, también se reconoce en este documento que se forma una cierta cantidad de células adherentes como se confirma en la patente internacional WO 2005/113747 A2, que describe un método para producir agregados multicelulares a partir de al menos dos tipos de hemocitoblastos adultos multipotentes o pluripotentes por cultivo en condiciones 25 estéricas. En el momento presente, los cuerpos organoides están restringidos a los hemocitoblastos mencionados... [Seguir leyendo]
Reivindicaciones:
1. Papila de novo que comprende un agregado celular de fibroblastos de papila pilosa dérmica (DPF) de mamífero, exhibiendo el agregado celular la forma y el tamaño de una papila dérmica (DP) fisiológica de un folículo piloso tras su aislamiento y después de su recubrimiento con proteínas de matriz extracelular, preferiblemente 5 colágeno IV, fibronectina y/o laminina, donde la papila de novo se produce mediante un método que comprende las etapas de:
(a) proporcionar al menos una papila dérmica (DP) de al menos un folículo piloso de mamífero, 10
(b) aislar fibroblastos de papila pilosa dérmica (las DPF) de la DP por fijación de manera mecánica de dicha DP en la superficie de un recipiente de cultivo celular, según lo cual la lámina basal se perfora para permitir que migren dichas DPF,
(c) extender las DPF aisladas en cultivo monocapa sin recubrimiento de colágeno, en el que dichas DPF se 15 hacen pasar al menos una vez,
(d) condensar las DPF extendidas en un agregado celular que presentan el tamaño y la forma de la DP fisiológica, en los que dichas DPF se diferencian en recipientes de cultivo no adhesivo en una concentración de células por superficie del recipiente de 1.000 a 100.000 DPF/cm2, y 20
(e) recubrir la papila de novo con proteínas de matriz extracelular, preferiblemente colágeno IV, fibronectina y/o laminina.
2. Papila de novo de la reivindicación 1, donde en la etapa (d) las DPF expandidas se condensan durante al menos 25 48h.
3. Papila de novo de la reivindicación 1 o 2, donde en la etapa (d) las DPF expandidas se condensan durante 2-21 días. 30
4. Papila de novo según una de las reivindicaciones 1-3, donde en la etapa (d) se condensan DPF no inductivas.
5. Microfolículo piloso compuesto por una papila de novo de una de las reivindicaciones 1-4 que está cubierta de forma estable por células de al menos otra población celular seleccionada del grupo de fibroblastos, queratinocitos y/o melanocitos, donde el microfolículo piloso se produce mediante un método que comprende las etapas de: 35
(a) proporcionar al menos una papila de novo de una de las reivindicaciones 1-4, (b) proporcionar al menos otra población celular seleccionada del grupo de fibroblastos, queratinocitos y/o melanocitos, y (c) co-cultivar la papila de novo de una de las reivindicaciones 1-4 con la otra u otras poblaciones celulares 40 en condiciones de cultivo no adherente.
6. Microfolículos pilosos según la reivindicación 5, donde la otra u otras poblaciones celulares se pueden derivar y/o se derivan de un folículo piloso de un mamífero, que se seleccionan del grupo de fibroblastos de la envoltura del tejido conjuntivo, queratinocitos y/o melanocitos. 45
7. Equivalente de piel que comprende un microfolículo piloso según una de las reivindicaciones 5-6 o una papila de novo según una de las reivindicaciones 1-4.
8. Implante que comprende como ingrediente activo un microfolículo piloso según una de las reivindicaciones 5-6 y/o 50 una papila de novo según una de las reivindicaciones 1-4, opcionalmente junto con adyuvantes farmacéuticamente tolerables.
9. Trasplante que comprende como ingrediente activo una cantidad eficaz de un equivalente de piel según la reivindicación 7, opcionalmente junto con adyuvantes farmacéuticamente tolerables. 55
10. Microfolículo piloso según una de las reivindicaciones 5-6, papila de novo según una de las reivindicaciones 1-4 y/o equivalente de piel según la reivindicación 7 para el tratamiento profiláctico o terapéutico de una afección de una cantidad de cabello reducida.
11. Kit que comprende un microfolículo piloso según una de las reivindicaciones 5-6, una papila de novo según una de las reivindicaciones 1-4, el equivalente de piel según la reivindicación 7, el implante según la reivindicación 8 y/o el trasplante según la reivindicación 9.
12. Uso de un microfolículo piloso según una de las reivindicaciones 5-6, una papila de novo según una de las reivindicaciones 1-4 y/o el equivalente de piel según la reivindicación 7 para la evaluación in vitro de los efectos moduladores del cabello de sustancias.
13. Uso de un microfolículo piloso según una de las reivindicaciones 5-6, una papila de novo según una de las 5 reivindicaciones 1-4 y/o el equivalente de piel según la reivindicación 7 para la evaluación in vitro de los efectos tóxicos de sustancias.
14. Método para la identificación sistemática de alto rendimiento de sustancias, que modulan propiedades del cabello, que comprende las etapas de: 10
proporcionar una muestra de papilas de novo según una de las reivindicaciones 1-4, microfolículos pilosos según una de las reivindicaciones 5-6 y/o el equivalente de piel según la reivindicación 7, dividir la respectiva muestra en porciones, incubar al menos una porción con sustancias que se han de someter a identificación sistemática y comparar parámetros de propiedades del cabello en la porción con otra porción que no se ha 15 incubado con las sustancias.
Patentes similares o relacionadas:
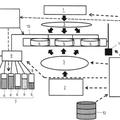 Procedimiento y dispositivo para producir un objeto multicelular tridimensional, del 29 de Julio de 2020, de TECHNISCHE UNIVERSITAT BERLIN: Procedimiento para producir un objeto multicelular tridimensional, con los pasos siguientes:
a) introducción de un primer líquido fotopolimerizable […]
Procedimiento y dispositivo para producir un objeto multicelular tridimensional, del 29 de Julio de 2020, de TECHNISCHE UNIVERSITAT BERLIN: Procedimiento para producir un objeto multicelular tridimensional, con los pasos siguientes:
a) introducción de un primer líquido fotopolimerizable […]
Matriz de soporte de injerto para reparación de cartílago y procedimiento de obtención de la misma, del 1 de Julio de 2020, de ETH ZURICH: Un procedimiento de proporción de una matriz de soporte de injerto para reparación de cartílagos, particularmente en un paciente humano, que comprende las etapas de: […]
Procedimiento de preparación de un material de aloinjerto, producto obtenido, y usos del mismo, del 27 de Mayo de 2020, de TBF Genie Tissulaire (TBF): Procedimiento de preparación de un material de aloinjerto que forma una membrana viroinactivada, liofilizada y estéril procedente de placenta de mamífero y constituida […]
Preparación de supercóntigos de tejido regenerativo, del 20 de Mayo de 2020, de LIFECELL CORPORATION: Un supercóntigo de tejido seco, que comprende: una "acellular tissue matrix" (matriz de tejido acelular - ATM) en forma de partículas; y un polímero; en donde […]
COMPOSICIÓN A BASE DE BIOPOLÍMEROS RECOMBINANTES Y USOS DE LA MISMA COMO BIOTINTA, del 23 de Abril de 2020, de UNIVERSIDAD DE VALLADOLID: La presente invención se refiere a composiciones que comprenden biopoiímeros recombinantes formados por combinaciones de monómeros de tipo "Recombinámeros […]
Composiciones y métodos para el tratamiento de huecos óseos y fracturas abiertas, del 22 de Abril de 2020, de Polypid Ltd: Una composición farmacéutica que comprende partículas de relleno óseo recubiertas y no recubiertas en una proporción entre aproximadamente 1:3 […]
Procedimientos de preparación de un hidrogel esterilizado de modo terminal que proviene de matriz extracelular, del 22 de Abril de 2020, de UNIVERSITY OF PITTSBURGH OF THE COMMONWEALTH SYSTEM OF HIGHER EDUCATION: Un procedimiento de preparación de un material digerido de matriz extracelular esterilizado de modo terminal capaz de gelificar, que comprende: (i) solubilizar la matriz […]
COMPOSICIÓN A BASE DE BIOPOLÍMEROS RECOMBINANTES Y USOS DE LA MISMA COMO BIOTINTA, del 20 de Abril de 2020, de UNIVERSIDAD DE VALLADOLID: Composición a base de biopolímeros recombinantes y usos de la misma como biotinta. La presente invención se refiere a composiciones que comprenden […]