Proceso para preparar compuestos de oxazolidina éster y su conversión en florfenicol.
Un proceso para preparar un compuesto de Fórmula XI:**Fórmula**
en la que:
R1 es -SO2CH3; y
R7 es CHCl2; comprendiendo dicho proceso:
a) hacer reaccionar un compuesto de Fórmula VI:**Fórmula**
en la que:
R1 es como se ha definido anteriormente;
R5 es hidrógeno, alquilo C1-6, cicloalquilo C3-8, bencilo, fenilo o fenilalquilo C1-6 con un reactivo de formación de oxazolidina para formar un compuesto de Fórmula XIV:**Fórmula**
en la que:
R1 y R5 son como se han definido anteriormente;
R2 es hidrógeno, grupos alquilo C1-6, haloalquilo C1-6, cicloalquilo C3-8, alquenilo C2-6, alquinilo C2-6, alcoxi C1-6, aralquilo C1-6, aralquenilo C2-6, arilo o heterocíclico C2-6;
R3 es hidrógeno, grupos alquilo C1-6, haloalquilo C1-6, cicloalquilo C3-8, alquenilo C2-6, alquinilo C2-6, alcoxi C1-6, aralquilo C1-6, aralquenilo C2-6, arilo o heterocíclico C2-6;
b) reducir in situ el compuesto de Fórmula XIV con un agente reductor en un disolvente alcohólico para formar un compuesto de Fórmula VIII:**Fórmula**
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2006/034370.
Solicitante: INTERVET INTERNATIONAL BV.
Nacionalidad solicitante: Países Bajos.
Dirección: WIM DE KORVERSTRAAT 35 5831 AN BOXMEER PAISES BAJOS.
Inventor/es: TOWSON, JAMES, C.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C07C315/00 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07C COMPUESTOS ACICLICOS O CARBOCICLICOS (compuestos macromoleculares C08; producción de compuestos orgánicos por electrolisiso electroforesis C25B 3/00, C25B 7/00). › Preparación de sulfonas; Preparación de sulfóxidos.
PDF original: ES-2459205_T3.pdf
Fragmento de la descripción:
Proceso para preparar compuestos de oxazolidina éster y su conversión en florfenicol 5 Campo técnico La presente invención se refiere a un nuevo proceso para preparar Florfenicol.
Antecedentes de la invención Florfenicol es un antibiótico de amplio espectro de Fórmula I
Tiene una aplicación de gran envergadura en medicina veterinaria para el tratamiento de bacterias tanto Gram positivas como Gram negativas así como infecciones por rickettsias. Florfenicol también se conoce como [R- (R*, S*) ]2, 2-Dicloro-N-[1- (fluorometil) -2-hidroxi-2-[4- (metilsulfonil) fenil]etil]acetamida.
La patente de Estados Unidos de cesión común Nº 5.663.361, cuya divulgación se incorpora en el presente documento por referencia, describe la síntesis de compuestos intermedios de Florfenicol y su uso en procesos para preparar Florfenicol. La ventaja principal que se analiza en la misma es que el proceso eliminó el requisito de la técnica anterior de aislar la aminodiol sulfona (ADS) del recipiente de reacción antes de continuar con la síntesis de Florfenicol.
Más recientemente, la patente de Estados Unidos Nº 2005/0075506 A1 describió un proceso para preparar un compuesto de Fórmula II que es útil como un compuesto intermedio en la síntesis de Florfenicol.
El proceso requiere la reacción de la sal de clorhidrato compuesto de aminodiol ópticamente puro de Fórmula III con acetona seguido de cloruro de acetilo para dar un compuesto de Fórmula II. El compuesto de Fórmula II se hace reaccionar a continuación adicionalmente para dar Florfenicol de Fórmula I.
Un inconveniente principal del proceso que se desvela en el documento 2005/0075506 A1 es el uso del material de partida aminodiol de Fórmula III. El compuesto de aminodiol de Fórmula III es caro. Además, es difícil de aislar y de manipular debido a su naturaleza anfótera.
La presente invención aborda esta limitación y además proporciona un método alternativo adicional para preparar compuestos intermedios útiles incluidos en la síntesis de Florfenicol.
Sumario de la invención La presente invención se refiere a un proceso para preparar Florfenicol, comprendiendo dicho proceso: a) hacer reaccionar un compuesto de Fórmula VI:
en la que:
R1 es SO2CH3;
R5 es hidrógeno, alquilo C1-6, cicloalquilo C3-8, bencilo, fenilo o fenilalquilo C1-6 con un reactivo de formación de oxazolidina para formar un compuesto de Fórmula XIV:
en la que:
R1 y R5 son como se han definido anteriormente; R2 es hidrógeno, grupo alquilo C1-6, haloalquilo C1-6, cicloalquilo C3-8, alquenilo C2-6, alquinilo C2-6, alcoxi C1-6, aralquilo C1-6, aralquenilo C2-6, arilo, o heterocíclico C2-6;
R3 es hidrógeno, grupo alquilo C1-6, haloalquilo C1-6, cicloalquilo C3-8, alquenilo C2-6, alquinilo C2-6, alcoxi C1-6, aralquilo C1-6, aralquenilo C2-6, arilo o heterocíclico C2-6;
b) reducir in situ el compuesto de Fórmula XIV con un agente reductor en un disolvente alcohólico para formar un compuesto de Fórmula VIII: 30
en la que: R1, R2 y R3 son como se han definido anteriormente; c) hacer reaccionar el compuesto de Fórmula VIII in situ con un agente de N-acilación para formar un compuesto aminodiol protegido con oxazolidina de Fórmula XII:
en la que: R1, R2 y R3 son como se han definido anteriormente; y R7 es CHCl2; d) fluorar el compuesto de Fórmula XII con un agente de fluoración en presencia de un disolvente orgánico para obtener un compuesto de Fórmula XIII:
en la que:
R1, R2, R3 y R7 son como se han definido anteriormente; y
e) hidrolizar selectivamente el compuesto de Fórmula XIII con un catalizador ácido o básico para formar Florfenicol.
En la actualidad, los solicitantes han encontrado sorprendentemente ventajas de procesamiento significativas para la 20 formación de compuestos de aminodiol protegidos con oxazolidina de Fórmula XII. Los compuestos de Fórmula XII,
o específicamente de Fórmula II, se obtienen cuando un precursor de éster para el compuesto de base libre de aminodiol de Fórmula III se usa como material de partida. Dichos ésteres corresponden generalmente a la Fórmula VI, y el éster de Fórmula IV es un éster particularmente preferente:
El uso de los ésteres de Fórmulas IV y VI generan el material de partida de base libre caro de Fórmula III in situ, eliminando de este modo la necesidad de aislar este compuesto difícil de aislar. Las pérdidas de rendimiento para el material de partida de base libre de Fórmula III debido al aislamiento se eliminan de este modo dando como resultado un rendimiento mayor y un coste menor para el compuesto de aminodiol protegido con oxazolidina de Fórmula XII, o específicamente el compuesto de Fórmula II.
Por lo tanto, la presente invención tiene la ventaja de ser un proceso eficaz y económico para preparar Florfenicol, sus análogos y compuestos intermedios de oxazolidina relacionados con el mismo.
Descripción detallada de las realizaciones Cuando se usan en la presente memoria descriptiva y en las reivindicaciones adjuntas, los términos que se indican a continuación en el presente documento, a menos que se indique de otro modo, se definen tal como sigue a continuación:
La expresión "disolvente alcohólico" incluye alcoholes C1 aC10 tales como metanol y etanol y mezclas de los mismos, dialcoholes C2 aC10 tales como etilenglicol y trialcoholes C1 aC10 tales como glicerina. Como alternativa, el disolvente alcohólico se puede mezclar con cualquier cosolvente adecuado. Dichos cosolventes pueden incluir otros disolventes que son miscibles con el disolvente alcohólico tales como alcanos C4 aC10, disolventes aromáticos tales como benceno, tolueno, xilenos, halobencenos tales como clorobenceno, y éteres tales como éter dietílico, éter terc-butilmetílico, éter isopropílico y tetrahidrofurano, o mezclas de cualquiera de los disolventes o cosolventes anteriores.
El término "alquilo" se refiere a un alquilo lineal o ramificado tal como metilo, etilo, propilo, o sec-butilo. Como alternativa, se puede especificar el número de carbonos en el alquilo. Por ejemplo, "alquilo C1 a C6" se refiere a un "alquilo" tal como se ha descrito anteriormente que contiene de 1 a 6 átomos de carbono. "Haloalquilo" se refiere a un "alquilo" tal como se ha descrito anteriormente en el que uno o más hidrógenos se reemplazan con halo.
El término "arilo" se refiere a fenilo, o fenilo sustituido con alquilo C1 a C6 o halo. "Bencilo sustituido" se refiere a bencilo sustituido con alquilo C1 a C6 o halo. El término "halo" se refiere a flúor, cloro, bromo o yodo. El término "halo arilo" se refiere a fenilo sustituido con halo.
El proceso que corresponde con la invención incluye las etapas de:
a) hacer reaccionar un compuesto de Fórmula VI en un recipiente con un reactivo de formación de oxazolidina para formar el compuesto de Formula XIV:
en la que:
R1, R2, R3 y R5 son como se han definido anteriormente;
b) hacer reaccionar el compuesto de Fórmula XIV en el recipiente sin aislamiento (es decir, in situ) con un agente 30 reductor en un disolvente alcohólico para formar un compuesto de Fórmula VIII:
en la que R1, R2 y R3 son como se han definido anteriormente; c) hacer reaccionar el compuesto de Fórmula VIII en el recipiente sin aislamiento (es decir, in situ) con un tercer agente de N-acilación para formar un compuesto de aminodiol protegido con oxazolidina de Fórmula XII:
en la que R1, R2, R3 y R7 son como se han definido anteriormente; d) fluorar el compuesto de Fórmula XII con un agente de fluoración en presencia de un disolvente orgánico para obtener un compuesto de Fórmula XIII:
en la que R1, R2, R3 y R7 son como se han definido anteriormente; e) hidrolizar selectivamente el compuesto de Fórmula XIII con un catalizador ácido o básico para formar el compuesto de Fórmula XI:
en la que R1 y R7 son como se han definido anteriormente; y f) si fuera necesario, purificar el compuesto de Fórmula XI con una mezcla de mono, di o trialcohol de alquilo C110 y agua para formar el compuesto puro de Fórmula XI.
En la realización preferente que se ha descrito anteriormente, existen determinados aspectos preferentes de la invención. Un aspecto preferente es que el compuesto de Fórmula VI reacciona en un recipiente con un reactivo de formación de oxazolidina. En la realización de la invención se puede usar una amplia gama de reactivos adecuados de formación de oxazolidina. Una lista no limitante de reactivos adecuados de formación de oxazolidina incluyen formaldehído, acetona, 2-metoxipropeno, 2, 2-dimetoxipropano, 2, 2-dietoxipropano y mezclas de los mismos. El disolvente... [Seguir leyendo]
Reivindicaciones:
1. Un proceso para preparar un compuesto de Fórmula XI:
en la que: R1 es -SO2CH3; y 10 R7 es CHCl2; comprendiendo dicho proceso: a) hacer reaccionar un compuesto de Fórmula VI:
en la que:
R1 es como se ha definido anteriormente; R5 es hidrógeno, alquilo C1-6, cicloalquilo C3-8, bencilo, fenilo o fenilalquilo C1-6 con un reactivo de formación de oxazolidina para formar un compuesto de Fórmula XIV:
en la que:
R1 y R5 son como se han definido anteriormente; R2 es hidrógeno, grupos alquilo C1-6, haloalquilo C1-6, cicloalquilo C3-8, alquenilo C2-6, alquinilo C2-6, alcoxi C1-6, aralquilo C1-6, aralquenilo C2-6, arilo o heterocíclico C2-6; R3 es hidrógeno, grupos alquilo C1-6, haloalquilo C1-6, cicloalquilo C3-8, alquenilo C2-6, alquinilo C2-6, alcoxi C1-6, aralquilo C1-6, aralquenilo C2-6, arilo o heterocíclico C2-6;
b) reducir in situ el compuesto de Fórmula XIV con un agente reductor en un disolvente alcohólico para formar un compuesto de Fórmula VIII:
en la que: R1, R2 y R3 son como se han definido anteriormente; c) hacer reaccionar el compuesto de Fórmula VIII in situ con un agente de N-acilación para formar un compuesto de aminodiol protegido con oxazolidina de Fórmula XII:
en la que:
R1, R2, R3 y R7 son como se han definido anteriormente;
d) fluorar el compuesto de Fórmula XII con un agente de fluoración en presencia de un disolvente orgánico para obtener un compuesto de Fórmula XIII:
en la que:
R1, R2, R3 y R7 son como se han definido anteriormente; y
e) hidrolizar selectivamente el compuesto de Fórmula XIII con un catalizador ácido o básico para formar el compuesto de Fórmula XI.
2. El proceso de la reivindicación 1, en el que R2 y R3 son H, metilo, etilo o propilo.
3. El proceso de la reivindicación 2, en el que R2 y R3 son metilo.
4. El proceso de la reivindicación 1, en el que R5 es metilo, etilo, n-propilo, isopropilo, butilo, t-butilo o pentilo.
5. El proceso de la reivindicación 1, en el que el compuesto de Fórmula VI es
6. El proceso de la reivindicación 1, en el que el compuesto de Fórmula VI es
7. El proceso de la reivindicación 1, en el que el reactivo de formación de oxazolidina se selecciona entre el grupo
que consiste en formaldehído, acetona, 2-metoxipropeno, 2, 2-dimetoxipropano, 2, 2-dietoxipropano y mezclas de los 10 mismos.
8. El proceso de la reivindicación 7, en el que el reactivo de formación de oxazolidina es 2, 2-dimetoxipropano.
9. El proceso de la reivindicación 8, en el que la relación de 2, 2-dimetoxipropano al compuesto de Fórmula VI es 15 entre 1:1 y 5:1.
10. El proceso de la reivindicación 9, en el que la relación de 2, 2-dimetoxipropano al compuesto de Fórmula VI es 1:1.
11. El proceso de la reivindicación 1, en el que el disolvente que forma oxazolidina éster es el reactivo de formación de oxazolidina en sí mismo o un disolvente alcohólico.
12. El proceso de la reivindicación 11, en el que el disolvente que forma oxazolidina éster es metanol, etanol,
propanol, isopropanol, butanol, pentanol y mezclas de los mismos. 25
13. El proceso de la reivindicación 12, en el que el disolvente que forma oxazolidina éster es metanol.
14. El proceso de la reivindicación 1, en el que la base que promueve oxazolidina éster es carbonato de litio,
trietilamina o trimetilamina. 30
15. El proceso de la reivindicación 14, en el que la base que promueve oxazolidina éster es carbonato de litio.
16. El proceso de la reivindicación 1, en el que la temperatura que promueve oxazolidina éster es inferior a 80 ºC. 35 17. El proceso de la reivindicación 1, en el que el compuesto de Fórmula XIV es:
18. El proceso de la reivindicación 1, en el que el compuesto de Fórmula XIV es:
19. El proceso de la reivindicación 17, en el que el compuesto de Fórmula XIV es:
20. El proceso de la reivindicación 18, en el que el compuesto de Fórmula XIV es:
21. El proceso de la reivindicación 1, en el que el agente reductor se selecciona entre el grupo que consiste en NaBH4, KBH4, Ca (BH4) 2 y LiBH4 y mezclas de los mismos.
22. El proceso de la reivindicación 21, en el que el agente reductor es KBH4.
23. El proceso de la reivindicación 22, en el que la relación molar de KBH4 al compuesto de Fórmula VI es entre 1:1 y 2:1.
24. El proceso de la reivindicación 23, en el que la relación molar de KBH4 al compuesto de Fórmula VI es 1, 5:1.
25. El proceso de la reivindicación 21, en el que la reducción se realiza a una temperatura inferior a 60 ºC.
26. El proceso de la reivindicación 25, en el que la reducción se completa en 6 horas. 25
27. El proceso de la reivindicación 1, en el que el disolvente alcohólico se selecciona entre el grupo que consiste en metanol, etanol, propanol, isopropanol, butanol, pentanol, etilenglicol, glicerina y mezclas de los mismos.
28. El proceso de la reivindicación 27, en el que el disolvente es metanol o etanol. 30
29. El proceso de la reivindicación 28, en el que el disolvente es metanol.
30. El proceso de la reivindicación 1, en el que el compuesto de Fórmula VIII es 31. El proceso de la reivindicación 1, en el que el agente de N-acilación tiene la fórmula R6COR7 5 en la que:
R6 es halo o alcoxi C1-6; y R7 es CHCl2.
32. El proceso de la reivindicación 31, en el que R6 es Cl, Br, metoxi o etoxi.
33. El proceso de la reivindicación 32, en el que R6 es Cl.
34. El proceso de la reivindicación 31, en el que el agente de N-acilación se selecciona entre el grupo que consiste 15 en dicloroacetato de metilo, dicloroacetato de etilo, cloruro de dicloroacetilo.
35. El proceso de la reivindicación 34, en el que el agente de N-acilación es dicloroacetato de metilo o cloruro de dicloroacetilo.
36. El proceso de la reivindicación 35, en el que el agente de N-acilación es cloruro de dicloroacetilo.
37. El proceso de la reivindicación 1, en el que la base de N-acilación se selecciona entre el grupo que consiste en carbonato potásico, carbonato sódico, trimetilamina y trietilamina.
38. El proceso de la reivindicación 37, en el que la base de N-acilación es carbonato potásico o trietilamina.
39. El proceso de la reivindicación 38, en el que la relación equivalente molar de la base de N-acilación al compuesto de Fórmula VIII es entre 1:1 y 3:1.
40. El proceso de la reivindicación 39, en el que la relación equivalente molar de la base de N-acilación al compuesto de Fórmula VIII es 1, 1:1.
41. El proceso de la reivindicación 40, en el que la relación molar de cloruro de dicloroacetilo al compuesto de Fórmula VIII es entre 1:1 y 3:1. 35
42. El proceso de la reivindicación 41, en el que la relación molar de cloruro de dicloroacetilo al compuesto de Fórmula VIII es de 1, 1 a 1.
43. El proceso de la reivindicación 34, en el que la etapa de N-acilación se realiza a una temperatura entr.
20. 30 40 ºC.
44. El proceso de la reivindicación 43, en el que la reacción de N-acilación se completa en 2-4 horas.
45. El proceso de la reivindicación 1, en el que el compuesto de Fórmula XII es:
46. El proceso de la reivindicación 1, en el que el agente de fluoración se selecciona entre el grupo que consiste en
N- (2-cloro-1, 1, 2-trifluoroetil) dietilamina, N- (2-cloro-1, 1, 2-trifluoroetil) dimetilamina, N- (2-cloro-1, 1, 2trifluoroetil) dipropilamina, N- (2-cloro-1, 1, 2-trifluoroetil) pirrolidina, N- (2-cloro-1, 1, 2-trifluoroetil) -2-metilpirrolidina, N- (2cloro-1, 1, 2-trifluoroetil) -4-metilpiperazina, N- (2-cloro-1, 1, 2-trifluoroetil) -morfolina, N- (2-cloro-1, 1, 2trifluoroetil) piperidina, 1, 1, 2, 2-tetrafluoroetil-N, N-dimetilamina, trifluoruro de (dietilamino) azufre, trifluoruro de bis- (2metoxietil) aminoazufre, N, N-dietil-1, 1, 2, 3, 3, 3-hexafluoro-1-propanamina (reactivo de Ishikawa) y mezclas de los mismos.
47. El proceso de la reivindicación 46, en el que el agente de fluoración es N, N-dietil-1, 1, 2, 3, 3, 3-hexafluoro-1propanamina.
48. El proceso de la reivindicación 47, en el que la relación molar de N, N-dietil-1, 1, 2, 3, 3, 3-hexafluoro-1-propanamina al compuesto de Fórmula XII es entre 1:1 y 2:1.
49. El proceso de la reivindicación 48, en el que la relación molar de N, N-dietil-1, 1, 2, 3, 3, 3-hexafluoro-1-propanamina al compuesto de Fórmula XII es 1, 5:1. 20
50. El proceso de la reivindicación 49, en el que la etapa de fluoración se realiza a una temperatura de 80 ºC a aproximadamente 110 ºC y a una presión de 41.000 Pa (60 psi) .
51. El proceso de la reivindicación 1, en el que el disolvente orgánico se selecciona entre el grupo que consiste en 25 1, 2-dicloroetano, cloruro de metileno, cloroformo, clorobenceno, hidrocarburos clorados y mezclas de los mismos.
52. El proceso de la reivindicación 51, en el que el disolvente orgánico es cloruro de metileno.
53. El proceso de la reivindicación 1, en el que el compuesto de Fórmula XIII es 30
54. El proceso de la reivindicación 1, en el que el catalizador ácido es ácido clorhídrico acuoso diluido, ácido sulfúrico, o ácido fosfórico, ácido metanosulfónico o ácido p-toluenosulfónico. 35
55. El proceso de la reivindicación 54, en el que el catalizador ácido es ácido p-toluenosulfónico.
56. El proceso de la reivindicación 1, en el que el catalizador básico es LiOH, NaOH, KOH, Li2CO3, Na2CO3, K2CO3,
metóxido sódico, etóxido sódico, metóxido potásico y etóxido potásico. 40
57. El proceso de la reivindicación 56, en el que el catalizador básico es K2CO3.
58. El proceso de la reivindicación 57, en el que la temperatura de la hidrólisis selectiva es inferior a 80 ºC.
59. El proceso de la reivindicación 1, en el que cloruro de metileno es el disolvente orgánico para la hidrólisis selectiva.
60. El proceso de la reivindicación 1, en el que el compuesto de Fórmula XI se purifica con una mezcla de mono, di o trialcohol de alquilo C1-10 y agua para formar la forma pura de un compuesto de Fórmula XI.
61. El proceso de la reivindicación 60, en el que la purificación se realiza en una mezcla de metanol, etanol,
propanol, isopropanol, butanol, sec-butanol, t-butanol, pentanol, etilenglicol, propilenglicol, butilenglicol o glicerina y agua.
62. El proceso de la reivindicación 61, en el que la purificación se realiza en una mezcla de metanol, etanol,
propanol, isopropanol, butanol, sec-butanol, t-butanol o pentanol y agua. 10
63. El proceso de la reivindicación 62, en el que la purificación se realiza en una mezcla de isopropanol y agua.
64. El proceso de la reivindicación 63, en el que la relación de isopropanol a agua es entre 1:5 y 5:1. 15 65. El proceso de la reivindicación 64, en el que la relación de isopropanol a agua es 1:1.
66. El proceso de la reivindicación 65, en el que la temperatura de disolución para purificación es el punto de reflujo de isopropanol y agua a 1:1.
67. El proceso de la reivindicación 60, en el que la reacción de purificación se enfría .
10. 30 ºC para cristalizar el compuesto deseado.
68. El proceso de la reivindicación 67 en el que la reacción de purificación se enfría .
20. 25 ºC para cristalizar el compuesto deseado.
Patentes similares o relacionadas:
Procesos para la preparación de (S)-1-(3-etoxi-4-metoxifenil)-2-metanosulfoniletilamina, del 8 de Enero de 2020, de Amgen (Europe) GmbH: Un proceso para preparar un compuesto de la Fórmula (II): **(Ver fórmula)** o una sal farmacéuticamente aceptable, hidrato, solvato o polimorfo del mismo, […]
Procedimientos para la preparación de (S)-1-(3-etoxi-4-metoxifenil)-2-metanosulfoniletilamina, del 5 de Junio de 2019, de CELGENE CORPORATION: Un procedimiento para preparar un compuesto de Fórmula (I):**Fórmula** o una de sus sales, hidratos, solvatos o polimorfos farmacéuticamente aceptables, en donde: R […]
Procedimientos para la preparación de (S)-1-(3-etoxi-4-metoxifenil)-2-metanosulfoniletilamina, del 30 de Mayo de 2018, de CELGENE CORPORATION: Un procedimiento para preparar un compuesto de Fórmula (II):**Fórmula** o una de sus sales, hidratos, solvatos o polimorfos farmacéuticamente aceptables, […]
Procedimiento para la fabricación de dihalodifenilsulfonas partiendo de ácidos orgánicos, del 14 de Junio de 2017, de Solvay Specialty Polymers USA, LLC: Un procedimiento para la preparación de una molécula (M) de la fórmula: X-[Ar1-SO2-Ar2]-[Ar3]n-[Ar1-SO2-Ar2]m-X (M) en la que n y m son independientemente 0, 1, 2, […]
2-Hidroxi-3-alcoxipropil sulfuros, sulfonas, y sulfóxidos: nuevos agentes tensioactivos, del 16 de Abril de 2014, de AIR PRODUCTS AND CHEMICALS, INC.: Una composición que comprende un compuesto de acuerdo con la fórmula (I) R4OCH2CH(OH)CR2R3ZR1 (I) en donde R4 se selecciona del grupo que consiste en radicales alquilo, […]
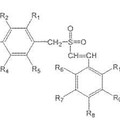 Estirilbencilsulfonas sustituidas para tratar trastornos proliferativos, del 28 de Octubre de 2013, de TEMPLE UNIVERSITY OF THE COMMONWEALTH SYSTEM OF HIGHER EDUCATION: compuesto de la fórmula **Fórmula**
en donde:
(a) (i) R1, R2, R4 y R5 están seleccionados, de manera independiente, del grupo consistente […]
Estirilbencilsulfonas sustituidas para tratar trastornos proliferativos, del 28 de Octubre de 2013, de TEMPLE UNIVERSITY OF THE COMMONWEALTH SYSTEM OF HIGHER EDUCATION: compuesto de la fórmula **Fórmula**
en donde:
(a) (i) R1, R2, R4 y R5 están seleccionados, de manera independiente, del grupo consistente […]
PROCEDIMIENTO PARA LA OBTENCION DE SALES DE SULFONILBENZOILGUANIDINIUM., del 16 de Abril de 2005, de MERCK PATENT GMBH: Procedimiento para la obtención de sales de adición con ácido de los compuestos de la fórmula I, en la que R1, R2 y R3 significan, independientemente entre sí, alquilo con 1 […]
2-HIDROXI-3-ALCOXIPROPIL SULFUROS, SULFONAS Y SULFOXIDOS: NUEVOS AGENTES SUPERFICIALMENTE ACTIVOS, del 14 de Octubre de 2010, de AIR PRODUCTS AND CHEMICALS, INC.: Una formulación que comprende entre el 0,1 y 99,9% en peso en total, de uno o más ingredientes seleccionados entre el grupo que consiste en tensioactivos y agentes de […]