Procedimientos de producción de 3-O-desacil-4''-monofosforil lípido A (3D-MLA).
Un procedimiento de extraer lipopolisacárido (LPS) de un cultivo de células de cepa bacteriana mutante rugosa profunda,
que comprende:
a. extraer las células con una solución que consiste esencialmente en al menos el 75 % en peso de un alcohol alifático que tiene de 1 a 4 átomos de carbono y en el agua del resto; produciendo de este modo células con contenido fosfolipídico reducido;
b. extraer las células con contenido fosfolipídico reducido con una solución que comprende cloroformo y metanol, produciendo de este modo una solución de LPS en cloroformo y metanol,
en el que la extracción con alcohol alifático se lleva a cabo a una temperatura entre 35 ºC y 65 ºC.
Tipo: Patente Europea. Resumen de patente/invención. Número de Solicitud: E11176340.
Solicitante: CORIXA CORPORATION.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: SUITE 200, 1124 COLUMBIA STREET SEATTLE, WA 98104 ESTADOS UNIDOS DE AMERICA.
Inventor/es: MYERS,KENT R, SNYDER,D. SCOTT.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K31/739 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › Lipopolisacáridos.
- A61P37/04 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › A61P 37/00 Medicamentos para el tratamiento de problemas inmunológicos o alérgicos. › Inmunoestimulantes.
- C08B37/00 QUIMICA; METALURGIA. › C08 COMPUESTOS MACROMOLECULARES ORGANICOS; SU PREPARACION O PRODUCCION QUIMICA; COMPOSICIONES BASADAS EN COMPUESTOS MACROMOLECULARES. › C08B POLISACARIDOS; SUS DERIVADOS (polisacáridos que contienen menos de seis radicales sacáridos unidos entre sí por enlaces glucosídicos C07H; procesos de fermentación o procesos que utilizan enzimas C12P 19/00; producción de celulosa D21). › Preparación de polisacáridos no previstos en los grupos C08B 1/00 - C08B 35/00; Sus derivados (celulosa D21).
- C12N1/20 C […] › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 1/00 Microorganismos, p.ej. protozoos; Composiciones que los contienen (preparaciones de uso médico que contienen material de protozoos, bacterias o virus A61K 35/66, de algas A61K 36/02, de hongos A61K 36/06; preparación de composiciones de uso médico que contienen antígenos o anticuerpos bacterianos, p. ej. vacunas bacterianas, A61K 39/00 ); Procesos de cultivo o conservación de microorganismos, o de composiciones que los contienen; Procesos de preparación o aislamiento de una composición que contiene un microorganismo; Sus medios de cultivo. › Bacterias; Sus medios de cultivo.
- C12N1/21 C12N 1/00 […] › modificados por la introducción de material genético extraño.
- C12P1/04 C12 […] › C12P PROCESOS DE FERMENTACION O PROCESOS QUE UTILIZAN ENZIMAS PARA LA SINTESIS DE UN COMPUESTO QUIMICO DADO O DE UNA COMPOSICION DADA, O PARA LA SEPARACION DE ISOMEROS OPTICOS A PARTIR DE UNA MEZCLA RACEMICA. › C12P 1/00 Preparación de compuestos o de composiciones, no prevista en los grupos C12P 3/00 - C12P 39/00, utilizando microorganismos o enzimas; Procedimientos generales de preparación de compuestos o composiciones que utilizan microorganismos o enzimas. › utilizando bacterias.
- C12P19/04 C12P […] › C12P 19/00 Preparación de compuestos que contienen radicales sacárido (ácido cetoaldónico C12P 7/58). › Polisacáridos, es decir, compuestos que contienen más de cinco radicales sacárido unidos entre ellos por enlaces glucosídicos.
PDF original: ES-2517391_T3.pdf
Fragmento de la descripción:
Procedimientos de producción de 3-0-desacil-4'-monofosforil lípido A (3D-MLA)
Antecedentes de la invención
1. Campo de la invención
La presente invención se refiere, en general, al campo de la producción biosintética de 3-0-desacil-4'-monofosforil lípido A (3D-MLA). Más particularmente, se refiere a procedimientos de mejora del rendimiento de congéneres de 3D- MLA deseados o de minimización del coste de purificación de precursores de lipopolisacáridos (LPS) de 3D-MLA.
2. Descripción de técnica relacionada
Desde hace tiempo se reconoce que los lipopolisacáridos enterobacterianos (LPS) son potentes estimulantes del sistema inmunitario. Puede provocarse una variedad de respuestas, tanto beneficiosas como perjudiciales, por cantidades submicrográmicas de LPS. El hecho de que algunas de las respuestas sean perjudiciales y algunas de estas puedan ser mortales, ha descartado el uso clínico de LPS por sí mismo. Se ha observado que el componente de LPS más responsable de la actividad endotóxica es el lípido A.
Por consiguiente, se ha hecho un gran esfuerzo por atenuar los atributos tóxicos de LPS o lípido A sin disminuir los beneficios inmunoestimulantes de estos compuestos. Entre estos esfuerzos fueron notables los de Edgar Ribi y sus colaboradores, que dieron como resultado la producción del derivado de lípido A 3-0-desacil-4'-monofosforil-lípido A (3D-MLA; composiciones que comprenden 3D-MLA están comercialmente disponibles con el nombre comercial MPL® de Corixa Corporation (Seattle, WA)). 3D-MLA ha mostrado que tiene esencialmente las mismas propiedades inmunoestimulantes que el lípido A pero menor endotoxicidad (Myers y col., patente de EE.UU. n.2:4.912.094). Myers y col. también informaron de un procedimiento para la producción de 3D-MLA, como sigue. Primero, LPS o lípido A obtenido de una cepa mutante rugosa profunda de una bacteria gram-negativa (por ejemplo, R595 de Salmonella minnesota) se somete a reflujo en soluciones de ácidos minerales de fuerza moderada (por ejemplo, HCI 0,1 N) durante un periodo de aproximadamente 30 min. Esto conduce a la desfosforilación en la posición 1 de la glucosamina del extremo reductor y a la descarbohidratación en la posición 6' de la glucosamina no reductora del lípido A. Segundo, el lípido A descarbohidratado desfosforilado (también conocido como monofosforil lípido A o MLA) se somete a una hidrólisis básica, por ejemplo, disolviendo en un disolvente orgánico tal como cloroformo:metanol (CM) 2:1 (v/v), saturando la solución con una solución acuosa de Na2CC>3 0,5 M a pH 10,5 y evaporando al vacío el disolvente. Esto conduce a eliminación selectiva del resto ácido (3-hidroximirístico en la posición 3 del lípido A, resultando 3-O-desacil- 4'-monofosforil-lípido A (3D-MLA).
La calidad del 3D-MLA producido mediante el procedimiento anterior es altamente dependiente de la pureza y composición de los LPS obtenidos de la bacteria gram-negativa. Por citar un ejemplo, el componente de lípido A de LPS es una mezcla de especies estrechamente relacionadas que contienen entre aproximadamente 5-7 restos de ácido graso. En la formación de 3D-MLA, como es evidente de la discusión anterior, un resto de ácido graso se elimina, produciendo 3D-MLA con entre aproximadamente 4-6 restos de ácidos grasos. Se mantiene generalmente que 3D- MLA con al menos 6 restos de ácido graso se prefiere en términos de la combinación de beneficios inmunoestimulantes mantenidos o potenciados, toxicidad reducida y otras propiedades deseables (Qureshi y Takayama, en "The Bacteria," vol. XI (Iglewski y Clark, eds.), Academic Press, 1990, pág. 319-338).
Por citar otro ejemplo, la extracción a escala comercial de LPS de bacterias gram-negativas normalmente implica el procedimiento de Chen (Chen y col., J. Infect. Dis. 128:543 (1973)); concretamente, la extracción con CM, que conduce a una fase de CM rica en LPS y fosfolípidos de la que luego puede purificarse LPS. Sin embargo, la purificación de LPS a partir de la fase de CM rica en LPS y fosfolípidos normalmente requiere múltiples etapas de precipitación para obtener LPS de suficiente pureza para usar en aplicaciones inmunoestimulantes tales como, por ejemplo, uso como adyuvante de vacuna.
Por tanto, sería deseable disponer de procedimientos para preparar convenientemente composiciones de LPS altamente puras. Además, sería deseable disponer de procedimientos para generar composiciones de LPS cuyas composiciones tuvieran 3D-MLA con niveles elevados de congéneres de hexaacilo.
Se han usado técnicas de fermentación conocidas para preparar cultivos de bacterias gram-negativas que comprenden LPS fácilmente purificables. Estas técnicas conocidas normalmente implican la recogida de cultivos bacterianos en fase estacionaria temprana, de acuerdo con prácticas bacteriológicas convencionales. Sin embargo, se ha observado que el grado de acilación del LPS producido de acuerdo con condiciones conocidas es variable. Por ejemplo, el contenido de especies de heptaacilo en el lípido A de R595 de S. minnesota puede variar del 20 % al 80 %, dependiendo del lote (Rietschel y col., Rev. Infect. Dis. 9:S527 (1987)). Esta variabilidad en el contenido de congéneres de heptaacilo daría como resultado las diferencias significativas en el contenido de congéneres de hexaacilo en el 3D-MLA preparado a partir de estos lotes de LPS.
Sumario de la invención
La presente invención se refiere a un procedimiento de extracción de lipopolisacárido (LPS) a partir de un cultivo de células de cepa bacteriana mutante rugosa profunda, que comprende:
a. extraer las células con una solución que consiste esencialmente en al menos el 75 % en peso de un alcohol alifático que tiene de 1 a 4 átomos de carbono y en el agua del resto; produciendo de este modo células con contenido fosfolipídico reducido;
b. extraer las células con contenido fosfolipídico reducido con una solución que comprende cloroformo y metanol, produciendo de este modo una solución de LPS en cloroformo y metanol, en la que la extracción con alcohol alifático se lleva a cabo a una temperatura entre 35 2C y 65 2C.
El procedimiento proporciona soluciones de LPS en CM que tienen contenido en fosfolípidos reducido y que por lo tanto son muy adecuados para modificación y peurificación adicionales de 3D-MLA. El procedimiento implica etapas relativamente simples y económicas.
Breve descripción de los dibujos
Los siguientes dibujos forman parte de la memoria descriptiva y están incluidos para demostrar adicionalmente ciertos aspectos de la presente invención. La invención puede entenderse mejor por referencia a uno o más de estos dibujos en combinación con la descripción detallada de realizaciones específicas presentadas en el presente documento.
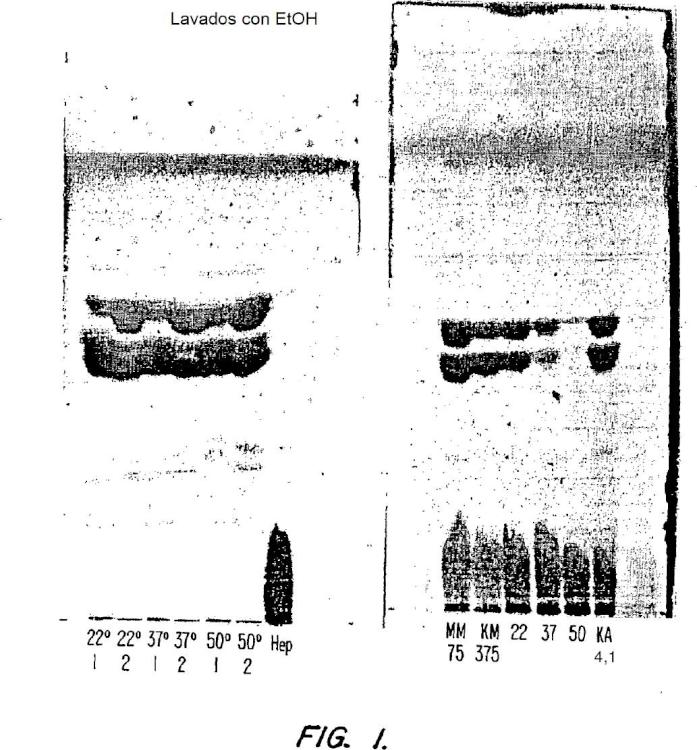
La Figura 1 muestra placas de CCF de extractos de etanol y muestras de LPS obtenidas con diferentes temperaturas durante las extracciones con etanol. La placa de la izquierda muestra, de izquierda a derecha, los extractos de etanol a temperaturas de 22 2C, 37 2C y 50 2C. La muestra en el extremo derecho de esta placa es una muestra de LPS auténtica. La placa a la derecha muestra los LPS obtenidos de cada preparación. Las muestras en los carriles 3, 4 y 5 se corresponden con LPS de células sometidas a pre-extracciones con etanol a 22 2C, 37 2C y 50 2C, respectivamente. Las bandas pesadas a Rf~0,6 se corresponden con fosfolípido e impurezas de ácidos grasos. Los niveles de estas impurezas se reducen aumentando la temperatura de las extracciones con etanol y son muy bajos en la muestra que se pre-extrajo a 50 2C.
Descripción de realizaciones ilustrativas
Los lipopolisacáridos son el principal constituyente lipídico en la valva externa de la membrana externa de bacterias gram-negativas. La fracción de lipopolisacáridos de una bacteria gram-negativa comprende, entre otros componentes, lípido A. Como se ha descrito, el lípido A puede descarbohidratarse y desfosforilarse parcialmente para proporcionar monofosforil-lípido A (MLA) y MLA puede desacilarse selectivamente en la posición 3 para proporcionar 3-0-desacil-4'-
monofosforil-lípido A (3D-MLA).
Sin embargo, el lípido A producido por bacterias gram-negativas normalmente comprende varias especies que tienen la misma estructura de lípido A global pero difieren en el número de restos de ácidos grasos que contienen. Grupos de especies del lípido A con el mismo número de ácidos grasos se denominan en el presente documento "congéneres". Los congéneres del lípido A que tienen de 4 a 7 restos de ácidos grasos se producen por cultivo a escala comercial convencional de bacterias gram-negativas tales como R595 de S. minnesota. Como resultado, 3D-MLA producido de, por ejemplo, lípido... [Seguir leyendo]
Reivindicaciones:
1. Un procedimiento de extraer lipopolisacárido (LPS) de un cultivo de células de cepa bacteriana mutante rugosa profunda, que comprende:
a. extraer las células con una solución que consiste esencialmente en al menos el 75 % en peso de un alcohol alifático 5 que tiene de 1 a 4 átomos de carbono y en el agua del resto; produciendo de este modo células con contenido
fosfolipídico reducido;
b. extraer las células con contenido fosfolipídico reducido con una solución que comprende cloroformo y metanol, produciendo de este modo una solución de LPS en cloroformo y metanol,
en el que la extracción con alcohol alifático se lleva a cabo a una temperatura entre 35 2C y 65 2C.
2. El procedimiento de la reivindicación 1, en el que la cepa bacteriana mutante rugosa profunda es del género
Salmonella o Escherichia.
3. El procedimiento de la reivindicación 2, en el que la cepa bacteriana mutante rugosa profunda del género Salmonella es de la especie Salmonella minnesota
4. El procedimiento de la reivindicación 3, en el que la cepa bacteriana mutante rugosa profunda de la especie 15 Salmonella minnesota es la cepa R595 de Salmonella minnesota
5. El procedimiento de la reivindicación 2, en el que la cepa bacteriana mutante rugosa profunda del género Escherichia es de la especie Escherichia coli.
6. El procedimiento de la reivindicación 5, en el que la cepa bacteriana mutante rugosa profunda de la especie Escherichia colies de la cepa D31m4 de Escherichia coli.
7. El procedimiento de la reivindicación 1, en el que el alcohol alifático tiene de 2 a 4 átomos de carbono.
8. El procedimiento de la reivindicación 7, en el que el alcohol alifático es etanol.
9. El procedimiento de la reivindicación 1, en el que la solución que comprende alcohol alifático comprende entre el 85 % en peso y el 95 % en peso de alcohol alifático.
10. El procedimiento de la reivindicación 1, en el que la temperatura está entre 45 2C y 55 2C.
11. El procedimiento de la reivindicación 1, que comprende adicionalmente evaporar el cloroformo y el metanol de la
solución de LPS, produciendo de esta forma un residuo de LPS seco.
12. El procedimiento de la reivindicación 11, que comprende adicionalmente someter el residuo de LPS a hidrólisis ácida y a hidrólisis básica secuenciales, para formar 3D-MLA.
Patentes similares o relacionadas:
Diversificación de los oligosacáridos de la leche humana (HMO) o sus precursores, del 8 de Julio de 2020, de Glycom A/S: Un metodo de preparacion de una mezcla diversificada que comprende dos o mas oligosacaridos de la leche humana (HMO), el metodo comprende las etapas de […]
Método de producción de compuestos de inclusión de flavonoide, del 3 de Junio de 2020, de TAIYO KAGAKU CO., LTD.: Un método de producción de un compuesto de inclusión de flavonoide, que comprende una etapa de escisión que comprende tratar un flavonoide escasamente […]
Construcción de nuevas variantes de dextransacarasa DSR-S por ingeniería genética, del 6 de Mayo de 2020, de CENTRE NATIONAL DE LA RECHERCHE SCIENTIFIQUE: 1. Una dextransacarasa que consiste en una secuencia que tiene el 90 %, el 95 % o el 98 % de similitud de secuencia con una secuencia de aminoácidos seleccionada del fragmento […]
Métodos para la degradación o la conversión de polisacáridos de la pared celular vegetal, del 6 de Mayo de 2020, de NOVOZYMES, INC.: Metodo para degradar o convertir los polisacaridos de la pared celular vegetal en uno o mas azucares, que comprende: tratar los polisacaridos de la pared celular vegetal con […]
Procedimiento para la purificación de hidrolizado de biomasa, del 29 de Abril de 2020, de CLARIANT INTERNATIONAL LTD.: Un procedimiento para la purificación de hidrolizado de biomasa que comprende las etapas a) Proporcionar un hidrolizado de biomasa, en el que el hidrolizado […]
Construcción de nuevas variantes de dextransacarasa DSR-S por ingeniería genética, del 22 de Abril de 2020, de CENTRE NATIONAL DE LA RECHERCHE SCIENTIFIQUE: Una secuencia de nucleótidos que consiste en una secuencia de nucleótidos como se define en SEQ ID NO: 1 o la secuencia complementaria a la secuencia como […]
Transsialidasas de photobacterium mutadas, del 15 de Abril de 2020, de Glycom A/S: Una α2,6-transsialidasa que tiene una secuencia de aminoácidos que es por lo menos un 90% idéntica a la secuencia de aminoácidos de la SEQ ID […]
Exopolisacárido para el tratamiento y/o cuidado de la piel, mucosas, cabello y/o uñas, del 11 de Marzo de 2020, de LUBRIZOL ADVANCED MATERIALS, INC.: Uso del exopolisacárido de la cepa de las especies de Vibrio sp. con número de depósito CNCM I-4277, para mejorar la hidratación de la piel, mucosas, […]