PROCEDIMIENTOS PARA DETECTAR LA EVOLUCIÓN DE LA DISPLASIA DE CUELLO UTERINO DE BAJO GRADO.
Un procedimiento para identificar a una paciente con riesgo de desarrollar carcinoma de cuello uterino invasivo,
comprendiendo el procedimiento: detectar cualquier amplificación genómica del cromosoma 3q en una muestra obtenida a partir de una paciente que tiene i) displasia de cuello uterino de bajo grado; o ii) que no tiene displasia identificando así a una paciente con riesgo de desarrollar carcinoma de cuello uterino invasivo si una amplificación genómica de cromosoma 3q se detecta
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2006/006116.
Solicitante: GOVERNMENT OF THE UNITED STATES OF AMERICA, as represented by THE SECRETARY, DEPARTMENT OF HEALTH AND HUMAN SERVICES.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: National Institutes of Health, Office of Technology Transfer, National Executive Boulevard, Suite 325 Rockville, MD 20852 ESTADOS UNIDOS DE AMERICA.
Inventor/es: RIED, THOMAS, LARSSON, CATHARINA, AUER,GERT, HESELMEYER-HADDAD,Kerstin, STEINBERG,Winfried, ANDERSSON,Sonia.
Fecha de Publicación: .
Fecha Solicitud PCT: 21 de Febrero de 2006.
Clasificación Internacional de Patentes:
- C12Q1/68M6B
Clasificación PCT:
- C12Q1/68 QUIMICA; METALURGIA. › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12Q PROCESOS DE MEDIDA, INVESTIGACION O ANALISIS EN LOS QUE INTERVIENEN ENZIMAS, ÁCIDOS NUCLEICOS O MICROORGANISMOS (ensayos inmunológicos G01N 33/53 ); COMPOSICIONES O PAPELES REACTIVOS PARA ESTE FIN; PROCESOS PARA PREPARAR ESTAS COMPOSICIONES; PROCESOS DE CONTROL SENSIBLES A LAS CONDICIONES DEL MEDIO EN LOS PROCESOS MICROBIOLOGICOS O ENZIMOLOGICOS. › C12Q 1/00 Procesos de medida, investigación o análisis en los que intervienen enzimas, ácidos nucleicos o microorganismos (aparatos de medida, investigación o análisis con medios de medida o detección de las condiciones del medio, p. ej. contadores de colonias, C12M 1/34 ); Composiciones para este fin; Procesos para preparar estas composiciones. › en los que intervienen ácidos nucleicos.
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Eslovenia, Finlandia, Rumania, Chipre, Lituania, Letonia.
PDF original: ES-2360954_T3.pdf


Fragmento de la descripción:
Declaración de derechos de la invención realizada dentro de una investigación financiada con fondos federales
Este trabajo se respaldó por el Instituto Nacional de Salud.
Antecedentes de la invención
La visualización de la aneuploidía cromosómica y los cambios en la cantidad de copias de genes asociados al cáncer específicos se ha convertido en un complemento importante en la evaluación morfológica de rutina de muestras citológicas.1 Este enfoque es biológicamente válido y exitoso ya que la aneuploidía cromosómica y los desequilibrios genómicos resultantes son específicos para células cancerosas, distintos para diferentes carcinomas, y se producen temprano durante la evolución de la enfermedad. 2,3 Algunos desequilibrios genómicos se correlacionan con un mal pronóstico y un fallo en el tratamiento,4-6 y otros, tales como la amplificación del oncogén Her2/neu en el cáncer de mama, pueden guiar las decisiones terapéuticas.7
Como la mayoría de los otros carcinomas humanos, los cánceres de cuello uterino se definen por una distribución conservada de desequilibrios genómicos. Además de la infección con el virus del papiloma humano de alto riesgo,9,10 la transformación secuencial del epitelio escamoso del cuello uterino requiere la adquisición de copias adicionales del brazo del cromosoma 3q,11 entre otras anormalidades citogenéticas.12 Los análisis de CGH de carcinomas de cuello uterino han mostrado que más del 85% de los carcinomas de cuello uterino invasivos portan desequilibrios genómicos específicos que dan como resultado un incremento de la cantidad de copias del brazo del cromosoma 3q.5,11,20-26 La región de solapamiento mínimo apunta a la banda de cromosoma 3q26, que contiene el gen para el componente de ARN de telomerasa humana (TERC).27
La implementación de programas de detección de cáncer de cuello uterino ha reducido enormemente la incidencia y la mortalidad de la enfermedad en países industrializados.16,17 Sin embargo, una única evaluación citológica permanece relativamente insensible, de ahí la necesidad de frecuentes investigaciones de seguimiento. Esto es atribuible a errores de muestreo o de interpretación, y al hecho de que puede que algunas lesiones tempranas no hayan adquirido alteraciones fenotípicas reconocibles.17 Los carcinomas de cuello uterino invasivos se desarrollan a través de estadios crecientes de displasia de cuello uterino y avanzan hasta CIN3, que se considera una lesión precancerosa auténtica que requiere intervención quirúrgica. Sin embargo, sólo aproximadamente el 10-15% de todas las lesiones displásicas de bajo grado siguen este trayecto de progresión lineal. La identificación de marcadores de la evolución de la enfermedad, sería por lo tanto de gran interés clínico.
Un estudio previo demostró que la visualización de copias adicionales de TERC puede servir como una prueba específica y sensible para la amplificación de 3q26 en muestras citológicas recogidas de manera rutinaria, incluyendo muestras de displasia de cuello uterino de bajo grado.8 Este hallazgo fue consistente con, pero no concluyente de, la hipótesis de que la ventaja en el crecimiento impuesto de 3q refleja un punto de no retorno durante la transformación maligna secuencial de las células epiteliales de cuello uterino. Por ejemplo, la solicitud de los EE.UU. con número de serie 10/857859, presentada el 4 de junio de 2004 y publicada como la publicación de la solicitud de los EE.UU. N.º 20050026190, indica que la amplificación de 3q26 se pueden usar para detectar selectivamente neoplasias intraepiteliales de cuello uterino de alto grado (CIN II y CIN III) y carcinomas malignos en una biopsia de cuello uterino y especímenes del frotis de Papanicolaou sin detectar neoplasia intraepitelial de cuello uterino de bajo grado. Así, se piensa que la amplificación de 3q26 es un factor de distinción entre adenocarcinomas y displasias de cuello uterino de bajo grado y de alto grado.
Sumario de la invención
Se ha demostrado ahora que la identificación de una amplificación de 3q en la displasia de cuello uterino de bajo grado puede proporcionar información relacionada con el potencial evolutivo de lesiones individuales para el cáncer y la displasia de cuello uterino de alto grado.
La presente invención proporciona un procedimiento para identificar a una paciente con riesgo de desarrollar carcinoma de cuello uterino invasivo, comprendiendo el procedimiento: detectar cualquier amplificación genómica del cromosoma 3q en una muestra obtenida de una paciente i) que tiene displasia de bajo grado, o ii) que no tiene displasia identificando así a una paciente con riesgo de desarrollar carcinoma de cuello uterino invasivo si se detecta una amplificación genómica del cromosoma 3q.
Se da a conocer un procedimiento para evaluar un cambio en una afección de una paciente de displasia de cuello uterino de bajo grado a una afección de cáncer o displasia de cuello uterino de alto grado, que comprende: detectar una amplificación genómica del cromosoma 3q en una muestra de una paciente que tiene o que tiene previamente displasia de cuello uterino de bajo grado para evaluar de este modo el cambio en la afección de una paciente a un cáncer o displasia de cuello uterino de alto grado. La detección de la amplificación genómica del cromosoma 3q indica la evolución de la afección de una paciente a displasia de cuello uterino de alto grado.
**(Ver fórmula)**
Se da a conocer adicionalmente un procedimiento para monitorizar un cambio a una afección de displasia de cuello uterino de alto grado a partir de una afección de displasia de cuello uterino de bajo grado en una paciente que comprende: someter a ensayo para determinar una amplificación genómica del cromosoma 3q en una muestra de una paciente que tiene o que tiene previamente displasia de cuello uterino de bajo grado para monitorizar de este modo un cambio a una afección de displasia de cuello uterino de alto grado a partir de una afección de displasia de cuello uterino de bajo grado. El procedimiento puede comprender adicionalmente determinar que la amplificación genómica del cromosoma 3q está presente en la muestra o que la amplificación genómica del cromosoma 3q no está presente en la muestra.
Las displasias de cuello uterino de bajo grado de la invención pueden ser, pero no se limitan a, neoplasias intraepiteliales de cuello uterino de grado 1. Las displasias de cuello uterino de alto grado de la invención incluyen, pero no se limitan a, neoplasias intraepiteliales de cuello uterino de grado 2, neoplasias intraepiteliales de cuello uterino de grado 3 y carcinomas in situ.
En una realización, la muestra obtenida de la paciente es una preparación a partir del cuello uterino, incluyendo, pero sin limitarse a, un frotis de Papanicolaou o una suspensión de células de capa fina (por ejemplo, mono-capa).
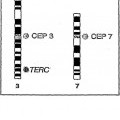
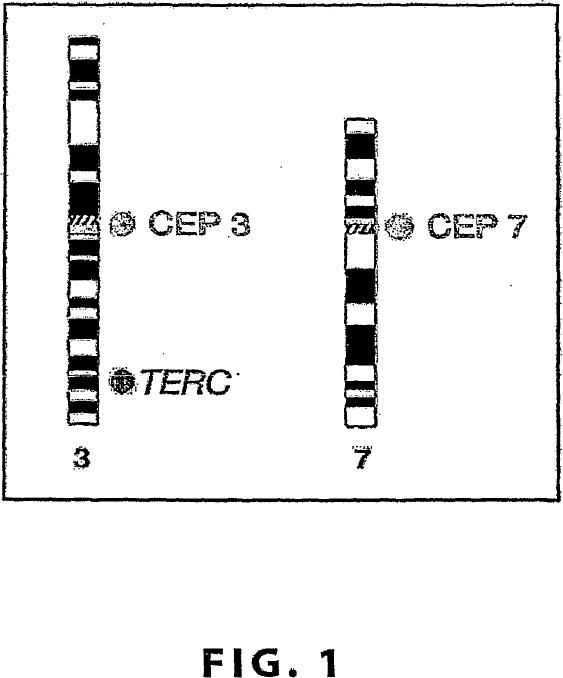
De acuerdo con realizaciones específicas de la invención, la amplificación genómica puede estar dentro del locus 3q26 del cromosoma 3q. Este locus incluye las secuencias de codificación del gen de la telomerasa (TERC). Así, en una realización, la amplificación genómica se detecta hibridando la muestra a una sonda que comprende un marcador detectable y una secuencia de ácidos nucleicos que es complementaria de una secuencia de ácidos nucleicos del locus 3q26. Los procedimientos de la invención pueden implicar adicionalmente hibridar la muestra a una sonda centromérica de enumeración que comprende un marcador detectable y una secuencia de ácidos nucleicos que es complementaria de una secuencia de ácidos nucleicos próxima al centrómero del cromosoma 3.
En una realización, la secuencia de ácidos nucleicos de la sonda es complementaria del gen de la telomerasa, o una parte del mismo.
En otras realizaciones, la secuencia de ácidos nucleicos de la sonda es complementaria de una secuencia de ácidos nucleicos del cromosoma 3q, o una parte del mismo, incluyendo, pero sin limitarse a, EVI1 (sitio de integración vírico ectópico 1, 3q24-3q28), MDS1 (síndrome de mielodisplasia 1, 3q26), MYNN (mioneurina, 3q26.2), GPR160 (receptor acoplado a proteína G 160, 3q26.2-3q27), PRKCI (proteína cinasa C, 3q26.3), SKIL (similar a SKI 3q26), CLDN11 (claudina 11, 3q26.2-3q26.3), EIF5A2 (factor de iniciación de traducción eucariota 5A2, 3q26.2), y TNIK (cinasa de interacción con TRAF2 y NCK, 3q26.2), PLD1 (fosfolipasa D1, 3q26), GHSR (receptor de secretagogos de hormona de crecimiento, 3q26.31), TNSF10 (factor de necrosis tumoral 10, 3q26), ECT2 (oncogén de secuencia de transformación de célula... [Seguir leyendo]
Reivindicaciones:
1. Un procedimiento para identificar a una paciente con riesgo de desarrollar carcinoma de cuello uterino invasivo,
comprendiendo el procedimiento: detectar cualquier amplificación genómica del cromosoma 3q en una muestra obtenida a partir de una paciente que tiene
i) displasia de cuello uterino de bajo grado; o ii) que no tiene displasia identificando así a una paciente con riesgo de desarrollar carcinoma de cuello uterino invasivo si una amplificación genómica de cromosoma 3q se detecta.
2. El procedimiento de la reivindicación 1, en el que la amplificación genómica está dentro del locus 3q26 del cromosoma 3q.
3. El procedimiento de la reivindicación 1, en el que la displasia de cuello uterino de bajo grado es una neoplasia intraepitelial de cuello uterino de grado 1.
4. El procedimiento de la reivindicación 1, en el que se obtiene un frotis de Papanicolaou normal de una paciente que no tiene displasia.
5. El procedimiento de la reivindicación 2, en el que la amplificación genómica se detecta hibridando la muestra a una sonda que comprende un marcador detectable y una secuencia de ácidos nucleicos que es complementaria de una secuencia de ácidos nucleicos del locus 3q26.
6. El procedimiento de la reivindicación 5, en el que la secuencia de ácidos nucleicos de la sonda es complementaria del gen de la telomerasa, o una parte del mismo.
7. El procedimiento de la reivindicación 6, en el que el marcador detectable emite una señal fluorescente.
8. El procedimiento de la reivindicación 6, en el que el marcador detectable es cromogénico.
9. El procedimiento de la reivindicación 5, que comprende adicionalmente hibridar la muestra a una sonda centromérica de enumeración que comprendeun marcador detectable y una secuencia de ácidos nucleicos que es complementaria de una secuencia de ácidos nucleicos próxima al centrómero del cromosoma 3.
10. El procedimiento de la reivindicación 2, en el que la amplificación genómica se detecta por la reacción en cadena de la polimerasa.
11. Los procedimientos de la reivindicación 2, en los que la amplificación genómica se detecta midiendo la cantidad del polipéptido de telomerasa.
12. El procedimiento de la reivindicación 1, en el que la muestra es una preparación a partir del cuello uterino.
13. El procedimiento de la reivindicación 12, en el que la preparación es un frotis de Papanicolaou o una suspensión de capa fina de células.
Patentes similares o relacionadas:
MARCADORES PARA LA SELECCIÓN DE TERAPIAS PERSONALIZADAS PARA EL TRATAMIENTO DEL CÁNCER, del 7 de Febrero de 2012, de FUNDACION INSTITUT DE RECERCA DE L'HOSPITAL UNIVERSITARI VALL D'HEBRON: La invención se relaciona con la identificación de los niveles de expresión de aprataxina (APTX) como marcador de respuesta a terapias basadas en inhibidores de topoisomerasa […]
MÉTODOS PARA SELECCIONAR REGÍMENES DE TRATAMIENTO Y PREDECIR RESULTADOS EN PACIENTES CON CÁNCER DE MAMA, del 6 de Febrero de 2012, de AMERICAN DIAGNOSTICA INC: Un método para seleccionar de dos o más regímenes de tratamiento, un régimen de tratamiento que tiene el mayor beneficio esperado para un […]
 METODO Y KIT PARA EL PRONOSTICO DEL LINFOMA DE CELULAS DEL MANTO, del 23 de Enero de 2012, de HOSPITAL CLINIC DE BARCELONA UNIVERSIDAD DE BARCELONA FUNDACIO CLINIC PER A LA RECERCA BIOMEDICA INSTITUT D'INVESTIGATIONS BIOMEDIQUES AUGUST PI I SUNYER (IDIBAPS): Método y kit para el pronóstico del linfoma de células del manto.
El método y el kit son útiles como herramientas para clasificar un paciente diagnosticado con linfoma […]
METODO Y KIT PARA EL PRONOSTICO DEL LINFOMA DE CELULAS DEL MANTO, del 23 de Enero de 2012, de HOSPITAL CLINIC DE BARCELONA UNIVERSIDAD DE BARCELONA FUNDACIO CLINIC PER A LA RECERCA BIOMEDICA INSTITUT D'INVESTIGATIONS BIOMEDIQUES AUGUST PI I SUNYER (IDIBAPS): Método y kit para el pronóstico del linfoma de células del manto.
El método y el kit son útiles como herramientas para clasificar un paciente diagnosticado con linfoma […]
PROCEDIMIENTOS Y COMPOSICIONES PARA EL DIAGNÓSTICO Y TRATAMIENTO DEL CÁNCER DE PULMÓN UTILIZANDO EL GEN DE PDGFRA, KIT O KDR COMO MARCADOR GENÉTICO, del 17 de Enero de 2012, de GENENTECH, INC.: Procedimiento para diagnosticar la presencia de un cáncer de pulmón en un mamífero, comprendiendo el procedimiento la detección de si el gen de PDGFRA está […]
MÉTODOS Y SONDAS PARA LA DETECCIÓN DEL CÁNCER, del 12 de Enero de 2012, de VYSIS, INC. MAYO FOUNDATION FOR MEDICAL EDUCATION AND RESEARCH: Un conjunto de sondas cromosómicas que comprende la siguiente combinación de cuatro sondas: una sonda específica del locus 5p15, una sonda específica del locus 8q24, […]
COMPOSICIÓN Y PROCEDIMIENTO PARA LA DETECCIÓN, DIAGNÓSTICO Y TERAPÍA DE NEOPLASIAS HEMATOLÓGICAS, del 22 de Diciembre de 2011, de CORIXA CORPORATION: Uso de una cantidad eficaz de un anticuerpo monoclonal aislado que se une específicamente a un polipéptido que comprende la secuencia expuesta en SEC ID Nº: 4 […]
MÉTODO NORMALIZADO Y OPTIMIZADO DE REACCIÓN EN CADENA DE LA POLIMERASA DE TRANSCRIPTASA INVERSA CUANTITATIVA EN TIEMPO REAL PARA LA DETECCIÓN DE MRD EN LEUCEMIA, del 14 de Diciembre de 2011, de UNIVERSITE DE LA MEDITERRANEE: Conjunto de ácidos nucleicos ABL para RQ-PCR que comprende una sonda nucleotídica que tiene la secuencia SEC ID N.º 2 y cebadores directo e inverso que tienen las secuencias […]
BIOMARCADORES Y PROCEDIMIENTOS PARA DETERMINAR LA SENSIBILIDAD A MODULADORES DEL RECEPTOR DEL FACTOR DE CRECIMIENTO EPIDÉRMICO, del 12 de Diciembre de 2011, de BRISTOL-MYERS SQUIBB COMPANY: Un procedimiento in vitro para predecir la probabilidad de que un mamífero responda terapéuticamente a un procedimiento de tratamiento del […]