Procedimientos y composiciones que implican miARN y moléculas inhibidoras de miARN.
Tipo: Patente Europea. Resumen de patente/invención. Número de Solicitud: E10183481.
Solicitante: Asuragen, Inc.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 2150 Woodward St Suite 100 Austin TX 78744 ESTADOS UNIDOS DE AMERICA.
Inventor/es: BROWN, DAVID, DEVROE,ERIC, FORD,LANCE, CHENG,ANGIE, JARVIS,RICH, BYROM,MIKE, OVCHARENKO,DMITRIY, KELNAR,KEVIN.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C12N15/11 QUIMICA; METALURGIA. › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 15/00 Técnicas de mutación o de ingeniería genética; ADN o ARN relacionado con la ingeniería genética, vectores, p. ej. plásmidos, o su aislamiento, su preparación o su purificación; Utilización de huéspedes para ello (mutantes o microorganismos modificados por ingeniería genética C12N 1/00, C12N 5/00, C12N 7/00; nuevas plantas en sí A01H; reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00; nuevas razas animales en sí A01K 67/00; utilización de preparaciones medicinales que contienen material genético que es introducido en células del cuerpo humano para tratar enfermedades genéticas, terapia génica A61K 48/00; péptidos en general C07K). › Fragmentos de ADN o de ARN; sus formas modificadas (ADN o ARN no empleado en tecnología de recombinación C07H 21/00).
- C12N15/113 C12N 15/00 […] › Acidos nucleicos no codificantes que modulan la expresión de genes, p.ej. oligonucleótidos antisentido.
PDF original: ES-2503739_T3.pdf
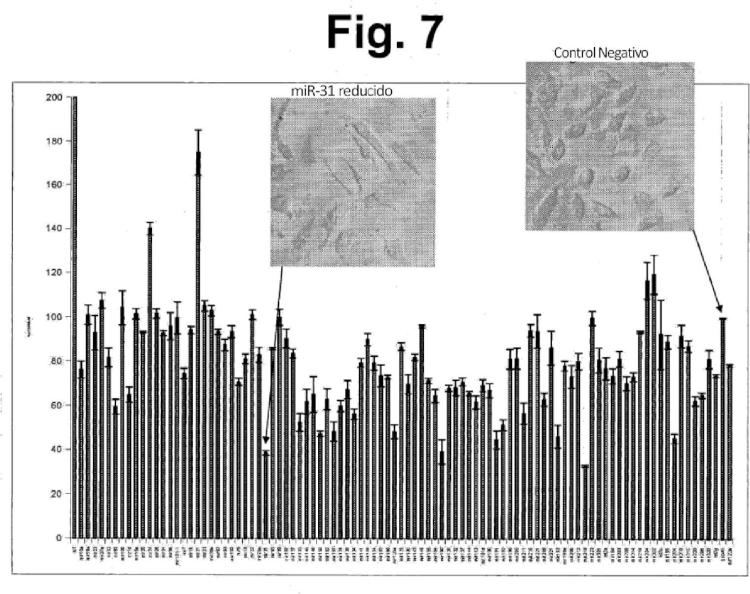
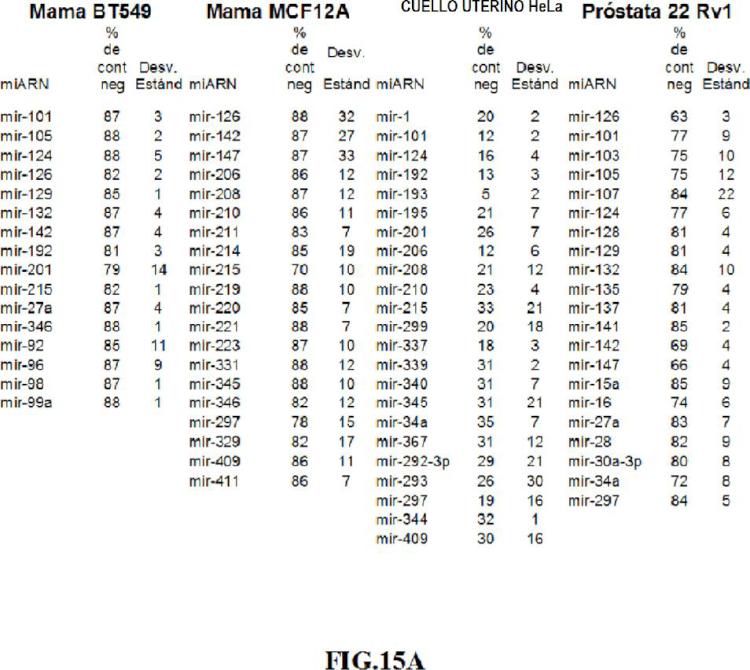
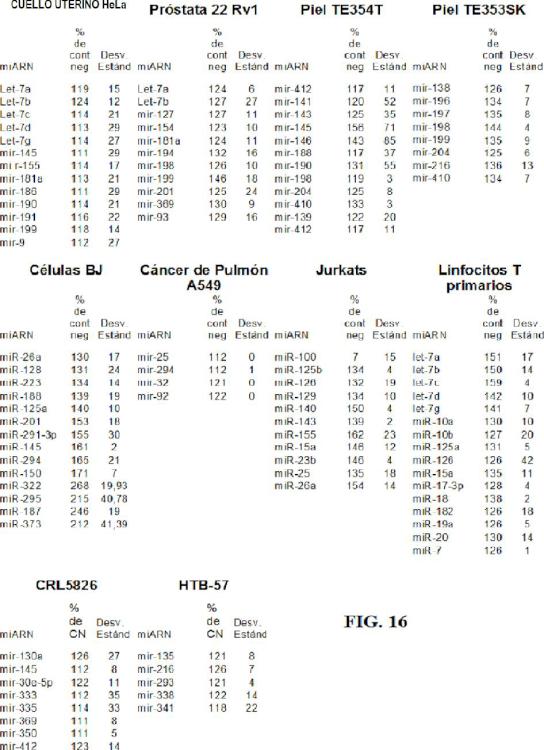
Fragmento de la descripción:
Procedimientos y composiciones que implican miARN y moléculas inhibidoras de miARN Campo de la invención
La presente invención se refiere, en general, al campo de la biología molecular. Más particularmente, concierne a procedimientos y composiciones que implican moléculas de ácidos nucleicos que estimulan microARN (miARN) y que inhiben miARN. Se describen los procedimientos y composiciones que implican moléculas sintéticas de miARN y moléculas inhibidoras de miARN. Además, también se describen procedimientos y composiciones para identificar miARN que contribuyen a los procesos celulares. Además, la identificación de miARN que contribuyen a los procesos celulares proporciona dianas para la intervención terapéutica así como el análisis diagnóstico y/o pronóstico.
Descripción de la técnica relacionada
En 2001, varios grupos utilizaron un nuevo procedimiento de clonación para aislar e identificar un gran grupo de microARN (miARN) de C. elegans, Drosophila, y seres humanos (Lagos-Quintana y col., 2001; Lau y col., 2001; Lee y Ambros, 2001). Se han identificado cientos de miARN en plantas y animales -incluyendo seres humanos- en los que no parece haber ARNsi endógenos. Por lo tanto, aunque son similares a los ARNsi, no obstante los miARN son distintos.
Los miARN observados tienen una longitud de aproximadamente 21-22 nucleótidos y provienen de precursores más largos, que ese transcriben a partir de genes que no codifican proteínas. Véase la revisión de Carrington y col. (2003). Las formas precursoras forman estructuras que se pliegan unas sobre otras; son procesadas por la nucleasa Dicer en los animales o DCL1 en las plantas. Las moléculas de miARN interrumpen la traducción por medio del emparejamiento de bases preciso o impreciso con sus dianas.
Unos miARN parece que están implicados en la regulación genética. Algunos miARN, que incluyen lin-4 y let-7 inhiben la síntesis proteica uniéndose a regiones 3 sin traducir (3 UTR) complementarias de los ARNm diana. Otros, incluyendo el miARN Scarecrow que se encuentra en plantas, funcionan como el ARNsi y se unen a secuencias de ARNm perfectamente complementarias para destruir la transcripción diana (Grishok y col., 2001).
La investigación en microARN se incrementa según los científicos están empezando a apreciar el amplio papel que estas moléculas tienen en la regulación de la expresión genética en eucariotas. Los dos miARN mejor conocidos, lin- 4 y let-7, regulan el tiempo de desarrollo en C. elegans regulando la traducción de una familia de miARN clave (revisado en Pasquinelli, 2002). Se han identificado varios cientos de miARN en C. elegans, Drosophila, ratón y seres humanos. Como sería de esperar en moléculas que regulan la expresión genética, los niveles de miARN muestran una variación entre tejidos y estadios de desarrollo. Además, un estudio muestra una fuerte correlación entre la expresión reducida de dos miARN y la leucemia linfocítica crónica, proporcionando un posible enlace entre los miARN y el cáncer (Calin, 2002). Aunque el campo aún es joven, hay una especulación sobre que los miARN podrían ser factores de transcripción importantes en la regulación de la expresión genética en eucariotas superiores.
Hay unos pocos ejemplos de que los miARN tienen papeles críticos en la diferenciación celular, el desarrollo temprano, y los procesos celulares tales como apoptosis y metabolismo de las grasas. Tanto lin-4 como let-7 regulan el paso de un estado larvario a otro durante el desarrollo de C. elegans (Ambros, 2003). El mir-15 y bantam son los miARN de Drosophila que regulan la muerte celular, aparentemente regulando la expresión de los genes implicados en la apoptosis (Brennecke y col., 2003, Xu y col., 2003). El miR14 también se ha implicado en el metabolismo graso (Xu y col., 2003). El Lsy-6 y miR-273 son miARN de C. elegans que regulan la asimetría en las neuronas quimiosensoriales (Chang y col., 2004). Otro miARN animal que regula la diferenciación celular es el miR-181, que dirige la diferenciación de células hematopoyéticas (Chen y col., 2004). Estas moléculas representan el intervalo total de miARN animales con funciones conocidas. Además, el documento W02004/076622 desvela el miARN miR- 133. La mejora del entendimiento de las funciones de los miARN sin duda revelará sistemas reguladores que contribuyen al desarrollo normal, diferenciación, comunicaciones Ínter e intra celulares, ciclo celular, angiogénesis, apoptosis, y muchos otros procesos celulares. Debido a sus importantes papeles en muchas funciones biológicas, es probable que los miARN ofrezcan puntos importantes para la intervención terapéutica o el análisis diagnóstico.
Caracterizar las funciones de biomoléculas como los miARN a menudo implica la introducción de las moléculas en las células o retirar las moléculas de las células y medir el resultado. Si se introduce un miARN en una célula y se produce apoptosis, entonces el miARN indudablemente participa en una ruta apoptótica. Los procedimientos para introducir y retirar miARN de las células se han descrito. Dos publicaciones recientes describen moléculas antisentido que se pueden utilizar para inhibir la actividad de miARN específicos (Meister y col., 2004; Hutvagner y col., 2004). Otra publicación describe el uso de plásmidos que se transcriben por ARN polimerasas y que producen miARN específicos cuando son transfectados en las células (Zeng y col., 2002). Estos dos grupos de reactivos se han utilizado para evaluar miARN sencillos.
Una limitación del sistema de expresión de miARN basado en plásmidos es que la eficacia de transfección de los plásmidos tiende a ser muy baja, con solo aproximadamente un 50% de células que expresan el ARN del plásmido en las células que son fáciles de transfectar. La eficacia de transfección para los plásmidos en células primarias son mucho más bajas con poco más del 10% de las células típicamente que expresan el ARN deseado. Por lo tanto, existe una necesidad para composiciones alternativas y procedimientos para introducir moléculas de miARN en células de forma que se puedan caracterizar y estudiar.
Sumario de la invención
La presente invención proporciona una molécula de ácido nucleico miARN sintético que comprende una secuencia con al menos un 80% de identidad de secuencia con la secuencia del miR-133 humano maduro para su uso en una terapia de un cáncer. También se proporciona un ácido nucleico miARN sintético de doble cadena de 17-30 nucleótidos de longitud que comprende un polinucleótido que tiene una secuencia con al menos un 80% de identidad de secuencia con una secuencia de miR-133 maduro que comprende los nucleótidos 54-75 de las SEC ID N2 94 o los nucleótidos 60-81, y un segundo polinucleótido por separado cuya secuencia de 5 a 3 es complementaria entre un 60% y el 100% para su uso como un medicamento.
También se proporciona el uso de un ácido nucleico miARN sintético como se ha mencionado anteriormente para reducir o aumentar la viabilidad celular o la proliferación celular o para inducir o inhibir la apoptosis, con la condición de que se excluyan los procedimientos de tratamiento del cuerpo humano o animal por medio de terapia. Más realizaciones de la invención se definen en las reivindicaciones. La siguiente descripción detallada se refiere a la presente invención en la medida del alcance de las reivindicaciones.
El término miARN se utiliza de acuerdo con su significado habitual y simple y se refiere a una molécula de microARN que se encuentra en las eucariotas que está implicada en la regulación genética basada en ARN. Véase, por ejemplo Carrington y col., 2003, que se incorpora en el presente documento por referencia. Generalmente, el término se utilizará para referirse a la molécula de ARN de cadena sencilla procesada a partir de un precursor. Se han identificado miARN individuales y se han secuenciado en distintos organismos, y se les ha dado nombres. Los nombres de los miARN y sus secuencias se proporcionan en el presente documento.
La presente invención se refiere, en algunas realizaciones de la invención, a moléculas cortas de ácido nucleico que funcionan como miARN o como inhibidores de miARN en una célula. El término corto se refiere a una longitud de un nucleótido simple que tenga 150 nucleótidos o poco más. Las moléculas de ácido nucleico son sintéticas. El término sintético significa que la molécula de ácido nucleico es aislada y no es idéntica a la secuencia (la secuencia entera) y/o estructura química de una molécula de ácido nucleico de origen natural, tal como una molécula precursora de miARN endógeno. Aunque en algunas realizaciones, los ácidos nucleicos de la invención no tienen una secuencia entera que es idéntica a una... [Seguir leyendo]
Reivindicaciones:
1. Una molécula de ácido nucleico miARN sintético que comprende una secuencia con al menos una identidad de secuencia de un 80% con la secuencia del miR-133 maduro humano para su uso en la terapia de un cáncer.
2. Un ácido nucleico miARN sintético para su uso en una terapia de un cáncer de acuerdo con la reivindicación 1 que además está definido como una molécula de ácido nucleico de entre 17 y 125 restos de longitud, que comprende
una región de miARN cuya secuencia de 5 a 3 es al menos idéntica en un 80% a un miARN maduro miR-133, y
una región complementaria cuya secuencia de 5 a 3 es complementaria entre un 60% y el 100% con la región de miARN.
3. Un ácido nucleico miARN sintético para su uso en una terapia de un cáncer de acuerdo con la reivindicación 1 o 2, que comprende una región de miARN cuya secuencia de 5 a 3 es idéntica en al menos un 85% a una secuencia de miR-133 maduro.
4. Un ácido nucleico miARN sintético para su uso en una terapia de un cáncer de acuerdo con la reivindicación 3, que comprende una región de miARN cuya secuencia de 5 a 3 es idéntica en al menos un 90% a una secuencia de miR-133 maduro.
5. Un ácido nucleico miARN sintético para su uso en una terapia de un cáncer de acuerdo con la reivindicación 3 o 4, que comprende una región de miARN cuya secuencia de 5 a 3 es idéntica a una secuencia de miR-133 maduro.
6. Un ácido nucleico miARN sintético para su uso en una terapia de un cáncer de acuerdo con una cualquiera de las reivindicaciones 1 a 5, en el que el ácido nucleico está comprendido de dos polinucleótidos separados.
7. Un ácido nucleico miARN sintético para su uso en una terapia de un cáncer de acuerdo con una cualquiera de las reivindicaciones 1 a 5, en el que el ácido nucleico es una molécula en horquilla.
8. Un ácido nucleico miARN sintético para su uso en una terapia de un cáncer de acuerdo con una cualquiera de las reivindicaciones 1 a 7, para su administración a una célula o a un paciente que tiene la célula identificada como que necesita una terapia de un cáncer.
9. Un ácido nucleico miARN sintético para su uso en una terapia de un cáncer de acuerdo con la reivindicación 8 en el que la célula está identificada como una célula que necesita terapia para un cáncer.
10. Un ácido nucleico miARN sintético para su uso en una terapia de un cáncer de acuerdo con una cualquiera de las reivindicaciones 1 a 9 para su uso en una terapia de tratamiento de un cáncer de pulmón, cáncer de colon, cáncer de piel, o leucemia.
11. Un ácido nucleico miARN sintético de cadena doble de 17-30 nucleótidos de longitud que comprende un polinucleótido que tiene una secuencia con una identidad de secuencia de al menos un 80% con una secuencia de miR-133 maduro que comprende los nucleótidos 54-75 de la SEC ID N2 94 o los nucleótidos 60-81 de la SEC ID N2 95, y un segundo polinucleótido separado cuya secuencia de 5 a 3 es complementaria entre un 60% y el 100% con el primer polinucleótido, para su uso como un medicamento.
12. Un ácido nucleico miARN sintético para su uso como un medicamento de acuerdo con la reivindicación 11, que se caracteriza porque el ácido nucleico está definido además como en una cualquiera de las reivindicaciones 2 a 7.
13. Un ácido nucleico miARN sintético para su uso como un medicamento de acuerdo con la reivindicación 11 u 12 que comprende además uno o más de los siguientes:
(i) un grupo de sustitución del fosfato o el hidroxilo del nucleótido en el extremo 5 de la cadena complementaria de la molécula de ARN;
(ii) una o más modificaciones en los azúcares de los primeros o últimos 1 a 6 restos de la región complementaria; o
(iii) una no complementariedad entre uno o más nucleótidos de los últimos 1 a 5 restos del extremo 3 de la región complementaria y los correspondientes nucleótidos de la región miARN.
14. Un ácido nucleico miARN sintético para su uso como un medicamento de acuerdo con la reivindicación 11 u 12, que comprende i) al menos un nucleótido modificado que bloquea el OH 5 o fosfato en el extremo 5, en el que la modificación del al menos un nucleótido es un NH2, biotina, un grupo amino, un grupo alquilamino inferior, un grupo acetilo o una modificación 2 oxígeno-metilo (2 O-Me), o ii) al menos una modificación de la ribosa seleccionada de entre 2F, 2NH2, 2N3, 4tio, o 2 O-CH3.
15. Un ácido nucleico miARN sintético para su uso como un medicamento de acuerdo con las reivindicaciones 11 a 14 que es un polinucleótido de cadena sencilla, que de preferencia además comprende una horquilla, o un polinucleótido de cadena doble.
16. El uso de un ácido nucleico miARN sintético como se define en una cualquiera de las reivindicaciones 1 a 15 5 para la reducción o el aumento de la viabilidad celular o la proliferación celular, con la condición de que se excluyan
los procedimientos para el tratamiento del cuerpo humano o animal por medio de cirugía o terapia.
Patentes similares o relacionadas:
Proteínas del factor VIII que tienen secuencias ancestrales, vectores de expresión, y usos relacionados con ellos, del 15 de Julio de 2020, de EMORY UNIVERSITY: Una proteína FVIII recombinante o quimérica que comprende una o más mutaciones ancestrales y una eliminación del dominio B, y en donde la secuencia […]
Vacuna subunitaria contra Mycoplasma spp., del 1 de Julio de 2020, de Agricultural Technology Research Institute: Una composición para prevenir una infección por Mycoplasma spp., que comprende: un principio activo, que comprende una proteína de PdhA; y un adyuvante […]
Método para romper un ácido nucleico y añadir un adaptador por medio de transposasa y reactivo, del 1 de Julio de 2020, de MGI Tech Co., Ltd: Un metodo para romper un acido nucleico y anadir un adaptador por medio de una transposasa, que comprende las siguientes etapas: interrumpir […]
Composiciones para modular la expresión de SOD-1, del 24 de Junio de 2020, de Biogen MA Inc: Un compuesto antisentido según la siguiente fórmula: mCes Aeo Ges Geo Aes Tds Ads mCds Ads Tds Tds Tds mCds Tds Ads mCeo Aes Geo mCes Te (secuencia […]
Oligonucleótidos para tratar una enfermedad ocular, del 13 de Mayo de 2020, de ProQR Therapeutics II B.V: Un oligonucleótido antisentido (OAS) que es capaz de inducir omisión del pseudoexón 40 (PE40) de pre-ARNm de USH2A humano, donde dicho OAS comprende una secuencia […]
Composiciones promotoras, del 6 de Mayo de 2020, de UNIVERSITY OF IOWA RESEARCH FOUNDATION: Una secuencia promotora aislada que comprende un ácido nucleico de entre 500 y 1700 nucleótidos de longitud que tiene por lo menos un 98% de identidad con la SEQ […]
Transfección mediada por células apoptóticas de células de mamífero con ARN de interferencia, del 22 de Abril de 2020, de LOMA LINDA UNIVERSITY: Una célula de mamífero apoptótica o preapoptótica para su uso en la prevención del rechazo de trasplantes, en la que la célula de mamífero […]
Ácidos ribonucleicos con nucleótidos modificados con 4-tio y procedimientos relacionados, del 15 de Abril de 2020, de Translate Bio, Inc: Una molécula de ARNm que tiene una región codificante y opcionalmente, una o más regiones no codificantes, en donde al menos el 25% de los residuos de nucleótidos del […]