Procedimiento y sistema para determinar la concentración de un complejo de analyte-enzima o conjugado de analyte-enzima, en especial para la detección electroquímica de los analytes.
Procedimiento para la detección electroquímica de un analyte, con las siguientes medidas:
- se utiliza una enzima, cuya concentración representa una medida para la concentración del analyte, pormedio de que está enlazada con el analyte directa o indirectamente o es desplazada por el analyte;
- se utiliza un sustrato, que se transforma desde la enzima mediante escisión hidrolítica, en donde se obtieneuna molécula reporter, que en ciertas condiciones puede transformarse electroquímicamente de formareversible, en donde el sustrato es estable;
- se utiliza un sensor con al menos un electrodo, en donde el electrodo está polarizado mientras dura unafase de medición (A), de tal modo que la molécula reporter se oxida o reduce, y en donde el electrodo estápolarizado mientras dura una fase de relajación (B), de tal modo que la forma oxidada o reducida de lamolécula reporter en el mismo electrodo 2 se reduce u oxida de nuevo;
- la corriente circulante durante la fase de medición (A) se detecta como medida para la concentración delsustrato transformado desde la enzima.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP2006/064842.
Solicitante: SIEMENS AKTIENGESELLSCHAFT.
Nacionalidad solicitante: Alemania.
Dirección: WITTELSBACHERPLATZ 2 80333 MUNCHEN ALEMANIA.
Inventor/es: GUMBRECHT, WALTER, DR., MUND, KONRAD, BARLAG,HEIKE.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- G01N27/49 FISICA. › G01 METROLOGIA; ENSAYOS. › G01N INVESTIGACION O ANALISIS DE MATERIALES POR DETERMINACION DE SUS PROPIEDADES QUIMICAS O FISICAS (procedimientos de medida, de investigación o de análisis diferentes de los ensayos inmunológicos, en los que intervienen enzimas o microorganismos C12M, C12Q). › G01N 27/00 Investigación o análisis de materiales mediante el empleo de medios eléctricos, electroquímicos o magnéticos (G01N 3/00 - G01N 25/00 tienen prioridad; medida o ensayo de variables eléctricas o magnéticas o de las propiedades eléctricas o magnéticas de los materiales G01R). › Sistemas que implican la fijación de la corriente en un valor único específico, o en un pequeño margen de valores, para una tensión aplicada, con el fin de producir la medida selectiva de una o varias especies iónicas particulares.
- G01N33/543 G01N […] › G01N 33/00 Investigación o análisis de materiales por métodos específicos no cubiertos por los grupos G01N 1/00 - G01N 31/00. › con un soporte insoluble para la inmovilización de compuestos inmunoquímicos.
PDF original: ES-2446241_T3.pdf
Fragmento de la descripción:
Procedimiento y sistema para determinar la concentración de un complejo de analyte-enzima o conjugado de analyte-enzima, en especial para la detección electroquímica de los analytes.
La invención se refiere a un procedimiento y a un sistema para determinar la concentración de un complejo de analyte-enzima o conjugado de analyte-enzima, en especial para la detección electroquímica de los analytes. En un procedimiento de este tipo se transforma desde la enzima un sustrato mediante escisión hidrolítica en una molécula reporter, cuya concentración o variación de concentración en el electrolito en reposo se determina mediante un procedimiento de medición amperométrico, que se basa en la oxidación y reducción de la molécula reporter en el mismo electrodo de metal noble.
Para determinar anticuerpos, antígenos o ADN en sangre, agua, aire o alimentos se usan los llamados biosensores. Se basan en el enlace específico de los analytes con una molécula de captador, es decir, por ejemplo un anticuerpo con un antígeno o una secuencia de ADN con la secuencia de captador ADN complementaria. La comprobación de este acontecimiento de enlace se realiza con frecuencia mediante procedimientos ópticos. Con ello se añaden colorantes fluorescentes, por ejemplo durante una análisis de ADN mediante la PCR en los analytes y, posteriormente, se leen en las posiciones con diferentes secuencias de captador. Estos sistemas ópticos son evidentemente de manipulación cara y compleja. Los aparatos necesarios son sensibles y no adecuados para pruebas de campo.
Una alternativa adecuada son aquí los bionsensores electroquímicos. Aquí se realiza la detección mediante la transformación de una sustancia electroquímica. Está muy extendida la detección electroquímica, por ejemplo en los sensores de glucosa. La glucosa se oxida mediante una enzima redox, la glucosa oxidasa, y al mismo tiempo se reduce el oxígeno presente. En perfeccionamientos de estos sensores de glucosa los mediadores sustituyen el oxígeno. Durante la oxidación de la glucosa mediante la enzima redox se reduce al mismo tiempo el mediador, por ejemplo 1, 1-dimetil ferrocenos. La oxidación electroquímica del mediador reducido enzimáticamente, para la determinación amperométrica de la concentración de glucosa, puede realizarse aquí con potenciales claramente inferiores, con lo que la medición se hace más precisa y menos propensa a fallos. En este contexto se han desarrollado numerosos procedimientos pulsatorios amperométricos, que no determinan la cantidad total en el mediador redox, sino sólo la parte reducida antes enzimáticamente.
Sin embargo, en el caso de la detección electroquímica de acontecimientos de enlace es necesario medir con la mayor sensibilidad posible la cantidad absoluta de una sustancia redox activa. El verdadero marcador para la presencia de los analytes en una posición de sensor es la propia enzima. Durante el análisis de ADN se añade, por ejemplo en la PCR, un marcador de biotina a los analytes. Sobre un biosensor están enlazados en las diferentes posiciones de sensor diferentes secuencias de captador de ADN. El analyte sólo se hibridiza en las secuencias ajustadas y el analyte no enlazado se extrae por lavado. Para reconocer este acontecimiento de enlace se enlaza a continuación con la molécula de marcador de biotina una estreptavidina-enzima, por ejemplo fosfatasa alcalina. Si se adiciona sustrato de enzima, por ejemplo p-aminofenilfosfato, sólo se libera p-aminofenol en las posiciones de sensor en las que se ha enlazado el analyte, mediante la escisión hidrolítica del fosfato.
La utilización de p-aminofenilfosfatos como sustrato para la fosfatasa alcalina se presenta en CLIN. CHEM. 36/11, páginas 1941 – 1944 (1990) , en donde se describe un inmunoensayo basado en gotas. Si se ha enlazado analyte con el anticuerpo inmovilizado en gotas, se indica también aquí mediante fosfatasa alcalina. Las gotas se incuban mediante p-aminofenilfosfato y después se analiza en la solución sobresaliente el p-aminofenilfosfato en un sistema de análisis de inyección en flujo. Con ello esta solución fluye a través de un sensor electroquímico, cuyo electrodo de trabajo está polarizado constantemente a unos +0, 1 V vs. electrodo de referencia de Ag/AgCI. La medición en el electrolito fluyente o en el volumen de muestra tiene la ventaja de que no tiene lugar empobrecimiento digno de mención del p-aminofenol delante del electrodo. Mediante el flujo se envía más tarde constantemente. Un sistema así evidentemente no tiene capacidad de microsistema. El sensor electroquímico sólo puede leer una muestra a la vez y los volúmenes necesarios son grandes.
Siempre que se desee utilizar un conjunto de sensores con diferentes captadores – ya se trate ahora de secuencias de captador de ADN o anticuerpos -, la detección electroquímica debe llevarse a cabo en electrolitos en reposo, para que los sensores detecten sólo la señal de los captadores inmovilizados sobre los mismos. La presencia de la enzima se indica mediante un aumento de la concentración de p-aminofenol. Para esto no son adecuados sensores electroquímicos sencillos, en los que el electrodo de trabajo está situado a un potencial constante. Mediante la transformación que se desarrolla constantemente del producto de enzima éste se consume. Al aumento de la concentración mediante la actividad de enzima se superpone por lo tanto una reducción de la concentración mediante la propia medición.
Para superar este problema se propone en el documento US 6 682 648 B1 el uso de conjuntos de electrodos interdigitales. Cada sensor se compone de dos electrodos interdigitales. Mediante un bipotenciostato se polariza uno de los electrodos positivamente y el otro negativamente. El p-aminofenol se oxida en el primer electrodo y con ello se consume. Si a continuación puede difundirse hacia el segundo electrodo, allí se reduce y la medición vuelve a estar disponible en el primer electrodo.
Sin embargo, la premisa para este último sistema de ciclaje redox es que la separación entre estos electrodos sea muy reducida, para que el transporte mediante difusión de p-aminofenol y el producto de oxidación quinonimina entre los electrodos tenga lugar con la suficiente velocidad, para lo que se hace referencia a la publicación K. Aoki,
J. Electroanal. Chem, 270 (1989) , página 35. En el documento ya citado US 6 682 648 B1 se propone para esto la utilización de electrodos interdigitales con dimensiones estructurales inferiores a 1 µm. De aquí se obtiene que la fabricación de un conjunto de biosensores con tales electrodos interdigitales es compleja y cara.
Se ofrecen otras indicaciones sobre la medición, en especial en fluidos o también para mediciones bioquímicas, en los documentos DE 43 35 241 A1, DE 41 31 731 A1, DE 197 17 809 U1 y DE 199 17 052 A1. Un procedimiento para la medición eletroquímica del ciclaje redox con una disposición de electrodos según la praxis se describe en detalle en el documento WO 01/67587 A1.
Partiendo del último estado de la técnica, la tarea de la invención consiste en proponer un procedimiento o sistema en el que sea posible la determinación de concentraciones de una sustancia redox-activa en concentraciones de µM en conjuntos de electrodos planos con diámetros º 30 µm, de forma preferida º 50 µm. Con ello el sistema no debe ser convectivo, es decir ni el electrodo ni la solución deben agitarse o moverse y la frecuencia de medición debe ser
º 1 Hz. Aparte de esto debe crearse un dispositivo de medición correspondiente.
La tarea es resuelta conforme a la invención, en un procedimiento de la clase citada al comienzo, mediante las medidas de la reivindicación 1. Un sistema correspondiente se indica en la reivindicación 12. Perfeccionamientos del procedimiento conforme a la invención y del sistema relacionado con ella son objeto de las reivindicaciones subordinadas.
En la invención se propone pulsar el potencial del electrodo de trabajo, lo que ya se ha propuesto en otro contexto. Además de esto, sin embargo, en la presente invención se forman a continuación alternativamente fases de medición así como fases de relajación, en donde las longitudes de pulso de las fases de medición se eligen de tal modo, que hacia el final del pulso la corriente capacitiva es pequeña con relación a la corriente de Faraday, y en donde las longitudes de pulso de las fases de relajación se eligen de tal modo, que hacia el final del pulso el gradiente de concentración está relajado, de tal manera que al principio de la siguiente fase de medición la variación de concentración del producto de enzima redox-activo – causada por el consumo del producto de enzima mediante la propia medición – se... [Seguir leyendo]
Reivindicaciones:
1. Procedimiento para la detección electroquímica de un analyte, con las siguientes medidas:
- se utiliza una enzima, cuya concentración representa una medida para la concentración del analyte, por medio de que está enlazada con el analyte directa o indirectamente o es desplazada por el analyte;
- se utiliza un sustrato, que se transforma desde la enzima mediante escisión hidrolítica, en donde se obtiene una molécula reporter, que en ciertas condiciones puede transformarse electroquímicamente de forma reversible, en donde el sustrato es estable;
- se utiliza un sensor con al menos un electrodo, en donde el electrodo está polarizado mientras dura una fase de medición (A) , de tal modo que la molécula reporter se oxida o reduce, y en donde el electrodo está
polarizado mientras dura una fase de relajación (B) , de tal modo que la forma oxidada o reducida de la molécula reporter en el mismo electrodo 2 se reduce u oxida de nuevo;
- la corriente circulante durante la fase de medición (A) se detecta como medida para la concentración del sustrato transformado desde la enzima.
2. Procedimiento según la reivindicación 1, caracterizado porque se utiliza un analyte con un elemento de 15 marcaje.
3. Procedimiento según la reivindicación 1, caracterizado porque se utiliza una enzima con un elemento de acoplamiento, el cual se enlaza específicamente con el elemento de marcaje del analyte.
4. Procedimiento según una de las reivindicaciones 1 a 3, caracterizado porque la enzima está enlazada con el analyte.
5. Procedimiento según la reivindicación 3 ó 4, caracterizado porque está inmovilizada sobre o cerca de un electrodo una molécula de captador, la cual se enlaza específicamente con el analyte.
6. Procedimiento según una de las reivindicaciones anteriores, caracterizado porque hacia el final de la fase de medición (A) la corriente capacitiva es pequeña con relación a la corriente de Faraday.
7. Procedimiento según la reivindicación 6, caracterizado porque hacia el final de la fase de relajación (B) se 25 reducen en gran medida de nuevo las moléculas reporter oxidadas durante la fase de medición (A) .
8. Procedimiento según la reivindicación 6, caracterizado porque hacia el final de la fase de relajación (B) se oxidan en gran medida de nuevo las moléculas reporter reducidas durante la fase de medición (A) .
9. Procedimiento según la reivindicación 8, caracterizado porque los potenciales se eligen de tal modo, que
las reacciones de reducción y oxidación de la molécula reporter se desarrollan en la región de corriente 30 límite de difusión.
10. Procedimiento según la reivindicación 8, caracterizado porque la tasa de repetición para la fase de medición (A) es de al menos 0, 5 Hz.
11. Procedimiento según una de las reivindicaciones anteriores, caracterizado porque la reducción o la oxidación de la molécula reporter durante la fase de relajación (B) se realiza por completo.
12. Sistema para la detección electroquímica de un analyte conforme al procedimiento según la reivindicación 1, con
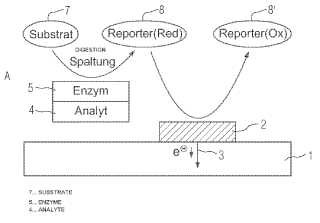
- una enzima (5) , cuya concentración representa una medida para la concentración del analyte (4) ,
- un sustrato (7) , que se transforma desde la enzima (5) mediante escisión hidrolítica,
-una molécula reporter (8, 8’) , que en las condiciones en las que el sustrato (7) es estable, puede 40 transformarse electroquímicamente de forma reversible, y
- un sensor (1) con al menos un electrodo (2) , que está configurado de tal modo que está polarizado mientras dura una fase de medición (A) , de tal modo que la molécula reporter (8, 8’) se oxida o reduce, y está polarizado mientras dura una fase de relajación (B) , de tal modo que la forma oxidada o reducida de la molécula reporter en el mismo electrodo (2) se reduce u oxida de nuevo, en donde la corriente circulante durante la fase de medición (A) es una medida para la concentración del sustrato transformado desde la enzima (5) .
13. Sistema según la reivindicación 12, caracterizado porque la enzima (5) contiene un elemento de acoplamiento, el cual se enlaza específicamente con el elemento de marcaje del analyte (5) .
14. Sistema según la reivindicación 12, caracterizado porque la enzima (5) puede enlazarse con el analyte (4) .
15. Sistema según la reivindicación 12, caracterizado porque está inmovilizada sobre o cerca de un electrodo una molécula de captador (4) , la cual puede enlazarse específicamente con el analyte (4) .
Patentes similares o relacionadas:
Método de determinación de la presencia y/o cantidad de moléculas diana, del 22 de Julio de 2020, de Canopy Biosciences, LLC: Método para el análisis de células individuales en una muestra de sangre mediante la determinación de la presencia y/o cantidad de una o más moléculas […]
Kit de reactivos utilizado para detectar gastrina-17 y método de preparación y aplicación para el kit de reactivos, del 15 de Julio de 2020, de Shenzhen New Industries Biomedical Engineering Co., Ltd: Un kit para detectar gastrina-17, caracterizado porque comprende un componente A y un componente B, en donde el componente A es un primer […]
Un sustrato para inmovilizar sustancias funcionales y un método para preparar las mismas, del 15 de Julio de 2020, de Temasek Polytechnic: Un sustrato sólido que tiene compuestos dispuestos sobre el mismo, en donde se inmoviliza una molécula funcional sobre los compuestos, teniendo cada compuesto una cadena que […]
Análisis biológico autónomo de alta densidad, del 1 de Julio de 2020, de BioFire Diagnostics, LLC: Recipiente para realizar reacciones de amplificación en un sistema cerrado que comprende una porción flexible que tiene una serie de blísteres […]
Chip de análisis y aparato de análisis de muestras, del 1 de Julio de 2020, de Takano Co., Ltd: Un chip de análisis que comprende: un sustrato conformado sustancialmente en forma de disco; un puerto de inyección formado […]
Dispositivo para la detección de analitos, del 1 de Julio de 2020, de TECHLAB, INC.: Un dispositivo para detectar por lo menos una sustancia de interés en una muestra líquida, comprendiendo el dispositivo: (a) una unidad que […]
Estructuras para controlar la interacción de luz con dispositivos microfluídicos, del 3 de Junio de 2020, de Opko Diagnostics, LLC: Un sistema de ensayo múltiplex que comprende: un artículo que soporta ensayos en fase sólida, comprendiendo dicho artículo un sustrato plano rígido y comprendiendo […]
Uso de un estándar para la detección de agregados de proteínas de una enfermedad por plegamiento incorrecto de proteínas, del 27 de Mayo de 2020, de FORSCHUNGSZENTRUM JULICH GMBH: Uso de un estándar, que comprende una nanopartícula inorgánica con un tamaño de 2 a 200 nm, en cuya superficie ya sea mediante i) ácido carboxílico-espaciador-maleimida […]