Procedimiento para la preparación de (R)-(-)-salbutamol ópticamente puro y sus sales farmacéuticamente aceptables.
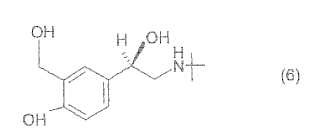
Procedimiento para la preparación de (R)-(-)-salbutamol ópticamente puro de fórmula (6)**Fórmula**
y sus sales farmacéuticamente aceptables,
comprendiendo dicho procedimientoa) disolver una mezcla racémica de 4-bencilsalbutamol (precursor de salbutamol) de fórmula (1):**Fórmula**
y ácido (+)-4-nitrotartranílico de fórmula (2):**Fórmula**
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/IN2006/000391.
Solicitante: AARTI HEALTHCARE LIMITED.
Nacionalidad solicitante: India.
Dirección: 71, UDYOG KSHETRA, 2ND FLOOR MULUND GOREGAON LINK ROAD MULUND (W) MUMBAI 400 080 MAH INDIA.
Inventor/es: DESAI PARIMAL,HANSMUKH, SALVI NARENDRA,JAGANNATH, PATRAVALE BHARATKUMAR,SURENDRA, SEETHARAMAN,SUBRAMANIAN, PATIL DILIP,JIBHAU, GHOGARE KHANDU,SHANKAR.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C07B57/00 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07B PROCESOS GENERALES DE QUIMICA ORGANICA; SUS APARATOS (preparación de ésteres de ácidos carboxílicos por telomerización C07C 67/47; procesos para la preparación de compuestos macromoleculares, p.ej. telomerzación C08F, C08G). › Separación de compuestos ópticamente activos.
- C07C213/10 C07 […] › C07C COMPUESTOS ACICLICOS O CARBOCICLICOS (compuestos macromoleculares C08; producción de compuestos orgánicos por electrolisiso electroforesis C25B 3/00, C25B 7/00). › C07C 213/00 Preparación de compuestos que contienen grupos amino e hidroxi, amino e hidroxi eterificados o amino e hidroxi esterificados unidos a la misma estructura carbonada. › Separación; Purificación; Estabilización; Empleo de aditivos.
- C07C215/60 C07C […] › C07C 215/00 Compuestos que contienen grupos amino e hidroxi unidos a la misma estructura carbonada. › teniendo la cadena dos átomos de carbono entre los grupos amino y el ciclo aromático de seis miembros o el sistema cíclico condensado que contenga este ciclo.
- C07C217/70 C07C […] › C07C 217/00 Compuestos que contienen grupos amino e hidroxi eterificados unidos a la misma estructura carbonada. › unidos a través de cadenas carbonadas con dos átomos de carbono entre los grupos amino y el ciclo aromático de seis miembros o el sistema cíclico condensado que contiene este ciclo.
PDF original: ES-2431844_T3.pdf
Fragmento de la descripción:
Procedimiento para la preparación de (R) - (-) -salbutamol ópticamente puro y sus sales farmacéuticamente aceptables.
Campo técnico de la invención La presente invención se refiere a un procedimiento para la preparación de (R) - (-) -salbutamol ópticamente puro y sus sales farmacéuticamente aceptables.
El salbutamol se conoce también como albuterol. El nombre químico del salbutamol es 2- (N-t-butilamino) -1- (4hidroxi-3-hidroximetilfenil) etanol. El salbutamol es un agonista de los receptores 2 adrenérgicos de acción corta que se utiliza para el alivio de los broncoespasmos en afecciones como el asma y la enfermedad pulmonar obstructiva crónica (EPOC) . Se encuentra habitualmente disponible como racemato. Se ha documentado el hecho de que el isómero R del salbutamol es más potente, aproximadamente 80 veces más potente, que su isómero S.
Antecedentes de la invención En Hartley et al. (Journal of Medicinal Chemistr y , vol.14, 895-896) , se da a conocer un método para la redisolución de un precursor del salbutamol mediante el uso de derivados del ácido tartárico, tal como el ácido di-ptoluoiltartárico.
El documento US 5.399.765 da a conocer un procedimiento para la preparación de los isómeros R y S ópticamente puros mediante la redisolución de una mezcla de enantiómeros de un precursor del albuterol, el 5-[2-[ (1, 1dimetiletil) amino]-1-hidroxietil]-2-hidroxibenzoato de metilo, utilizando un ácido quiral como agente de redisolución. El ácido quiral se selecciona de entre el grupo que comprende ácido (-) -di-toluoil-L-tartárico y ácido (+) -di-toluoil-Dtartárico. Dicho procedimiento da lugar a una sal diastereoisomérica con un 80-99% de exceso enantiomérico (e. e.) de los enantiómeros deseados del albuterol, que, mediante el tratamiento con una base, libera los enantiómeros de salbutamol deseados. Dicho procedimiento no es rentable, ya que el rendimiento de los isómeros R y S ópticamente puros está comprendido dentro del intervalo 21-43%.
El documento US nº 5.442.118 describe un procedimiento para la preparación de los isómeros R y S ópticamente puros del albuterol y etanolaminas similares mediante la reducción asimétrica de iminocetonas con borano como agente reductor, tal como sulfuro de boranodimetilo o borano-tetrahidrofurano, en presencia de un catalizador de 1, 3, 2-oxazaborol quiral. Dicho procedimiento utiliza reactivos costosos y proporciona una pureza óptica baja, del orden del 93-95% de e. e.
El documento US 6.365.756 describe un procedimiento para la producción de (R) -albuterol o (S) -albuterol ópticamente enriquecidos preparando en primer lugar un nuevo derivado cetálico del albuterol, concretamente el 2 (N-t-butilamino) -1- (+2, 2-dimetil-1, 2-benzodioxin-6-il) etanol. La redisolución se lleva a cabo con un derivado del ácido tartárico quiral, tal como el ácido (+) -di-O-benzoiltartárico o (-) -di-O-benzoiltartárico o el ácido di-toluiltartárico. El procedimiento es un procedimiento complejo de varias etapas que comprende la redisolución del derivado cetálico. Dicho procedimiento también da lugar a un exceso enantiomérico bajo, del orden del 65% (sobre la base de los valores indicados en los ejemplos) , lo que disminuye su viabilidad económica. Dicho procedimiento también requiere cristalizaciones adicionales, con lo que se reduce el rendimiento global.
El documento WO02/48090 da a conocer un procedimiento para la preparación de (R) -salbutamol y/o (S) -salbutamol ópticamente puros mediante la redisolución de una mezcla racémica u ópticamente impura de enantiómeros de salbutamol o su precursor utilizando ácido (L) -tartárico o (D) -tartárico quiral. Dicho procedimiento da lugar a un buen exceso enantiomérico. El agente de redisolución no se recupera ni se reutiliza. El isómero S no deseado del salbutamol tampoco se convierte en el isómero R deseado.
El documento WO2005/113481 da a conocer un procedimiento para la preparación de (R) -salbutamol. Se trata una mezcla de salbutamol racémico con ácido D-di-benzoiltartárico en una relación molar comprendida entre 1:0, 5 y 1:1, 3 y en presencia de un alcohol C1 a C4 para obtener (R) -salbutamol.ácido D-di-benzoiltartárico. El producto en bruto se cristaliza mediante inseminación con (R) -salbutamol.ácido D-di-benzoiltartárico. A continuación, el producto se recristaliza en metanol. Dicho procedimiento da lugar a un gran exceso enantiomérico, pero también a un bajo rendimiento global (sobre la base de los valores indicados en los ejemplos) y, por consiguiente, no resulta económicamente viable.
El documento US nº 7.049.469 da a conocer un procedimiento para la preparación de (R) -salbutamol. Dicho procedimiento comprende la hidrogenación asimétrica de salbutamona proquiral en presencia de rodio y un ligando de fosfina bidentado quiral como sistema catalizador. Dicho procedimiento utiliza un catalizador muy costoso y da lugar a un exceso enantiomérico bajo. El coste del reactivo y el exceso enantiomérico bajo reducen la viabilidad del procedimiento a escala industrial.
El documento WO95/32178A da a conocer la preparación enantioselectiva de albuterol ópticamente puro.
En general, la mayoría de los procedimientos según la técnica anterior no recuperan ni reutilizan el agente de redisolución, lo que los hace costosos. A pesar de los muchos intentos de la técnica anterior para preparar 5 salbutamol ópticamente puro, persiste la necesidad de desarrollar procedimientos rentables sin sacrificar la pureza óptica del salbutamol.
Objetivos de la invención Un objetivo de la presente invención consiste en dar a conocer un procedimiento eficiente y rentable para la preparación de (R) -salbutamol con una pureza óptica elevada y con un rendimiento elevado mediante la redisolución de una mezcla racémica de precursor de salbutamol con un ácido (+) -4-nitrotartranílico como agente de redisolución en presencia de un sistema de disolvente binario que consiste en acetato de alquilo y un alcohol C1 a C4 de cadena ramificada o normal con una recuperación simultánea del ácido (+) -4-nitrotartranílico.
Otro objetivo de la presente invención consiste en dar a conocer un procedimiento eficiente y rentable para la preparación de (R) -salbutamol con una pureza óptica elevada y con un rendimiento elevado mediante la redisolución de una mezcla racémica de precursor de salbutamol con un ácido (+) -4-nitrotartranílico como agente de redisolución en presencia de un sistema de disolvente binario que consiste en acetato de alquilo y un alcohol C1 a C4 de cadena ramificada o normal con una recuperación simultánea del isómero S no deseado del salbutamol y trazas del isómero R, y la racemización de los mismos en una mezcla racémica de 4-bencilsalbutamol para su utilización en el procedimiento según la presente invención, con el fin de reducir al mínimo el desperdicio de los reactivos.
Descripción detallada de la invención Según la presente invención, se da a conocer un procedimiento para la preparación de (R) - (-) -salbutamol ópticamente puro de fórmula (6) :
Fórmula (6)
y sus sales farmacéuticamente aceptables, comprendiendo dicho procedimiento a) la disolución de una mezcla racémica de 4-bencilsalbutamol (precursor de salbutamol) de fórmula (1) :
Fórmula (1)
y ácido (+) -4-nitrotartranílico de fórmula (2) :
40
Fórmula (2)
en un sistema de disolvente binario que comprende acetato de alquilo y un alcohol C1 - C4 de cadena ramificada o normal a la temperatura de reflujo a fin de formar una solución;
b) el enfriamiento de la solución para que cristalice la sal del ácido 4-nitrotartranílico del isómero R del 4bencilsalbutamol de fórmula (3) :
Fórmula (3)
y el aislamiento del compuesto de fórmula (3) por filtración a fin de dejar la sal del ácido 4-nitrotartranílico del 15 isómero S del 4-bencilsalbutamol de fórmula (7) :
Fórmula (7)
y trazas del compuesto de fórmula (3) en el filtrado;
b) la purificación de la sal del ácido 4-nitrotartranílico del isómero R del 4-bencilsalbutamol de fórmula (3) mediante su tratamiento con un sistema de disolvente binario que comprende acetato de alquilo y un alcohol C1 a C4 de cadena ramificada o normal, y el aislamiento del compuesto de fórmula (3) por filtración;
c) el tratamiento de la sal del ácido 4-nitrotartranílico del isómero R del 4-bencilsalbutamol de fórmula (3) con una solución de ácido fórmico al 5-15% a fin de obtener la sal del ácido fórmico del isómero R del 4-bencilsalbutamol de fórmula (4) :
y la liberación de ácido (+) -4-nitrotartranílico de fórmula (2) ;
d) la separación del ácido (+) -4-nitrotartranílico de fórmula... [Seguir leyendo]
Reivindicaciones:
1. Procedimiento para la preparación de (R) - (-) -salbutamol ópticamente puro de fórmula (6)
y sus sales farmacéuticamente aceptables, comprendiendo dicho procedimiento Fórmula (1)
y ácido (+) -4-nitrotartranílico de fórmula (2) :
Fórmula (2)
en un sistema de disolvente binario que comprende acetato de alquilo y un alcohol C1 - C4 de cadena ramificada o normal a la temperatura de reflujo a fin de formar una solución;
b) enfriar la solución para que cristalice la sal del ácido 4-nitrotartranílico del isómero R del 4-bencilsalbutamol de 25 fórmula (3) :
Fórmula (3)
y aislar el compuesto de fórmula (3) por filtración a fin de dejar la sal del ácido 4-nitrotartranílico del isómero S del 4bencilsalbutamol de fórmula (7) :
Fórmula (7)
y trazas del compuesto de fórmula (3) en el filtrado;
b) purificar la sal del ácido 4-nitrotartranílico del isómero R del 4-bencilsalbutamol de fórmula (3) mediante su tratamiento con un sistema de disolvente binario que comprende acetato de alquilo y un alcohol C1 a C4 de cadena ramificada o normal, y aislar el compuesto de fórmula (3) por filtración;
c) tratar la sal del ácido 4-nitrotartranílico del isómero R del 4-bencilsalbutamol de fórmula (3) con una solución de ácido fórmico al 5-15% a fin de obtener la sal del ácido fórmico del isómero R del 4-bencilsalbutamol de fórmula (4) :
Fórmula (4)
y liberar el ácido (+) -4-nitrotartranílico de fórmula (2) ;
d) separar el ácido (+) -4-nitrotartranílico de fórmula (2) por filtración;
e) enfriar el filtrado que contiene la sal del ácido fórmico del isómero R del 4-bencilsalbutamol de fórmula (4) a una temperatura comprendida entre 5ºC y 10ºC, seguido de la basificación del filtrado a un pH comprendido entre 9 y 9, 5 mediante la adición de una base, tal como amoníaco, a fin de obtener el isómero R enantioméricamente puro del 4bencilsalbutamol de fórmula (5) :
Fórmula (5)
y aislar el isómero R mediante su extracción con cloruro de metileno, seguido de la destilación del disolvente a fin de obtener un residuo, tratar dicho residuo con tolueno .
8. 85ºC, enfriar la solución a 0-5ºC para precipitar el isómero R ópticamente puro y filtrar el isómero R ópticamente puro de fórmula (5) ;
f) desbencilar el isómero R de fórmula (5) a fin de obtener el isómero R ópticamente puro del salbutamol de fórmula 35 (6) :
Fórmula (6) 5 y g) opcionalmente, convertir el isómero R ópticamente puro de salbutamol de fórmula (6) en su sal de clorhidrato o sulfato.
2. Procedimiento según la reivindicación 1, que comprende la racemización de la sal del ácido 4-nitrotartranílico del isómero S del 4-bencilsalbutamol de fórmula (7) :
Fórmula (7) y trazas de la sal del ácido 4-nitrotartranílico del isómero R del 4-bencilsalbutamol de fórmula (3) :
Fórmula (3)
contenida en el filtrado de las etapas (a) y (b) sometiendo dicho filtrado a destilación al vacío para obtener un residuo, seguido del tratamiento de dicho residuo con una solución de ácido fórmico al 5-10% para obtener una masa gomosa que comprende la sal del ácido fórmico del isómero S del 4-bencilsalbutamol de fórmula (8) :
Fórmula (8)
y la sal del ácido fórmico del isómero R del 4-bencilsalbutamol de fórmula (4) y liberar ácido (+) -4-nitrotartranílico de fórmula (2) ; separar el compuesto de fórmula (2) por filtración;
basificar el filtrado a un pH comprendido entre 9 y 9, 5 mediante la adición de una base, tal como amoniaco, a una temperatura comprendida entre 5ºC y 10ºC para obtener una mezcla de reacción que comprende el isómero S del 4bencilsalbutamol de fórmula (9) :
Fórmula (9)
y trazas del isómero R del 4-bencilsalbutamol de fórmula (4) ;
tratar la mezcla de reacción con anhídrido acético a la temperatura de reflujo, seguido de destilación al vacío para obtener un residuo que comprende la sal de diacetato del isómero S del 4-bencilsalbutamol de fórmula (10) :
Fórmula (10) 15 y trazas de la sal de diacetato del isómero R del 4-bencilsalbutamol de fórmula (11) :
Fórmula (11)
hidrolizar el residuo mediante su tratamiento con una base, tal como una solución de hidróxido de sodio o una solución de hidróxido de potasio, a una temperatura comprendida entre 80ºC y 85ºC, enfriar la mezcla de reacción para precipitar una mezcla racémica de 4-bencilsalbutamol y aislar dicha mezcla racémica por filtración.
3. Procedimiento según la reivindicación 1, en el que el acetato de alquilo que se utiliza en el sistema de disolvente binario de las etapas (a) o (b) es acetato de metilo, acetato de etilo o acetato de isopropilo.
4. Procedimiento según la reivindicación 1, en el que el alcohol C1-C4 de cadena ramificada o normal que se utiliza
en el sistema de disolvente binario de las etapas (a) o (b) se selecciona de entre un grupo constituido por metanol, etanol, isopropanol, butanol o terc-butanol.
5. Procedimiento según la reivindicación 1, en el que la relación entre el acetato de alquilo y el alcohol C1-C4 de cadena ramificada o normal que se utiliza en el sistema de disolvente binario de las etapas (a) o (b) está 35 comprendida entre 20:80 y 40:50 v/v.
6. Procedimiento según la reivindicación 1, en el que la relación entre el acetato de alquilo y el alcohol C1-C4 de cadena ramificada o normal que se utiliza en el sistema de disolvente binario de las etapas (a) o (b) es de 40:60 v/v.
7. Procedimiento según la reivindicación 1, en el que el volumen del sistema de disolvente binario que se utiliza para purificar la sal del ácido 4-nitrotartranílico del isómero R del 4-bencilsalbutamol de fórmula (3) está comprendido entre 3 y 3, 5 p/v.
Patentes similares o relacionadas:
Polimorfos de clorhidrato de 4-metilbenzoato de 4-[2-dimetilamino-1-(1-hidroxiciclohexil)etil]fenilo, métodos para la preparación de los mismos y uso de los mismos, del 6 de Noviembre de 2019, de Shan Dong Luye Pharmaceutical Co., Ltd: Una Forma Cristalina II de [clorhidrato de 4-metilbenzoato de 4-[2-dimetilamino-1-(1-hidroxiciclohexil)etil]fenilo], caracterizada porque la Forma Cristalina II muestra […]
Procedimiento para la preparación de cristales de clorhidrato de fingolimod, del 3 de Julio de 2019, de SYNTHON BV: Un procedimiento de preparación de la Forma 1 del clorhidrato de fingolimod cristalino de fórmula (1a):**Fórmula** representada por el patrón de […]
Síntesis de compuestos de carbomoilpiridona policíclica, del 27 de Febrero de 2019, de GILEAD SCIENCES, INC.: Un proceso para preparar un compuesto de Fórmula ß-1•J-1 de acuerdo con el siguiente esquema:**Fórmula** en el 15 que el proceso comprende hacer […]
Método para producir tensioactivo catiónico, del 10 de Diciembre de 2018, de KAO CORPORATION: Método para producir un tensioactivo catiónico que comprende las siguientes etapas: etapa 1: una etapa de obtener un éster de alcanolamina […]
Procedimiento para la fabricación de Ivabradina y de intermediarios de síntesis de la misma, del 27 de Abril de 2016, de LABORATORIO CHIMICO INTERNAZIONALE S.P.A.: Procedimiento para la preparación de (1S)-4,5-dimetoxi-1-(amoniometil)-benzociclobutano de fórmula (B) que comprende: (i) hacer reaccionar 4,5-dimetoxi-1-(amoniometil)-benzociclobutano […]
Compuestos que tienen una actividad antagonista de un receptor muscarínico y agonista de un receptor beta-2 adrenérgico, del 30 de Noviembre de 2015, de CHIESI FARMACEUTICI S.P.A.: Un compuesto de fórmula general I**Fórmula** En donde Q es un grupo de fórmula Q1, Q2, Q3, Q4, Q5 o Q6**Fórmula** Z es H u OH; Y es seleccionado […]
Separación de una mezcla de enantiómeros de (R)- y (S)-3-amino-1-butanol, del 30 de Julio de 2014, de BASF SE: Procedimiento para la separación de una mezcla de enantiómeros de (R)- y (S)-3-amino-1-butanol dado el caso protegidos en el átomo de oxígeno, que comprende […]
Separación de N,N,N''-trimetilbisaminoetiléter de mezclas que comprenden aminas terciarias o aminoalquiléteres terciarios, del 16 de Abril de 2014, de HUNTSMAN INTERNATIONAL LLC: Método para recuperar N,N,N'-trimetilbisaminoetiléter (A) a partir de su amida (B) que comprende las siguientes etapas: (a) transamidación […]