Procedimiento para la preparación de L-aminoácidos utilizando cepas de la familia Enterobacteriaceae.
Procedimiento para la preparación de L-aminoácidos, caracterizado por que se llevan a cabo las siguientes etapas:
1.1 fermentación de microorganismos recombinantes secretores de L-aminoácidos de la familia Enterobacteriaceae o de las bacterias corineformes que contienen un gen glpK que codifica un polipéptido con actividad de glicerol quinasa (ATP-dependiente), cuya secuencia de aminoácidos es al menos un 95% idéntica a la de SEQ ID NO: 2, 4 ó 6, en donde el polipéptido posee una longitud de 502 aminoácidos, conteniendo el polipéptido en la posición 428 cualquier aminoácido proteinogénico, exceptuada glicina, en un medio a una temperatura deseada, empleándose como fuente de carbono, en esencia, glicerol o, en esencia, glicerol y uno o más de los azúcares seleccionados del grupo de glucosa, sacarosa y fructosa, y
1.2 acumulación en el caldo de fermentación del L-aminoácido producido.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP2008/051780.
Solicitante: EVONIK DEGUSSA GMBH.
Nacionalidad solicitante: Alemania.
Dirección: RELLINGHAUSER STRASSE 1-11 45128 ESSEN ALEMANIA.
Inventor/es: RIEPING, MECHTHILD, THIERBACH, GEORG, KREUTZER, CAROLINE.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C12N15/00 QUIMICA; METALURGIA. › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › Técnicas de mutación o de ingeniería genética; ADN o ARN relacionado con la ingeniería genética, vectores, p. ej. plásmidos, o su aislamiento, su preparación o su purificación; Utilización de huéspedes para ello (mutantes o microorganismos modificados por ingeniería genética C12N 1/00, C12N 5/00, C12N 7/00; nuevas plantas en sí A01H; reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00; nuevas razas animales en sí A01K 67/00; utilización de preparaciones medicinales que contienen material genético que es introducido en células del cuerpo humano para tratar enfermedades genéticas, terapia génica A61K 48/00; péptidos en general C07K).
- C12P13/04 C12 […] › C12P PROCESOS DE FERMENTACION O PROCESOS QUE UTILIZAN ENZIMAS PARA LA SINTESIS DE UN COMPUESTO QUIMICO DADO O DE UNA COMPOSICION DADA, O PARA LA SEPARACION DE ISOMEROS OPTICOS A PARTIR DE UNA MEZCLA RACEMICA. › C12P 13/00 Preparación de compuestos orgánicos que contienen nitrógeno. › alfa- o beta-Aminoácidos.
- C12R1/01 C12 […] › C12R SISTEMA DE INDEXACION ASOCIADO A LAS SUBCLASES C12C - C12Q, RELATIVO A LOS MICROORGANISMOS. › C12R 1/00 Microorganismos. › Bacterias o actinomicetos.
PDF original: ES-2519016_T3.pdf
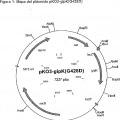
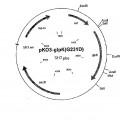
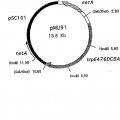
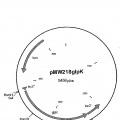



Fragmento de la descripción:
Procedimiento para la preparación de L-aminoácidos utilizando cepas de la familia Enterobacteriaceae La invención se refiere a un procedimiento para la preparación fermentativa de L-aminoácidos, en particular L-treonina, L-triptófano, L-lisina, L-valina y L-homoserina, utilizando glicerol como fuente de carbono y con ayuda de microorganismos de la familia Enterobacteriaceae, o de las bacterias corineformes que poseen alelos del gen glpK que codifican variantes de la glicerol quinasa.
Estado conocido de la técnica L-aminoácidos encuentran aplicación en la medicina humana y en la industria farmacéutica, en la industria alimentaria y, de manera muy particular, en la alimentación animal.
Es conocido que los L-aminoácidos se preparan por fermentación de cepas de Enterobacteriaceae, en particular Escherichia coli (E. coli) y Serratia marcescens, y de cepas de bacterias corineformes, en particular Cor y nebacterium glutamicum (C. glutamicum) . Debido a la gran importancia, se trabaja constantemente para mejorar el procedimiento de producción. Las mejoras del procedimiento pueden afectar a medidas técnicas de fermentación tales como, por ejemplo, agitación y suministro de oxígeno, o la composición de los medios nutricios tales como, por ejemplo, la elección del azúcar o la concentración del azúcar utilizado durante la fermentación, o el tratamiento para dar la forma del producto, por ejemplo, mediante, cromatografía de intercambio iónico, o las propiedades intrínsecas de rendimiento de los propios microorganismos.
Para mejorar las características de rendimiento de estos microorganismos se utilizan métodos de mutagénesis, selección y selección de mutantes. De esta manera se obtienen cepas que son resistentes frente a antimetabolitos tales como, por ejemplo, el análogo de treonina ácido α-amino-β-hidroxivalérico (AHV) , o auxotróficas para metabolitos de importancia reguladora, y que producen L-aminoácidos tales como, por ejemplo, L-treonina. Resistencia frente al análogo de triptófano 5-metil-DL-triptófano (5-MT) distingue, por ejemplo, una cepa productora de L-triptófano.
Desde hace algunos años, también se utilizan métodos de tecnología de ADN recombinante para la mejora de cepas productoras o secretoras cepas de L-aminoácidos de la familia Enterobacteriaceae, amplificando, por ejemplo, genes de la biosíntesis de aminoácidos individuales o alterando las propiedades de genes especiales e investigando el efecto sobre la producción. Informaciones recopilatorias sobre la biología celular y molecular de Escherichia coli y Salmonella se pueden encontrar en Neidhardt (comp.) : Escherichia coli and Salmonella, Celular and Molecular Biology, 2ª edición, ASM Press, Washington, D.C., EE.UU., (1996) .
Para la preparación de L-aminoácidos, hoy en día se emplea generalmente por la industria de la fermentación glucosa o sacarosa como fuente de carbono. Se está constantemente buscando nuevas y económicas fuentes de materias primas.
El glicerol (propanotriol) está presente en los aceites y grasas en forma químicamente unida. Conecta como un "puente" las moléculas de ácidos grasos en los triglicéridos. En la fabricación de combustible a partir de aceite de colza (biodiesel, éster metílico de colza) se produce glicerol como un producto de acoplamiento (subproducto) . Por lo tanto, éste se encuentra en una medida digna de mención como materia prima en la industria de la fermentación.
Es conocido que cepas productoras de L-treonina de Escherichia coli se desarrollan en glicerol como única fuente de carbono (documento US-A-5.175.107) .
Exposiciones recopilatorias para el metabolismo del glicerol de Enterobacteriaceae se encuentran en Lin (En: Neidhardt (comp.) , Escherichia coli y Salmonella, American Society for Microbiology, Washington, D.C., EE.UU.: 307-342 (1996) ) .
La glicerol quinasa, que se presenta asociada en su forma enzimáticamente activa con el facilitador de GlpF, se fosforila utilizando ATP de glicerol citoplásmico (Voegele et al., Journal of Bacteriology 175 (4) : 1087-94 (1993) ) para formar glicerol-3-fosfato. La actividad de la glicerol quinasa GlpK es inhibida alostéricamente por la fructosa-1, 6-bisfosfato (FBP) y la enzima IIAGlc, el fosfoportador dependiente de fosfoenolpiruvato específico para la glucosa: sistema de azúcar-fosfotransferasa (PTS) . Según Holtman et al. (Journal of Bacteriology 183: 3336-3344 (2001) ) FBP domina el control alostérico de la enzima.
La secuencia de nucleótidos de la forma salvaje del gen que codifica la glicerol-quinasa de Escherichia coli fue determinado por Pettigrew et al. (Journal of Biological Chemistr y 263: 135-139 (1988) ) y está disponible, en general, en el banco de datos del Centro Nacional de Información Biotecnológica (NCBI) de la Biblioteca Nacional de Medicina (Bethesda, MD, EE.UU.) bajo el número de acceso (accession number) U00096 (Región: 4113737-4115245) .
Además, puede deducirse de la solicitud de patente EP 1715055 como secuencia nº 15.
En el documento EP 1715055 se describe una mejora en la producción fermentativa de L-aminoácidos por 5 microorganismos recombinantes de la familia Enterobacteriaceae mediante la amplificación del gen glpK.
Son conocidos mutantes de glpK de E. coli, en los que está reducida la inhibición de la glicerol quinasa por parte de la enzima IIAGlc del PTS (Liu et al., Biochemistr y 33: 10120-10126 (1994) ; Pettigrew et al., Journal of Bacteriology 178: 2846-2852 (1996) ; Pettigrew et al., Biochemistr y 37: 4875-4883 (1998) ) o bien la mutación conduce a una activación de la glicerol quinasa por parte de la enzima IIAGlc (Pawlyk y Pettigrew, Proceedings of the National Academy of Science USA 99 (17) : 11115-11120 (2002) ) .
Además de ello, son conocidos mutantes de glpK de E. coli con (1) actividad incrementada de la glicerol quinasa, en los que (2) está reducida la inhibición por parte de FBP (Herring et al., Nature Genetics 38 (12) : 1406-1412 (2006) ;
Pettigrew et al., Journal of Bacteriology 178: 2846-2852 (1996) ; Honisch et al., Genome Research 14: 2495-2502 (2004) ) y en los que (3) adicionalmente está neutralizado el control de la utilización de glicerol por parte del azúcar PTS (Holtman et al., Journal of Bacteriology 183 : 3336-3344 (2001) ) .
Como azúcares PTS se designan azúcares que son recogidos por el sistema PTS. Éstos inhiben la absorción y la utilización de azúcar no PTS o fuentes de carbono no PTS ("represión catabólica") simultáneamente presentes. A los azúcares PTS en Enterobacteriaceae pertenecen, entre otros, glucosa, sacarosa, fructosa, trehalosa, maltosa, celobiosa, manosa, manitol, N-acetilglucosamina, β-glucósidos y glucitol.
Misión de la invención Los autores de la invención se han propuesto la misión de proporcionar nuevas medidas para la preparación fermentativa mejorada de L-aminoácidos, en particular L-treonina, L-triptófano, L-lisina, L-valina y L-homoserina, usando glicerol.
Descripción de la invención Objeto de la invención es un método para la preparación de L-aminoácidos, preferiblemente L-treonina, L-triptófano, Llisina, L-valina y L-homoserina, caracterizado porque se llevan a cabo las etapas siguientes:
a) fermentación de microorganismos recombinantes secretores de L-aminoácidos de la familia Enterobacteriaceae o de las bacterias corineformes que contienen un alelo glpK que codifica un polipéptido con actividad de glicerol quinasa (ATP-dependiente) , cuya secuencia de aminoácidos es al menos un 95% idéntica a la de SEQ ID NO: 2, SEQ ID NO: 4 o SEQ ID NO: 6, preferiblemente SEQ ID NO: 2, en donde el polipéptido posee una longitud de 502 aminoácidos y en la posición 428 contiene a cualquier aminoácido proteinogénico, preferiblemente ácido L-glutámico, ácido L-aspártico, L-isoleucina, L-histidina, L-triptófano y Lfenilalanina, de manera particularmente preferida ácido L-aspártico, en un medio a una temperatura deseada, empleándose como fuente de carbono, en esencia, glicerol o, en esencia, glicerol y uno o más de los azúcares seleccionados del grupo de glucosa, sacarosa y fructosa, y
b) acumulación en el caldo de fermentación del L-aminoácido producido.
Por una glicerol quinasa se entiende una enzima que cataliza la fosforilación de glicerol a glicerol-3-fosfato.
Por aminoácidos proteinogénicos se entienden los aminoácidos que se presentan en proteínas naturales, es decir, en 50 proteínas de microorganismos, plantas, animales y seres humanos. A ellos pertenecen, en particular, L-aminoácidos seleccionados del grupo ácido L-aspártico, L-asparagina, L-treonina, L-serina, ácido L-glutámico, L-glutamina, glicina, Lalanina, L-cisteína, L-valina, L-metionina,... [Seguir leyendo]
Reivindicaciones:
1. Procedimiento para la preparación de L-aminoácidos, caracterizado por que se llevan a cabo las siguientes etapas:
1.1 fermentación de microorganismos recombinantes secretores de L-aminoácidos de la familia Enterobacteriaceae o de las bacterias corineformes que contienen un gen glpK que codifica un polipéptido con actividad de glicerol quinasa (ATP-dependiente) , cuya secuencia de aminoácidos es al menos un 95% idéntica a la de SEQ ID NO: 2, 4 ó 6, en donde el polipéptido posee una longitud de 502 aminoácidos, conteniendo el polipéptido en la posición 428 cualquier aminoácido proteinogénico, exceptuada glicina, en un medio a una temperatura deseada, empleándose como fuente de carbono, en esencia, glicerol o, en esencia, glicerol y uno o más de los azúcares seleccionados del grupo de glucosa, sacarosa y fructosa, y
1.2 acumulación en el caldo de fermentación del L-aminoácido producido.
2. Procedimiento según la reivindicación 1, caracterizado por que el aminoácido proteinogénico en la posición 428 es ácido L-glutámico, ácido L-aspártico, L-isoleucina, L-histidina, L-triptófano o L-fenilalanina.
3. Procedimiento según la reivindicación 2, caracterizado por que en el caso del aminoácido proteinogénico en la posición 428 se trata de ácido L-aspártico. 20
4. Procedimiento según las reivindicaciones 1 a 3, caracterizado por que el polipéptido codificado comprende la secuencia de aminoácidos de SEQ ID NO: 2, SEQ ID NO:4 o SEQ ID NO: 6, incluido el intercambio de aminoácidos mencionado en la posición 428, teniendo la secuencia de aminoácidos adicionalmente una o varias de las características elegidas del grupo uno o a lo sumo 10 intercambios de aminoácidos conservativos, una prolongación en el extremo C de uno hasta a lo sumo 20 aminoácidos.
5. Procedimiento según las reivindicaciones 1 a 4, caracterizado por que el polipéptido codificado comprende la secuencia de aminoácidos de SEQ ID NO: 2, SEQ ID NO:4 o SEQ ID NO: 6, incluido el intercambio de aminoácidos mencionado en la posición 428.
6. Procedimiento según la reivindicación 4 ó 5, caracterizado por que el polipéptido codificado comprende la secuencia de aminoácidos de SEQ ID NO: 2, incluido el intercambio de aminoácidos mencionado en la posición 428.
7. Procedimiento según las reivindicaciones 1 a 6, caracterizado por que para la preparación de los L-aminoácidos se
fermentan microorganismos de la familia Enterobacteriaceae, en los que adicionalmente se debilita al mismo tiempo el gen glpR que codifica el represor del regulón glp.
8. Procedimiento según las reivindicaciones 1 a 7, caracterizado por que para la preparación de los L-aminoácidos se fermentan microorganismos de la familia Enterobacteriaceae, en los que se refuerzan, en particular sobre-expresan, al
mismo tiempo uno o más de los genes seleccionados del grupo: a) el gen glpA que codifica la subunidad grande de la sn-glicerol-3-fosfato-deshidrogenasa (anaerobia) ,
b) el gen glpB que codifica la subunidad para el anclaje a membrana de la sn-glicerol-3-fosfato-deshidrogenasa (anaerobia) , 45 c) el gen glpC que codifica la subunidad pequeña de la sn-glicerol-3-fosfato-deshidrogenasa (anaerobia) ,
d) el gen glpD que codifica la glicerol-3-fosfato-deshidrogenasa (aerobia) ,
e) el gen glpE que codifica la azufre-transferasa,
f) el gen glpF que codifica el facilitador del glicerol GlpF,
g) el gen glpG,
h) el gen glpQ que codifica la glicerolfosfodiesterasa periplasmática,
i) el gen glpT que codifica la glicerol-3-fosfato-permeasa,
j) el gen glpX que codifica la fructosa-1, 6-bisfosfatasa II,
k) el gen tpiA que codifica la triosafosfato-isomerasa,
l) el gen gldA que codifica la glicerol-deshidrogenasa (NAD-dependiente) , m) el gen dhaK que codifica el dominio N-terminal de la dihidroxiacetona-quinasa,
n) el gen dhaL que codifica el dominio C-terminal de la dihidroxiacetona-quinasa, o) el gen dhaM que codifica la subunidad de la proteína PTS de la dihidroxiacetona-quinasa, p) el gen dhaR que codifica el activador del operón dha,
q) el gen fsa que codifica la fructosa-6-fosfato aldolasa I, y r) el gen talC que codifica la fructosa-6-fosfato aldolasa II.
9. Procedimiento según las reivindicaciones 1 a 8, caracterizado por que en el caso de los microorganismos de la familia Enterobacteriaceae se trata de un microorganismo seleccionado de los géneros Escherichia, Erwinia, Providencia y Serratia.
10. Procedimiento según las reivindicaciones 1 a 9, caracterizado por que como fuente de carbono se emplea 20 esencialmente glicerol.
11. Procedimiento según las reivindicaciones 1 a 9, caracterizado por que como fuente de carbono se emplea esencialmente glicerol y uno o varios de los azúcares seleccionados del grupo de glucosa, sacarosa y fructosa, ascendiendo la proporción de glicerol a al menos 10%.
12. Procedimiento según una o varias de las reivindicaciones 1 a 11, caracterizado por que se trata de un procedimiento por lotes, un procedimiento por lotes alimentados, un procedimiento por lotes alimentados repetidos o un procedimiento continuo.
13. Procedimiento según las reivindicaciones 1 a 12, caracterizado por que se purifica y aísla el L-aminoácido deseado.
14. Procedimiento según las reivindicaciones 1 a 13, caracterizado por que se obtiene un producto con contenido en Laminoácidos, en el que los componentes del caldo de fermentación y/o la biomasa permanecen en el producto en su totalidad o en proporciones (> 0 a 100%) del mismo.
62
Patentes similares o relacionadas:
Heparinasas obtenidas de Sphingobacterium daejeonense, su preparación y su aplicación, del 22 de Julio de 2020, de Shenzhen Hepalink Pharmaceutical Group Co., Ltd: Una heparinasa de Sphingobacterium daejeonense, en la que la heparinasa es heparinasa SDhep I o heparinasa SDhep II; en la que el peso molecular de la heparinasa SDhep […]
Cepa de Faecaslibacterium Prausnitzii CNCM I-4573 para el tratamiento y la prevención de una inflamación gastrointestinal, del 15 de Julio de 2020, de Institut national de recherche pour l'agriculture, l'alimentation et l'environnement: Cepa bacteriana de la especie Faecalibacterium prausnitzii depositada en la CNCM bajo el número de acceso CNCM I-4573, para su utilización en el tratamiento y/o la prevención […]
ENZIMA CON ACTIVIDAD ALFA-AMILASA CON EXTREMA TERMOTOLERANCIA Y TERMOESTABILIDAD, PARA LA INDUSTRIA DEL PROCESAMIENTO DEL ALMIDÓN, del 9 de Julio de 2020, de UNIVERSIDAD DE ANTOFAGASTA: La presente invención se relaciona con una enzima hidrolasa modificada tipo alfa-amilasa termoestable y termorresistente, que comprende una secuencia […]
Métodos para producir ácido graso poliinsaturado y lípido que contiene ácido graso poliinsaturado, del 17 de Junio de 2020, de SUNTORY HOLDINGS LIMITED: Un método para producir ácido araquidónico (ARA) y/o ácido dihomo-gamma-linolénico (DGLA), comprendiendo el método el cultivo Mortierella alpina capaz de producir […]
Método para la producción de L-aminoácido, del 3 de Junio de 2020, de AJINOMOTO CO., INC.: Método para producir un L-aminoácido mediante fermentación que comprende cultivar un microorganismo que tiene la capacidad de producción de L-aminoácido en […]
Biotensioactivos glicolipopeptídicos, del 3 de Junio de 2020, de CRODA INTERNATIONAL PLC: Un biotensioactivo purificado que comprende un componente lipídico hidrófobo que comprende un extremo carboxilo y un extremo hidroxilo, en donde el componente […]
Una nueva cepa de Paenibacillus, compuestos antifúngicos y procedimientos para su uso, del 22 de Abril de 2020, de BAYER CROPSCIENCE LP: Una composición que comprende un cultivo biológicamente puro de una cepa fungicida de Paenibacillus sp. que comprende una variante de la fusaricidina […]
Composiciones que comprenden bacterias y métodos de uso de los mismos para el tratamiento y / o prevención de enfermedades gastrointestinales, metabólicas y / o de otras enfermedades, del 11 de Marzo de 2020, de Wageningen Universiteit: Una bacteria aislada del intestino humano que comprende un conjunto de genes de la ruta de la lisina que permite a dicha bacteria convertir L-lisina en ácido butírico […]