Procedimiento para la preparación de ácidos dicarboxílicos insaturados a partir de cicloalquenos y de ácido acrílico mediante una metátesis.
Procedimiento para la preparación de ácidos dicarboxílicos insaturados,
caracterizado por que
se hacen reaccionar unos hidrocarburos cíclicos insaturados y el ácido acrílico con un catalizador de rutenio a través de una reacción de metátesis, a unas concentraciones en el substrato de >1 mol/l del hidrocarburo cíclico insaturado, precipitando el ácido dicarboxílico resultante en este caso al sobrepasarse el producto de solubilidad
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP2009/054599.
Solicitante: EVONIK DEGUSSA GMBH.
Nacionalidad solicitante: Alemania.
Dirección: RELLINGHAUSER STRASSE 1-11 45128 ESSEN ALEMANIA.
Inventor/es: ROOS, MARTIN, DR., HAGER, HARALD, DR., HANNEN,Peter.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C07C51/347 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07C COMPUESTOS ACICLICOS O CARBOCICLICOS (compuestos macromoleculares C08; producción de compuestos orgánicos por electrolisiso electroforesis C25B 3/00, C25B 7/00). › C07C 51/00 Preparación de ácidos carboxílicos o sus sales, haluros o anhídridos. › por reacciones que no dan lugar a grupos carboxilo.
- C07C57/13 C07C […] › C07C 57/00 Compuestos insaturados que tienen grupos carboxilo unidos a átomos de carbono acíclicos. › Acidos dicarboxílicos.
PDF original: ES-2522690_T3.pdf
Fragmento de la descripción:
Procedimiento para la preparación de ácidos dicarboxílicos insaturados a partir de cicloalquenos y de ácido acrílico mediante una metátesis A partir de ciertos hidrocarburos cíclicos tales como ciclooctadieno (COD) , ciclododeceno (CDEN) , ciclododecatrieno (CDT) , ciclohepteno, ciclohexeno y ciclopenteno, pasando por una reacción de metátesis por medio de un catalizador adecuado, se pueden preparar unos ácidos dicarboxílicos insaturados en α, β (Esquema 1) .
** (Ver fórmula) **
Esquema 1: Representación general para la preparación de unos ácidos dicarboxílicos insaturados (2) a partir de unos hidrocarburos insaturados cíclicos (1) a través de una metátesis con ácido acrílico.
A partir de los ácidos dicarboxílicos insaturados en α, β que se obtienen, mediante una policondensación con diaminas o dioles, se pueden obtener de una manera correspondiente unas poliamidas o respectivamente unos poliésteres. Una característica especial de estos materiales sintéticos es la posibilidad de una reticulación a través de los enlaces dobles. A través de una hidrogenación, se llega en una etapa a los correspondientes ácidos dicarboxílicos saturados. Por lo demás, estos compuestos se pueden convertir químicamente sin gran esfuerzo en los correspondientes dioles y diaminas. Junto a los poliésteres, los dioles se podrían utilizar también para la preparación de poliuretanos.
Estado de la técnica:
El procedimiento aquí descrito constituye un considerable mejoramiento con respecto a los procedimientos habituales. (Morgan, John, P., Morrill, Christie; Grubbs, Robert, H.; Choi, Tae-Lim, documento de solicitud de patente internacional WO 02/079127 A1.
Choi, T-L.; Lee, C. W.; Chatterjee, A. K.; Grubbs, R. H. J. Am. Chem. Soc. 2001, 123, 10417-10418. Randl, S.; Connon, S. J.; Blechert, S. J. Chem. Soc., Chem. Commun. 2001, 1796-1797.)
El documento WO 02/079127 A describe un procedimiento para la preparación de ácidos dicarboxílicos insaturados mediante la metátesis de Krezs con apertura del anillo (ROCM, acrónimo del alemán "ringöffnenden Krezsmetathese") a partir de unas olefinas y unos ácidos dicarboxílicos insaturados en α, β en presencia de unos catalizadores de rutenio.
Hasta ahora, en el caso de la conversión química descrita más arriba se tenía que trabajar en una alta dilución con el fin de reprimir la oligomerización o respectivamente la polimerización, que transcurre como una reacción de competencia, Además de ello, como disolvente pasa a emplearse predominantemente el diclorometano, lo que es desventajoso para una realización a escala técnica debido a su potencial peligroso para la salud.
Por fin, se encontró sorprendentemente que mediante un procedimiento de acuerdo con las reivindicaciones es posible desplazar el equilibrio totalmente en dirección al producto deseado sin trabajar en una gran dilución. Además 45 de ello, mediante el procedimiento descrito es posible un reciclamiento eficaz del catalizador. Esto se consigue mediante el recurso de que, al contrario que en la práctica actual, se trabaja con unas concentraciones en el substrato de > 1 mol/l del hidrocarburo cíclico insaturado. En el transcurso de la reacción, al sobrepasarse el producto de solubilidad, se precipita el ácido dicarboxílico insaturado en α, β y se substrae por consiguiente del equilibrio (en la fase homogénea) .
Una ventaja decisiva del invento que se describe aquí es por consiguiente el hecho de que el producto precipita al realizar la reacción como un material sólido. Puesto que en el caso de la metátesis cruzada con apertura del anillo se trata de una reacción en equilibrio, -adicionalmente a la puesta en libertad del etileno -subsiste por lo tanto la posibilidad de desplazar el equilibrio hacia el lado del producto deseado. Si bien la conversión química en un 55 momento x no es completa o respectivamente el producto permanece en una parte en solución, mediante un modo de proceder continuo se puede alcanzar a fin de cuentas una conversión química completa del educto (es decir del producto de partida.
Junto al eficaz influjo sobre el equilibrio de la reacción en favor de producto, la fácil separación de los productos y, acompañando a ésta, la recuperación del catalizador, constituyen un gran facilitamiento en la conducción del proceso. El catalizador empleado permanece en solución y puede ser reciclado.
En los procedimientos actuales, la mezcla de reacción tiene que ser tratada como un conjunto. Esto se realiza separando por destilación el disolvente y purificando el residuo por cromatografía. En particular, la purificación por cromatografía del producto en bruto requiere el empleo de grandes cantidades de un disolvente y de energía para eliminar al mismo, lo que es impracticable para una conversión química a escala técnica.
La reacción descrita se lleva a cabo a unas temperaturas de 10 a 100º C, de manera preferida a 20 hasta 80º C y de manera especialmente preferida a 20 hasta 60º C.
La reacción descrita se lleva a cabo mediando utilización de un disolvente. Como tal disolvente se adecuan unos hidrocarburos tanto acíclicos como también cíclicos. Se adecuan especialmente unos hidrocarburos aromáticos 15 halogenados y de manera muy especialmente preferida se adecuan ciertos compuestos aromáticos con grupos alquilo.
En el caso de la realización en solución se prefieren unas concentraciones de 1 a 2 M y se prefieren especialmente unas concentraciones de 2 a 4 M de un cicloalqueno, referidas al disolvente.
En el caso del procedimiento descrito, el catalizador se emplea, referido a la cantidad de un cicloalqueno insaturado, en unas proporciones de 5 a 0, 0001% en moles. Se prefieren unas proporciones de 2 a 0, 001% en moles, y se prefieren especialmente unas proporciones de 1 a 0, 5% en moles del catalizador, referidas a la cantidad de sustancia del cicloalqueno insaturado empleado.
Con el fin de obtener el ácido dicarboxílico insaturado en α, β en una calidad de grado de polimerización, se recomienda la purificación a través de una cristalización, de una destilación o de una combinación de ambas.
Como catalizadores se adecuan unos compuestos complejos con rutenio y un carbeno que, como una de sus particularidades más características, llevan un ligando de un carbeno heterocíclico con N. Unos ejemplos de unos catalizadores preferidos se encuentran en la Figura 1. En este caso se prefieren especialmente unos catalizadores del tipo 7, con un grupo atractor de electrones R' en el ligando de bencilideno.
** (Ver fórmula) **
Figura 1: Ejemplos de los catalizadores de rutenio que pasan a emplearse 35
Ejemplos:
Ejemplo comparativo 1. El dicloruro de 1, 3-bis (2, 4, 6-trimetil-fenil) -4, 5-dihidro-imidazol-2-iliden[2- (i-propoxi) -5- (N, N-dimetilaminosulfonil) fenil]metilen rutenio (Il) (1% en moles referido al cicloalqueno) se dispone previamente en un recipiente de Schlenk en el seno de tolueno (2, 25 ml) bajo argón. Una solución del ciclopenteno (0, 3 g, 4, 4 mmol) y del ácido acrílico (0, 79 g, 11 mmol) en tolueno (2, 25 ml) se añade gota a gota a la solución del catalizador. La mezcla de reacción se agita durante una hora a 60º C y a continuación se enfría a la 45 temperatura ambiente. El material sólido que se deposita, es separado por filtración, lavado con un poco de tolueno frío y secado en vacío. El producto se obtuvo como un material sólido de color blanco (0, 128 g, 16%) . Mediante una analítica por RMN (resonancia magnética nuclear) se determinó una pureza de 98, 9%.
Ejemplos conformes al invento 2. El dicloruro de 1, 3-bis (2, 4, 6-trimetil-fenil) -4, 5-dihidro-imidazol-2-iliden[2- (i-propoxi) -5-N, N-dimetilaminosulfonil) fenil]metilen rutenio (II) (1% en moles referido al cicloalqueno) se dispone previamente en un recipiente de Schlenk en el seno de tolueno (1, 75 ml) bajo argón. Una solución del ciclohexeno (0, 3 g, 3, 65
mmol) y del ácido acrílico (0, 66 g, 9, 13 mmol) en tolueno (1, 75 ml) se añade gota a gota a la solución del catalizador. La mezcla de reacción se agita durante una hora a 60º C y a continuación se enfría a la 3
temperatura ambiente. El material sólido que se deposita, es separado por filtración, lavado con un poco de
tolueno frío y secado en vacío. El producto se obtuvo como un material sólido de color blanco (0, 272 g,
38%) . Mediante una analítica por RMN se determinó una pureza de 99, 2%.
3 El dicloruro de 1, 3-bis (2, 4, 6-trimetil-fenil) -4, 5-dihidro-imidazol-2-iliden[2- (i-propoxi) -5- (N, N-dimetilamino
sulfonil) fenil]metilen rutenio (II) (1% en moles referido al cicloalqueno) se dispone previamente... [Seguir leyendo]
Reivindicaciones:
1. Procedimiento para la preparación de ácidos dicarboxílicos insaturados, caracterizado por que se hacen reaccionar unos hidrocarburos cíclicos insaturados y el ácido acrílico con un catalizador de rutenio a través de una reacción de metátesis, a unas concentraciones en el substrato de > 1 mol/l del hidrocarburo cíclico insaturado, precipitando el ácido dicarboxílico resultante en este caso al sobrepasarse el producto de solubilidad.
2. Procedimiento de acuerdo con la reivindicación 1, caracterizado por que como hidrocarburos cíclicos insaturados se emplean ciclooctadieno, ciclododeceno, ciclododecatrieno, ciclohepteno, ciclohexeno o ciclopenteno.
3. Procedimiento de acuerdo con la reivindicación 1, Caracteriza-do por que en el caso de la realización de la reacción en una solución, el hidrocarburo cíclico insaturado se presenta en unas concentraciones de 2 a 4 moles/l.
4. Procedimiento de acuerdo con una de las reivindicaciones precedentes, caracterizado por que como catalizadores se emplean unos compuestos complejos con rutenio y un carbeno, que llevan un ligando heterocíclico con N.
5. Procedimiento de acuerdo con una de las reivindicaciones precedentes, caracterizado por que los catalizadores de rutenio se emplean en unas proporciones de 5 a 0, 0001% en moles, referidas a la cantidad de sustancia del hidrocarburo cíclico insaturado.
6. Procedimiento de acuerdo con una de las reivindicaciones precedentes, caracterizado por que los catalizadores de rutenio se emplean en unas proporciones de 2 a 0, 001% en moles, referidas a la cantidad de sustancia del hidrocarburo cíclico insaturado.
7. Procedimiento de acuerdo con una de las reivindicaciones precedentes, caracterizado por que los catalizadores de rutenio se emplean en unas proporciones de 1 a 0, 5% en moles, referidas a la cantidad de sustancia del hidrocarburo cíclico insaturado.
8. Procedimiento de acuerdo con una de las reivindicaciones precedentes, caracterizado por que como disolvente se emplean unos hidrocarburos tanto acíclicos como también cíclicos.
9. Procedimiento de acuerdo con una de las reivindicaciones precedentes, caracterizado por que como disolvente se emplean unos hidrocarburos aromáticos halogenados.
10. Procedimiento de acuerdo con una de las reivindicaciones precedentes, caracterizado por que el ácido dicarboxílico insaturado obtenido se hidrogena en una segunda etapa.
11. Procedimiento de acuerdo con una de las reivindicaciones precedentes, caracterizado por que los catalizadores de rutenio disueltos en el material filtrado son reciclados.
12. Procedimiento de acuerdo con una de las reivindicaciones precedentes, caracterizado por que el ácido dicarboxílico insaturado obtenido se purifica mediante una cristalización, una destilación o una combinación de ambas.
Patentes similares o relacionadas:
Nuevos compuestos naturales antineurodegenerativos aislados a partir de Alpiniae oxyphyllae fructus y síntesis total de los mismos, del 8 de Mayo de 2019, de University of Macau: Compuesto de formula I:**Fórmula** donde R1 y R3 son independientemente alquilo (C1-C3) no sustituido o sustituido; y R2 y R4 son […]
Métodos para sintetizar un análogo de prostaciclina, del 31 de Enero de 2018, de Cayman Chemical Company, Incorporated: Un método para generar un compuesto de Fórmula I **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, que comprende las etapas de: […]
Procedimiento para la preparación de ácidos ciclohexanodicarboxílicos y sus derivados, del 1 de Noviembre de 2017, de BASF SE: Procedimiento para la preparación de un ácido ciclohexanodicarboxílico, sus monoésteres o diésteres, el cual comprende las siguientes secuencias de los pasos a […]
Aplicación de un complejo de iridio en la hidrogenación catalítica asimétrica de ácidos carboxílicos insaturados, del 4 de Mayo de 2016, de Zhejiang Jiuzhou Pharmaceutical Co., Ltd: Procedimiento de preparación de ácidos carboxílicos quirales, tal que se lleva a cabo la hidrogenación catalítica asimétrica de los ácidos carboxílicos […]
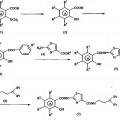 Método para producir un derivado de aminotiazol y un intermedio de producción, del 29 de Julio de 2015, de ZERIA PHARMACEUTICAL CO., LTD.: Un método de producción de un compuesto representado por la fórmula :**Fórmula**
(en la que el anillo
A representa un anillo benceno o un heterociclo […]
Método para producir un derivado de aminotiazol y un intermedio de producción, del 29 de Julio de 2015, de ZERIA PHARMACEUTICAL CO., LTD.: Un método de producción de un compuesto representado por la fórmula :**Fórmula**
(en la que el anillo
A representa un anillo benceno o un heterociclo […]
PROCEDIMIENTO DE CO-PRODUCCIÓN DE OLEFINAS Y DE DIÉSTERES O DE DIÁCIDOS MEDIANTE HOMOMETÁTESIS DE CUERPOS GRASOS INSATURADOS EN LÍQUIDOS IÓNICOS NO ACUOSOS, del 9 de Mayo de 2011, de INSTITUT FRANCAIS DU PETROLE: Procedimiento para producir a la vez una fracción olefínica y una composición de diésteres o de diácidos, caracterizado por que se somete a una reacción […]
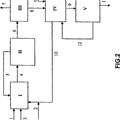 PROCEDIMIENTO DE COPRODUCCION DE OLEFINAS Y DIESTERES O DIACIDOS A PARTIR DE CUERPOS GRASOS INSATURADOS, del 31 de Marzo de 2010, de INSTITUT FRANCAIS DU PETROLE: Procedimiento para producir simultáneamente una fracción olefínica y una composición de diésteres o de diácidos a partir de cuerpos grasos insaturados, caracterizado […]
PROCEDIMIENTO DE COPRODUCCION DE OLEFINAS Y DIESTERES O DIACIDOS A PARTIR DE CUERPOS GRASOS INSATURADOS, del 31 de Marzo de 2010, de INSTITUT FRANCAIS DU PETROLE: Procedimiento para producir simultáneamente una fracción olefínica y una composición de diésteres o de diácidos a partir de cuerpos grasos insaturados, caracterizado […]
PROCEDIMIENTO PARA LA PREPARACION DE ARIL-AMINOPROPANOLES, del 11 de Noviembre de 2009, de BAYER AKTIENGESELLSCHAFT: Procedimiento para la preparación de compuestos de fórmula (I) enantioméricamente enriquecidos** ver fórmula** en la que Ar representa un resto 2-tiofen-ilo o 3-tiofen-ilo […]