PROCEDIMIENTO PARA LA PREPARACIÓN DE BOSENTÁN.
Procedimiento para la preparación de 4-terc-butil-N-[6-(2-hidroxi-etoxi)-5-(2-metoxi-fenoxi)-[2,
2']bipirimidinil- 4-il]-bencenosulfonamida, de fórmula (I), o una sal o forma hidratada de la misma,**Fórmula**
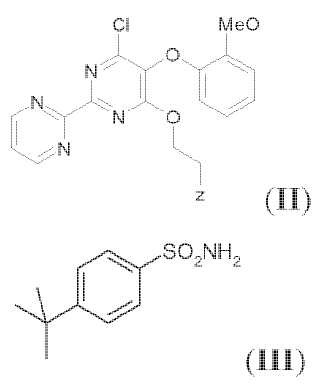
que comprende la reacción de un compuesto de fórmula (II), o una sal del mismo, **Fórmula**
en la que Z es un grupo hidroxilo opcionalmente protegido, con un compuesto de fórmula (III) o una sal del mismo, **Fórmula**
en presencia de una base; y, si es necesario, la eliminación del grupo protector de hidroxilo, y/o, si se desea, la conversión de un compuesto de fórmula (I) en una sal del mismo, o viceversa.
Tipo: Patente Europea. Resumen de patente/invención. Número de Solicitud: E08170830.
Solicitante: DIPHARMA FRANCIS S.R.L..
Nacionalidad solicitante: Italia.
Dirección: VIA BISSONE, 5 20021 BARANZATE (MI) ITALIA.
Inventor/es: RAZZETTI, GABRIELE, MANTEGAZZA, SIMONE, ALLEGRINI, PIETRO, Taddei,Maurizio, Naldini,Diletta.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C07D239/52 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07D COMPUESTOS HETEROCICLICOS (Compuestos macromoleculares C08). › C07D 239/00 Compuestos heterocíclicos que contienen ciclos de diazina-1,3 o diazina-1,3 hidrogenada. › Dos átomos de oxígeno.
PDF original: ES-2376375_T3.pdf
Fragmento de la descripción:
Procedimiento para la preparación de bosentán Campo de la invención La presente invención se refiere a un procedimiento para la preparación de compuestos de bencenosulfonamida, en particular 4-terc-butil-N-[6- (2-hidroxietoxi) -5- (2-metoxi-fenoxi) -[2, 2']bipirimidinil-4-il]-benceno-sulfonamida, concretamente bosentán, y productos intermedios útiles para su síntesis.
Antecedentes tecnológicos El bosentán (1) es un antagonista de los receptores de endotelina conocido por el documento US 5.292.740, que da a conocer su preparación según el procedimiento esquematizado a continuación:
Dicho procedimiento tiene varias desventajas desde el punto de vista industrial. En particular, la última etapa de reacción hace uso de la sal sódica de etilenglicol, que es un reactivo difícil de preparar y usar ya que es tóxico e 20 irritante.
Además, este procedimiento implica la formación de impurezas: en particular la pirimidinona (13) y el dímero (12) representados a continuación en el presente documento.
Se requieren procedimientos de purificación complejos del producto final con el fin de eliminar estos subproductos, implicando de ese modo desventajas tanto operativas como económicas. 30 Además, la última etapa de reacción hace uso de un gran exceso de etilenglicol que es difícil de eliminar del producto final, dado que es de alto punto de ebullición, afectando negativamente a los costes del procedimiento.
Se da a conocer un método de síntesis adicional, por ejemplo, en el documento US 6.136.971, según el procedimiento esquematizado a continuación:
Dicho método de síntesis hace uso de la sal sódica de etilenglicol monoprotegida, que es más costosa que el etilenglicol e implica los mismos problemas de seguridad que el procedimiento descrito en el documento US
5.292.740. Dicho método también implica la formación de impurezas en el producto final, en particular los compuestos (13) y (18) descritos anteriormente.
Por tanto existe la necesidad de un procedimiento alternativo novedoso, que emplee materiales de partida económicos y permita obtener bosentán libre de las impurezas mencionadas anteriormente.
Sumario de la invención Se ha encontrado ahora un procedimiento alternativo, que proporciona bosentán a partir de materiales de partida de bajo coste, que se realiza en condiciones más suaves que en los métodos conocidos. Más particularmente, este procedimiento proporciona bosentán con alto nivel de pureza. Esto hace que el procedimiento de la invención sea más ventajoso y económico que los de la técnica anterior.
Breve descripción de los métodos analíticos Se caracterizó la forma cristalina de bosentán mediante difracción de polvo de rayos X (XRPD) , espectrometría de resonancia magnética nuclear 1H-RMN y calorimetría diferencial de barrido (CDB) .
Se registraron los espectros de difracción de rayos X (XRPD) con un difractómetro automático APD-2000 θ/θ para polvos y líquidos fabricados por Ital-Structures, en las siguientes condiciones operativas: radiación CuKα (λ = 1, 5418
A) , barrido con intervalo angular de 3-40º en 2θ con paso angular de 0, 03º durante 1 s.
Se registraron termogramas de CDB con el calorímetro diferencial de barrido Mettler-Toledo DSC 822e, en las siguientes condiciones operativas: cápsulas de aluminio, intervalo de 30-300º C a la velocidad de 10º C/min., con nitrógeno como gas de purga (80 ml/min.) .
Se determinó el contenido en agua en los compuestos mediante titulación según Karl - Fischer.
Se determinó el tamaño de partícula con la técnica de dispersión de luz láser conocida usando un instrumento Malvern Mastersizer MS1 en las siguientes condiciones operativas: a) lentes de 300RF mm, con longitud de rayo láser de 2, 4 mm; y b) 500 mg de muestra dispersados en 10 ml de hexano (reactivo ACS) con SPAN 85® al 1%, sin sonicación previa, velocidad de agitación 2500 rpm.
Breve descripción de las figuras Figura 1: espectro de XRPD de bosentán. Figura 2: termograma de CDB de bosentán.
Descripción detallada de la invención Un objeto de la invención es un procedimiento para la preparación de 4-terc-butil-N-[6- (2-hidroxi-etoxi) -5- (2-metoxifenoxi) -[2, 2']bipirimidinil-4-il]-bencenosulfonamida, de fórmula (I) , o una sal o forma hidratada de la misma, que comprende la reacción de un compuesto de fórmula (II) o una sal del mismo, en la que Z es un grupo hidroxilo opcionalmente protegido, con un compuesto de fórmula (III) o una sal del mismo, en presencia de una base; y, si es necesario, la eliminación del grupo protector de hidroxilo, y/o, si se desea, la conversión de un compuesto de fórmula (I) en una sal del mismo, o viceversa.
Un grupo protector de hidroxilo puede ser por ejemplo uno de los grupos protectores usados en la química de los alcoholes, normalmente un grupo acilo, por ejemplo un grupo alcanoílo C1-C6, preferiblemente un grupo alcanoílo 35 C1-C4, en particular formilo, acetilo o propionilo; un grupo aril-alcanoílo C1-C6, por ejemplo fenilacetilo, fenilpropionilo o aroílo, por ejemplo benzoílo, en el que el anillo de fenol está opcionalmente sustituido con de uno a tres sustituyentes seleccionados independientemente de, por ejemplo, halógeno, en particular cloro, bromo o yodo, y ciano; un grupo aril-alquilo C1-C6, por ejemplo bencilo, feniletilo o naftalenilmetilo; o un grupo trialquil (C1-C6) -sililo, por ejemplo trimetilsililo, terc-butil-dimetilsililo. Preferiblemente un grupo alcanoílo C1-C6, más preferiblemente un grupo alconoílo C1-C4, en particular formilo o acetilo.
Una base puede ser una base orgánica, por ejemplo un alcóxido C1-C6 de metal alcalino, tal como metóxido, etóxido o terc-butóxido de sodio o potasio; hidruro de sodio, 1, 8-diazabiciclo[5.4.0]undec-7-eno (DBU) , 1, 4diazabiciclo[2.2.2]octano (DABCO) ; o una base inorgánica, por ejemplo un hidróxido, carbonato o fosfato de metal alcalino o alcalinotérreo, por ejemplo hidróxido de sodio, potasio o bario, carbonato de sodio o potasio, o fosfato de sodio o potasio. La base es preferiblemente una base inorgánica, más preferiblemente un fosfato de metal alcalino o alcalinotérreo; en particular fosfato de sodio o potasio.
La razón molar de un compuesto de fórmula (III) con respecto a un compuesto de fórmula (II) puede oscilar aproximadamente entre 1 y 2; de manera preferible aproximadamente entre 1 y 1, 5; en particular alrededor de 1, 2.
La razón molar de la base con respecto a un compuesto de fórmula (II) puede oscilar aproximadamente entre 1 y 10; de manera preferible aproximadamente entre 2 y 5; en particular alrededor de 3.
Opcionalmente, la reacción puede llevarse a cabo en presencia de un catalizador, y, si es necesario, de un ligando.
Un catalizador puede, por ejemplo, basarse en un metal de transición, normalmente cobre. El catalizador se usa normalmente como una sal; ejemplos preferidos son sales de cobre (I) , tales como yoduro, cloruro, bromuro, ortotriflato o acetato de cobre (I) ; preferiblemente yoduro de cobre (I) .
Cuando se usa el catalizador en presencia de un ligando, éste puede ser un ligando orgánico, normalmente un aminoácido, seleccionado de, por ejemplo, glicina, cisteína, lisina, α-alanina, β-alanina. El ligando es preferiblemente un aminoácido; normalmente glicina o α-alanina, en particular glicina.
La razón molar del catalizador con respecto a un compuesto de fórmula (II) puede oscilar aproximadamente entre 0, 01 y 0, 5; de manera preferible aproximadamente entre 0, 03 y 0, 2; en particular alrededor de 0, 04 - 0, 1.
La reacción, independientemente del uso de un catalizador, puede llevarse a cabo en un disolvente, normalmente un disolvente orgánico, seleccionado de por ejemplo un disolvente aprótico dipolar, normalmente dimetilformamida, dimetilacetamida, acetonitrilo, dimetilsulfóxido; un éter, por ejemplo dietil éter, metil terc-butil éter, tetrahidrofurano o dioxano; un disolvente clorado, por ejemplo, diclorometano, cloroformo o clorobenceno; un disolvente apolar, tal como un hidrocarburo alifático, por ejemplo hexano o ciclohexano, o un hidrocarburo aromático, por ejemplo benceno o tolueno; un éster, por ejemplo acetato de etilo o metilo; una cetona, por ejemplo acetona, metil etil cetona, metil isobutil cetona; un alcanol C1-C6, por ejemplo metanol, etanol, isopropanol o terc-butanol; o una mezcla de dos
... [Seguir leyendo]
Reivindicaciones:
1. Procedimiento para la preparación de 4-terc-butil-N-[6- (2-hidroxi-etoxi) -5- (2-metoxi-fenoxi) -[2, 2']bipirimidinil4-il]-bencenosulfonamida, de fórmula (I) , o una sal o forma hidratada de la misma, que comprende la reacción de un compuesto de fórmula (II) , o una sal del mismo, en la que Z es un grupo hidroxilo opcionalmente protegido, con un compuesto de fórmula (III) o una sal del mismo, en presencia de una base; y, si es necesario, la eliminación del grupo protector de hidroxilo, y/o, si se desea, la conversión de un compuesto de fórmula (I) en una sal del mismo, o viceversa.
2. Procedimiento según la reivindicación 1, en el que el grupo protector se selecciona de un grupo acilo; un grupo aril-alquilo C1-C6; y un grupo trialquil (C1-C6) -sililo.
3. Procedimiento según la reivindicación 1, en el que la base se selecciona de un alcóxido C1-C6 de metal alcalino; un hidróxido, carbonato o fosfato de metal alcalino o alcalinotérreo. 25
4. Procedimiento según la reivindicación 2, en el que la base es un fosfato de metal alcalino o alcalinotérreo.
5. Procedimiento según la reivindicación 1, en el que la razón molar de un compuesto de fórmula (III) con
respecto a un compuesto de fórmula (II) oscila aproximadamente entre 1 y 2. 30
6. Procedimiento según la reivindicación 1, en el que la razón molar de la base con respecto a un compuesto de fórmula (II) oscila aproximadamente entre 1 y 5.
7. Procedimiento según la reivindicación 1, en el que la reacción se lleva a cabo en presencia de un 35 catalizador, y, si es necesario de un ligando.
8. Compuesto de fórmula (II) o una sal del mismo, con etilenglicol, en presencia de una base.
en la que Z es grupo hidroxilo protegido. 5 9. Compuesto de fórmula (II) según la reivindicación 8, que es: • éster formílico de 2- (5- (2-metoxi-fenoxi) -6-cloro-2- (pirimidin-2-il) pirimidin-4-iloxi) etanol; • éster acetílico de 2- (5- (2-metoxi-fenoxi) -6-cloro-2- (pirimidin-2-il) pirimidin-4-iloxi) etanol; 10 • éster benzoílico de 2- (5- (2-metoxi-fenoxi) -6-cloro-2- (pirimidin-2-il) pirimidin-4-iloxi) etanol; • trimetilsilil éter de 2- (5- (2-metoxi-fenoxi) -6-cloro-2- (pirimidin-2-il) pirimidin-4-iloxi) etanol; 15 • terc-butil-dimetilsilil éter de 2- (5- (2-metoxi-fenoxi) -6-cloro-2- (pirimidin-2-il) pirimidin-4-iloxi) etanol; • bencil éter de 2- (5- (2-metoxi-fenoxi) -6-cloro-2- (pirimidin-2-il) pirimidin-4-iloxi) etanol; • feniletil éter de 2- (5- (2-metoxi-fenoxi) -6-cloro-2- (pirimidin-2-il) pirimidin-4-iloxi) etanol; o 20 • naftalenilmetil éter de 2- (5- (2-metoxi-fenoxi) -6-cloro-2- (pirimidin-2-il) pirimidin-4-iloxi) etanol. 10. Procedimiento según la reivindicación 1, en el que un compuesto de fórmula (II) , o una sal del mismo, se obtiene mediante un procedimiento que comprende la reacción de un compuesto de fórmula (IV) 2511. Procedimiento según la reivindicación 10, en el que la base se selecciona de una trialquil (C1-C6) -amina, diazabiciclooctano y diazabicicloundeceno o mezclas de los mismos.
12. Procedimiento según la reivindicación 10, en el que la reacción se lleva a cabo en presencia de un exceso de etilenglicol. 35
13. Procedimiento según la reivindicación 10, en el que la reacción se lleva a cabo en presencia de un disolvente orgánico, y la razón molar de etilenglicol con respecto a un compuesto de fórmula (IV) oscila aproximadamente entre 1 y 5.
Patentes similares o relacionadas:
Combinaciones que comprenden derivados de 5-fenoxi-3H-pirimidin-4-ona y sus usos para la profilaxis o el tratamiento de la infección por VIH, del 20 de Noviembre de 2019, de MERCK SHARP & DOHME CORP: Una combinación que comprende (i) un compuesto de Fórmula I: **(Ver fórmula)** o una sal farmacéuticamente aceptable, y (ii) uno o más agentes […]
Método para preparar azoxistrobina, del 13 de Noviembre de 2019, de CAC Nantong Chemical Co., Ltd: Un método de preparación para azoxistrobina, en donde el método de preparación comprende hacer reaccionar 2- cianofenol o una sal del mismo con un compuesto […]
Nueva forma cristalina de la sal de monosodio del foramsulfurón, del 11 de Septiembre de 2019, de BAYER CROPSCIENCE AKTIENGESELLSCHAFT: Sal de monosodio del foramsulfurón en una forma cristalina, caracterizada porque el difractograma de rayos X en polvo de esta sal, con el uso de radiación Cu […]
Nuevos carboxilatos de 4-aminopiridina y 6-aminopirimidina como herbicidas, del 9 de Mayo de 2019, de DOW AGROSCIENCES LLC: Un compuesto de fórmula (I): **Fórmula** en donde X es N o CY, en donde Y es hidrógeno, halógeno, alquilo C1-C3, haloalquilo C1-C3, alcoxi […]
Procedimiento de preparación de derivados de 4,6-bis (ariloxi) pirimidina, del 11 de Abril de 2018, de CHEMINOVA A/S: Un procedimiento de preparación de un compuesto de fórmula general (I)**Fórmula** que comprenden ya sea: a) la reacción de un compuesto […]
Polimorfos de 3-(E)-2-{2-[6-(2-cianofenoxi)pirimidin-4-iloxi]fenil}-3-metoxiacrilato, del 3 de Enero de 2018, de ADAMA MAKHTESHIM LTD: Forma polimorfa cristalina B de (E)-2-{2-[6-(2-cianofenoxi)pirimidin-4-iloxi]fenil}-3-metoxiacrilato de metilo caracterizada por que presenta las propiedades siguientes: […]
Método para la producción de 4,6-dialcoxi-2-cianometilpirimidina e intermedio sintético de la misma, del 8 de Noviembre de 2017, de KUMIAI CHEMICAL INDUSTRY CO., LTD.: Un método para la producción de una 4,6-dialcoxi-2-cianometilpirimidina representada por la siguiente fórmula general **(Ver fórmula)** […]
Derivados de 5-fenoxi-3H-pirimidin-4-ona y su uso como inhibidores de la transcriptasa inversa del VIH, del 20 de Septiembre de 2017, de MERCK SHARP & DOHME CORP: Un compuesto de Fórmula I:**Fórmula** o una de sus sales farmacéuticamente aceptables, en la que: M es CH2, CH2CH2, CH2CH2CH2, CH(CH3), C(CH3)2 o C(O)N(RA); […]