Procedimiento para la preparación de adamantanaminas.
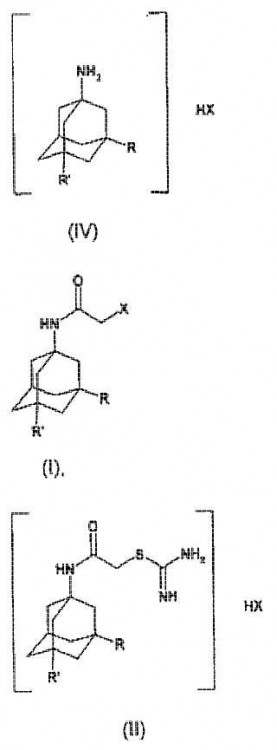
Un procedimiento para preparar un compuesto de fórmula (I)
en la que X es cloro y R y R' son cada uno metilo,
que comprende hacer reaccionar un compuesto de fórmula (III)
en la que R1 es bromo, con un haloacetonitrilo XCH2-CN, en el que X es cloro, en un medio ácido.
Tipo: Patente Europea. Resumen de patente/invención. Número de Solicitud: E06003477.
Solicitante: HEXAL AG.
Nacionalidad solicitante: Alemania.
Dirección: INDUSTRIESTRASSE 25 83607 HOLZKIRCHEN ALEMANIA.
Inventor/es: Schickaneder,Christian.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C07C209/62 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07C COMPUESTOS ACICLICOS O CARBOCICLICOS (compuestos macromoleculares C08; producción de compuestos orgánicos por electrolisiso electroforesis C25B 3/00, C25B 7/00). › C07C 209/00 Preparación de compuestos que contienen grupos amino unidos a una estructura carbonada. › por rotura de enlaces carbono-nitrógeno, azufre-nitrógeno o fósforo-nitrógeno, p. ej. hidrólisis de amidas, N-desalquilación de aminas o de compuestos de amonio cuaternario (C07C 209/24 tiene prioridad).
- C07C211/38 C07C […] › C07C 211/00 Compuestos que contienen grupos amino unidos a una estructura carbonada. › que contiene sistemas cíclicos condensados.
- C07C233/06 C07C […] › C07C 233/00 Amidas de ácidos carboxílicos. › con el átomo de nitrógeno de al menos uno de los grupos carboxamido unido a un átomo de carbono de un ciclo distinto de un ciclo aromático de seis miembros.
- C07C335/32 C07C […] › C07C 335/00 Tioureas, es decir, compuestos que contienen uno de los grupos en que los átomos de nitrógeno no forman parte de grupos nitro o nitroso. › que tienen átomos de azufre de grupos isotiourea unidos a átomos de carbono acíclicos.
PDF original: ES-2379181_T3.pdf
Fragmento de la descripción:
Procedimiento para la preparación de adamantanaminas La invención se refiere a un procedimiento para preparar ciertas adamantanaminas, a productos intermedios usados en el procedimiento y a procedimientos para preparar tales productos intermedios.
Las adamantanaminas se conocen desde hace mucho como una clase de productos farmacéuticos valiosos. Por ejemplo, el hidrocloruro de memantina (hidrocloruro de 1-amino-3, 5-dimetiladamantano, fórmula IVa)
es un antagonista del receptor de NMDA (N-metil-D-aspartato) no competitivo que se usa como un nuevo tratamiento para la enfermedad de Alzheimer. El hidrocloruro de memantina introducido en el mercado como Axura®
es el primer compuesto terapéutico para la enfermedad de Alzheimer que actúa a través de este mecanismo de acción. La memantina se ha comercializado durante más de 20 años en Alemania para el tratamiento de la espasticidad y el síndrome de demencia.
El hidrocloruro de amantadina (1-aminoadamantano, fórmula IVb)
es un antiviral usado para tratar ciertas infecciones por influenza (tipo A) . El compuesto también es un antidiscinético usado para tratar la enfermedad de Parkinson.
US 3.391.142 describe un procedimiento para preparar hidrocloruro de memantina partiendo de 1-bromo-3, 5dimetiladamantano, que se hace reaccionar con acetonitrilo en ácido sulfúrico concentrado para dar el derivado acetamídico, que a continuación se segmenta bajo condiciones de hidrólisis básica.
De acuerdo con WO 01/053234, el adamantano se convierte en N- (1-adamantil) acetamida en un medio de reacción que contiene acetonitrilo seco, flúor y un ácido de Lewis. Este compuesto puede segmentarse bajo condiciones ácidas o básicas dando aminoadamantano.
Para evitar una reacción con HCN altamente tóxico, varios procedimientos describen la reacción de dimetiladamantanos con urea o formamida (WO 05/023753, RU 2246482, DE 2318461, EP 0392059, CZ 288445) .
Existe un número de problemas encontrados con los procedimientos convencionales para preparar adamantanaminas. Los rendimientos de al menos alguna de las etapas son bajos, el tiempo de reacción es relativamente alto, se requieren condiciones de reacción y/o disolventes peligrosos y/o el uso de algunos disolventes provoca dificultades en la purificación del producto final.
Por lo tanto, existe una necesidad de un procedimiento mejorado para preparar adamantanaminas altamente puras, en particular hidrocloruro de memantina o hidrocloruro de amantadina, que venza los problemas susodichos y de ese modo proporcione un procedimiento que sea económico y viable a escala comercial.
Por lo tanto, la presente invención trata de un procedimiento para preparar un compuesto de fórmula (I)
en la que X es cloro y R y R' son cada uno metilo, que comprende hacer reaccionar un compuesto de fórmula (III)
en la que R1 es bromo, con un haloacetonitrilo X-CH2-CN, en el que X es cloro, en un medio ácido.
El medio ácido usado para la reacción del compuesto de fórmula (III) con el haloacetonitrilo, en particular cloroacetonitrilo, comprende adecuadamente un ácido mineral fuerte, en particular ácido sulfúrico. Componentes opcionales adicionales del medio ácido comprenden uno o más disolventes, por ejemplo un ácido orgánico, por ejemplo ácido propiónico o en particular ácido acético; y/o un disolvente aprótico polar, por ejemplo N, N
dimetilformamida (DMF) ; y un catalizador de sal metálica, por ejemplo sulfato de hierro (III) .
Una realización de la invención comprende la reacción de 1-bromo-3, 5-dimetiladamantano (compuesto de fórmula (III) , en la que R es bromo) con cloroacetonitrilo en una solución que comprende ácido sulfúrico, DMF, sulfato de hierro (III) , y opcionalmente un ácido orgánico, en particular ácido acético.
La reacción del compuesto de fórmula (III) con el haloacetonitrilo se lleva a cabo ventajosamente bajo condiciones suaves, por ejemplo a una temperatura de 0 a 70º C, preferiblemente de 0º C a temperatura ambiente y en particular de 0 a 10º C. En general, el ácido mineral fuerte se añade a la mezcla de los reaccionantes, el disolvente o los disolventes y el catalizador opcional de modo que la temperatura no supere los límites dados anteriormente. Después de la adición del ácido mineral, la mezcla de reacción, si es necesario, puede mantenerse a temperatura ambiente o a una temperatura elevada, por ejemplo a una temperatura de 50 a 100º C, preferiblemente de 70 a 80º C, durante un tiempo adecuado para completar la reacción, por ejemplo durante hasta 120 minutos y preferiblemente durante de 30 a 90 minutos. Finalmente, la mezcla de reacción se trata de modo habitual, por ejemplo al hidrolizar la mezcla de reacción con agua a condiciones ambientales, lavar, separar y secar el residuo orgánico, obteniendo así el compuesto de fórmula (I) , en la que R y R' son cada uno metilo.
Los compuestos de fórmula (I) en la que R y R' con cada uno hidrógeno se conocen, por ejemplo, de A. Jirgensons 25 et ál., Synthesis 2000, 12, 1709, y pueden obtenerse, por ejemplo, según se describe allí.
En un aspecto adicional de la presente invención, el compuesto de fórmula (I) se hace reaccionar con tiourea de acuerdo con el procedimiento de la reivindicación 9.
Los compuestos de fórmula (II) se tratan subsiguientemente en un medio ácido.
Un medio ácido preferido es, por ejemplo, un medio ácido acuoso o una mezcla de un alcohol C1-C4 y un ácido o una mezcla de un alcohol C1-C4, agua y un ácido. Un ácido adecuado en la etapa de conversión del compuesto de fórmula (II) es, por ejemplo, un ácido carboxílico C1-C4 orgánico, por ejemplo ácido acético, ácido propiónico o ácido butanoico, en particular ácido acético. Alcoholes útiles son como los definidos anteriormente, por ejemplo etanol o isopropanol. En general, el compuesto de fórmula (II) se trata en el medio ácido bajo reflujo durante un período de tiempo suficiente para completar la conversión, que es, por ejemplo, un período de tiempo de hasta 12 horas y preferiblemente de 4 a 8 horas.
La reacción de los compuestos de fórmula (I) con tiourea se lleva a cabo ventajosamente en un disolvente apropiado a una temperatura de, por ejemplo, 60 a 120º C, preferiblemente a la temperatura de reflujo de la mezcla de reacción, dentro de un período de tiempo de, por ejemplo, aproximadamente 4 horas a aproximadamente 10 horas. Un disolvente adecuado es, por ejemplo, un alcohol C1-C4, por ejemplo metanol, etanol o n- o isopropanol, en particular etanol o isopropanol. Los compuestos resultantes de fórmula (II) pueden aislarse de modo convencional, por ejemplo mediante retirada del disolvente, lavado, cristalización y/o secado.
La etapa de aislamiento del compuesto de fórmula (II) puede omitirse, y los compuestos de fórmula (I) pueden convertirse directamente en la adamantanamina deseada o un hidrohalogenuro de la misma mediante un tratamiento del compuesto de fórmula (I) con tiourea, por ejemplo, bajo reflujo en un medio de reacción según se describe anteriormente, en particular en un medio de reacción que comprende un ácido según se describe anteriormente, agua y/o un alcohol C1-C4.
La adamantanamina resultante puede aislarse en cada caso de la mezcla de reacción en forma de su base libre, por ejemplo, al alcalinizar la solución de reacción y aislar y purificar el producto resultante de modo conocido. Por ejemplo, la mezcla de reacción se trata con un hidróxido alcalino tal como hidróxido sódico. Después de la adición de un disolvente orgánico adecuado, puede realizarse una separación de fases, y la capa orgánica puede someterse a continuación a etapas de acabado típicas tales como etapas de concentración, cristalización y/o secado.
La adamantanamina en forma de su base libre puede convertirse fácilmente en el hidrohalogenuro respectivo mediante un tratamiento con el ácido hidrohalogénico respectivo en un medio que comprende, por ejemplo, un alcohol C1-C4 y opcionalmente agua. Las adamantanaminas, hidrocloruro de memantina o hidrocloruro de amantadina, se obtienen ventajosamente al tratar memantina o amantadina en una solución que comprende un alcohol C1-C4, en particular etanol o isopropanol, y ácido clorhídrico acuoso. Preferiblemente, se añade lentamente ácido clorhídrico concentrado a la solución de memantina o amantadina en un alcohol C1-C4.
En lugar de aislar memantina... [Seguir leyendo]
Reivindicaciones:
1. Un procedimiento para preparar un compuesto de fórmula (I)
en la que X es cloro y R y R' son cada uno metilo, que comprende hacer reaccionar un compuesto de fórmula (III)
en la que R1 es bromo, con un haloacetonitrilo XCH2-CN, en el que X es cloro, en un medio ácido.
2. El procedimiento de acuerdo con la reivindicación 1, en el que el medio ácido comprende un ácido mineral fuerte.
3. El procedimiento de acuerdo con la reivindicación 2, en el que el ácido mineral fuerte es ácido sulfúrico.
4. El procedimiento de acuerdo con cualquier reivindicación precedente, en el que el medio ácido comprende un catalizador de sal metálica.
5. El procedimiento de acuerdo con la reivindicación 4, en el que el catalizador de sal metálica es sulfato de hierro (III) .
6. El procedimiento de acuerdo con cualquier reivindicación precedente, en el que el medio ácido comprende uno o 15 más disolventes seleccionados de un ácido orgánico y un disolvente aprótico polar.
7. El procedimiento de acuerdo con la reivindicación 6, en el que el ácido orgánico se selecciona de ácido propiónico y ácido acético.
8. El procedimiento de acuerdo con la reivindicación 6, en el que el disolvente aprótico polar es N, Ndimetilformamida.
9. El procedimiento de acuerdo con cualquier reivindicación precedente, en el que el compuesto de fórmula (I) se hace reaccionar con tiourea para formar un compuesto de fórmula (II)
10. El procedimiento de acuerdo con la reivindicación 9, en el que el compuesto de fórmula (II) se somete a un tratamiento ácido y la adamantanamina resultante de fórmula (IV)
en la que X es cloro, se aísla.
11. El procedimiento de acuerdo con la reivindicación 10, en el que el tratamiento ácido comprende tratar el compuesto de fórmula (II) en un medio que comprende un ácido carboxílico C1-C4 y uno o más disolventes seleccionados del grupo que consiste en agua y un alcohol C1-C4.
12. El procedimiento de acuerdo con la reivindicación 11, en el que el ácido carboxílico C1-C4 es ácido acético.
13. El procedimiento de acuerdo con las reivindicaciones 10 a 12, en el que la adamantanamina se aísla como la 10 base libre al alcalinizar la solución de reacción.
14. El procedimiento de acuerdo con la reivindicación 13, que comprende, como una etapa adicional, la conversión de la base de adamantanamina libre en un hidrohalogenuro de adamantanamina mediante un tratamiento con un ácido hidrohalogénico, en particular con ácido clorhídrico.
15. El procedimiento de acuerdo con cualquier reivindicación precedente, en el que el compuesto de fórmula (I) se
convierte directamente en la adamantanamina sin aislamiento del compuesto de fórmula (II) mediante reacción con tiourea en un medio que comprende un ácido carboxílico C1-C4 y uno o más disolventes seleccionados del grupo que consiste en agua y un alcohol C1-C4.
16. El procedimiento de acuerdo con la reivindicación 15, en el que la adamantanamina se convierte directamente en el hidrohalogenuro de adamantanamina sin aislamiento de la base libre al añadir el ácido hidrohalogénico a la 20 mezcla de reacción que comprende la adamantanamina en bruto.
Patentes similares o relacionadas:
Composiciones terapéuticamente activas y su método de uso, del 20 de Marzo de 2019, de Agios Pharmaceuticals, Inc: Un compuesto de fórmula II:**Fórmula** o una sal farmacéuticamente aceptable del mismo, donde: R1 se selecciona entre ciclohexilo, ciclopentilo, […]
PROCEDIMIENTO DE PREPARACIÓN DE ALGUNOS MONOSULFUROS SUSTITUIDOS CON HALÓGENO Y SUS EQUIVALENTES DE HIDROXI-MONOSULFURO O BROMURO DE ISOTIOURONIO COMO INTERMEDIOS, del 23 de Noviembre de 2011, de ASTRAZENECA AB: Un procedimiento para preparar un compuesto intermedio de fórmula (II) en donde n un número entero de 3 a 14; R 1 es haloalquilo C1-C10; y R 2 es […]
COMPUESTOS BICICLICOS COMO LIGANDOS DEL RECEPTOR H3., del 16 de Noviembre de 2006, de ORTHO MCNEIL PHARMACEUTICALS, INC.: Un compuesto de fórmula (I): donde cada uno de W1 y W2 es H; X1 es seleccionado entre Ga, RaGa, LaGa y RaLaGa; X2 es seleccionado entre Gb, RbGb, LbGb y RbLbGb; […]
NAFTALENO-UREAS COMO POTENCIADORES DE LA CAPTACION DE GLUCOSA., del 16 de Junio de 2005, de TELIK, INC.: Compuesto de la fórmula: **(Fórmula)** caracterizado porque R1 y R2 son sustituyentes de los anillos A y son, independientemente, -SO2NR72, -C(O)NR72, […]
COMPUESTOS ANTIVIRALES POLIAROMATICOS., del 1 de Septiembre de 2003, de PHARMACIA & UPJOHN COMPANY: La presente invención se refiere a compuestos poliaromáticos que poseen actividad antivírica útil frente a virus de la familia de los herpes, a una composición que […]
COMPOSICIONES FARMACEUTICAS QUE COMPRENDEN DERIVADOS DEL S-ALQUILISOTIOURONIO., del 1 de Marzo de 2003, de MEDITOR PHARMACEUTICALS LTD.: LA INVENCION SE REFIERE A SALES DE S-ALQUILISOTIOURONIUM CON ACIDOS QUE CONTIENEN FOSFORO, QUE INCLUYEN ALGUNOS COMPUESTOS NUEVOS QUE SON UTILES PARA SU USO COMO […]
PREPARACION DE SALES DE ACIDO 6,8-BIS(AMIDINIUMTIO)OCTANOICO., del 1 de Noviembre de 2001, de ASTA MEDICA AKTIENGESELLSCHAFT: LA INVENCION TRATA DE LA OBTENCION Y PURIFICACION DE SALES DEL ACIDO 6,8-BIS(AMIDINIOTIO)-OCTANO , SUS ENANTIOMEROS (+)-6,8-BIS(AMIDINIOTIO)-OCTANO Y -6,8-BIS(AMIDINIOTIO)-OCTANO […]
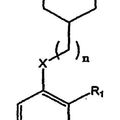 NO-IMIDAZOL ARILOXIPIPERIDINA COMO LIGANDOS DEL RECEPTOR H3, del 16 de Octubre de 2007, de ORTHO MCNEIL PHARMACEUTICALS, INC.: Un compuesto de **fórmula**, donde X es O; n es un entero de 0 a 3; R5 es alquilo C1-C10, alquenilo C3-C8, cicloalquilo C3-C8, cicloalquil(C3-C8)alquilo […]
NO-IMIDAZOL ARILOXIPIPERIDINA COMO LIGANDOS DEL RECEPTOR H3, del 16 de Octubre de 2007, de ORTHO MCNEIL PHARMACEUTICALS, INC.: Un compuesto de **fórmula**, donde X es O; n es un entero de 0 a 3; R5 es alquilo C1-C10, alquenilo C3-C8, cicloalquilo C3-C8, cicloalquil(C3-C8)alquilo […]