Procedimiento novedoso de prevención o tratamiento de infección por M. tuberculosis.
Una composición farmacéutica que comprende:
(i) una proteína de fusión Mtb72f o un fragmento inmunógeno de la misma de una especie de Mycobacterium del complejo de la tuberculosis y un adyuvante,
o
(ii) un ácido nucleico que codifica una proteína de fusión Mtb72f o un fragmento inmunógeno de la misma de una especie de Mycobacterium del complejo de la tuberculosis;
para su uso como un medicamento para administración con uno o más agentes quimioterapéuticos efectivos contra una infección por M. tuberculosis.
Tipo: Patente Europea. Resumen de patente/invención. Número de Solicitud: E11190080.
Solicitante: GLAXOSMITHKLINE BIOLOGICALS S.A..
Nacionalidad solicitante: Bélgica.
Dirección: RUE DE L'INSTITUT, 89 1330 RIXENSART BELGICA.
Inventor/es: LOBET, YVES, REED,STEVEN, COLER,Rhea.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K39/04 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 39/00 Preparaciones medicinales que contienen antígenos o anticuerpos (materiales para ensayos inmunológicos G01N 33/53). › Mycobacterium, p. ej. Mycobacterium tuberculosis.
- C07K14/35 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 14/00 Péptidos con más de 20 aminoácidos; Gastrinas; Somatostatinas; Melanotropinas; Sus derivados. › de Mycobacteriaceae (F).
PDF original: ES-2524572_T3.pdf
Fragmento de la descripción:
Procedimiento novedoso de prevención o tratamiento de infección por M. tuberculosis Campo de la invención La presente invención se refiere a procedimientos para reducir el curso del tiempo de la quimioterapia contra una infección por M. tuberculosis.
Antecedentes de la invención La tuberculosis es una enfermedad infecciosa crónica causada por la infección con M. tuberculosis y otras especies de Mycobacterium. Es una enfermedad principal en los países en desarrollo, así como un problema creciente en las áreas desarrolladas del mundo, con aproximadamente 8 millones de nuevos casos y 3 millones de muertes cada año. Aunque la infección puede ser asintomática durante un período de tiempo considerable, la enfermedad se manifiesta más comúnmente como una inflamación aguda de los pulmones, dando como resultado fiebre y una tos no productora. Si no se trata, resultan típicamente complicaciones graves y la muerte.
Aunque la tuberculosis se puede controlar en general empleando terapia prolongada con antibióticos, este tratamiento no es suficiente para evitar la propagación de la enfermedad. Los individuos infectados pueden ser asintomáticos, pero contagiosos, durante algún tiempo. Además, aunque es crítico el cumplimiento con el régimen de tratamiento, es difícil monitorear el comportamiento del paciente. Algunos pacientes no terminan el periodo de tratamiento, lo que puede conducir a un tratamiento inefectivo y al desarrollo de resistencia a los fármacos. Inclusive cuando se ha terminado un curso completo de tratamiento, la infección con M. tuberculosis no se erradica del individuo infectado, sino que permanece como una infección latente que se puede reactivar.
Con el objeto de controlar la propagación de la tuberculosis, es de primordial importancia una vacunación efectiva y un diagnóstico precoz preciso de la enfermedad. En la actualidad, la vacunación con bacterias vivas es el procedimiento más eficiente para inducir una inmunidad protectora. La micobacteria más común empleada para este propósito es Bacillus Calmette-Guerin (BCG) , una cepa avirulenta de M. bovis. Sin embargo, la seguridad y eficacia de BCG es una fuente de controversia y algunos países, tales como los Estados Unidos, no vacunan al público en general con este agente.
El diagnóstico de la tuberculosis se logra comúnmente utilizando una prueba de piel, que involucra la exposición intradérmica a la tuberculina PPD (derivado purificado de proteína) . Las respuestas de las células-T específicas del antígeno dan como resultado una induración mensurable en el sitio de inyección a las 48-72 horas después de la inyección, lo que indica la exposición a los antígenos micobacterianos. Sin embargo, la sensibilidad y la especificidad han sido un problema con esta prueba y los individuos vacunados con BCG no se pueden distinguir de los individuos infectados.
Aunque se ha demostrado que los macrófagos actúan como los efectores principales de la inmunidad a Mycobacterium, las células-T son los inductores predominantes de esta inmunidad. El papel esencial de las células-T en la protección contra la infección por Mycobacterium se ilustra por la frecuente aparición de infección por Mycobacterium en los pacientes de SIDA, debido al agotamiento de las células-T CD4+ asociado con la infección por el virus de inmunodeficiencia humana (VIH) . Se ha demostrado que las células-T CD4+ que reaccionan con Mycobacterium son potentes productores del interferón- (IFN-) , que, a su vez, se ha demostrado que desencadena los efectos anti-micobacterianos de los macrófagos en los ratones. Aunque está menos claro el papel del IFN- en los seres humanos, los estudios han demostrado que la 1, 25-dihidroxi-vitamina D3, ya sea sola o en combinación con IFN- o con el factor de necrosis tumoral-alfa, activa los macrófagos humanos para inhibir la infección por M. tuberculosis. Adicionalmente, se sabe que el IFN- estimula los macrófagos humanos para hacer la 1, 25-dihidroxivitamina D3. De una manera similar, se ha demostrado que la interleucina-12 (IL-12) tiene un papel en el estímulo de la resistencia a la infección por M. tuberculosis. Para una revisión de la inmunología de la infección por M. tuberculosis, véase Chan y Kaufmann, Tuberculosis: Pathogenesis, Protection and Control (Bloom, editor, 1994) , Tuberculosis (2ª edición, Rom y Garay, editores, 2003) y Harrison's Principles of Internal Medicine, Capítulo 150, páginas 953-966 (16ª edición, Braunwald y colaboradores, editores, 2005) .
Brandt y colaboradores Infection and Immunity 2004 72 (11) : 6622-6632 muestra como el efecto protector de la vacuna de Mycobacterium bovis BCG se puede incrementar por coadministración con la Mtb72F en cobayas.
Descripción de las secuencias enumeradas
SEC ID Nº :1: Mtb72f con etiqueta 6 His N-terminal (ADN) .
SEC ID Nº :2: Mtb72f con etiqueta 6 His N-terminal (proteína) .
SEC ID Nº :3: M72 (variante de Mtb72f) con inserción de 2 His N-terminal (ADN) .
2
SEC ID Nº :4: M72 (variante de Mtb72f) con inserción de 2 His N-terminal (proteína) .
SEC ID Nº :5: Mtb72f sin inserción de His N-terminal (ADN) .
SEC ID Nº :6: Mtb72f sin inserción de His N-terminal (proteína) .
Breve sumario de la invención La presente invención proporciona composiciones farmacéuticas que comprenden una proteína de fusión Mtb72f o un fragmento inmunógeno de la misma, de una especie de Mycobacterium del complejo de tuberculosis junto con uno o más adyuvantes, incluyendo AS01B y AS02A, para uso como un medicamento para administración con uno o más agentes quimioterapéuticos efectivos contra una infección por M. tuberculosis.
También se proporciona una composición farmacéutica que comprende un ácido nucleico que codifica una proteína de fusión Mtb72f o un fragmento inmunógeno de la misma, de una especie de Mycobacterium del complejo de tuberculosis para uso como un medicamento para administración con uno o más agentes quimioterapéuticos efectivos contra una infección por M. tuberculosis.
Las composiciones se pueden emplear en procedimientos para reducir el tiempo de la quimioterapia contra una infección por M. tuberculosis. Al reducir el tiempo de la quimioterapia contra una infección por M. tuberculosis, los procedimientos también son efectivos para mejorar la conformidad de un individuo que esté siendo tratado por una infección por M. tuberculosis, en la realización de un periodo entero de tratamiento.
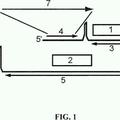
Breve descripción de los dibujos La Figura 1 muestra una representación gráfica del modelo de reactivación de M. tuberculosis en ratones Swiss Webster (SWR/J) . La figura muestra los puntos del tiempo para la infección, el tratamiento con quimioterapia (50 miligramos de rifampina/85 miligramos de isoniazida por litro del agua para beber) , las inmunizaciones y la enumeración de la carga bacteriana/las unidades formadoras de colonias (CFU) .
La Figura 2 muestra las respuestas inmunes de los anticuerpos IgG1 e IgG2a en ratones SWR/J infectados con M. tuberculosis tratados con quimioterapia y luego inmunizados con Mtb72f. Los ratones se dejaron sin tratamiento, se trataron con quimioterapia (50 miligramos de rifampina/85 miligramos de isoniazida por litro del agua potable) , o bien se trataron con quimioterapia y se inmunizaron tres veces intramuscularmente con 8 microgramos por dosis de Mtb72f formulada sin adyuvante. 10 días después de la última inmunización, los ratones se sangraron y se probaron los sueros para determinar la respuesta del anticuerpo anti-Mtb72f para ambos isótopos IgG1 (rojo) e IgG2a (negro) mediante ELISA.
La Figura 3 muestra las respuestas inmunes de los anticuerpos IgG1 e IgG2a en los ratones SWR/J infectados por M. tuberculosis tratados con quimioterapia y luego inmunizados con Mtb72f. Los ratones se dejaron sin tratamiento, se trataron con quimioterapia (50 miligramos de rifampina/85 miligramos de isoniazida por litro del agua potable) , o se trataron con quimioterapia y se inmunizaron tres veces intramuscularmente con 8 microgramos por dosis de Mtb72f formulada con el adyuvante AS01B. 10 días después de la última inmunización, los ratones se sangraron y se probaron los sueros para determinar la respuesta del anticuerpo anti-Mtb72f para ambos isótopos IgG1 (rojo) e IgG2a (negro) mediante ELISA.
La Figura 4 muestra las respuestas del interferón-gamma (IFN-) en los ratones SWR/J infectados por M. tuberculosis tratados con quimioterapia y luego inmunizados con Mtb72f. Se obtuvieron células de bazo de los ratones en diferentes puntos del tiempo y se estimularon in vitro durante 3 días con 10 microgramos/mililitro ya sea de rMtb72f o bien de los componentes (Mtb32C y Mtb39) , como se indica. Como... [Seguir leyendo]
Reivindicaciones:
1. Una composición farmacéutica que comprende:
(i) una proteína de fusión Mtb72f o un fragmento inmunógeno de la misma de una especie de Mycobacterium del complejo de la tuberculosis y un adyuvante, o
(ii) un ácido nucleico que codifica una proteína de fusión Mtb72f o un fragmento inmunógeno de la misma de una especie de Mycobacterium del complejo de la tuberculosis;
para su uso como un medicamento para administración con uno o más agentes quimioterapéuticos efectivos contra una infección por M. tuberculosis.
2. La composición farmacéutica de la reivindicación 1, que comprende una proteína de fusión Mtb72f o un fragmento inmunógeno de la misma de una especie de Mycobacterium del complejo de la tuberculosis y un adyuvante, para su uso como un medicamento para administración con uno o más agentes quimioterapéuticos efectivos contra una infección por M. tuberculosis.
3. La composición farmacéutica de la reivindicación 1, que comprende un ácido nucleico que codifica una proteína de fusión Mtb72f o un fragmento inmunógeno de la misma de una especie de Mycobacterium del complejo de la tuberculosis para uso como un medicamento para administración con uno o más agentes quimioterapéuticos efectivos contra una infección por M. tuberculosis.
4. La composición farmacéutica para uso de acuerdo con la reivindicación 2, en la que la Mtb72f es un polipéptido que comprende residuos 8-729 de la SEC ID Nº : 2.
5. La composición farmacéutica para uso de acuerdo con la reivindicación 2, en la que la Mtb72f es un polipéptido que comprende residuos 4-725 de la SEC ID Nº : 4.
6. La composición farmacéutica para uso de acuerdo con la reivindicación 2, en la que el adyuvante es seleccionado del grupo que consiste e.
3. MPL y QS21 en una formulación de liposomas .
3. MPL y QS21 y una emulsión de aceite en agua.
7. La composición farmacéutica para uso de acuerdo con la reivindicación 2, en la que los uno o más agentes quimioterapéuticos son seleccionados de isoniazida y rifampicina.
8. La composición farmacéutica de la reivindicación 3, para su uso en prevenir o tratar reactivación de tuberculosis en un mamífero ya infectado con Mycobacterium tuberculosis.
9. Uso de:
(i) una proteína de fusión Mtb72f o un fragmento inmunógeno de la misma de una especie de Mycobacterium del complejo de la tuberculosis y un adyuvante, o
(ii) un ácido nucleico que codifica una proteína de fusión Mtb72f o un fragmento inmunógeno de la misma de una especie de Mycobacterium del complejo de la tuberculosis;
en la fabricación de una composición farmacéutica para administración con uno o más agentes quimioterapéuticos efectivos contra una infección por M. tuberculosis.
10. El uso de acuerdo con la reivindicación 9, de una proteína de fusión de Mtb72f o un fragmento inmunógeno de la misma de una especie de Mycobacterium del complejo de la tuberculosis y un adyuvante en la fabricación de una composición farmacéutica para administración con uno o más agentes quimioterapéuticos efectivos contra una infección por M. tuberculosis.
11. El uso de acuerdo con la reivindicación 9, de un ácido nucleico que codifica una proteína de fusión Mtb72f o un fragmento inmunógeno de la misma de una especie de Mycobacterium del complejo de la tuberculosis en la fabricación de una composición farmacéutica para administración con uno o más agentes quimioterapéuticos efectivos contra una infección por M. tuberculosis.
12. El uso de acuerdo con la reivindicación 9, en la Mtb72f es un polipéptido que comprende residuos 8-729 de SEC ID Nº : 2.
13. El uso de acuerdo con la reivindicación 9, en la Mtb72f es un polipéptido que comprende residuos 4-725 de SEC ID Nº : 4.
14. El uso de acuerdo con la reivindicación 9, en el que el adyuvante es seleccionado del grupo que consiste e.
3. MPL y QS21 en una formulación de liposomas .
3. MPL y QS21 y una emulsión de aceite en agua. 59
15. El uso de acuerdo con la reivindicación 9, en el que el uno o más agentes quimioterapéuticos son seleccionados de isoniazida y rifampicina.
16. El uso de acuerdo con la reivindicación 9, de un ácido nucleico que codifica una proteína de fusión Mtb72f o un fragmento inmunógeno de la misma de una especie de Mycobacterium del complejo de la tuberculosis en la fabricación de una composición farmacéutica para prevención o tratamiento de reactivación de tuberculosis en un mamífero ya infectado con Mycobacterium tuberculosis con uno o más agentes quimioterapéuticos efectivos contra una infección por M. tuberculosis.
Figura 4A
días de tratamiento SWR Medio Días después de la infección Figura 4B
días de tratamiento SWR Mtb72f
Días después de la infección Figura 4C
días de tratamiento SWR conA
Días después de la infección Figura 4D
días de tratamiento SWR MtbH9
Días después de la infección Figura 4E
días de tratamiento SWR PPD
Días después de la infección Figura 4F
días de tratamiento SWR MtbRa12
Días después de la infección Figura 4G
días de tratamiento SWR Lisado de BCG
Días después de la infección Figura 5A
días de tratamiento, 72f + ASO1B SWR
Medio Días después de la infección Figura 5B
días de tratamiento, 72f + ASO1B SWR
Mtb72f
Días después de la infección Figura 5C
días de tratamiento, 72f + ASO1B SWR
conA
Días después de la infección Figura 5D
días de tratamiento, 72f + ASO1B SWR
MtbRa12
Días después de la infección Figura 5E
días de tratamiento SWR PPD
Días después de la infección Figura 5F
días de tratamiento SWR MtbTbH9
Días después de la infección Figura 5G
días de tratamiento SWR Lisado de BCG
Días después de la infección
Patentes similares o relacionadas:
Composiciones inmunogénicas de PCV2 multivalentes y métodos para producir dichas composiciones, del 27 de Mayo de 2020, de Boehringer Ingelheim Animal Health USA Inc: Una vacuna combinada multivalente para uso en un método para (i) la prevención de una infección por PCV2, o de reinfección por PCV2 o (ii) la reducción o eliminación […]
Arginina desiminasa con reactividad cruzada reducida hacia anticuerpos para ADI - PEG 20 para el tratamiento del cáncer, del 6 de Mayo de 2020, de TDW Group: Una composición terapéutica que comprende una arginina desiminasa (ADI) aislada y un vehículo farmacéuticamente aceptable, en donde la ADI aislada comprende la secuencia de […]
Mycobacterium recombinante como vacuna para uso en seres humanos, del 18 de Marzo de 2020, de VAKZINE PROJEKT MANAGEMENT GMBH: Una célula de Mycobacterium bovis recombinante de la cepa Danesa subtipo Praga que es deficiente en ureasa y que comprende una molécula de ácido nucleico […]
VACUNA MULTIVALENTE PARA EL TRATAMIENTO Y PREVENCIÓN DE LA TUBERCULOSIS, LISTERIOSIS Y NEUMONÍA, del 26 de Diciembre de 2019, de FUNDACIÓN INSTITUTO DE INVESTIGACIÓN MARQUÉS DE VALDECILLA: La presente invención se refiere a una vacuna sintética multivalente eficaz en el tratamiento y/o prevención de la tuberculosis, listeriosis y neumonías. Las vacunas terapéuticas […]
VACUNA MULTIVALENTE PARA EL TRATAMIENTO Y PREVENCIÓN DE LA TUBERCULOSIS, LISTERIOSIS Y NEUMONÍA, del 23 de Diciembre de 2019, de FUNDACIÓN INSTITUTO DE INVESTIGACIÓN MARQUÉS DE VALDECILLA: Vacuna multivalente para el tratamiento y prevención de la tuberculosis, listeriosis y neumonía. La presente invención se refiere a una vacuna sintética […]
 Composición antigénica de micobacterias, del 31 de Julio de 2019, de GLAXOSMITHKLINE BIOLOGICALS S.A.: Una composición inmunogénica que comprende un antígeno relacionado con M72, en la que el antígeno relacionado con M72 comprende una secuencia […]
Composición antigénica de micobacterias, del 31 de Julio de 2019, de GLAXOSMITHKLINE BIOLOGICALS S.A.: Una composición inmunogénica que comprende un antígeno relacionado con M72, en la que el antígeno relacionado con M72 comprende una secuencia […]
 Vacunas antimicobacterianas, del 31 de Julio de 2019, de UNIVERSITE DE GENEVE: Una partícula de virus infeccioso de la coriomeningitis linfocítica deficiente en la replicación para uso como una vacuna en un método para tratar o prevenir una infección […]
Vacunas antimicobacterianas, del 31 de Julio de 2019, de UNIVERSITE DE GENEVE: Una partícula de virus infeccioso de la coriomeningitis linfocítica deficiente en la replicación para uso como una vacuna en un método para tratar o prevenir una infección […]
Vacuna TB contra la tuberculosis para impedir la reactivación, del 28 de Mayo de 2019, de STATENS SERUM INSTITUT: Vacuna para la utilización en el bloqueo de la reactivación de la tuberculosis en individuos con infección latente por M. tuberculosis, que comprende […]