PROCEDIMIENTO DE IDENTIFICACION DE COMPUESTOS ANTITUMORALES INHIBIDORES DE LA DIMERIZACION DE LAS PROTEINAS ERK.
Procedimiento de identificación de compuestos antitumorales inhibidores de la dimerización de las proteínas ERK.
La presente invención describe un procedimiento para identificar y evaluar compuestos antitumorales. El procedimiento se basa en la búsqueda de compuestos inhibidores de la dimerización de las proteínas ERK. La inhibición de dicho proceso disminuye la malignización, proliferación y progresión tumoral
Tipo: Patente de Invención. Resumen de patente/invención. Número de Solicitud: P200801139.
Solicitante: CONSEJO SUPERIOR DE INVESTIGACIONES CIENTIFICAS (CSIC).
Nacionalidad solicitante: España.
Provincia: MADRID.
Inventor/es: CRESPO BARAJA,PEDRO.
Fecha de Solicitud: 21 de Abril de 2008.
Fecha de Publicación: .
Fecha de Concesión: 29 de Septiembre de 2010.
Clasificación Internacional de Patentes:
- C12N15/11B5
- C12Q1/48B
Clasificación PCT:
- A61P35/00 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › Agentes antineoplásicos.
- C12N15/11 QUIMICA; METALURGIA. › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 15/00 Técnicas de mutación o de ingeniería genética; ADN o ARN relacionado con la ingeniería genética, vectores, p. ej. plásmidos, o su aislamiento, su preparación o su purificación; Utilización de huéspedes para ello (mutantes o microorganismos modificados por ingeniería genética C12N 1/00, C12N 5/00, C12N 7/00; nuevas plantas en sí A01H; reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00; nuevas razas animales en sí A01K 67/00; utilización de preparaciones medicinales que contienen material genético que es introducido en células del cuerpo humano para tratar enfermedades genéticas, terapia génica A61K 48/00; péptidos en general C07K). › Fragmentos de ADN o de ARN; sus formas modificadas (ADN o ARN no empleado en tecnología de recombinación C07H 21/00).
- C12Q1/48 C12 […] › C12Q PROCESOS DE MEDIDA, INVESTIGACION O ANALISIS EN LOS QUE INTERVIENEN ENZIMAS, ÁCIDOS NUCLEICOS O MICROORGANISMOS (ensayos inmunológicos G01N 33/53 ); COMPOSICIONES O PAPELES REACTIVOS PARA ESTE FIN; PROCESOS PARA PREPARAR ESTAS COMPOSICIONES; PROCESOS DE CONTROL SENSIBLES A LAS CONDICIONES DEL MEDIO EN LOS PROCESOS MICROBIOLOGICOS O ENZIMOLOGICOS. › C12Q 1/00 Procesos de medida, investigación o análisis en los que intervienen enzimas, ácidos nucleicos o microorganismos (aparatos de medida, investigación o análisis con medios de medida o detección de las condiciones del medio, p. ej. contadores de colonias, C12M 1/34 ); Composiciones para este fin; Procesos para preparar estas composiciones. › en los que interviene una transferasa.
Fragmento de la descripción:
Procedimiento de identificación de compuestos antitumorales inhibidores de la dimerización de las proteínas ERK.
Sector de la técnica
Sector biotecnológico con aplicaciones en salud humana, y más concretamente procedimiento de identificación de compuestos con aplicaciones terapéuticas para los seres humanos.
Estado de la técnica
En todos los organismos pluricelulares, el mantenimiento del número adecuado de células es consecuencia de una estricta y exquisita regulación de los procesos de proliferación y supervivencia celular. En condiciones fisiológicas, dichos procesos se regulan en respuesta a señales extracelulares en forma de péptidos solubles, tanto factores de crecimiento como hormonas. La recepción de estas señales en el exterior celular, desata una serie de reacciones en cadena, mediante las cuales la señal se transmite por el interior de la célula, a través de complejas interacciones moleculares, hacia el núcleo, desde donde finalmente se pondrán en funcionamiento los programas genéticos y procesos celulares necesarios para iniciar la división celular y/o promover la supervivencia celular. Un funcionamiento defectuoso o una regulación inapropiada de los mecanismos de señalización molecular implicados en estos procesos son causa de muchas patologías caracterizadas por una proliferación/supervivencia celular descontrolada, tal y como el cáncer.
De todas las proteínas implicadas en rutas de señalización molecular, posiblemente unas de las que más interés han despertado en las últimas décadas, son las pertenecientes a la familia de las MAP quinasas (Mitogen-Activated Protein Kinases). Las MAPKs son activadas por estímulos de muy diversa naturaleza y su activación es un paso crítico en la traducción de estímulos extracelulares en respuestas intracelulares, mediante la fosforilación y consiguiente activación de múltiples sustratos, a través de los cuales se regulan procesos como la expresión génica, dinámica citoesquelética, metabolismo celular, entre otros mecanismos esenciales para la proliferación, diferenciación y supervivencia celular. Dentro de las MAPKs, la familia ERK (Extracellular signal-Regulated Kinases) es la más estudiada. Las ERKs cuentan con dos isoformas: p44 ERK1 y p42 ERK2, con una homología cercana al 80%. Ambas son activadas por gran variedad de estímulos, en particular los mitogénicos. Dicha activación se realiza a través de una cascada de fosforilaciones regulada inicialmente por la GTPasa Ras, en la que participan las serina/treoninas quinasas citoplasmáticas de la familia Raf y la quinasa de especificidad dual MEK. En estado basal, las ERKs se localizan fundamentalmente en el citoplasma, ancladas en esta ubicación mediante su interacción con MEK. Al ser fosforiladas por MEK se rompe dicha interacción y las ERKs se distribuyen por toda la célula, translocándose también al núcleo, donde llevan a cabo la fosforilación/activación de sus sustratos (Robinson, M. J., y Cobb, M. H. (1997). Mitogen-Activated Protein kinases pathways. Curr Opin Cell Biol 9, 180-186).
En la cascada de activación de las ERKs intervienen también una serie de proteínas denominadas proteínas de andamiaje (scaffolds), donde se ensamblarían los distintos componentes de la cascada de señalización de una manera específica, aislando la señal de otras similares y optimizando la eficiencia de la interacción entre los distintos componentes de dicha cascada. Además, algunas de estas proteínas de andamiaje tienen la capacidad de seleccionar sustratos y sus funciones podrían también estar determinadas por la sublocalización celular (Kolch, W. (2005). Coordinating ERK/MAPK signalling through scaffolds and inhibitors. Nat Rev Mol Cell Biol 6, 827-837). No obstante se desconocen todavía muchos detalles sobre el papel desempeñado por las proteínas de andamiaje en la activación de las ERKs.
Una característica de las ERKs es que al ser activadas forman dímeros. Estos dímeros son siempre homodímeros, ya que los heterodímeros ERK1/ERK2 son inestables (Khokhlatchev, A. V., Canagarajah, B., Wilsbacher, J., Robinson, M., Atkinson, M., Goldsmith, E., y Cobb, M. H. (1998). Phosphorylation of the MAP kinase ERK2 promotes its homodimerization and nuclear translocation. Cell 93, 605-615). La dimerización tiene lugar mediante una "cremallera de leucinas" no helical, entre las leucinas 333, 336 y 344, y dos pares fónicos flanqueantes, proporcionados por la histidina 176 y el ácido glutámico 343 (Wilsbacher, J. L., Juang, Y. C., Khokhlatchev, A. V., Gallagher, E., Binns, D., Goldsmith, E. J., y Cobb, M. H. (2006). Characterization of mitogen-activated protein kinase (MAPK) dimers. Biochemistry 45, 13175-13182). Aunque los detalles estructurales de estos dímeros están bastante bien caracterizados, su papel en las funciones bioquímicas, biológicas y fisiopatológicas de las ERKs es absolutamente desconocido.
Debido a su papel esencial en la regulación de la proliferación celular, la ruta de activación de las ERKs presenta un potencial evidente como diana terapéutica, en particular para la acción de fármacos antitumorales. Los ensayos clínicos realizados en esta línea han mostrado que los principales problemas que afrontan estos ensayos son la toxicidad y los efectos secundarios no deseados. Sin embargo, los inventores han identificado que la dimerización de las proteínas ERKs es una diana altamente específica para identificar compuestos antitumorales que solucionen el problema que afrontan los compuestos antitumorales con acción sobre la ruta ERK desarrollados hasta la fecha.
Descripción de la invención
La presente invención se basa en que los inventores han demostrado que la inhibición de las señales citoplasmáticas de las ERKs mediante el bloqueo de su dimerización es suficiente para contrarrestar la malignización, proliferación y progresión tumoral. De lo que se deduce que el proceso de dimerización de las ERKs ofrece de forma novedosa una diana de intervención terapéutica antitumoral. Muchas de las estrategias seguidas hasta la fecha, buscando inhibidores de la ruta ERKs, se han basado en inhibidores de la actividad catalítica de las distintas quinasas que componen la ruta. En la mayoría de los casos, los resultados no han sido totalmente satisfactorios debido, fundamentalmente, a que este tipo de inhibidores presentan una alta inespecificidad, fruto de la alta homología dentro de la gran familia de las quinasas. Sin embargo, la dimerización de ERKs presenta una diana potencialmente específica para bloquear esta ruta, ya que la superficie de dimerización entre dos moléculas de ERK es única, lo que posibilitaría la síntesis de inhibidores altamente específicos.
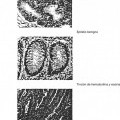
Así, los inventores han demostrado por primera vez que la inhibición de la formación de dímeros bloquea la transformación celular. Los inventores han utilizado un mutante de ERK2, ERK2 H176E, L4A (ERK2 HL) (Khokhlatchev, A. V., Canagarajah, B., Wilsbacher, J., Robinson, M., Atkinson, M., Goldsmith, E., y Cobb, M. H. (1998). Phosphorylation of the MAP kinase ERK2 promotes its homodimerization and nuclear translocation. Cell 93, 605-615), incapaz de dimerizar, para ensayar los efectos de la inhibición de la dimerización de ERKs sobre la transformación de fibroblastos murinos NIH3T3 inducida por distintos tipos de oncogenes, tales como H-RasV12, v-Src y Dbl. La inhibición de la formación de dímeros ERK2 bloquea en un 90% la transformación celular (Fig. 2, panel inferior), lo que pone en evidencia la importancia de estos procesos en las fases iniciales de la génesis tumoral.
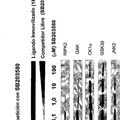
Siguiendo en esta línea, los inventores han establecido sublíneas que expresan ERK2 HL establemente en líneas celulares derivadas de tumores humanos, en concreto las líneas HCT116, T24 y H1299 procedentes de carcinoma colorrectal, de vejiga y de pulmón respectivamente. En todas estas sublíneas, la cantidad de dímeros ERK2 disminuye dramáticamente, sin que eso afecte en absoluto a los niveles totales de activación de ERK2 (Fig. 3). Asimismo, la tasa de proliferación celular de estas líneas celulares se reduce en aproximadamente un 50% en comparación con las líneas salvajes (Fig. 4).
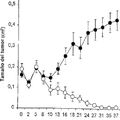
Para comprobar la necesidad de la dimerización de ERKs para el crecimiento tumoral in vivo, los inventores han realizado xenotransplantes en ratones "desnudos" (inmunodeprimidos), inyectando dichas sublíneas tumorales defectivas para la dimerización de ERK2. Posteriomente, han monitorizado el crecimiento...
Reivindicaciones:
1. Procedimiento in vivo o in vitro para identificar y evaluar la eficacia de compuestos para terapia antitumoral, que comprende:
a) Poner en contacto el compuesto candidato con una muestra de proteínas ERKs, en las condiciones y durante el tiempo apropiado para permitir que interaccionen, ya sea in vivo o in vitro,
b) Cuantificar el nivel de dimerización de las proteínas ERKs, y
c) Comparar dicho nivel con el de una muestra de proteínas ERKs en las mismas condiciones pero sin tratar con el compuesto candidato.
2. Procedimiento según la reivindicación 1 caracterizado porque las proteínas ERKs de a) están constituidas por un único tipo de ERK, perteneciente al siguiente grupo:
- ERK1 (SEQ ID NO2), y
- ERK2 (SEQ ID NO4).
3. Procedimiento según reivindicación 1 caracterizado porque la técnica utilizada para la cuantificación del nivel de dimerización de las proteínas ERKs de b) pertenece al siguiente grupo: electroforesis en condiciones nativas, complementación fluorescente bimolecular, cromatografía de exclusión por tamaño, ultracentrifugación analítica, dispersión de luz, fluorescencia, resonancia magnética nuclear, dicroísmo circular, yeast two-hybrid y microarrays de proteínas.
4. Uso de un agente inhibidor de la dimerización de ERKs en la elaboración de un medicamento o composición farmacéutica para el tratamiento de una enfermedad que curse con proliferación y malignización celular, como el cáncer.
5. Uso de un agente inhibidor según reivindicación 4 para el tratamiento de carcinoma colorrectal, de vejiga y de pulmón.
6. Uso de un agente inhibidor según reivindicaciones 4 y 5 caracterizado porque el agente inhibidor está constituido por una proteína mutante de ERK2 o un fragmento de una proteína mutante de ERK2 con mutaciones en el dominio de dimerización de ERK2.
7. Uso de un agente inhibidor según reivindicación 6 caracterizado porque el agente inhibidor está constituido por una proteína mutante de ERK2, ERK2 H176E, L4A (ERK2 HL) (SEQ ID NO6).
8. Uso de los polinucleótidos codificantes de las proteínas mutantes de ERK2 según reivindicaciones 6 y 7 en un proceso de terapia génica.
9. Composición farmacéutica que comprende un compuesto o agente inhibidor según reivindicaciones 4 a 7 útil para el tratamiento de una enfermedad que curse con proliferación y malignización celular, como el cáncer.
10. Composición farmacéutica según reivindicación 9 útil para el tratamiento de carcinoma colorrectal, de vejiga y de pulmón.
Patentes similares o relacionadas:
INDICADOR BIOLÓGICO, del 22 de Noviembre de 2011, de HEALTH PROTECTION AGENCY: Uso de una cinasa termoestable como indicador para validar un proceso de tratamiento para reducir la cantidad o actividad de un agente biológico contaminante en una muestra; […]
ENSAYO GENÉRICO DE DETECCIÓN DE ACTIVIDAD QUINASA/FOSFATASA CON UNA ÚNICA LECTURA, del 21 de Noviembre de 2011, de F. HOFFMANN-LA ROCHE AG: Un método para detectar una actividad quinasa o actividad fosfatasa que comprende los pasos: a) incubar una muestra con actividad quinasa […]
USO DE UN AGENTE MODULADOR QUE ACTÚA SOBRE UN PRECURSOR DE FACTOR DE CRECIMIENTO CON EL FIN DE INHIBIR EL TRATAMIENTO DEL PRECURSOR DE FACTOR DE CRECIMIENTO, del 16 de Noviembre de 2011, de MAX-PLANCK-GESELLSCHAFT ZUR FORDERUNG DER WISSENSCHAFTEN E.V.: Uso de un agente modulador que actúa sobre un precursor de factor de crecimiento, que inhibe el tratamiento del precursor de factor de crecimiento, inhibiendo de esta […]
ANTICUERPO ANTI HER3 PARA EL DIAGNÓSTICO, PREVENCIÓN Y TRATAMIENTO DE ENFERMEDADES HIPERPROLIFERATIVAS, del 25 de Agosto de 2011, de MAX-PLANCK-GESELLSCHAFT ZUR FORDERUNG DER WISSENSCHAFTEN E.V.: Uso de un inhibidor de HER3 para la fabricación de un medicamento para el diagnóstico, prevención o tratamiento de una enfermedad hiperproliferativa […]
 ANTICUERPOS DE PAK FOSFOESPECÍFICOS Y KITS DE DIAGNÓSTICO, del 3 de Mayo de 2011, de SUGEN, INC.: Un procedimiento para seleccionar un mamífero susceptible al tratamiento con un modulador de la actividad de PAK4, que comprende: (i) determinar la relación […]
ANTICUERPOS DE PAK FOSFOESPECÍFICOS Y KITS DE DIAGNÓSTICO, del 3 de Mayo de 2011, de SUGEN, INC.: Un procedimiento para seleccionar un mamífero susceptible al tratamiento con un modulador de la actividad de PAK4, que comprende: (i) determinar la relación […]
 AMPLIFICACION PROTEOMICA DE PEQUEÑAS MOLECULAS QUE SE UNEN A PROTEINAS CELULARES DIANA, del 1 de Diciembre de 2010, de MAX-PLANCK-GESELLSCHAFT ZUR FORDERUNG DER WISSENSCHAFTEN E.V.: Procedimiento para evaluar la afinidad de unión de un componente diana de un analito a un compuesto que comprende (a) poner en contacto una primera alícuota […]
AMPLIFICACION PROTEOMICA DE PEQUEÑAS MOLECULAS QUE SE UNEN A PROTEINAS CELULARES DIANA, del 1 de Diciembre de 2010, de MAX-PLANCK-GESELLSCHAFT ZUR FORDERUNG DER WISSENSCHAFTEN E.V.: Procedimiento para evaluar la afinidad de unión de un componente diana de un analito a un compuesto que comprende (a) poner en contacto una primera alícuota […]
 METODOS PARA EL TRATAMIENTO DE TRASTORNOS PROLIFERATIVOS CELULARES, del 2 de Noviembre de 2010, de ONCOLYTICS BIOTECH, INC.: Un método para determinar la susceptibilidad de una célula a infección con reovirus midiendo la señalización constitutiva de ras-MAP en dicha […]
METODOS PARA EL TRATAMIENTO DE TRASTORNOS PROLIFERATIVOS CELULARES, del 2 de Noviembre de 2010, de ONCOLYTICS BIOTECH, INC.: Un método para determinar la susceptibilidad de una célula a infección con reovirus midiendo la señalización constitutiva de ras-MAP en dicha […]
Profármacos de gemcitabina, del 29 de Julio de 2020, de NuCana plc: Una formulación farmacéutica que comprende gemcitabina-[fenil-benzoxi-L-alaninil)]-(S)-fosfato 3: **(Ver fórmula)** o una sal o solvato […]