Polipéptido VKORC1 de reciclaje de la vitamina K-epóxido, una diana terapéutica de la cumarina y sus derivados.
Método para la gamma-carboxilación de un polipéptido dependiente de la vitamina K en una célula huésped que comprende introducir en dicha célula huésped un ácido nucleico que codifica VKORC1 de manera que el ácido nucleico que codifica VKORC1 se expresa recombinantemente en dicha célula,
donde el ácido nucleico que codifica VKORC1 codifica para:
a) una secuencia polipeptídica de VKORC1;
b) una secuencia polipeptídica de un alelo de la secuencia polipeptídica definida en a);
c) una secuencia polipeptídica de que tiene al menos un 90% de identidad con la secuencia polipeptídica definida en a) o b) donde la secuencia polipeptídica tiene actividad de VKORC1;
d) una secuencia polipeptídica de un fragmento de la secuencia polipeptídica definida en a), b) o c) que tiene actividad de VKORC1,
donde la expresión de dicho VKORC1 en dicha célula huésped aumenta la actividad basal de VKORC1 de dicha célula, donde el ácido nucleico comprende una secuencia de SEQ ID NO:2, SEQ ID NO:13, SEQ ID NO:18, SEQ ID NO:22, SEQ ID NO:26, SEQ ID NO:28, o una secuencia que tiene al menos una identidad del 90% con éstas y que codifica para una proteína de VKORC1 activa, y donde dicho método no es un método de tratamiento del cuerpo humano o animal mediante cirugía o terapia.
Tipo: Patente Europea. Resumen de patente/invención. Número de Solicitud: E10011278.
Solicitante: BAXTER INTERNATIONAL INC..
Nacionalidad solicitante: Estados Unidos de América.
Dirección: ONE BAXTER PARKWAY DEERFIELD, IL 60015 ESTADOS UNIDOS DE AMERICA.
Inventor/es: OLDENBURG,JOHANNES, MULLER-REIBLE,CLEMENS,R, FREGIN,ANDREAS, ROST,SIMONE, STROM,TIM-MATHHIAS.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A01K67/027 NECESIDADES CORRIENTES DE LA VIDA. › A01 AGRICULTURA; SILVICULTURA; CRIA; CAZA; CAPTURA; PESCA. › A01K CRÍA DE ANIMALES; AVICULTURA; APICULTURA; PISCICULTURA; PESCA; ANIMALES PARA CRIA O REPRODUCCIÓN, NO PREVISTOS EN OTRO LUGAR; NUEVAS VARIEDADES DE ANIMALES. › A01K 67/00 Cría u obtención de animales, no prevista en otro lugar; Nuevas razas de animales. › Nuevas razas de vertebrados.
- A01N43/16 A01 […] › A01N CONSERVACION DE CUERPOS HUMANOS O ANIMALES O DE VEGETALES O DE PARTES DE ELLOS (conservación de alimentos o productos alimenticios A23 ); BIOCIDAS, p. ej. EN TANTO QUE SEAN DESINFECTANTES, PESTICIDAS O HERBICIDAS (preparaciones de uso médico, dental o para el aseo que eliminan o previenen el crecimiento o la proliferación de organismos no deseados A61K ); PRODUCTOS QUE ATRAEN O REPELEN A LOS ANIMALES; REGULADORES DEL CRECIMIENTO DE LOS VEGETALES. › A01N 43/00 Biocidas, productos que atraen o repelen a los animales perjudiciales, o reguladores del crecimiento de los vegetales, que contienen compuestos heterocíclicos (que contienen anhídridos cíclicos, imidas cíclicas A01N 37/00; que contienen compuestos de fórmula , que no tienen más que un heterociclo en los que m≥1 y n≥0 y es una pirrolidina, una piperidina, una morfolina, una tiomorfolina, una piperazina o una polimetilenoimina, no sustituida o sustituida por un alcoilo, que tiene al menos cuatro grupos CH 2 A01N 33/00 - A01N 41/12; que contienen ácidos ciclopropanocarbhoxílicos o sus derivados, p. ej. ésteres con heterociclos, A01N 53/00). › con oxígeno como heteroátomo del ciclo.
- A61K38/44 A […] › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 38/00 Preparaciones medicinales que contienen péptidos (péptidos que contienen ciclos beta-lactama A61K 31/00; dipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina 2,5-dionas, A61K 31/00; péptidos basados en la ergolina A61K 31/48; que contienen compuestos macromoleculares que tienen unidades aminoácido repartidas estadísticamente A61K 31/74; preparaciones medicinales que contienen antígenos o anticuerpos A61K 39/00; preparaciones medicinales caracterizadas por los ingredientes no activos, p. ej. péptidos como soportes de fármacos, A61K 47/00). › Oxidoreductasas (1).
- C07H21/04 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07H AZUCARES; SUS DERIVADOS; NUCLEOSIDOS; NUCLEOTIDOS; ACIDOS NUCLEICOS (derivados de ácidos aldónicos o sacáricos C07C, C07D; ácidos aldónicos, ácidos sacáricos C07C 59/105, C07C 59/285; cianohidrinas C07C 255/16; glicales C07D; compuestos de constitución indeterminada C07G; polisacáridos, sus derivados C08B; ADN o ARN concerniente a la ingeniería genética, vectores, p. ej. plásmidos o su aislamiento, preparación o purificación C12N 15/00; industria del azúcar C13). › C07H 21/00 Compuestos que contienen al menos dos unidades mononucleótido que tienen cada una grupos fosfato o polifosfato distintos unidos a los radicales sacárido de los grupos nucleósido, p. ej. ácidos nucleicos. › con desoxirribosilo como radical sacárido.
- C07K16/40 C07 […] › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 16/00 Inmunoglobulinas, p. ej. anticuerpos mono o policlonales. › contra enzimas.
- C12N15/52 C […] › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 15/00 Técnicas de mutación o de ingeniería genética; ADN o ARN relacionado con la ingeniería genética, vectores, p. ej. plásmidos, o su aislamiento, su preparación o su purificación; Utilización de huéspedes para ello (mutantes o microorganismos modificados por ingeniería genética C12N 1/00, C12N 5/00, C12N 7/00; nuevas plantas en sí A01H; reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00; nuevas razas animales en sí A01K 67/00; utilización de preparaciones medicinales que contienen material genético que es introducido en células del cuerpo humano para tratar enfermedades genéticas, terapia génica A61K 48/00; péptidos en general C07K). › Genes que codifican enzimas o proenzimas.
- C12N5/06
- C12N5/10 C12N […] › C12N 5/00 Células no diferenciadas humanas, animales o vegetales, p. ej. líneas celulares; Tejidos; Su cultivo o conservación; Medios de cultivo para este fin (reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00). › Células modificadas por introducción de material genético extraño, p. ej. células transformadas por virus.
- C12N9/02 C12N […] › C12N 9/00 Enzimas, p. ej. ligasas (6.); Proenzimas; Composiciones que las contienen (preparaciones para la limpieza de los dientes que contienen enzimas A61K 8/66, A61Q 11/00; preparaciones de uso médico que contienen enzimas A61K 38/43; composiciones detergentes que contienen enzimas C11D ); Procesos para preparar, activar, inhibir, separar o purificar enzimas. › Oxidorreductasas (1.), p. ej. luciferasa.
- C12N9/04 C12N 9/00 […] › actúan sobre grupos CHOH como dadores, p. ej. glucosa oxidasa de glucosa, deshidrogenasa láctica (1.1).
- C12Q1/68 C12 […] › C12Q PROCESOS DE MEDIDA, INVESTIGACION O ANALISIS EN LOS QUE INTERVIENEN ENZIMAS, ÁCIDOS NUCLEICOS O MICROORGANISMOS (ensayos inmunológicos G01N 33/53 ); COMPOSICIONES O PAPELES REACTIVOS PARA ESTE FIN; PROCESOS PARA PREPARAR ESTAS COMPOSICIONES; PROCESOS DE CONTROL SENSIBLES A LAS CONDICIONES DEL MEDIO EN LOS PROCESOS MICROBIOLOGICOS O ENZIMOLOGICOS. › C12Q 1/00 Procesos de medida, investigación o análisis en los que intervienen enzimas, ácidos nucleicos o microorganismos (aparatos de medida, investigación o análisis con medios de medida o detección de las condiciones del medio, p. ej. contadores de colonias, C12M 1/34 ); Composiciones para este fin; Procesos para preparar estas composiciones. › en los que intervienen ácidos nucleicos.
- G01N33/50 FISICA. › G01 METROLOGIA; ENSAYOS. › G01N INVESTIGACION O ANALISIS DE MATERIALES POR DETERMINACION DE SUS PROPIEDADES QUIMICAS O FISICAS (procedimientos de medida, de investigación o de análisis diferentes de los ensayos inmunológicos, en los que intervienen enzimas o microorganismos C12M, C12Q). › G01N 33/00 Investigación o análisis de materiales por métodos específicos no cubiertos por los grupos G01N 1/00 - G01N 31/00. › Análisis químico de material biológico, p. ej. de sangre o de orina; Ensayos mediante métodos en los que interviene la formación de uniones bioespecíficas con grupos coordinadores; Ensayos inmunológicos (procedimientos de medida o ensayos diferentes de los procedimientos inmunológicos en los que intervienen enzimas o microorganismos, composiciones o papeles reactivos a este efecto, procedimientos para preparar estas composiciones, procedimientos de control sensibles a las condiciones del medio en los procedimientos microbiológicos o enzimáticos C12Q).
PDF original: ES-2515216_T3.pdf


Fragmento de la descripción:
Polipéptido VKORC1 de reciclaje de la vitamina K-epóxido, una diana terapéutica de la cumarina y sus derivados
Campo de la Invención La invención se refiere a un método para la gamma-carboxilación de un polipéptido dependiente de la vitamina K en una célula huésped, el cual comprende introducir en dicha célula huésped un ácido nucleico que codifica VKORC1 de manera que tal ácido nucleico que codifica VKORC1 se expresa de forma recombinante en dicha célula. Además, la presente invención se refiere al uso de una ácido nucleico recombinante de VKORC1 para la gamma-carboxilación de un polipéptido dependiente de la vitamina K en una célula huésped.
Antecedentes de la Invención La represión de la coagulación sanguínea prematura es la opción terapéutica seleccionada para el tratamiento agudo y la prevención a largo plazo de eventos trombóticos. De entre los anticoagulantes, las cumarinas se utilizan ampliamente para la prevención de la trombosis, por ejemplo en pacientes inmovilizados después de una cirugía, en pacientes con insuficiencia cardíaca crónica, en pacientes con enfermedad vascular ateroesclerótica, en pacientes con tumores malignos y en mujeres embarazadas. Además, las cumarinas son los anticoagulantes orales más utilizados para el tratamiento y la profilaxis de la trombosis [Suttie, 1987]. Las cumarinas son derivados típicos de 6-hidroxicumarina, por ejemplo 3- (actonilbencil) -4-hidroxicumarina (COUMADIN®) .
Las cumarinas tienen como objetivo la cascada de coagulación sanguínea indirectamente mediante la inhibición del ciclo de la vitamina K.
La vitamina K es un cofactor esencial para la activación post-traducción por la gamma-carboxilación de un grupo de proteínas reguladoras, las proteínas Gla. En diversas vías metabólicas, algunas proteínas clave necesitan una carboxilación para funcionar adecuadamente. La cascada de coagulación sanguínea es el ejemplo mejor estudiado. Aquí, los factores procoagulantes II, VII, IX y X, así como los factores anticoagulantes proteína C, proteína S, proteína Z, dependen de la gamma-carboxilación. Esta modificación post-traducción permite la fijación de las proteínas modificadas, en presencia de calcio, a las membranas fosfolipídicas bicapa, lo que representa una etapa esencial en la activación de la coagulación sanguínea [Sperling y col., 1978; Esmon y col., 1975]. Otras proteínas que requieren de la gamma-carboxilación son la proteína de matriz gla y la osteocalcina, ambas reguladoras del metabolismo óseo [Price, 1988] y "el gen específico de la inhibición del crecimiento", una proteína señal de transducción del ciclo celular [Manfioletti y col., 1993; Stitt y col., 1995].
Durante la gamma-carboxilación se introduce un grupo carboxilo en los residuos glutamato de las proteínas diana mediante la enzima gamma-glutamil carboxilasa (GGCX) en los microsomas del hígado [Furie & Furie, 1988; Suttie, 1987]. La reacción requiere como cofactor cantidades estequiométricas de vitamina K1hidroquinona reducida (vitamina K1H2) , que se oxida a vitamina K-2, 3-epóxido [Cain y col., 1997]. La regeneración del cofactor activo es mediada por un complejo multiproteína denominado vitamina K-2, 3-epóxido reductasa (VKOR) [Wallin & Martin, 1985]. El mismo complejo es el objetivo de los venenos de tipo cumarina utilizados en el control plaguicida de roedores. Este "ciclo de la vitamina K" se ha caracterizado bioquímicamente de forma detallada, pero los componentes moleculares no han sido purificados todavía hasta homogeneidad [Guenthner y col., 1981]. Además, la naturaleza molecular de la actividad de la cumarina y las moléculas que interactúan con las cumarinas siguen siendo imprecisas.
En general se aprecia en la técnica que, a pesar de su gran eficacia, existe diversas limitaciones al uso de las cumarinas. En primer lugar, algunos seres humanos son insensibles al tratamiento con cumarina. El término resistencia a la warfarina (WR) se utiliza para individuos que mantienen actividades normales del factor de coagulación a pesar de la anticoagulación oral con cumarinas (Acceso OMIM Nº 122700) . Se ha observado una transmisión autosómica dominante en varios linajes [O'Reilly y col., 1964; O'Reilly, 1970]. La deficiencia combinada de todos los factores de coagulación dependientes de la vitamina K (VKCFD) es un trastorno de sangrado muy raro en humanos con herencia autosómica recesiva, 14 casos descritos hasta la fecha [McMillan & Roberts, 1966; Fischer, 1966; Johnson y col., 1980; Goldsmith y col., 1982; Vicente y col., 1984; Ekelund y col., 1986; Pauli y col., 1987; Leonard, 1988; Pechlaner y col., 1992; Boneh & Bar-Ziv, 1996; Brenner y col., 1998; Spronk y col., 2000; Oldenburg y col, 2000]. Los síntomas clínicos de la enfermedad incluyen episodios de hemorragias intracerebrales perinatales, a veces con resultado fatal. Habitualmente, la tendencia al sangrado se invierte por completo mediante la administración oral de vitamina K. Los síntomas adicionales en recién nacidos se asemejan a la embriopatía por warfarina con hipoplasia falangiana basal y distal y calcificación prematura de la epífisis [Pauli y col., 1987]. La enfermedad puede resultar de una resorción/transporte defectuoso de la vitamina K al hígado [Prentice, 1985] o de mutaciones en uno de los genes implicados en la gammacarboxilación. En el subtipo 1 (VKCFD1, OMIM # 277450) , las mutaciones en el gen GGCX sobre el cromosoma 2p12 resultan en una carboxilación insuficiente de los factores de coagulación [Brenner y col., 1998; Spronk y col., 2000]. Se ha descrito una conexión de dos familias con la deficiencia múltiple familiar del factor de coagulación (FMFD, ahora renombrado: VKCFD2, OMIM # 607473) a un intervalo de 20 Mb de la región pericéntrica del cromosoma 16p12-q21 [Fregin y col., 2002]. Los pacientes con VKCFD2 mostraron niveles de suero con un notable aumento de vitamina K-epóxido, sugiriendo así un defecto en una de las subunidades del complejo VKOR. En su conjunto, es evidente que existen pacientes que presentan resistencia a la warfarina. Como consecuencia, existe la necesidad de identificar nuevos derivados de cumarinas que sean anticoagulantes eficaces para tratar a estos pacientes, así como métodos para identificar estos derivados de la cumarina.
El uso de cumarinas se asocia con un riesgo de sangrado espontáneo, con un índice de mortalidad significativo. Además, la predicción de la dosis exacta de mantenimiento de la cumarina es difícil. En ausencia de la molécula diana sobre la que la cumarina ejerce un efecto, el régimen de tratamiento debe establecerse en base a cada paciente. Mientras el régimen óptimo no se ha establecido todavía, el paciente tiene un mayor riesgo de trombogénesis o de sangrado. Por tanto, es necesario un método para determinar el régimen óptimo de tratamiento lo más rápido y seguro posible. Además, el establecimiento de un régimen de tratamiento óptimo se complica por el hecho de que existe un retraso considerable entre la administración de las cumarinas y el desencadenamiento de su actividad anticoagulante. Dada la acción retardada de la cumarina y considerando el hecho de que la cumarina tiende a acumularse con el tiempo, existe la necesidad de derivados de cumarina que permitan la coagulación sanguínea de forma más rápida que las cumarinas conocidas en la técnica. De la misma manera, existe también la necesidad de cumarinas que se metabolicen más rápidamente, de forma que se pueda impedir o mejorar la acumulación de cumarina y, consecuentemente, reducir o suprimir el riesgo de sobredosis.
Se entenderá que cuando el tratamiento con cumarina se inicia durante un estado trombótico, los niveles de proteína C y S disminuyen, creando así temporalmente un potencial trombogénico que normalmente es compensado superponiendo la administración de heparina y cumarina durante varios días. De nuevo, se necesita identificar la diana molecular de acción de la cumarina con el fin de poder buscar nuevos derivados de cumarina que no tengan estas limitaciones o al menos las tengan en menor medida.
A menudo, la terapia con cumarina provoca necrosis de la piel en el paciente y, cuando se aplica durante el embarazo, puede causar embriopatía, creando la necesidad de nuevos derivados de cumarina que no provoquen estos efectos.
Existen diversas interacciones entre los medicamentos y las cumarinas. Algunos de estos medicamentos, como el Fenobarbital, inducen niveles plasmáticos más bajos de las cumarinas debido a la mayor metabolización de la cumarina, que se piensa se debe a las oxidasas de función mixta, como las oxidasas de función mixta citocromo P450. Dicha interacción es de importancia clínica cuando se ha determinado el régimen apropiado, por ejemplo Fenobarbital... [Seguir leyendo]
Reivindicaciones:
1. Método para la gamma-carboxilación de un polipéptido dependiente de la vitamina K en una célula huésped que comprende introducir en dicha célula huésped un ácido nucleico que codifica VKORC1 de manera que el ácido nucleico que codifica VKORC1 se expresa recombinantemente en dicha célula, donde el ácido nucleico que codifica VKORC1 codifica para:
a) una secuencia polipeptídica de VKORC1; b) una secuencia polipeptídica de un alelo de la secuencia polipeptídica definida en a) ; c) una secuencia polipeptídica de que tiene al menos un 90% de identidad con la secuencia polipeptídica
definida en a) o b) donde la secuencia polipeptídica tiene actividad de VKORC1;
d) una secuencia polipeptídica de un fragmento de la secuencia polipeptídica definida en a) , b) o c) que tiene actividad de VKORC1,
donde la expresión de dicho VKORC1 en dicha célula huésped aumenta la actividad basal de VKORC1 de dicha célula, donde el ácido nucleico comprende una secuencia de SEQ ID NO:2, SEQ ID NO:13, SEQ ID NO:18, SEQ ID NO:22, SEQ ID NO:26, SEQ ID NO:28, o una secuencia que tiene al menos una identidad del 90% con éstas y que codifica para una proteína de VKORC1 activa, y donde dicho método no es un método de tratamiento del cuerpo humano o animal mediante cirugía o terapia.
2. Método según la reivindicación 1, caracterizado porque la citada proteína dependiente de la vitamina K se selecciona de entre el grupo consistente en factores de coagulación sanguínea II, VII, IX, X, proteína C, proteína S, proteína Z, proteína de matriz gla y osteocalcina.
3. Método según la reivindicación 1, caracterizado porque dicho ácido nucleico que codifica VKORC1 se expresa en combinación con un ácido nucleico que codifica para la gamma-glutamil-carboxilasa.
4. Método según la reivindicación 1, caracterizado porque las células que expresan dicho VKORC1 tienen una actividad basal incrementada en aproximadamente un 15% o más en comparación con la actividad basal de VKORC1 de dicha célula en ausencia de la expresión recombinante del VKORC1 en la célula huésped.
5. Uso de un ácido nucleico recombinante de VKORC1 que codifica una secuencia polipeptídica seleccionada de entre el grupo consistente en:
a) una secuencia polipeptídica de VKORC1; b) una secuencia polipeptídica de un alelo de la secuencia polipeptídica definida en a) ; c) una secuencia polipeptídica que tiene al menos un 90% de identidad con la secuencia polipeptídica
definida en a) o b) , donde la secuencia polipeptídica tiene actividad de VKORC1;
d) una secuencia polipeptídica de un fragmento de la secuencia polipeptídica definida en a) , b) o c) que tiene actividad de VKORC1,
para la gamma-carboxilación de un polipéptido dependiente de la vitamina K en una célula huésped, donde la expresión de dicho VKORC1 en dicha célula huésped aumenta la actividad basal de VKORC1, donde el ácido nucleico comprende una secuencia de SEQ ID NO:2, SEQ ID NO:13, SEQ ID NO:18, SEQ ID NO:22, SEQ ID NO:26, SEQ ID NO:28, o una secuencia que tiene al menos una identidad del 90% con éstas y que codifica una proteína de VKORC1 activa, y donde dicho uso no es un uso para el tratamiento del cuerpo humano o animal mediante cirugía o terapia.
6. Uso según la reivindicación 5, caracterizado porque el citado polipéptido dependiente de la vitamina K se selecciona de entre el grupo consistente en factores de coagulación sanguínea II, VII, IX, X, proteína C, proteína S, proteína Z, proteína de matriz gla y osteocalcina.
7. Uso según la reivindicación 5, caracterizado porque dicho ácido nucleico de VKORC1 se utiliza en combinación con un ácido nucleico que codifica para la gamma-glutamil-carboxilasa.
8. Uso según la reivindicación 5, caracterizado porque dichas células que expresan dicho VKORC1 tienen una actividad basal incrementada en aproximadamente un 15% o más en comparación con la actividad basal de VKORC1 de dicha célula en ausencia de la expresión recombinante del VKORC1 en la célula huésped.
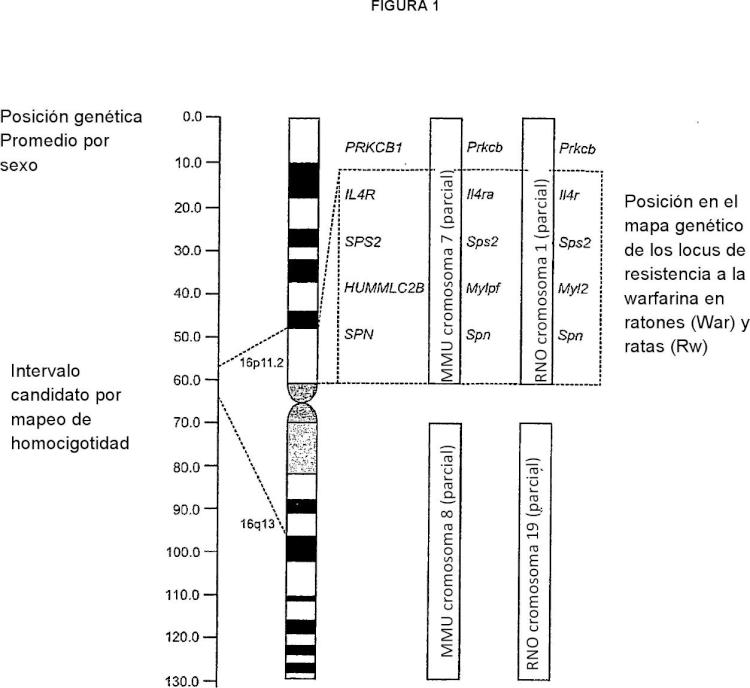
FIGURA 1
Posición genética Promedio por sexo Intervalo candidato por
mapeo de homocigotidad
MMU cromosoma 8 (parcial) MMU cromosoma 7 (parcial)
RNO cromosoma 19 (parcial)
RNO cromosoma 1 (parcial)
Posición en el mapa genético de los locus de resistencia a la warfarina en ratones (War) y ratas (Rw)
FIGURA 2 FIGURA 3 FIGURA 4
CorazónCerebroPlacentaPulmónHígadoMúsculo esqueletalRiñónPáncreas
CerebroCorazónRiñónHígadoPulmón FIGURA 5
superpuesto superpuesto superpuesto FIGURA 6
FIGURA 7
Localizaciones de las dianas de ARNsi en la secuencias de codificación de la subunidad 1 del complejo vitamina K-epóxido reductasa de Homo sapiens (Hs_VKORC1)
FIGURA 9
TABLA DE SECUENCIAS
SEQ ID NO: Nombre Especie
1 Secuencia proteica de la subunidad 1 del complejo vitamina K-epóxido reductasa (Hs_VKORC1) Homo sapiens
2 Secuencia de codificación de la subunidad 1 del complejo vitamina K-epóxido reductasa de Homo sapiens (Hs_VKORC1) Homo sapiens
3 Factor de coagulación dependiente de la vitamina K, de tipo 2 (VKCFD2) -mutación (292C>T; R98W) de la secuencia Hs_VKORC1 Homo sapiens
4 Resistencia a warfarina (WR) -secuencia 1 de mutación (85G>T; V29L) de la secuencia de Hs_VKORC1 Homo sapiens
5 Resistencia a warfarina (WR) -secuencia 2 de mutación (134T>C; V45A) de la secuencia de Hs_VKORC1 Homo sapiens
6 Resistencia a warfarina (WR) -secuencia 3 de mutación (172A>G; R58G) de la secuencia de Hs_VKORC1 Homo sapiens
7 Resistencia a warfarina (WR) -secuencia 4 de mutación (383T>G; L128R) de la secuencia de Hs_VKORC1 Homo sapiens
8 Polimorfismo de nucleótido único (SNP) 1 (129C>T, C43C) de la secuencia de la subunidad 1 del complejo vitamina K-epóxido reductasa de Homo sapiens (Hs_VKORC1) Homo sapiens
9 SNP 2 (358C>T, L120L) de la secuencia de la subunidad 1 del complejo vitamina K-epóxido reductasa de Homo sapiens (Hs_VKORC1) Homo sapiens
10 Secuencia proteica de la proteína 1 de tipo VKORC1 de Homo sapiens (Hs_VKORC1L1) Homo sapiens
11 Secuencia de codificación de la proteína 1 de tipo VKORC1 de Homo sapiens (Hs_VKORC1L1) Homo sapiens
12 Secuencia proteica de la subunidad 1 del complejo vitamina K-epóxido reductasa de Rattus norvegicus (Rn_VKORC1) Rattus norvegicus
13 Secuencia de codificación de la subunidad 1 del complejo vitamina K-epóxido reductasa de Rattus norvegicus (Rn_VKORC1) Rattus norvegicus
14 Resistencia a warfarina de la rata (Rw) -secuencia de mutación (416A>G; Y139C) de la secuencia de Rn_VKORC1 Rattus norvegicus
15 Secuencia proteica de la proteína 1 de tipo VKORC1 de Rattus norvegicus (Rn_VKORC1L1) Rattus norvegicus
16 Secuencia de codificación de la proteína 1 de tipo VKORC1 de Rattus norvegicus (Rn_VKORC1L1) Rattus norvegicus
17 Secuencia proteica de la subunidad 1 del complejo vitamina K-epóxido reductasa de Mus musculus (Mm_VKORC1) Mus musculus
18 Secuencia de codificación de la subunidad 1 del complejo vitamina K-epóxido reductasa de Mus musculus (Mm_VKORC1) Mus musculus
19 Secuencia proteica de la proteína 1 de tipo VKORC1 de Mus musculus (Mm_VKORC1L1) Mus musculus
20 Secuencia de codificación de la proteína 1 de tipo VKORC1 de Mus musculus (Mm_VKORC1L1) Mus musculus
21 Secuencia proteica de la subunidad 1 del complejo de vitamina K-epóxido reductasa de Fugu rubripes (Fr_VKORC1) Fugu rubripes
22 Secuencia de codificación de la subunidad 1 del complejo de vitamina K-epóxido reductasa de Fugu rubripes (Fr_VKORC1) Fugu rubripes
23 Secuencia proteica de la proteína 1 de tipo VKORC1 de Fugu rubripes (Fr_VKORC1L1) Fugu rubripes
24 Secuencia de codificación de la proteína 1 de tipo VKORC1 de Fugu rubripes (Fr_VKORC1L1) Fugu rubripes
25 Secuencia proteica de la subunidad 1 del complejo de vitamina K-epóxido reductasa de Xenopus laevis (XI_VKORC1) Xenopus laevis
26 Secuencia de codificación de la subunidad 1 del complejo de vitamina K-epóxido reductasa de Xenopus laevis (XI_VKORC1) Xenopus laevis
27 Secuencia proteica de la subunidad 1 del complejo de vitamina K-epóxido reductasa de Anopheles gambiae (Ag_VKORC1L1) Anopheles gambiae
28 Secuencia de codificación de la subunidad 1 del complejo de vitamina K-epóxido reductasa de Anopheles gambiae (Ag_VKORC1L1) Anopheles gambiae
29 Secuencia 1 de ARNsi de la subunidad 1 del complejo de vitamina K-epóxido reductasa de Homo sapiens (Hs_VKORC1)
30 Secuencia 2 de ARNsi de la subunidad 1 del complejo de vitamina K-epóxido reductasa de Homo sapiens (Hs_VKORC1)
31 Cebador 1 aguas abajo para la secuencia de ARNsi de la subunidad 1 del complejo de vitamina K-epóxido reductasa de Homo sapiens (Hs_VKORC1)
32 Cebador 2 aguas abajo para la secuencia de ARNsi de la subunidad 1 del complejo de vitamina K-epóxido reductasa de Homo sapiens (Hs_VKORC1)
33 Secuencia 3 de ARNsi de la subunidad 1 del complejo de vitamina K-epóxido reductasa de Homo sapiens (Hs_VKORC1)
34 Secuencia 4 de ARNsi de la subunidad 1 del complejo de vitamina K-epóxido reductasa de Homo sapiens (Hs_VKORC1)
35 Cebador 3 aguas abajo para la secuencia de ARNsi de la subunidad 1 del complejo de vitamina K-epóxido reductasa de Homo sapiens (Hs_VKORC1)
36 Cebador 4 aguas abajo para la secuencia de ARNsi de la subunidad 1 del complejo de vitamina K-epóxido reductasa de Homo sapiens (Hs_VKORC1)
37 Secuencia 5 de ARNsi de la subunidad 1 del complejo de vitamina K-epóxido reductasa de Homo sapiens (Hs_VKORC1)
38 Secuencia 6 de ARNsi de la subunidad 1 del complejo de vitamina K-epóxido reductasa de Homo sapiens (Hs_VKORC1)
39 Cebador 5 aguas abajo para la secuencia de ARNsi de la subunidad 1 del complejo de vitamina K-epóxido reductasa de Homo sapiens (Hs_VKORC1)
40 Cebador 6 aguas abajo para la secuencia de ARNsi de la subunidad 1 del complejo de vitamina K-epóxido reductasa de Homo sapiens (Hs_VKORC1)
41 Secuencia 7 de ARNsi de la subunidad 1 del complejo de vitamina K-epóxido reductasa de Homo sapiens (Hs_VKORC1)
42 Secuencia 8 de ARNsi de la subunidad 1 del complejo de vitamina K-epóxido reductasa de Homo sapiens (Hs_VKORC1)
43 Cebador 7 aguas abajo para la secuencia de ARNsi de la subunidad 1 del complejo de vitamina K-epóxido reductasa de Homo sapiens (Hs_VKORC1)
44 Cebador 8 aguas abajo para la secuencia de ARNsi de la subunidad 1 del complejo de vitamina K-epóxido reductasa de Homo sapiens (Hs_VKORC1)
45 Secuencia 9 de ARNsi de la subunidad 1 del complejo de vitamina K-epóxido reductasa de Homo sapiens (Hs_VKORC1)
46 Secuencia 10 de ARNsi de la subunidad 1 del complejo de vitamina K-epóxido reductasa de Homo sapiens (Hs_VKORC1)
47 Cebador 9 aguas abajo para la secuencia de ARNsi de la subunidad 1 del complejo de vitamina K-epóxido reductasa de Homo sapiens (Hs_VKORC1)
48 Cebador 10 aguas abajo para la secuencia de ARNsi de la subunidad 1 del complejo de vitamina K-epóxido reductasa de Homo sapiens (Hs_VKORC1)
49 Secuencia 11 de ARNsi de la subunidad 1 del complejo de vitamina K-epóxido reductasa de Homo sapiens (Hs_VKORC1)
50 Secuencia 12 de ARNsi de la subunidad 1 del complejo de vitamina K-epóxido reductasa de Homo sapiens (Hs_VKORC1)
51 Cebador 11 aguas abajo para la secuencia de ARNsi de la subunidad 1 del complejo de vitamina K-epóxido reductasa de Homo sapiens (Hs_VKORC1)
52 Cebador 12 aguas abajo para la secuencia de ARNsi de la subunidad 1 del complejo de vitamina K-epóxido reductasa de Homo sapiens (Hs_VKORC1)
53 Cebador para PCR para la amplificación de la secuencia de codificación completa de la subunidad 1 del complejo de vitamina K-epóxido reductasa de Homo sapiens (VKORC1-HindIII-F)
54 Cebador para PCR para la amplificación de la secuencia de codificación completa de la subunidad 1 del complejo de vitamina K-epóxido reductasa de Homo sapiens (VKORC1-HindIII-F)
55 Cebador para PCR para la amplificación de la secuencia de Homo sapiens Hs_VKORC1-Ex1-F
56 Cebador para PCR para la amplificación de la secuencia de Homo sapiens Hs_VKORC1-Ex1-R
57 Cebador para PCR para la amplificación de la secuencia de Homo sapiens Hs_VKORC1-Ex2-F
58 Cebador para PCR para la amplificación de la secuencia de Homo sapiens Hs_VKORC1-Ex2-R
59 Cebador para PCR para la amplificación de la secuencia de Homo sapiens Hs_VKORC1-Ex3-F
60 Cebador para PCR para la amplificación de la secuencia de Homo sapiens Hs_VKORC1-Ex3-R
61 Cebador para PCR para la amplificación de la secuencia de Homo sapiens Hs_VKORC1-ADNc-F
62 Cebador para PCR para la amplificación de la secuencia de Homo sapiens Hs_VKORC1-ADNc-R
63 Cebador para PCR para la amplificación de la secuencia de Rattus norvegicus Rn_VKORC1-ADNc-F
64 Cebador para PCR para la amplificación de la secuencia de Rattus norvegicus Rn_VKORC1-ADNc-R
65 Cebador para PCR para la amplificación de la secuencia de Rattus norvegicus Rn_VKORC1-ADNc-F-nes
66 Cebador para PCR para la amplificación de la secuencia de Rattus norvegicus Rn_VKORC1-ADNc-R-nes
67 Cebador para PCR para la amplificación de la secuencia de Fugu rubripes Fr_VKORC1-ADNc-F
68 Cebador para PCR para la amplificación de la secuencia de Fugu rubripes Fr_VKORC1-ADNc-R
69 Cebador para PCR para la amplificación de la secuencia de Fugu rubripes Fr_VKORC1-ADNc-F-nes
70 Cebador para PCR para la amplificación de la secuencia de Fugu rubripes Fr_VKORC1-ADNc-R-nes
71 Cebador para PCR para la amplificación de la secuencia de Homo sapiens Hs_VKORC1L1-ADNc-F
72 Cebador para PCR para la amplificación de la secuencia de Homo sapiens Hs_VKORC1L1-ADNc-R
73 Cebador para PCR para la amplificación de la secuencia de Homo sapiens Hs_VKORC1L1-ADNc-F-nes
74 Cebador para PCR para la amplificación de la secuencia de Homo sapiens Hs_VKORC1L1-ADNc-R-nes
75 Cebador para PCR para la amplificación de la secuencia de Fugu rubripes Fr_VKORC1L1-ADNc-F
76 Cebador para PCR para la amplificación de la secuencia de Fugu rubripes Fr_VKORC1L1-ADNc-R
77 Cebador para PCR para la amplificación de la secuencia de Fugu rubripes Fr_VKORC1L1-ADNc-F-nes
78 Cebador para PCR para la amplificación de la secuencia de Fugu rubripes Fr_VKORC1L1-ADNc-R-nes
79 Cebador para PCR para la amplificación de la secuencia de Rattus norvegicus Rn_VKORC1L1-ADNc-F
80 Cebador para PCR para la amplificación de la secuencia de Rattus norvegicus Rn_VKORC1L1-ADNc-R
81 Cebador para PCR para la amplificación de la secuencia de Rattus norvegicus Rn_VKORC1L1-ADNc-F-nes
82 Cebador para PCR para la amplificación de la secuencia de Rattus norvegicus Rn_VKORC1L1-ADNc-R-nes
83 Cebador para PCR para la amplificación de la secuencia de Rattus norvegicus Rn_VKORC1L1-ADNc-R-corto
84 Cebador para PCR para la amplificación de la secuencia de Mus musculus Mm_VKORC1L1-ADNc-F
85 Cebador para PCR para la amplificación de la secuencia de Mus musculus Mm_VKORC1L1-ADNc-R
86 Cebador para PCR para la amplificación de la secuencia de Mus musculus Mm_VKORC1L1-ADNc-F-nes
87 Cebador para PCR para la amplificación de la secuencia de Mus musculus Mm_VKORC1L1-ADNc-R-nes
88 Cebador para PCR para rVKORC1-outerF
89 Cebador para PCR para rVKORC1-outerR
90 Cebador para PCR para rVKORC1-innerF
91 Cebador para PCR para rVKORC1-innerR
92 Cebador para PCR para VKORC1-pcdna3-F
93 Cebador para PCR para VKORC1-pcdna3-R
94 VKORC1 de Homo sapiens con mutación 416A>G de resistencia a warfarina en rata
FIGURA 10
Actividades1de VKOR de células HEK293 transfectadas con constructos de ADNc de VKORC1
Warfarina [μM] FIGURA 11
Secuencia de aminoácidos del polipéptido de reciclaje de vitamina K-epóxido de Homo sapiens
(HS_VKORC1; SEQ ID NO:1) FIGURA 12
Secuencia de codificación de ácido nucleico del polipéptido de reciclaje de vitamina K-epóxido de Homo sapiens (HS_VKORC1; SEQ ID NO:2) FIGURA 13
Detección de la mutación Y139C (416A>G) de resistencia a warfarina del gen VKORC1 en el genoma de Rattus norvegicus por ARMS-PCR
Patentes similares o relacionadas:
Método y medios para purificar vectores retrovíricos, del 29 de Julio de 2020, de Autolus Limited: Una célula productora de retrovirus que expresa una proteína de marcaje en la superficie celular, de tal manera que los vectores retrovíricos producidos por la célula se […]
Biblioteca de péptidos y su uso, del 8 de Julio de 2020, de DAIICHI SANKYO COMPANY, LIMITED: Una biblioteca de péptidos que comprende una pluralidad de péptidos diferentes en la que los péptidos comprenden cada uno una secuencia de aminoácidos […]
Marcador de células endoteliales corneales, del 17 de Junio de 2020, de OSAKA UNIVERSITY: Método para producir una célula endotelial corneal, comprendiendo el método la etapa de clasificar, a partir de una población celular que comprende una célula […]
Vectores de AAV dirigidos a oligodendrocitos, del 10 de Junio de 2020, de THE UNIVERSITY OF NORTH CAROLINA AT CHAPEL HILL: Un ácido nucleico que codifica una cápside de AAV, comprendiendo el ácido nucleico una secuencia codificante de la cápside de AAV que es al menos el 96 % idéntica […]
Anticuerpo contra péptido codificado por exón-21 de periostina y composición farmacéutica para prevenir o tratar enfermedades asociadas a inflamación que contienen el mismo, del 6 de Mayo de 2020, de OSAKA UNIVERSITY: Anticuerpo que se une a uno o más péptidos seleccionados del grupo que consiste en un péptido codificado por el exón-21 de periostina que […]
Reconocimiento de unión a diana celular mediante un agente bioactivo usando transferencia de energía de resonancia de bioluminiscencia intracelular, del 6 de Mayo de 2020, de PROMEGA CORPORATION: Un sistema de ensayo que comprende: (a) una biblioteca de agentes bioactivos, cada uno de los cuales está fijado a un fluoróforo; (b) una diana celular fusionada a […]
Combinación de dos elementos genéticos para el control del desarrollo del tipo floral de una planta dicotiledónea, y utilización en procedimientos de detección y selección, del 1 de Abril de 2020, de Institut national de recherche pour l'agriculture, l'alimentation et l'environnement: Utilización de una combinación de dos elementos genéticos para el control del desarrollo del tipo floral de una planta dicotiledónea, comprendiendo dicha combinación, respectivamente: […]
Producción de proteínas en medios de cultivo celular libres de glutamina, del 25 de Marzo de 2020, de F. HOFFMANN-LA ROCHE AG: Un procedimiento para producir un polipéptido en una célula huésped de mamífero que expresa dicho polipéptido, que comprende cultivar la célula […]