Perturbación genética homocigota aleatoria para mejorar la producción de anticuerpos.
Un método para aumentar la tasa de productividad específica de la expresión de un anticuerpo en una línea celular de mamífero que expresa un anticuerpo de interés,
que comprende:
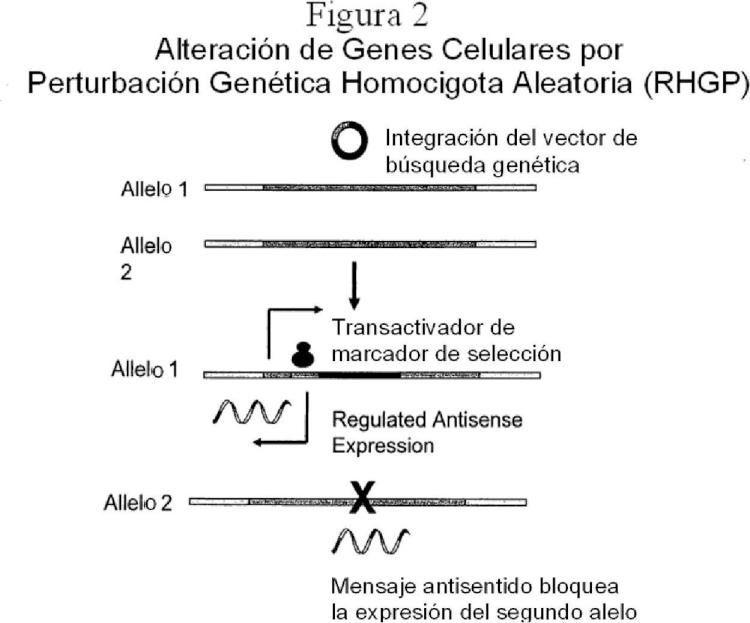
alterar el patrón de expresión de al menos un gen del genoma de dicha línea celular distinto de dicho anticuerpo por medio de perturbación genética homocigota aleatoria (RHGP) por inserción de un vector de búsqueda genética (GSV) en el genoma de dicha línea celular, cuyo GSV al integrarse, o aumentará o disminuirá el nivel de expresión de dicho gen,
explorar las células de dicha línea celular transformada por RHGP para identificar las células transformadas que presentan una tasa de productividad específica (SPR) más alta para el anticuerpo de interés en comparación con los miembros de la misma línea celular no transformada por RHGP,
cultivar dichas células que presentan una SPR más alta para obtener una población de células que expresan dicho anticuerpo de interés con una SPR aumentada en comparación con dicha línea celular cuando no se aumenta por RHGP.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2007/082972.
Solicitante: ELI LILLY AND COMPANY.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: LILLY CORPORATE CENTER INDIANAPOLIS, IN 46285 ESTADOS UNIDOS DE AMERICA.
Inventor/es: GOLDBLATT, MICHAEL, DUAN, ROXANNE.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C07K16/00 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › Inmunoglobulinas, p. ej. anticuerpos mono o policlonales.
- C12N15/10 C […] › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 15/00 Técnicas de mutación o de ingeniería genética; ADN o ARN relacionado con la ingeniería genética, vectores, p. ej. plásmidos, o su aislamiento, su preparación o su purificación; Utilización de huéspedes para ello (mutantes o microorganismos modificados por ingeniería genética C12N 1/00, C12N 5/00, C12N 7/00; nuevas plantas en sí A01H; reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00; nuevas razas animales en sí A01K 67/00; utilización de preparaciones medicinales que contienen material genético que es introducido en células del cuerpo humano para tratar enfermedades genéticas, terapia génica A61K 48/00; péptidos en general C07K). › Procedimientos para el aislamiento, la preparación o la purificación de ADN o ARN (preparación química de ADN o ARN C07H 21/00; preparación de polinucleótidos no estructurales a partir de microorganismos o con la ayuda de enzimas C12P 19/34).
- C12N15/63 C12N 15/00 […] › Introducción de material genético extraño utilizando vectores; Vectores; Utilización de huéspedes para ello; Regulación de la expresión.
- C12P21/00 C12 […] › C12P PROCESOS DE FERMENTACION O PROCESOS QUE UTILIZAN ENZIMAS PARA LA SINTESIS DE UN COMPUESTO QUIMICO DADO O DE UNA COMPOSICION DADA, O PARA LA SEPARACION DE ISOMEROS OPTICOS A PARTIR DE UNA MEZCLA RACEMICA. › Preparación de péptidos o de proteínas (proteína monocelular C12N 1/00).
PDF original: ES-2548522_T3.pdf
Fragmento de la descripción:
Perturbación genética homocigota aleatoria para mejorar la producción de anticuerpos
Antecedentes
Campo de la técnica
La presente invención se refiere a métodos de alteración de células para mejorar la producción de proteínas, que se han cultivado para expresarlas. Particularmente, esta invención se dirige al uso de la Perturbación Genética Homocigota Aleatoria para mejorar la expresión de anticuerpos en un huésped que expresa anticuerpos, por la Inserción dirigida de ADN o bien para deprimir la expresión endógena de una proteína huésped, o para mejorar la expresión de una proteína huésped que se expresa escasamente, estando relacionado el cambio en la expresión con un aumento de la expresión del anticuerpo que se expresa por la célula huésped.
Antecedentes de la tecnología
Los anticuerpos, particularmente los anticuerpos monoclonales, han llegado a ser productos biológicos importantes tanto en el arsenal de la humanidad contra la enfermedad, como en la investigación y desarrollo, Aunque no son una "bala mágica" como se creyó una vez, se han aprobado más de una veintena de anticuerpos monoclonales, a veces denominados mAb, para su uso terapéutico. Solo unos pocos de estos incluyen el anticuerpo Trastuzumab, el principio activo del Herceptin® aprobado para el tratamiento de algunos cánceres de mama, Palivizumab, el mAb del Synagis® aprobado para la prevención/tratamiento del RSV, y Bevacizumab, un mAb presente en Avastin®, aprobado para el tratamiento del cáncer colorrectal, e indicado como eficaz en el tratamiento de otras afecciones. Se conocen muchos más.
Por el contrario, hay literalmente cientos de anticuerpos, mAb y policlonales, que se emplean como caballos de batalla en los laboratorios e Instalaciones de investigación por todo el mundo. Los anticuerpos son útiles como agentes de diagnóstico, como agentes para unirse y aislar moléculas diana, para diferenciar células para su ensayo, y otros usos que se aprovechan de las propiedades de unión específica de las IgG para seleccionar un antígeno único, típicamente una molécula biológica, unida o no unida, que puede ser de interés. La producción de anticuerpos es un asunto fundamental.
Los métodos de producción de anticuerpos están bien establecidos, aunque se añaden refinamientos constantemente. La información básica se expuso ya en 1975, Kohler& Mllsteln, Nature, 256: 495 -497 (1975). Para preparar anticuerpos monoclonales, un huésped, típicamente un conejo o similar, se Inyecta con el antígeno contra el que se busca un mAb. A continuación de la inmunización, se extraen el bazo, y posiblemente los ganglios linfáticos del huésped y se separan en células únicas. Estas células se exponen al antígeno diana. Las células que expresan el mAb deseado en su superficie se unirán al antígeno inmovilizado. Estas células se cultivan y se dejan crecer, y se fusionan con células de mieloma o con otras células inmortales para formar un hlbrldoma, que se puede cultivar para recuperar el anticuerpo que se expresa.
La mayoría de los anticuerpos, y virtualmente todos los anticuerpos terapéuticos, tienen que modificarse para evitar la inducción de una reacción de rechazo en un paciente. El ADN que codifica el anticuerpo que expresa el hibridoma se aísla, y se puede modificar por la inserción o eliminación de bases, perfiles de glicosilación alterados, y modificación de las regiones de estructura y regiones determinantes de complementariedad, que afectan a la afinidad y avidez con la que el anticuerpo se une a su antígeno diana. Los anticuerpos resultantes son humanizados o "humanos" o modificados de otra manera (los anticuerpos quiméricos y los revestidos son comunes en la técnica). El estado de la técnica desde 1995 se refleja en la Patente de EE. UU 6.054.561.
Una vez preparado y aislado, el ADN que codifica el anticuerpo se puede transferir a una línea celular de mamífero preferida para le expresión en cantidades de comerciales o "producción". Hace mucho que se reconoce que las células de ovario de hámster chino (células CHO) son excelentes vehículos de expresión para ADN recombinante o no endógeno. Véase la Patente de EE. UU. 4.816.567. Donde se ha desarrollado una serie de cepas de células CHO deficientes en DHFR, que permiten la amplificación de ADN insertado que codifica proteínas específicas o secuencias de ADN como se expone en la Patente de EE. UU. 5.981.214. Esta última patente describe el uso de recombinación homologa con un gen específico o región de expresión de una célula - en el caso en cuestión, para inducir la expresión de un gen heterólogo. Otras líneas celulares adecuadas incluyen las células 293HEK, células HeLa, células COS, células NIH3T3, células Jurkat, células NS0 y células HUVEC. Otras líneas celulares de mamífero adecuadas para la expresión de proteínas recombinantes se han identificado en la bibliografía, y son Igualmente adecuadas para su uso en la invención de esta solicitud.
Una vez estabilizados, los métodos actuales para aumentar la producción de anticuerpos valiosos, tienden a enfocarse en el aumento de la productividad total, es decir, una alta productividad volumétrica, ya que una cantidad determinada de células produce una cantidad determinada de anticuerpos. Estos métodos tienden a enfocarse en la mejora de los métodos y ambientes que se utilizan para cultivar las células, para mejorar la producción total de
anticuerpos. En general, se necesita una producción de anticuerpos mayor de aproximadamente 1 g/l para ser un proceso ¡ndustrialmente competitivo. Las células CHO individuales expresan típicamente un intervalo de 10-15 pg/célula/día.
La recombinación homologa se ha utilizado en muchos contextos desde 1985. Originalmente se empleaba como una herramienta de "anulación", permitiendo la supresión de un gen expresado, para estudiar la respuesta de la célula que se modificaba. Se desarrollaron procedimientos posteriormente para permitir el silenciamiento de los genes diana. El uso de construcciones de anulación anti-sentido utilizando un método de anulación homocigoto aleatorio (RHKO) se describe, por ejemplo, en L¡ et al, Cell 85: 319 - 329 (1996). En la Publicación de Patente de EE. UU. 20060240021 (Solicitud de Patente de EE. UU. 10/524426, presentada el 18 de agosto de 2003) se desvela el uso de técnicas RHKO para identificar los genes implicados en la resistencia a rapamicina. La capacidad para insertar una construcción en un alelo, identificar las células en las que ese alelo se ha modificado satisfactoriamente por búsqueda rápida de producción, tal como por ejemplo por FACS (clasificador celular activado por fluorescencia) y métodos similares, hace que esta sea una técnica superior para la identificación selectiva y la modificación del genoma de una célula. La Patente de EE. UU. 6.835.816 desvela el uso de esta técnica en conjunción con genes que reflejan susceptibilidad tumoral, Incluyendo los genes TSG101.
En consecuencia, aún persiste el objetivo en la Industria de encontrar una manera para aumentar la expresión de anticuerpos, particularmente de anticuerpos preparados recombinantemente, a partir de huéspedes de expresión tipo células CHO, células 293HEK, células HeLa, células COS, células NIH3T3, células Jurkat, células NS0 y células HUVEC, y otras, de una manera estable y reprodúcele, utilizando técnicas disponibles para modificar el genoma de la célula.
Bohm et al, Blotechnology and Bloenglneerlng 88 (6): 699-706 (2004) describen la exploración de una actuación celular mejorada: selección de subclones con cinéticas de producción alterada o estabilidad mejorada por clasificación celular.
Sumario
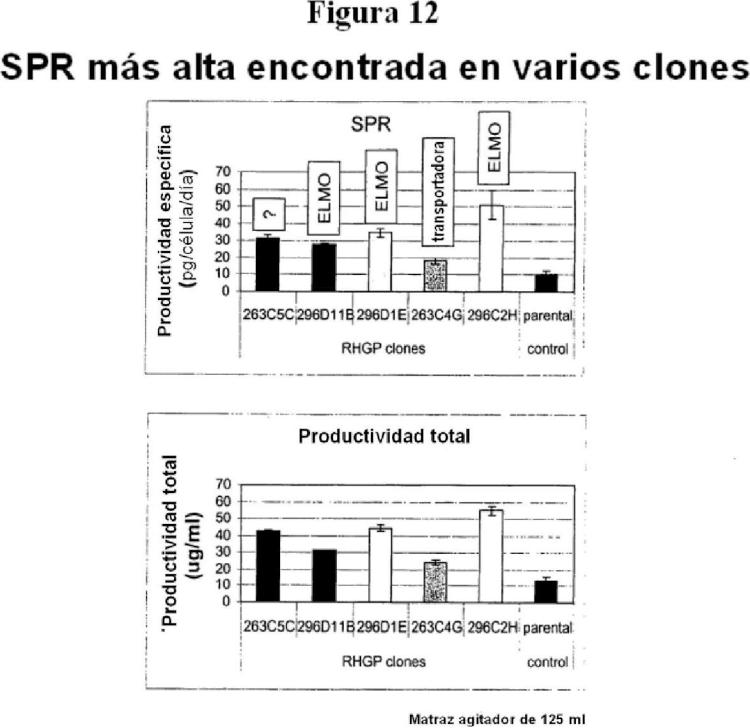
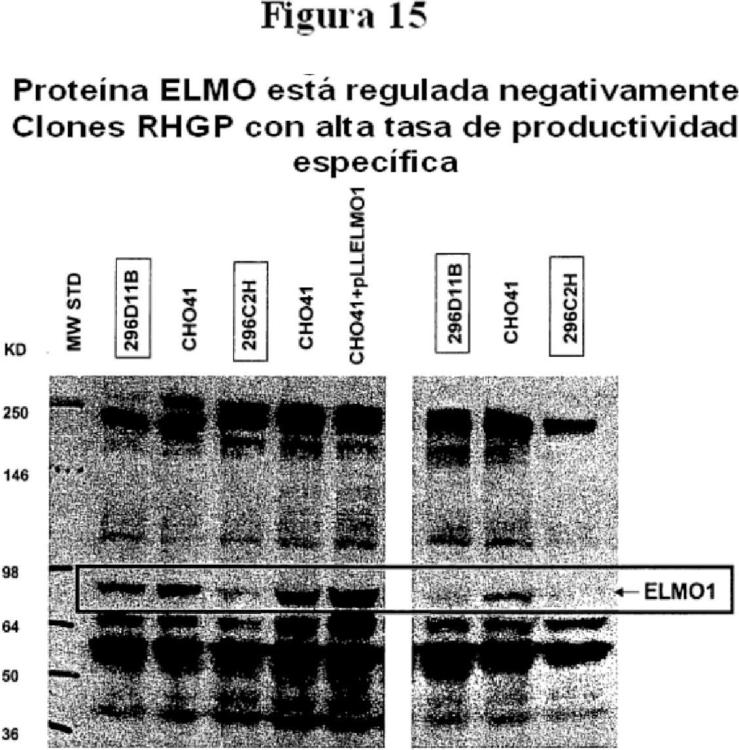
La invención demuestra que las células que son buenos vehículos de expresión para anticuerpos recombinantes se pueden modificar para aumentar la tasa de productividad específica (SPR) de células productoras de anticuerpos por un factor de 1,5, 2 o incluso 3 veces por encima del intervalo de expresión que es capaz la célula sin tal modificación. Por lo tanto, alterando selectivamente el perfil de expresión de la célula utilizando técnicas de anulación (Perturbación genética homocigota aleatoria o RHGP) o técnicas de aumento de la expresión insertando promotores de expresión mejor que ARN anti-sentido u otras construcciones de supresión de la expresión, se puede aumentar la producción de anticuerpos por la célula. El aumento de los valores de 3 veces o más, SPR, se han conseguido por supresión de la expresión de proteínas dirigidas. El SPR que se aumenta da lugar a un mayor volumen de productividad, lo que permite la recolección comercial de mAb en una base que se deseaba hasta ahora pero que no se había conseguido.
... [Seguir leyendo]
Reivindicaciones:
1. Un método para aumentar la tasa de productividad específica de la expresión de un anticuerpo en una línea celular de mamífero que expresa un anticuerpo de interés, que comprende:
alterar el patrón de expresión de al menos un gen del genoma de dicha línea celular distinto de dicho anticuerpo por medio de perturbación genética homocigota aleatoria (RHGP) por inserción de un vector de búsqueda genética (GSV) en el genoma de dicha línea celular, cuyo GSV al integrarse, o aumentará o disminuirá el nivel de expresión de dicho gen,
explorar las células de dicha línea celular transformada por RHGP para identificar las células transformadas que presentan una tasa de productividad específica (SPR) más alta para el anticuerpo de interés en comparación con los miembros de la misma línea celular no transformada por RHGP,
cultivar dichas células que presentan una SPR más alta para obtener una población de células que expresan dicho anticuerpo de interés con una SPR aumentada en comparación con dicha línea celular cuando no se aumenta por RHGP.
2. El método de la reivindicación 1, donde dicha alteración del patrón de expresión da como resultado el dicho al menos un gen que se expresa a una tasa menor que la expresión de dicho gen por dicha línea celular sin la transformación RHGP.
3. El método de la reivindicación 1, donde dicha alteración del patrón de expresión da como resultado el dicho al menos un gen que se expresa a una tasa mayor que la expresión de dicho gen por dicha línea celular sin la transformación RHGP.
4. El método de la reivindicación 1, donde dichas células transformadas por RHGP se exploran por FACS para identificar una pequeña fracción de células transformadas con la mayor SPR para dicho anticuerpo de interés para producir una colección de células seleccionadas,
dicha colección de células seleccionadas se expanden y se someten a una segunda exploración por FACS para identificar una pequeña fracción de la colección de células seleccionadas con la mayor SPR para dicho anticuerpo de interés para producir una segunda colección de células seleccionadas,
explorar dichas células de dicha segunda colección de células seleccionadas colocándolas en placas de célula única para identificar una colección de células que tiene una SPR mayor para dicho anticuerpo de interés que la de dicha colección de células seleccionadas o dicha segunda colección de células seleccionadas.
5. El método de la reivindicación 1, donde dichas células que expresan dicho anticuerpo de interés con una mayor SPR en comparación con dicha línea celular cuando no se ha transformado por RHGP presentan una SPR de al menos 1,5 veces la de las células de dicha línea celular cuando no se aumenta por RHGP.
6. El método de la reivindicación 5, donde dichas células que expresan dicho anticuerpo de interés con una mayor SPR en comparación con dicha línea celular cuando no se ha transformado por RHGP presentan una SPR de al menos 3,0 veces la de las células de dicha línea celular cuando no se aumenta por RHGP.
7. El método de la reivindicación 1, donde dicha línea celular es una línea celular de Ovario de Hámster Chino (CHO), línea celular 293HEK, línea celular HeLa, células COS, línea celular NIH3T3, línea celular Jurkat, línea celular NS0 o línea celular HUVEC.
8. El método de la reivindicación 7, donde dicha línea celulares una línea celular CHO.
9. Una línea celular de mamífero que expresa un anticuerpo de interés, habiendo sido transformada dicha línea celular por RHGP integrando un GSV en el genoma de dicha línea celular para alterar el patrón de expresión de al menos un gen del genoma de dicha línea celular distinto de dicho anticuerpo por medio de RHGP aleatoria para o aumentar o disminuir el nivel de expresión de dicho gen, donde dicha célula presenta una SPR mayor para dicho anticuerpo que la de células de dicha línea celular sin que se haya transformado por RHGP.
10. La línea celular de mamífero de la reivindicación 9, donde dicha célula presenta una SPR para dicho anticuerpo que es al menos 1,5 veces mayor que la de las células de dicha línea celular sin que se haya transformado por RHGP.
11. La línea celular de mamífero de la reivindicación 10, donde dicha célula presenta una SPR para dicho anticuerpo que es al menos 3,0 veces mayor que la de las células de dicha línea celular sin que se hayan transformado pro RHGP.
12. La línea celular de mamífero de la reivindicación 9, donde dicho patrón de expresión se ha alterado para disminuir la expresión de dicho al menos un gen del genoma de dicha línea celular distinto de dicho anticuerpo.
13. La línea celular de mamífero de la reivindicación 9, donde dicho patrón de expresión se ha alterado para aumentar la expresión de dicho al menos un gen del genoma de dicha línea celular distinto de dicho anticuerpo.
14. Una línea celular de mamífero de acuerdo con la reivindicación 9, donde dicha línea celular se selecciona de 5 entre el grupo que consiste en una línea celular de Ovarlo de Hámster Chino (CHO), línea celular 293HEK, línea
celular HeLa, células COS, línea celular NIH3T3, línea celular Jurkat, línea celular NSO o línea celular HUVEC.
15. Una línea celular de mamífero de acuerdo con la reivindicación 14, donde dicha línea celular es una línea celular CHO.
Patentes similares o relacionadas:
 Métodos para producir proteínas bicatenarias en bacterias, del 29 de Julio de 2020, de GENENTECH, INC.: Un método para producir un receptor de linfocitos T monoclonal de movilización inmunitaria contra el cáncer (ImmTAC) que comprende una cadena alfa del receptor de linfocitos […]
Métodos para producir proteínas bicatenarias en bacterias, del 29 de Julio de 2020, de GENENTECH, INC.: Un método para producir un receptor de linfocitos T monoclonal de movilización inmunitaria contra el cáncer (ImmTAC) que comprende una cadena alfa del receptor de linfocitos […]
 Animales no humanos que tienen un locus de cadena ligera lambda de inmunoglobulina modificado por ingeniería, del 29 de Julio de 2020, de REGENERON PHARMACEUTICALS, INC.: Un roedor cuyo genoma de la línea germinal comprende un locus de cadena ligera λ de inmunoglobulina endógeno que comprende:
(a) uno o más segmentos […]
Animales no humanos que tienen un locus de cadena ligera lambda de inmunoglobulina modificado por ingeniería, del 29 de Julio de 2020, de REGENERON PHARMACEUTICALS, INC.: Un roedor cuyo genoma de la línea germinal comprende un locus de cadena ligera λ de inmunoglobulina endógeno que comprende:
(a) uno o más segmentos […]
Composiciones farmacéuticas que contienen una leucocidina E mutada, del 22 de Julio de 2020, de NEW YORK UNIVERSITY: Una composición que comprende: una proteína Leucocidina E (LukE) aislada que comprende la secuencia de aminoácidos de la SEQ ID NO: 4, o un polipéptido […]
Formulación anti-IFNAR1 estable, del 24 de Junio de 2020, de ASTRAZENECA AB: Una formulacion de anticuerpo que comprende: a. De 100 mg/ml a 200 mg/ml de anifrolumab; b. Lisina HCl 40 mM a 60 mM; c. Trehalosa […]
Proteínas y péptidos modificados, del 24 de Junio de 2020, de GLAXO GROUP LIMITED: Un dominio variable de inmunoglobulina único, que se une a TNFR1 y que se selecciona de cualquiera de las siguientes secuencias de aminoácidos: (a) DOM1h-131-206 caracterizada […]
Métodos para purificar una proteína objetivo de una o más impurezas en una muestra, del 17 de Junio de 2020, de EMD Millipore Corporation: Un metodo para purificar una proteina objetivo que contiene una region Fc de una o mas impurezas en una muestra, el metodo comprende las etapas de: a) poner en contacto […]
Dominios variables de inmunoglobulina, del 10 de Junio de 2020, de Ablynx NV: Dominio variable individual de inmunoglobulina de cadena pesada (ISVD), en que el residuo aminoacídico en la posición 89 es L y el residuo […]
Criterio de valoración terapéutico equivalente para inmunoterapia de enfermedades basada en antiCTLA-4, del 10 de Junio de 2020, de E. R. Squibb & Sons, L.L.C: Un anticuerpo antiCTLA-4 para su uso en el tratamiento de cáncer en un sujeto, tratamiento que comprende inducir un acontecimiento liminar […]