Péptidos para suprimir reacciones de inflamación en hemodiálisis.
Construcción S-L-P que comprende una superficie S de un soporte sólido,
un grupo de unión L y un péptido P, en la que el péptido P está inmovilizado sobre la superficie S a través del grupo de unión L, en la que el grupo de unión L comprende un resto poli(óxido de alquileno) y en la que el péptido P comprende un extremo C-terminal según la fórmula general (I)**Fórmula**
en la que R1 es -H o -C(≥O)-alifato C1-8, y
en la que la línea de puntos de la fórmula general (I) representa el resto de la construcción S-L-P.
Tipo: Patente Europea. Resumen de patente/invención. Número de Solicitud: E11002917.
Solicitante: FRESENIUS MEDICAL CARE DEUTSCHLAND GMBH.
Nacionalidad solicitante: Alemania.
Dirección: ELSE-KRONER-STRASSE 1 61352 BAD HOMBURG ALEMANIA.
Inventor/es: CATANIA, ANNA, FISLAGE,RAINER, STEPPAN,Sonja, PASSLICK-DEETJEN,JUTTA PROF. DR, GATTI,STEFANO DR, KUHN,ANJA DR.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K38/34 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 38/00 Preparaciones medicinales que contienen péptidos (péptidos que contienen ciclos beta-lactama A61K 31/00; dipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina 2,5-dionas, A61K 31/00; péptidos basados en la ergolina A61K 31/48; que contienen compuestos macromoleculares que tienen unidades aminoácido repartidas estadísticamente A61K 31/74; preparaciones medicinales que contienen antígenos o anticuerpos A61K 39/00; preparaciones medicinales caracterizadas por los ingredientes no activos, p. ej. péptidos como soportes de fármacos, A61K 47/00). › Hormona melanotropa [MSH], p. ej. alfa o beta-melanotropina.
- A61P13/12 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › A61P 13/00 Medicamentos para el tratamiento del aparato urinario (diuréticos A61P 7/10). › de los riñones.
- A61P29/00 A61P […] › Agentes analgésicos, antipiréticos o antiinflamatorios que no actúan sobre el sistema nervioso central, p. ej. agentes antirreumáticos; Antiinflamatorios no esteroideos (AINEs).
PDF original: ES-2514322_T3.pdf




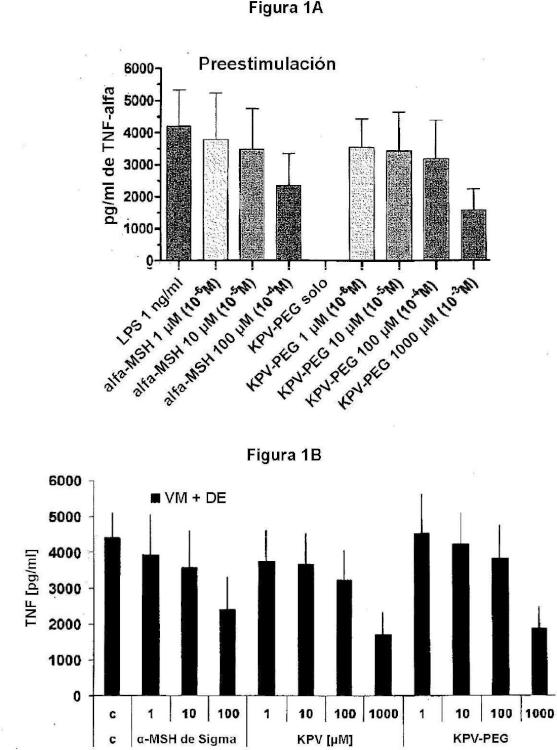
Fragmento de la descripción:
Péptidos para suprimir reacciones de inflamación en hemodiálisis
La invención se refiere a una construcción S-L-P que comprende una superficie S de un soporte sólido, un grupo de unión L y un péptido P, en la que el péptido P está inmovilizado sobre la superficie S a través del grupo de unión L tal como se define en las reivindicaciones. También se da a conocer un conjugado L-P que comprende un grupo de unión L de este tipo y un péptido P de este tipo. El conjugado L-P puede emplearse como producto intermedio en la preparación de la construcción S-L-P. Además, la construcción S-L-P es útil en hemodiálisis, particularmente para la prevención y/o supresión de respuestas y procesos inflamatorios.
La diálisis es un método de limpieza de la sangre de un individuo cuando los riñones dejan de funcionar apropiadamente. La diálisis elimina la sal de más, los desechos y el agua del cuerpo, y ayuda a controlar la tensión
arterial.
Se distinguen habitualmente dos tipos de diálisis: hemodiálisis y diálisis peritoneal. En la hemodiálisis, se conecta un paciente mediante tubos a un riñón artificial. Se bombea la sangre fuera del cuerpo al riñón artificial que filtra la sangre, y entonces se devuelve la sangre al cuerpo. En la diálisis peritoneal, se usa el revestimiento interior de la cavidad peritoneal del paciente como filtro natural. Se retiran los desechos por medio de un líquido, el dializado, que se lava dentro y fuera de la cavidad peritoneal en ciclos.
En la hemodiálisis, se usa un riñón artificial (hemodializador) para retirar desechos, productos químicos de más y líquido en exceso de la sangre. Para transferir la sangre de un paciente de diálisis al interior del riñón artificial, se requiere un acceso vascular. Se realiza un acceso común conectando una arteria a una vena debajo de la piel y creando así una fístula. Entonces se penetra la fístula, permitiendo el acceso a la sangre.
Ocasionalmente, se realiza un acceso por medio de un catéter, que se inserta en una vena grande en el cuello. Este tipo de acceso puede ser temporal, pero en muchos casos puede usarse para tratamiento a largo plazo. Como con cualquier tratamiento con catéter o acceso vascular, el catéter crea una comunicación directa entre el entorno interno aséptico de un paciente y el mundo exterior. Complicaciones comunes de esta comunicación son infecciones, inflamaciones y bloqueo trombótico o infiltrante del acceso.
La inflamación representa una complicación médica principal asociada con la diálisis. De hecho, aunque son numerosos los beneficios de la hemodiálisis y la diálisis peritoneal, muchas de las complicaciones asociadas con cada una pueden ser potencialmente mortales. Cada técnica tiene sus propias o similares complicaciones incluyendo, pero sin limitarse a, fallo de la ultrafiltración, conformidad, obesidad, aclaramiento y escasa conformidad del líquido.
La inflamación es un factor principal para la alta mortalidad en pacientes con nefropatía terminal (end stage renal disease, ESRD). Se considera que la inflamación desempeña un papel primordial en el daño arterial en pacientes de diálisis. Aunque los mecanismos precisos que conducen a este estado inflamatorio en ESRD no están claros, se comentan infección leve, exposición repetida a filtros para diálisis y productos de autooxidación como factores desencadenantes probables en estos pacientes (véanse C. Zocalli et al., Blood purification, 2003, 21, 29-36; y P. Stenvinkel et al., Semin. Dial., 2002, 15, 329-37).
Existe una demanda de métodos que provoquen menos inflamación en pacientes de hemodiálisis.
a-MSH (hormona estimulante de melanocitos) se deriva de una hormona precursora, concretamente propiomelanocortina (POMC). El procesamiento postraduccional de POMC produce hormonas peptídicas tales como ACTH, a-MSH - y-MSH y (3-endorfina.
a-MSH tiene múltiples efectos sobre el huésped.
El efecto estimulante de a-MSH en células pigmentarias se ha conocido durante más de 50 años. Hallazgos más recientes indican que a-MSH controla la ingesta de alimento y secreciones exocrinas, modula la fiebre (véase D. B. Richards et al., Peptides 1984, 5 (4), 815-7) y reacciones inflamatorias y tiene un efecto antimicrobiano (véase por ejemplo A. Catania et al., J Leukoc Biol. 2000, 67 (2), 233-9). a-MSH induce la expresión de Fos en neuronas productoras de oxitocina supraópticas (N. Sabatier et al., J. Neuroscience, 2003, 23 (32), 10351-8).
[Nle4-d-Phe7]-a-MSH (NDP-MSH) se ha descrito como un análogo de a-MSH estable a proteasas (véase T. K. Sawyer etal., Proc. Nati. Acad. Sci. USA, 1980, 77 (10), 5754-58).
Se ha mostrado que Ac-Lys-Pro-Val-NH2 (KPV), el tripéptido terminal de a-MSH, que está N-acetilado y C-amidado
presenta casi el mismo efecto antiinflamatorio que a-MSH de longitud completa.
El documento WO 88/00833 da a conocer un tripéptido antipirético, que tiene la secuencia de aminoácidos lisina- prolina-valina, y un método para utilizar el tripéptido para reducir la fiebre y la inflamación en mamíferos.
El documento US 2009/0069242 describe análogos peptídicos de a-MSH, que presentan una eficacia aumentada en comparación con el péptido de a-MSH nativo.
Los documentos US 2005/0130901 y US 2006/0122121 se refieren a péptidos con actividad antimicrobiana. Los péptidos son péptidos octoméricos modificados a partir de a-MSH.
El documento WO 2004/004551 da a conocer una composición y un método para controlar la respuesta del huésped a trasplante e injerto de órganos y/o tejidos. a-MSH protege al órgano y tejido tras el trasplante controlando factores dentro del donante, el huésped y el órgano o tejido que va a trasplantarse.
Los documentos US 2010/143438 y WO 2010/129248 dan a conocer construcciones de S-L-alfa-MSH para su uso en el tratamiento de inflamación.
El documento WO 00/56353 se refiere a un sistema de acondicionamiento genitourinario que comprende un portador, al menos un polipéptido que incluye una secuencia de aminoácidos de KPV o un equivalente biológicamente funcional de la misma; en el que el portador porta el polipéptido. El polipéptido puede incluir un dímero formado a partir de la secuencia de aminoácidos.
J. M. Kelly et al., Peptides, 2006, 27, 431-7 dan a conocer que la hormona estimulante de melanocitos-a 10-13 (GKPV) inhibe la actividad de NF-kB estimulada por el factor de necrosis tumoral-a.
La capacidad del dímero (CKPV)2 para inhibir reacciones del huésped inducidas por endotoxinas sugiere que puede ser útil en el tratamiento de trastornos inflamatorios (S. Gatti et al., J Surg Res, 2006, 131 (2), 209-14).
También se conocen la síntesis y la actividad del dímero [Ac-CKPV]2 (véase A. Catania et al., J Pept Res., 2005, 66
(1), 19-26).
Se sabe que las concentraciones de a-MSH están elevadas en pacientes en hemodiálisis crónica. Se observan concentraciones de hasta 30 ng/l mientras que pacientes sanos muestran concentraciones de hasta 25 ng/l sólo. La concentración de a-MSH está particularmente elevada cuando puede observarse simultáneamente una concentración elevada de endotoxlna. Posiblemente, se Induce liberación de a-MSH por atocinas con el fin de limitar su efecto (véase L. Alraghi et al., Nephrol Dial Transplant, 2000, 15, 1212-6).
También se investigaron los efectos antllnflamatorlos de tripéptidos relacionados con a-MSH in vitro e in vivo (Broska et al., Endocrine reviews, 2008, 29 (5), 581-602).
El documento WO 03/094990 se refiere a ollgo y pollsacárldos que contienen el elemento estructural de azúcar N- acilglucosamina o N-acilgalactosamina, además del uso de los mismos para producir superficies hemocompatibles y métodos para recubrir superficies con dichos oligo y pollsacárldos, que constituyen las sustancias precursoras de biosíntesis comunes de heparina, sulfatas de heparano y quitosano.
Los documentos US 2005/074485 y WO 2004/104019 dan a conocer una composición y un método de tratamiento en el que se usan péptidos antimicrobianos y antiinflamatorlos, preferiblemente KPV o un dímero del mismo, para hemodiálisis y diálisis peritoneal en dializado y gel. Los péptidos antimicrobianos y antiinflamatorios pueden usarse en diálisis peritoneal para aumentar la diuresis. Otras realizaciones incluyen el uso de los péptidos antimicrobianos y antiinflamatorios en disoluciones de sellado usadas para catéteres y otros tubos de acceso vascular o tubos de acceso peritoneal.
Sin embargo, estas composiciones no son satisfactorias en cada sentido y existe una demanda de mejoras adicionales de la hemodiálisis.
Un objeto de la invención es proporcionar mejoras para la hemodiálisis y otros métodos en los... [Seguir leyendo]
Reivindicaciones:
1. Construcción S-L-P que comprende una superficie S de un soporte sólido, un grupo de unión Ly un péptido P, en la que el péptido P está inmovilizado sobre la superficie S a través del grupo de unión L, en la que el grupo de unión L comprende un resto poli(óxido de alquileno) y en la que el péptido P comprende un extremo C-terminal según la 5 fórmula general (I)
**(Ver fórmula)**en la que R1 es -H o -C(=0)-alifato Ci.8, y
en la que la línea de puntos de la fórmula general (I) representa el resto de la construcción S-L-P.
2. Construcción según la reivindicación 1, en la que el péptido P comprende un extremo C-terminal según la fórmula general (II)
**(Ver fórmula)**OI)
en la que R1 y R2 son independientemente entre sí -H o -C(=O)-alifat0 C-i-8, y
en la que la línea de puntos de la fórmula general (II) representa el resto de la construcción S-L-P.
3. Construcción según la reivindicación 1 ó 2, en la que el péptido P consiste en residuos de a-aminoácido que
tienen configuración L.
4. Construcción según cualquiera de las reivindicaciones anteriores, en la que el péptido P incluye
- no más de 4 residuos de a-aminoácido unidos directamente entre sí a través de enlaces peptídicos o
- dos subsecuencias que incluyen cada una no más de 4 residuos de a-aminoácido unidos directamente entre sí a 20 través de enlaces peptídicos, en la que dichas dos subsecuencias están unidas entre sí a través de un enlace no
peptídico.
5. Construcción según cualquiera de las reivindicaciones anteriores, en la que el péptido P comprende un dímero según la fórmula general (III)
**(Ver fórmula)**en la que R1, R1, R2 y R2 son independientemente entre sí -H o -C(=0)-alifato C1-8, y
en la que la línea de puntos de la fórmula general (III) representa el resto de la construcción S-L-P.
6. Construcción según cualquiera de las reivindicaciones anteriores, en la que el grupo de unión L no incluye ningún
residuo de a-aminoácido.
7. Construcción según cualquiera de las reivindicaciones anteriores, en la que la superficie S está adaptada para ponerse en contacto con un líquido corporal.
8. Construcción según cualquiera de las reivindicaciones anteriores, en la que el soporte sólido es un componente 10 de un circuito extracorpóreo.
9. Procedimiento para la fabricación de una construcción S-L-P según cualquiera de las reivindicaciones 1 a 8 que comprende la etapa de unir un péptido P según cualquiera de las reivindicaciones 1 a 5 a una superficie S de un soporte sólido a través de un grupo de unión L.
10. Construcción según cualquiera de las reivindicaciones 1 a 8, para su uso en hemodiálisis, hemofiltración, 15 plasmaféresis, aféresis, oxigenación por membrana extracorpórea o circulación sanguínea asistida.
Patentes similares o relacionadas:
Composiciones y métodos para el cuidado de la piel que comprenden agonistas selectivos del receptor de melanocortina 1, del 13 de Noviembre de 2019, de UNIVERSITY OF CINCINNATI: Un agonista selectivo de péptidos del receptor de melanocortina 1 (MC1R) según la siguiente fórmula: Ar(CH2)mX1-X2-CO-X3-X4-X5-(Trp)n-NX6R […]
Lipopéptidos antimicrobianos cortos, del 31 de Octubre de 2019, de HELIX BIOMEDIX INC: Una composición para su uso en la prevención o tratamiento de una infección microbiana de la piel o el tejido mucoso de un mamífero, comprendiendo la composición […]
Análogos peptídicos de hormonas estimulantes de alfa melanocitos, del 3 de Junio de 2019, de GENZYME CORPORATION: Un compuesto que se une selectivamente al receptor de melanocortina 1 (MC1R), dicho compuesto comprende un polipéptido que tiene la secuencia: Xaa1 Xaa2 Xaa3 Xaa4 Xaa5 Xaa6 […]
Composiciones farmacéuticas que comprenden agonistas selectivos del receptor de melanocortina 1 y su uso en métodos terapéuticos, del 8 de Mayo de 2019, de UNIVERSITY OF CINCINNATI: Una composición farmacéutica que comprende: (a) una cantidad efectiva de un agonista peptídico selectivo del receptor de melanocortina 1 (MC1R) de […]
Análogos de alfa-MSH terapéuticamente activos, del 25 de Febrero de 2019, de AbbVie Inc: Un péptido que asciende a un total de 19 residuos de aminoácidos, donde el péptido se selecciona del grupo que consiste en: Lys-Lys-Lys-Lys-Lys-Lys-Ser-Ser-Ile-Ile-Ser-His-Phe-Arg-Trp-Gly-Lys-Pro-Val […]
Bioactivador metabólico cutáneo, del 11 de Abril de 2018, de THOREL, JEAN-NOEL: Composición cosmética que comprende un sistema bioactivo que asocia: - por una parte, una forma estable en solución acuosa de ATP (adenosín […]
Terapia para el vitíligo, del 13 de Diciembre de 2017, de Clinuvel Pharmaceuticals Limited: Composición farmacéutica que comprende un análogo de alfa-MSH el cual es un derivado de alfa-MSH que exhibe actividad agonista para el receptor de melanocortina-1 […]
Composiciones farmacéuticas de ligandos del receptor de melanocortina, del 1 de Noviembre de 2017, de IPSEN PHARMA S.A.S: Una composición farmacéutica de una solución, un gel o un semisólido, o una suspensión, que comprende una sal pamoato de Ac-Arg-ciclo (Cys-D-Ala-His-D-Phe-Arg-Trp-Cys)-NH2, […]