PÉPTIDOS MIMÉTICOS Y SU UTILIZACIÓN COMO INHIBIDORES DEL PROTEASOMA 20S, DEL PROTEASOMA 26S Y DEL INMUNOPROTEASOMA.
Compuesto de fórmula **(Ver fórmula)**en el que R1es Boc, Z, Ac o H,
10 L es Leu, X es Asp(OR4), 15 R2 es CH2-CH(CH3)2, R3 es CH2-OH, CH=O, CH(OH)-C≡C-fenilo, CH(OH)-C(O)-NH-R5 o C(O)-C(O)-NHR5, R4es t-butilo, bencilo o H, R5 es bencilo, 3-picolilo o fenilo, y las sales farmacéuticamente aceptables del mismo
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP2006/001975.
Solicitante: TECHNISCHE UNIVERSITÄT DARMSTADT
CHARITÉ - UNIVERSITÄTSMEDIZIN BERLIN.
Nacionalidad solicitante: Alemania.
Dirección: PETERSENSTRASSE 30 64287 DARMSTADT ALEMANIA.
Inventor/es: KLOETZEL,PETER-MICHAEL, SCHMIDT,BORIS, UMBREEN,SUMAIRA,C/O FRAU BRIGITTE HERDLER, BRAUN,HANNES, KUCKELKORN,ULRIKE.
Fecha de Publicación: .
Fecha Solicitud PCT: 3 de Marzo de 2006.
Fecha Concesión Europea: 1 de Septiembre de 2010.
Clasificación Internacional de Patentes:
- C07K5/06A1B1
- C07K5/08A1B
Clasificación PCT:
- A61K38/06 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 38/00 Preparaciones medicinales que contienen péptidos (péptidos que contienen ciclos beta-lactama A61K 31/00; dipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina 2,5-dionas, A61K 31/00; péptidos basados en la ergolina A61K 31/48; que contienen compuestos macromoleculares que tienen unidades aminoácido repartidas estadísticamente A61K 31/74; preparaciones medicinales que contienen antígenos o anticuerpos A61K 39/00; preparaciones medicinales caracterizadas por los ingredientes no activos, p. ej. péptidos como soportes de fármacos, A61K 47/00). › Tripéptidos.
- A61P25/28 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › A61P 25/00 Medicamentos para el tratamiento de trastornos del sistema nervioso. › de los problemas neurodegenerativos del sistema nervioso central, p. ej. noótropos, activadores del conocimiento, medicamentos para el tratamiento del Alzheimer o de otras formas de demencia.
- A61P35/00 A61P […] › Agentes antineoplásicos.
- C07K5/08 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 5/00 Péptidos con hasta cuatro aminoácidos en una secuencia totalmente determinada; Sus derivados. › Tripéptidos.
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Eslovenia, Finlandia, Rumania, Chipre, Lituania, Letonia.
Fragmento de la descripción:
DESCRIPCIÓN DE LA INVENCIÓN
La presente invención se refiere a compuestos peptidomiméticos, a la síntesis y utilización de los mismos para la inhibición de los proteasomas y la inducción de la apoptosis en células tumorales. Además, la presente invención se refiere a composiciones farmacéuticas que comprenden los compuestos y a la utilización de dichos compuestos para el tratamiento de enfermedades, particularmente cáncer y enfermedades neurodegenerativas.
ANTECEDENTES DE LA INVENCIÓN
El equilibrio entre los procesos de síntesis y de degradación de las proteínas resulta esencial para el mantenimiento de la homeostasis celular. Las células presentan dos rutas metabólicas principales de degradación proteínica. Un número elevado de proteínas es digerido por enzimas proteolíticas en los lisosomas o a través del sistema ubiquitino-proteasómico. Un desequilibrio entre los procesos de síntesis y de degradación de las proteínas conduce a una serie de procesos patológicos (1).
Los proteasomas 26S son complejos de proteasa compuestos por múltiples subunidades, y llevan a cabo la degradación dependiente de ATP de las proteínas poliubiquitiniladas. Son responsables de la mayoría de las proteólisis no lisosómicas en las células eucariotas. Están constituidos por las partículas proteolíticas del núcleo del proteasoma 20S y presentan una tapa en uno de sus extremos, o en ambos, formada por las partículas de tapa reguladoras de 19S (2, 3). La partícula de núcleo 20S es un conjunto cilíndrico de 28 subunidades dispuestas en 4 anillos heptámeros amontonados. 2 anillos están formados por 7 subunidades de tipo α y 2 anillos por 7 subunidades de tipo β (4, 5). Los dos anillos interiores de tipo β forman la zona central del cilindro y contienen los centros proteolíticos. A diferencia de los proteasomas 20S procariotas, que consisten en 14 subunidades alfa y 14 subunidades idénticas proteolíticamente activas de tipo β, los proteasomas 20S eucariotas presentan únicamente tres subunidades proteolíticamente activas por anillo de tipo β. Los proteasomas pertenecen a la familia de las hidrolasas nucleofílicas N-terminales (6, 7). La estimulación de las células de mamífero con interferón γ provoca el intercambio de tres subunidades β activas β1, β2y β5 por las homólogas inmunes β1i, β2i y β5i, lo que conduce a la formación de las inmunoproteasomas, que generan un patrón de escisión modificado de los sustratos peptídicos. Se puso de manifiesto que la integridad funcional del proteasoma es esencial para multitud de funciones celulares, tales como, por ejemplo, la adaptación metabólica, la diferenciación celular, el control del ciclo celular, la respuesta a la tensión, la degradación de las proteínas anómalas y la generación de epítopes presentados a través de receptores MHC de clase I (para una revisión, véase (8, 9)). Los proteasomas son productores importantes, aunque no exclusivos, de péptidos antigénicos (10, 11).
La desregulación de la ruta metabólica de la degradación proteínica ubiquitinoproteasómica provoca diversas enfermedades en el humano, tales como, por ejemplo, cáncer, enfermedades neurodegenerativas, enfermedades autoinmunes y enfermedades metabólicas. La inhibición de los proteasomas afecta a la estabilidad de muchas proteínas, tales como las implicadas en la regulación del ciclo celular. Por consiguiente, los inhibidores selectivos de las subunidades proteasómicas multicatalíticas son objetivos atractivos en el desarrollo de fármacos (12).
La mayoría de células tratadas con inhibidores proteasómicos están sensibilizadas para la apoptosis (13, 14). Habitualmente, lo que constituye una característica interesante, las células tumorales son más sensibles a la inhibición proteasómica que las células normales. Las células sanas sufren una detención del ciclo celular cuando se tratan con inhibidores proteasómicos, pero sin embargo, a diferencia de las células tumorales, tienen menos tendencia a sufrir apoptosis (15, 16).
Hasta el presente, se han caracterizado diferentes inhibidores proteasómicos (véase figura 1). Se hace una distinción entre inhibidores selectivos (4, lactacistina; 5, TMC-95A; 6, epoxomicina) e inhibidores no selectivos (1, dicloroviniléster; 3, MG132) (17).
El inhibidor proteasómico más importante es el compuesto 2, también designado Bortezomib® o VELCADE™ (véase figura 1). El Bortezomib® ha sido registrado por la
U.S. Food and Drug Administration (FDA) como fármaco disponible únicamente bajo receta para el tratamiento del mieloma múltiple (18-20).
Otro inhibidor proteasómico importante es el MG132 (compuesto 3 de la figura 1). Una desventaja decisiva del MG132 es su nula o baja selectividad en la inhibición de los proteasomas (1, 17, 22, 38).
El documento WO 95/24914 describe numerosos aldehídos peptídicos similares a los de la presente invención, pero no idénticos. La mejora del efecto de los compuestos presentes es debida al grupo/sustituyente Asp(OR4). Este hecho da lugar a una inhibición selectiva. Esta importante unidad estructural no está incluida en la definición de sustituyente R2 (en la página 13).
El documento Sorg y otros (2005), J. Peptide Science (11): 142-153, describe la síntesis de aldehídos tripeptídicos y tetrapeptídicos sobre un soporte sólido. Sin embargo, los compuestos más activos según la presente invención no se pueden sintetizar mediante este procedimiento, dado que este éster es inestable en las condiciones de reacción. Por consiguiente, no se describen aldehídos tripeptídicos o tetrapeptídicos con ácido glutárico
o ácido aspártico en la posición 2. Solo se describe un efecto biológico de las sustancias para las caspasas.
El documento Iqbal y otros (1977), Bioorganic & Medicinal Chemistry letter 7:539544, describe la inhibición de calpaína I mediante aldehídos dipeptídicos y tripeptídicos, particularmente con P2 = Leu, Phe, Ser, Thr, Trp. Ninguno de los péptidos mencionados presenta los aminoácidos polares Glu, Asp, Asn, Gln o derivados en P2.
En el documento Saito y otros (1992), Biochem. Biophys. Res. Comm. (184):419126, se describe una inhibición de proteasas indefinida mediante aldehídos dipéptidos de fórmula general Ac-Leu-Leu-X-CHO y Z-Leu-Leu-X-CHO de proteasas desconocidas. Se intentó llevar a cabo una identificación de la proteasa activa por cromatografía de afinidad, sin éxito. Únicamente se puso de manifiesto la inhibición de la catepsina L. No se mencionan los proteasomas 20S ó 26S. El proteasoma también es una proteasa no secretada.
Además, el documento WO 96/13266 describe compuestos peptídicos de ácido y 5 éster borónico adecuados como inhibidores de la función proteasómica.
La hidrólisis amídica proteasómica difiere de la hidrólisis amídica de todas las
demás clases de proteasas. Para ello, las características particulares son las treoninas N-
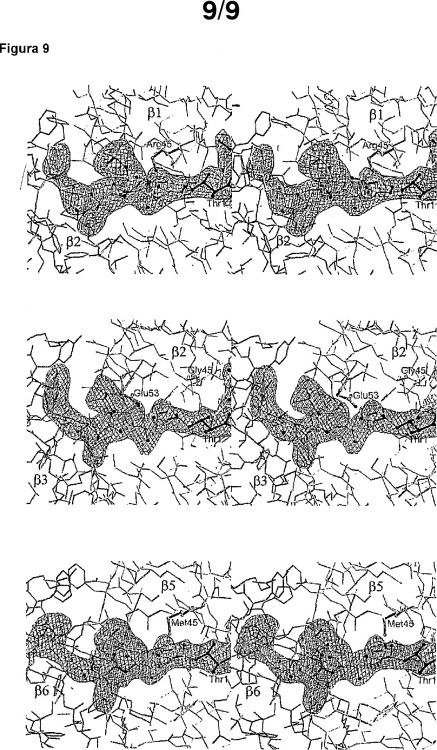
terminales. El mecanismo se representa en la figura 2. Al analizar la estructura cristalina del proteasoma 20S, se puso de manifiesto que la Thr10γ funciona como nucleófilo y el grupo amino N-terminal como portador de acilo (6). Los inhibidores covalentes se pueden enlazar en el centro activo, particularmente a través del grupo hidroxilo de la Thr10γ o simultáneamente a través del terminal N libre y la Thr10γ (para una revisión, véase 17).
15 De este modo, los inhibidores in vivo eficaces del proteasoma 20S requieren una selectividad elevada y, al mismo tiempo, una buena capacidad de penetrar en las membranas celulares. Además, se pueden caracterizar por el hecho de que se enlazan covalentemente a la treonina N-terminal.
20 Por consiguiente, el objetivo de la presente invención consiste en desarrollar inhibidores mejorados del proteasoma caracterizados particularmente por su selectividad con respecto al mismo, así como por su irreversibilidad, y que pueden penetrar en las membranas celulares.
25 Según la presente invención, este objetivo se alcanza proporcionando compuestos de fórmula
**(Ver fórmula)**
30 en los que R1 a R5 y X se seleccionan independientemente los unos de los otros, y en los que R1 es Boc, Z, Ac o H, 35 Les Leu, X es Leu o Asp(OR4), R2 es CH2-CH(CH3)2, 40 R3 es CH2-OH, CH═O, CH(OH)-C≡C-fenilo, CH(OH)-C(O)-NH-R5 o C(O)-C(O)-NH-R5,
R4 es t-butilo, bencilo o H, R5 es bencilo,...
Reivindicaciones:
1. Compuesto de fórmula
**(Ver fórmula)**
en el que
R1es Boc, Z, Ac o H, 10
L es Leu, X es Asp(OR4), 15 R2 es CH2-CH(CH3)2, R3 es CH2-OH, CH═O, CH(OH)-C≡C-fenilo, CH(OH)-C(O)-NH-R5 o C(O)-C(O)-NHR5, R4es t-butilo, bencilo o H, R5 es bencilo, 3-picolilo o fenilo, y las sales farmacéuticamente aceptables del mismo.
2. Compuesto según la reivindicación 1, en el que
R1es Boc o Z, 30
L es Leu, X es Asp(OR4), 35 R2 es CH2-CH(CH3)2,
R3 es CH2-OH,
R4 es t-butilo. 40
3. Compuesto según la reivindicación 1, en el que R1 es Boc, Z o Ac, L es Leu,
X es Asp(OR4),
R2 es CH2-CH(CH3)2,
R3es CH═O,
R4 es t-butilo o bencilo.
4. Procedimiento para preparar un compuesto según la reivindicación 1, que comprende la condensación de dipéptidos protegidos de la manera habitual y aminoácidos con aminoalcoholes, y su posterior oxidación para proporcionar aldehídos peptídicos.
5. Procedimiento según la reivindicación 4, caracterizado porque la oxidación se lleva a cabo utilizando reactivos de yodo hipervalente, en particular IBX en DMSO.
6. Compuesto según una de las reivindicaciones 1 a 3 para el tratamiento de enfermedades.
7. Composición farmacéutica, que comprende un compuesto según una de las reivindicaciones 1 a 3, o una sal farmacéuticamente aceptable del mismo y portadores y/o excipientes farmacéuticamente aceptables.
8. Composición farmacéutica según la reivindicación 7, caracterizada porque el compuesto está presente en una cantidad tal que la concentration está comprendida entre 0,001 y 100 µM durante el tratamiento in vivo.
9. Composición farmacéutica según la reivindicación 7 u 8, caracterizada porque el compuesto está presente en una cantidad que inhibe de manera eficaz la función del proteasoma en una célula o un mamífero.
10. Utilización de un compuesto según una de las reivindicaciones 1 a 3 para preparar un medicamento para inducir la apoptosis en las células.
11. Utilización de un compuesto según una de las reivindicaciones 1 a 3 para preparar un medicamento para inhibir la actividad proteolítica del proteasoma 20S, el proteasoma 26S y el inmunoproteasoma.
12. Utilización según la reivindicación 11, en la que la actividad de tipo tripsina del proteasoma 20S y el proteasoma 26S se inhibe de manera específica.
5 13. Utilización según la reivindicación 11, en la que la actividad de tipo quimiotripsina del proteasoma 20S y el proteasoma 26S se inhibe de manera específica.
14. Utilización según la reivindicación 11, en la que las actividades de tipo quimiotripsina, tipo tripsina y tipo caspasa del proteasoma 20S y el proteasoma 26S se inhiben de manera simultánea.
15. Procedimiento ex vivo para inhibir el crecimiento de una célula cancerosa, que comprende poner en contacto una célula y un compuesto según una de las reivindicaciones 1 a 3, o una célula y una composición farmacéutica según una de las reivindicaciones 7 a 9.
Patentes similares o relacionadas:
 NONADEPSIPEPTIDOS ACILADOS DE TIPO LISOBACTINA, del 7 de Diciembre de 2009, de AICURIS GMBH & CO. KG: Compuesto de la fórmula ** ver fórmula** en la que R1 significa hidrógeno, cicloalquilo C3-C6, cicloalquenilo C5-C6, cicloalquil C3-C6-metilo, heterociclilmetilo […]
NONADEPSIPEPTIDOS ACILADOS DE TIPO LISOBACTINA, del 7 de Diciembre de 2009, de AICURIS GMBH & CO. KG: Compuesto de la fórmula ** ver fórmula** en la que R1 significa hidrógeno, cicloalquilo C3-C6, cicloalquenilo C5-C6, cicloalquil C3-C6-metilo, heterociclilmetilo […]
INHIBIDORES DEL VIRUS DE LA HEPATITIS C, del 21 de Julio de 2011, de BRISTOL-MYERS SQUIBB COMPANY: Un compuesto que tiene la fórmula en la que: (a) R1 es alquilo C1-8, cicloalquilo C3-7 o alquilcicloalquilo C4-10; (b) m es 1 ó 2; (c) n es 1 […]
DERIVADOS DE MACROLACTONA, del 13 de Julio de 2011, de SANOFI-AVENTIS: Compuesto de la fórmula (I) **Fórmula** en la que X e Y, independientes uno del otro, son OH, O-(C1-C6)-alquilo, NH2 o NH-(C1-C6)-alquilo, o X e Y forman juntos […]
PÉPTIDOS MACROCÍCLICOS CON ACCIÓN CONTRA EL VIRUS DE LA HEPATITIS C, del 9 de Mayo de 2011, de BOEHRINGER INGELHEIM INTERNATIONAL GMBH: Un compuesto de fórmula (I) **Fórmula** , donde R1 es hidroxilo o NHSO2R11 con R11 igual a alquilo (C1-6), alquenilo (C2-6), cicloalquilo (C3-7), cicloalquil( […]
COMPUESTOS MACROCÍCLICOS DEFINIDOS ESPACIALMENTE ÚTILES PARA EL DESCUBRIMIENTO DE FÁRMACOS, del 20 de Abril de 2011, de TRANZYME PHARMA INC: Un compuesto que tiene la estructura de la fórmula II: **Fórmula** en la que W, A 1, A 2, A 3 y T se definen como sigue con los NH de A 1 unidos a T, los C=O de […]
SULFAMIDAS HETEROCÍCLICAS COMO INHIBIDORES DEL VIRUS DE LA HEPATITIS C, del 20 de Enero de 2011, de BRISTOL-MYERS SQUIBB COMPANY: Un compuesto que tiene la fórmula **Fórmula** en la que: (a) R1 es Het no sustituido o sustituido, en la que el término "Het" representa un radical monovalente […]
 NUEVOS COMPUESTOS COMO INHIBIDORES DE LA SERINA PROTEASA NS3 DEL VIRUS DE LA HEPATITIS C, del 30 de Diciembre de 2010, de SCHERING CORPORATION: Un compuesto, o enantiómeros, estereoisómeros, rotámeros, tautómeros o racematos de dicho compuesto, o una sal farmacéuticamente aceptable, […]
NUEVOS COMPUESTOS COMO INHIBIDORES DE LA SERINA PROTEASA NS3 DEL VIRUS DE LA HEPATITIS C, del 30 de Diciembre de 2010, de SCHERING CORPORATION: Un compuesto, o enantiómeros, estereoisómeros, rotámeros, tautómeros o racematos de dicho compuesto, o una sal farmacéuticamente aceptable, […]
NUEVO COMPUESTO DE PIPERIDINA, del 31 de Mayo de 2010, de MITSUBISHI TANABE PHARMA CORPORATION: Un compuesto de piperidina representado por la fórmula [I]: