Dispositivo osmótico que contiene amantadina y una sal osmótica.
Los dispositivos osmóticos de la presente invención contienen unnúcleo unitario que comprende una sal de amantadina y una sal osótica,
donde las dos sales poseen un ion en común. La velocidad e liberación de amantadina es modificada pasando de un perfil deliberación de primer orden a un perfil de liberación de cero ordn, pseudo cero orden o sigmoideo, al incrementar la cantidad de a sal osmótica en el núcleo del dispositivo. El dispositivo osmóico incluye una membrana semipermeable que posee una porosidad cntrolada que puede ser adaptada según la necesidad para cooperarcon la sal osmótica en proveer un perfil de liberación de droga redeterminado. La sal osmótica no necesita ser recubierta y estámezclada con la sal de amantadina
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/CR2005/000005.
Solicitante: OSMOTICA KERESKEDELMI ÉS SZOLGÁLTATÓ KFT.
Inventor/es: FAOUR, JOAQUINA, MEYER, GLENN A., RICCI,MARCELO,A, FELEDER,ETHEL C, COPPARI,MARCELO,A, VERGEZ,Juan A, BEFUMO,MARCELO E.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K31/13 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › Aminas, p. ej. Amantadina (A61K 31/04 tiene prioridad).
- A61K9/20 A61K […] › A61K 9/00 Preparaciones medicinales caracterizadas por un aspecto particular. › Píldoras, pastillas o comprimidos.
- A61K9/28 A61K 9/00 […] › Grageas; Píldoras o comprimidos con revestimientos.
PDF original: ES-2549581_T3.pdf




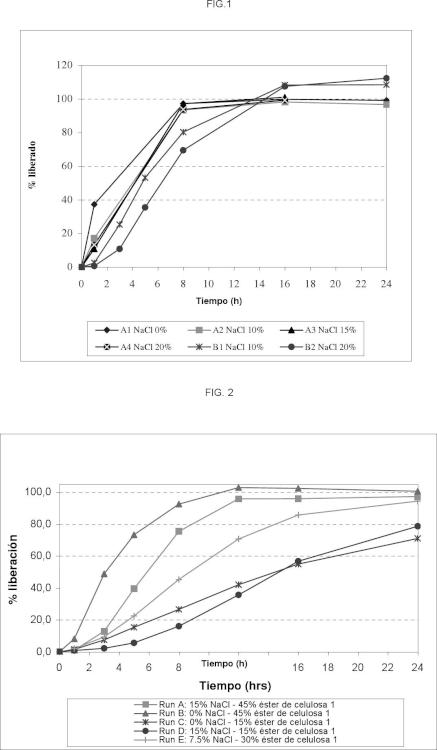
Fragmento de la descripción:
Dispositivo osmótico que contiene amantadina y una sal osmótica CAMPO DE LA INVENCIÓN
La presente invención pertenece a un dispositivo osmótico que contiene un fármaco activo y una sal osmótica en el núcleo, donde la velocidad de liberación del fármaco activa es reducida y el perfil de liberación del fármaco activa es modificado por el incremento de la cantidad de la sal osmótica en el núcleo. En una realización, el dispositivo osmótico contiene hidrocloruro de amantadina y cloruro de sodio en el núcleo. El dispositivo osmótico es capaz de proporcionar una liberación sigmoidea controlada de hidrocloruro de amantadina.
ANTEDECENTES DE LA INVENCIÓN
Los dispositivos osmóticos han demostrado ser útiles para proporcionar agentes activos tales como medicinas, nutrientes, productos alimenticios, pesticidas, herbicidas, germicidas, alguicidas, reactivos químicos, y otros conocidos por los expertos en la materia, a un ambiente de uso de manera controlada durante periodos prolongados de tiempo. Los dispositivos conocidos incluyen comprimidos, pastillas, píldoras o cápsulas y otros que utilizan la presión osmótica para controlar la liberación del agente activo contenido en el núcleo del dispositivo osmótico. Algunos dispositivos osmóticos también pueden incluir capas que comprenden uno o más materiales que están sometidos a erosión o que se disuelven lentamente en el ambiente de uso, dispensando de esta manera gradualmente el agente activo.
Las sales osmóticas que muestran un gradiente presión osmótica frente a un fluido externo a través de la pared semipermeable de los dispositivos osmóticos han sido utilizadas en el núcleo de los dispositivos osmóticos durante mucho tiempo. Las Patentes de EE.UU. N° 3.977.404, N° 4.008.719, N° 4.014.334, N° 4.034.758, y N° 4.077.407 de Theeuwes et al., N° 4.036.227 y N° 4.093.708 de Zaffaroni et al., describen que las sales osmóticas se utilizan mezcladas con un agente que posee solubilidad limitada en el fluido externo donde la sal osmótica forma una solución saturada que contiene el agente que es liberado osmóticamente desde el dispositivo. Las sales osmóticas son utilizadas por mezcla homogénea o heterogénea de la sal osmótica o una mezcla de ellas con un agente activo, ya sea antes de que se carguen en el depósito o por mezclado después de que se carguen en el depósito. Durante la operación, la sal osmótica atrae el fluido en el dispositivo produciendo una solución de la sal osmótica que se provee desde el dispositivo concomitantemente transportando agente no disuelto y disuelto al exterior del dispositivo. Las Patentes de EE UU. N° 6.248.359 y N° 6.599.532 de Faour, y N° 6.569.456, N° 6.572.890, N° 6.599.284, N° 6.599.532, N° 6.605.302, y N° 6.613.357 de Faour et al., y N° 6.521.255 de Vergez et al., describen que las sales osmóticas ayudarán tanto en la suspensión o disolución del fármaco activo en el núcleo. Las sales osmóticas pueden ser incorporadas al núcleo del dispositivo osmótico para controlar la liberación del fármaco activo del mismo. Todas las descripciones mencionadas anteriormente no describen que la velocidad de liberación del fármaco activo se reduce y el perfil de liberación del fármaco activo es modificado desde un orden a otro o desde una forma a otra por el incremento de la cantidad de sal osmótica en el núcleo.
La liberación controlada de agentes activos desde el dispositivo osmótico puede ocurrir según diferentes perfiles de liberación: primer orden, pseudo primer orden, orden cero, orden pseudo cero, sigmoideo, retrasado, velocidad constante de liberación, pulsátil y algunas combinaciones de los mismos. Típicamente, un fármaco debe tener una solubilidad dentro del intervalo de 50-300 mg/ml para poder ser liberada de forma efectiva por un dispositivo osmótico.
Es de conocimiento general que las sales de fármacos altamente solubles son difíciles de formular en dispositivos osmóticos. Cuanto más solubles son, generalmente son más difíciles de formular en dispositivos osmóticos. Esto es debido a que las sales de fármacos tienden a disolverse demasiado rápido conduciendo a la liberación prematura del fármaco, descarga del fármaco o una liberación rápida en vez de controlada del fármaco. Según McClelland et al. (Pharm. Res. (1991), 8(1), 88-92), los fármacos con una solubilidad en agua <50 mg/ml deberían ser liberados por un dispositivo osmótico de manera controlada para que >95% de la carga de fármaco se libere según una cinética de orden cero. Los fármacos con una solubilidad en agua alta (por ejemplo, >300 mg/ml) deberían ser liberados por un dispositivo osmótico de manera controlada para que sólo un pequeño porcentaje de la carga de fármaco se libere según una cinética de orden cero. Por lo tanto, McClelland et al. proponen la modulación de la solubilidad del fármaco en un intento de cambiar el perfil de liberación del fármaco de primer orden a orden cero. McClelland et al. indican específicamente que el NaCI debe estar presente en forma de liberación controlada como cristales de NaCI recubiertos con acetato butirato de celulosa para formar pequeñas bombas osmóticas. Ellos indican, "Este diseño bomba-en-una-bomba fue necesario para prevenir la rápida depleción, y la gran variación de concentración acompañante, del agente modulador de la solubilidad (cloruro de sodio) dentro del ambiente del núcleo del comprimido de hidrocloruro de diltiazem." Por consiguiente, McClelland et al. muestran que el efecto deseado proporcionado por el cloruro de sodio no puede ser logrado con cristales de cloruro de sodio sin recubrir. Aparentemente de acuerdo a McClelland et al. el cloruro de sodio sin recubrir se disuelve demasiado rápido para disminuir la velocidad de liberación del diltiazem.
Debido a la complejidad de las interacciones que ocurren dentro del núcleo de un dispositivo osmótico, no se ha
desarrollado ninguna postura aplicable generalmente para controlar y reducir la velocidad de disolución de fármacos muy solubles en agua. De hecho, algunos excipientes del dispositivo osmótico aceleran en vez de desacelerar la velocidad de liberación del fármaco.
La utilización de cloruro de sodio como osmoagente en un dispositivo osmótico es ampliamente conocida. La técnica generalmente muestra que el Incremento de la cantidad de osmoagente da como resultado un Incremento de la presión osmótica y por lo tanto un Incremento de la velocidad de liberación del fármaco desde el núcleo del dispositivo osmótico. La técnica anterior describe dispositivos osmóticos que tienen un núcleo bicapa o multicapa, en donde al menos una de las capas es de "empuje" o "desplazamiento" que comprende cloruro de sodio en combinación con un osmopolímero o un polímero hinchable en agua. El NaCI sirve para atraer agua dentro de la matriz polimérica, de esta manera humedeciendo e hinchando el polímero.
Se conoce un dispositivo osmótico que posee un núcleo unitario que comprende una sal farmacéuticamente aceptable de un fármaco en combinación con cloruro de sodio y otros excipientes. En particular, la técnica describe dispositivos osmóticos que poseen un núcleo unitario que comprende fármacos tales como hidrocloruro de pseudoefedrina (Johnson et al. en la Patente de EE.UU. N° 6.537.573; Faour et al. en la Patente de EE.UU. N° 6.004.582; Hamel et al. en la Patente de EE.UU. N° 4.801.461; Chen et al. en las Patentes de EE.UU. N° 5.458.887, N° 5.654.005, y N° 5.558.879), hidrocloruro de venlafaxina (Faour et al. en la Patente de EE.UU. N° 6.352.721), metansulfonato de reboxetina (Seroff et al. en la Patente de EE.UU. N° 6.387.403), carbamazepina (Puthli et al. en la Patente de EE.UU. N° 6.534.090), rofecoxib (Faour et al. en la Patente de EE.UU. N° 6.491.949), monohidrato de cisaprida (Faour et al. en la Patente de EE.UU. N° 6.004.582), nifedipina (Kettelhoit et al. en la Patente de EE.UU. N° 6.294.201); y otros fármacos (Chen et al. en las Patentes de EE.UU. N° 5.736.159 y 5.837.379) en combinación con cloruro de sodio y otros excipientes. La técnica también describe dispositivos osmóticos que poseen núcleos bicapa o multicapa, en donde una de las capas incluye un fármaco y cloruro de sodio entre otros excipientes (Wong et al. en la Patente de EE.UU. N° 5.785.994; Kuczynski et al. en la Patente de EE.UU. N° 5.866.164). Los dispositivos osmóticos que poseen un núcleo bicapa que comprende un fármaco activo y cloruro de sodio en la capa que contiene el fármaco se describen en la Patente de EE.UU. N° 6.352.721 de Faour, que describe alrededor de tres dispositivos osmóticos que contienen una capa del núcleo que comprende hidrocloruro de venlafaxina y cloruro de sodio, cisaprida y cloruro de sodio y nifedipina y cloruro de sodio, respectivamente,... [Seguir leyendo]
Reivindicaciones:
1. Un dispositivo osmótico que posee un núcleo unitario rodeado por una membrana semipermeable que posee al menos un pasaje en la misma caracterizado porque:
a) el núcleo unitario comprende una mezcla de sal de amantadina, sal osmótica y al menos otro excipiente farmacéuticamente aceptable;
b) la sal osmótica no está recubierta con un recubrimiento que controla la velocidad de liberación;
c) la permeabilidad de la membrana semipermeable se adapta para cooperar con la sal osmótica para controlar el perfil de liberación de la sal de amantadina del dispositivo osmótico;
d) la sal de amantadina y la sal osmótica poseen un ión en común; en donde la sal de amantadina es hidrocloruro de amantadina y la sal osmótica es cloruro de sodio;
e) la sal de amantadina se libera a través de la una o más pasajes según un perfil de liberación controlada sigmoideo, opcionalmente en donde la liberación de la sal de amantadina se retrasa durante un periodo de tiempo, cuando el dispositivo osmótico se expone a un ambiente acuoso de uso;
f) la relación en peso de sal de amantadina a sal osmótica varia de 4:1 a 30:1, la membrana semipermeable comprende un acetato de celulosa de grado 1 y un acetato de celulosa de grado 2, en donde la proporción en peso de acetato de celulosa de grado 1 a la cantidad total de acetatos de celulosa es de 0,3:1 a 0,7:1, y el dispositivo osmótico proporciona un perfil de liberación sigmoideo de sal de amantadina;
g) el acetato de celulosa comprende un acetato de celulosa de grado 1 que tiene 7-10% en peso de grupos hidroxilo, 30-36% en peso de grupos de acetilo y una viscosidad de 200-280 segundos, y un acetato de celulosa de grado 2 que tiene 3-5 % en peso de grupos hidroxilo, 37-43% en peso de grupos acetilo y una viscosidad de 6,0-45,0 segundos, determinándose dichas viscosidades como se establece en los métodos ASTM D817 (Fórmula A) y ASTM D1343; y
h) el núcleo unitario comprende menos de 6% de NaCI p/p, basado en el peso del núcleo sin recubrir, y la membrana semipermeable comprende más de 25% p/p de acetato de celulosa de grado 1, basado en el peso de la membrana semipermeable.
2. El dispositivo osmótico de la reivindicación 1, donde la membrana semipermeable posee una permeabilidad adaptada para cooperar con el cloruro de sodio en el núcleo de forma tal que el dispositivo osmótico proporcione un perfil de liberación sigmoideo para la amantadina.
3. El dispositivo osmótico de la reivindicación 1, que además comprende un recubrimiento externo que comprende un fármaco activo.
4. El dispositivo osmótico de la reivindicación 3, donde el fármaco activo es un antidepresivo.
5. El dispositivo osmótico de la reivindicación 4, donde el antidepresivo es citalopram.
6. El dispositivo osmótico de la reivindicación 3, donde el fármaco activo es un agente ansiolitico.
7. El dispositivo osmótico de la reivindicación 6, donde el agente ansiolitico es buspirona.
8. El dispositivo osmótico de la reivindicación 1, donde además comprende un segundo fármaco activo en el núcleo.
9. El dispositivo osmótico de la reivindicación 2, donde el segundo fármaco activo es un fármaco antiparkinsoniano.
10. El dispositivo osmótico de la reivindicación 9, donde el segundo fármaco antiparkinsoniano se selecciona del grupo que consiste de ropinirol, selegilina, y levodopa-carbidopa.
11. El dispositivo osmótico de la reivindicación 10, donde el segundo fármaco antiparkinsoniano es ropinirol.
12. El dispositivo osmótico de la reivindicación 10, donde el segundo fármaco antiparkinsoniano es selegilina.
13. El dispositivo osmótico de la reivindicación 10, donde el segundo fármaco antiparkinsoniano es levodopa- carbidopa.
14. Un dispositivo osmótico de la reivindicación 1, en donde:
a) el cloruro de sodio no está recubierto con un recubrimiento de control de la velocidad de liberación; y
b) el hidrocloruro de amantadina se libera del núcleo como sigue, en donde el ensayo del perfil de disolución ¡n vltro se realiza con un aparato de disolución de tipo II USP (palas), en 900 mi de agua destilada con una velocidad de agitación fija de 50 revoluciones por minuto, mantenida a una temperatura de 37±0,5°C. Las muestras se ensayaron mediante cromatografía de gas.
| Tiempo (horas) | Cantidad liberada |
| 0-3 | No menor que 5% |
| 0-5 | No menor que 18% |
| 0-8 | No menor que 39% |
| 0-16 | No menor que 76% |
15. El dispositivo osmótico de la reivindicación 1, en donde la amantadina se libera según el siguiente perfil en donde el ensayo del perfil de disolución in vitro se realiza con un aparato de disolución de tipo II USP (palas), en 900 mi de agua destilada con una velocidad de agitación fija de 50 revoluciones por minuto, mantenida a una temperatura de 37±0,5°C. Las muestras se ensayaron mediante cromatografía de gas.
| Tiempo | Fuñe, mínima | Fuñe, máxima |
| (h) | (%) | (%) |
| 0 | ||
Patentes similares o relacionadas:
Preparación sólida que contiene colorante, del 29 de Julio de 2020, de DAIICHI SANKYO COMPANY, LIMITED: Preparación farmacéutica sólida que comprende monobencenosulfonato de ácido [(1R,5S,6S)-6-(aminometil)-3- etilbiciclo[3.2.0]hept-3-en-6-il]acético […]
Formulación de vitamina D de liberación modificada estabilizada y método de administración de la misma, del 22 de Julio de 2020, de EirGen Pharma Ltd: Una formulacion oral de liberacion controlada de un compuesto de vitamina D que comprende uno o ambos de 25- hidroxivitamina D2 y 25-hidroxivitamina D3, la formulacion […]
Métodos y composiciones para la administración oral de proteínas, del 22 de Julio de 2020, de Entera Bio Ltd: Una única composición farmacéutica oral que comprende una proteína que tiene un peso molecular de hasta 100.000 Daltons, siendo dicha proteína PTH; […]
Composición farmacéutica que comprende un agente antipsicótico atípico y método para su preparación, del 15 de Julio de 2020, de PHARMATHEN S.A.: Comprimido de liberación controlada de Paliperidona en forma de comprimido de varias capas que comprende: a) un núcleo de matriz que comprende […]
Composiciones y métodos para tratar el virus de la hepatitis C, del 15 de Julio de 2020, de Gilead Pharmasset LLC: Una composición farmacéutica que comprende: a) de aproximadamente el 25% a aproximadamente el 35% p/p de GS-7977 cristalino que tiene la estructura **(Ver […]
Macrogols para aplicación a la mucosa, y sus usos terapéuticos, del 15 de Julio de 2020, de S.I.I.T. S.R.L.-SERVIZIO INTERNAZIONALE IMBALLAGGI TERMOSALDANTI: Composición farmacéutica en forma sólida que comprende, por unidad de dosificación, entre 5 y 400 mg de un PEG con un grado de 3000 o más, para uso en el tratamiento […]
Composición farmacéutica novedosa, del 1 de Julio de 2020, de NOVARTIS AG: Un comprimido farmaceutico que comprende: a) un farmaco que es el solvato con sulfoxido de dimetilo de N-{3-[3-ciclopropil-5-(2-fluoro-4-5 yodofenilamino)-6,8- dimetil-2,4,7-trioxo-3,4,6,7-tetrahidro-2H-pirido[4,3-d]pirimidin-1-il]fenil}acetamida […]
Preparación para el control del peso corporal a base de quitosano y celulosa, del 1 de Julio de 2020, de S.I.I.T. S.R.L.-SERVIZIO INTERNAZIONALE IMBALLAGGI TERMOSALDANTI: Una composición oral sólida que contiene una combinación de quitosano de hongos o levaduras, celulosa amorfa en polvo y opcionalmente excipientes.