NUEVOS CLONES VIRALES RECOMBINANTES BASADOS EN EL VIH Y USO DE LOS MISMOS EN MÉTODOS ANALÍTICOS.
La presente invención se refiere a clones vírales recombinantes basados en VIH que poseen la estructura general representada en la figura 8 y son el resultado de las siguientes manipulaciones genéticas:
-deleción de fragmentos de VIH (por ejemplo, gen Nef) sin perder capacidad infectiva, -inserción de un gen no expresado en células humanas, -inserción del gen LacZ, -introducción de sitios de restricción para extraer fragmentos de ADN del provirus matriz y sustituirlos por genes de pacientes a valorar. Asimismo, la invención se refiere a la aplicación de dichos clones en métodos analíticos relacionados con el SIDA.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/ES2005/000250.
Solicitante: FUNDACIÓN PARA LA INVESTIGACIÓN Y LA PREVENCIÓN DEL SIDA EN ESPAÑA.
Nacionalidad solicitante: España.
Inventor/es: ALCAMI PERTEJO,JOSE, GARCIA PEREZ,JAVIER, SANCHEZ PALOMINO,SONSOLES, GONZALEZ FERNANDEZ,NURIA.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C12N15/867 QUIMICA; METALURGIA. › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 15/00 Técnicas de mutación o de ingeniería genética; ADN o ARN relacionado con la ingeniería genética, vectores, p. ej. plásmidos, o su aislamiento, su preparación o su purificación; Utilización de huéspedes para ello (mutantes o microorganismos modificados por ingeniería genética C12N 1/00, C12N 5/00, C12N 7/00; nuevas plantas en sí A01H; reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00; nuevas razas animales en sí A01K 67/00; utilización de preparaciones medicinales que contienen material genético que es introducido en células del cuerpo humano para tratar enfermedades genéticas, terapia génica A61K 48/00; péptidos en general C07K). › Vectores retrovirales.
- C12Q1/70 C12 […] › C12Q PROCESOS DE MEDIDA, INVESTIGACION O ANALISIS EN LOS QUE INTERVIENEN ENZIMAS, ÁCIDOS NUCLEICOS O MICROORGANISMOS (ensayos inmunológicos G01N 33/53 ); COMPOSICIONES O PAPELES REACTIVOS PARA ESTE FIN; PROCESOS PARA PREPARAR ESTAS COMPOSICIONES; PROCESOS DE CONTROL SENSIBLES A LAS CONDICIONES DEL MEDIO EN LOS PROCESOS MICROBIOLOGICOS O ENZIMOLOGICOS. › C12Q 1/00 Procesos de medida, investigación o análisis en los que intervienen enzimas, ácidos nucleicos o microorganismos (aparatos de medida, investigación o análisis con medios de medida o detección de las condiciones del medio, p. ej. contadores de colonias, C12M 1/34 ); Composiciones para este fin; Procesos para preparar estas composiciones. › en los que intervienen virus o bacteriófagos.
PDF original: ES-2375652_T3.pdf
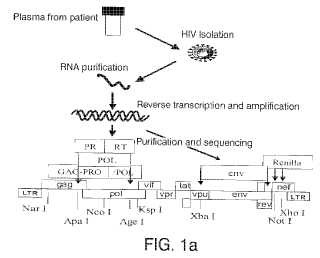
Fragmento de la descripción:
Nuevos clones virales recombinantes basados en el VIH y uso de los mismos en métodos analíticos.
Campo técnico de la invención
Dentro del amplio campo de la investigación que se está realizando en relación con el SIDA y más específicamente en el desarrollo de nuevas familias de fármacos, la presente invención se centra en la generación de algunos de los nuevos clones virales recombinantes basados en el genoma del Virus de la Inmunodeficiencia Humana (VIH) destinados para usarse ventajosamente en ensayos de sensibilidad a fármacos, ensayos de detección de anticuerpos neutralizantes, estudio de tropismo y capacidad replicativa viral y métodos de selección y caracterización de compuestos con actividad antiviral, etc.
Estado de la técnica anterior a la invención
En los últimos cinco años la evolución clínica de los pacientes infectados por el VIH ha mejorado espectacularmente gracias a la introducción de nuevas familias de fármacos antirretrovirales (Havlir y Lange, 1998) , y en consecuencia se ha producido una disminución en el número de casos de SIDA, de incidencia de infecciones oportunistas y de mortalidad como resultado de esta enfermedad.
Sin embargo, los éxitos conseguidos con dichos fármacos lamentablemente no han posibilitado la erradicación de la enfermedad dado que, a pesar de la disminución de la carga viral plasmática a niveles indetectables, la replicación viral persiste a bajo nivel en órganos linfoides (Chun y cols., 1997; Finzi y cols, 1997; Wong y cols., 1997) . Además, la carga proviral, que refleja el conjunto de linfocitos infectados por el VIH, no disminuye con tratamiento antirretroviral o lo hace muy lentamente. (Sharkey y cols., 2000; Ramratnam y cols., 2000) . Por último, la suspensión de la medicación antirretroviral conduce a una rápida subida de la carga viral a niveles basales, incluso en pacientes que se encontraban en supresión virológica aparentemente completa (<5 copias de ARN/ml) durante dos años (García y cols., 1999) . Todos estos datos sugieren que la perspectiva de erradicación del SIDA con los fármacos actualmente disponibles parece improbable (Ho. 1998; Wein y cols., 1998, Zhang y cols 1999; Furtado y cols., 1999, Pomerantz. 1999) . Esta posibilidad de erradicación conlleva el desarrollo a medio plazo de virus resistentes a los fármacos antirretrovirales utilizados en cada paciente.
En esta situación, continúan en marcha una serie de estrategias contra esta enfermedad que pueden resumirse en los siguientes puntos:
- Desarrollo de nuevos fármacos y, especialmente de nuevas familias de compuestos con dianas diferentes de
las contempladas actualmente por los fármacos antirretrovirales. -Desarrollo de vacunas terapéuticas y preventivas. -Desarrollo de estrategias de inmunoterapia dirigidas a reforzar el sistema inmunológico del paciente.
Concomitantemente al desarrollo de estas estrategias para combatir la enfermedad, es imprescindible el desarrollo de métodos y técnicas analíticas para evaluar estos nuevos enfoques: modelos de determinación de resistencias a antirretrovirales, caracterización biológica de aspectos cualitativos de la biología del virus y desarrollo de modelos para la generación de plataformas para exploración y caracterización de la actividad antiviral de nuevos compuestos. En los párrafos siguientes se hará referencia a algunos de los métodos analíticos que se están empleando en la actualidad, y en los que la presente invención tiene una especial incidencia por sus ventajosas aportaciones.
- Sistemas de determinación de resistencias fenotípicas a fármacos antirretrovirales.
Las determinaciones de resistencias fenotípicas no se realizan de forma rutinaria en los pacientes con infección por VIH que presentan fracaso virológico, debido a su extrema laboriosidad y elevado coste. Estos ensayos de resistencias fenotípicas se realizan habitualmente por un método seleccionado entre uno de los dos grupos de sistemas siguientes:
a, Sistemas clásicos: en una primera etapa, consisten en el aislamiento del VIH a partir de cultivos de linfocitos del paciente y, en un una segunda etapa, la infección de células diana en presencia de diferentes antirretrovirales para determinar la concentración inhibitoria de los fármacos (CI50) sobre un aislado concreto. Estos sistemas son terriblemente costosos, largos, tediosos y requieren sistemas de bioseguridad accesibles a muy pocos laboratorios de virología (Richman y cols., 1993; Nagy y cols., 1994) .
b: Sistemas basados en técnicas de recombinación genética. En esta tecnología, las secuencias del gen pol se amplifican en base al plasma del paciente y se transfectan junto con el provirus seleccionado en estas secuencias, en líneas celulares. Por medio de reacciones de ligamiento "in vivo", en el interior de estas células, se recombina un virus que lleva las secuencias Transcriptasa Inversa y Proteasa del virus del paciente. La progenie viral recombinante generada se utiliza para evaluar la CI50 en la infección de células diana. Existen distintas variantes de esta tecnología en cuanto a las secuencias y etapas de amplificación, células diana y utilización de marcadores (Boucher y cols., 1996; Hertogs y cols., 1998; Ruiz y cols, 1998; Little y cols., 1999; Borden y cols., 1999) . A pesar de estos desarrollos que simplifican los sistemas clásicos, las técnicas de ensayos de recombinación viral tienen limitaciones como las bajas tasas de recombinación in vivo y su coste y laboriosidad todavía elevados.
Debido a su complejidad y dificultades de normalización, los ensayos de resistencia fenotípica a fármacos antirretrovirales están disponibles en la práctica en un pequeño número de laboratorios y se utilizan esencialmente con fines diagnósticos.
Existe, por tanto, la necesidad de nuevas técnicas más sencillas y asequibles que permitan realizar estas determinaciones en cualquier laboratorio, de forma rápida, simple y económica.
- Sistemas para la determinación de la capacidad replicativa del VIH.
Entre las características cualitativas existentes entre los distintos aislados del VIH se encuentra la "capacidad replicativa" o "eficacia biológica" viral (Ruiz Jarabo y cols., 2002; Domingo y cols., 2001) . La eficacia biológica viral es el resultado final de un conjunto múltiple de características del virus en el proceso de adaptación a su hospedador. Sin embargo en algunas situaciones se ha observado que una eficacia biológica viral disminuida se asocia con la evolución clínica de la enfermedad (Tersmette y cols 1995; Learmont y cols 1995) . En particular, en un porcentaje elevado de pacientes supervivientes a largo plazo es extremadamente difícil aislar sus virus en cultivo debido a su baja capacidad replicativa (Cao y cols., 1995; Pantaleo y cols., 1995, Michael y cols., 1995) . Quizás de mayor relevancia clínica es el hecho de que virus de pacientes multirresistentes parecen replicar con una menor capacidad (Mammano y cols., 2000; Martinez-Picado y cols., 2000; Nijhuis y cols., 2001; Spira y cols., 2003) .
Los sistemas de determinación de eficacia biológica viral se basan en estudios de competencia en cultivo entre un virus silvestre y un virus que presenta diferentes mutaciones (Yuste y cols., 1999; Iglesias y cols., 2002) . Estos métodos requieren cultivos prolongados por lo que son extremadamente laboriosos, costosos y difíciles de normalizar. Sólo recientemente se ha propuesto la utilización de virus recombinantes para determinar la eficacia biológica viral (Deeks y cols., 2001; Barbour y cols., 2002) aunque esta técnica no se encuentra adecuadamente normalizada en el momento actual. Con el fin de poder evaluar de manera precisa la capacidad replicativa del virus, es imprescindible poder disponer de técnicas sencillas, fiables, asequibles y rápidas.
- Sistemas para la detección de la presencia de anticuerpos neutralizantes como parámetro de respuesta de eficacia de vacunas experimentales y de tratamientos inmunomoduladores.
La infección por un virus induce en el hospedador una doble respuesta inmune específica: activación de linfocitos citotóxicos y producción de anticuerpos (McMichael A., 2001; Burton DR., 2002) . De estos últimos, sólo los anticuerpos que bloquean la entrada del virus en la célula diana por distintos mecanismos poseen eficacia en el control de la infección. Este tipo de anticuerpos se denominan "neutralizantes" y la importancia de su papel en la infección por el VIH la han demostrado distintos trabajos en los últimos años (Burton DR., 2002; Moore J y Burton... [Seguir leyendo]
Reivindicaciones:
1. Clones virales recombinantes basados en VIH, caracterizados porque comprenden el gen Lacz clonado sustituyendo una secuencia del genoma, y porque comprenden una estructura general que contiene, en dirección 5' a 3, los siguientes elementos:
- secuencias LTR o terminales redundantes (R) que contienen numerosas secuencias consenso para factores de transcripción que regulan la expresión viral; -el gen gag -el gen pol cuyo extremo 5' solapa con el elemento gag; -el gen vif cuyo extremo 5' solapa con el elemento pol y su extremo 3' con el elemento vpr; -el gen vpr cuyo extremo 5' solapa con el elemento vif; -tat cuyo segundo exón está contenido dentro de la secuencia env; -el gen vpu; -el gen env; -el gen rev cuyo segundo exón está contenido dentro de la secuencia env; -el gen nef que codifica la proteína Nef, y que está truncado en las bases en las posiciones 8.796 y 8.887 del genoma viral; -NotI es un sitio de restricción para la enzima NotI, que se ha introducido por mutagénesis dirigida en la posición 8.796 del genoma viral; -XhoI es un sitio de restricción para la enzima XhoI, en la posición 8.887 del genoma viral; -Renilla es el gen que codifica la proteína indicadora luciferasa de Renilla y que se ha clonado en los sitios de restricción NotI-XhoI en las posiciones 5' y 3', respectivamente; y -LTR cuyo extremo 5' solapa con el extremo 3' del elemento nef.
2. Clon viral recombinante de acuerdo con la reivindicación 1, caracterizado porque dicho clon es el clon IP HIV NL LacZ/rt Ren, depositado en la Colección Española de Cultivos Tipo como CECT 5845, que posee un sitio único de restricción para la enzima NcoI, que se ha introducido por mutagénesis dirigida en la posición 2.593 de la secuencia de ADN, y el gen LacZ está clonado entre los sitios de restricción Ncol-Agel en las posiciones 5' y 3' respectivamente, sustituyendo el fragmento del gen pol que codifica la transcriptasa inversa.
3. Clon viral recombinante de acuerdo con la reivindicación 1, caracterizado porque dicho clon es el clon IP HIV NL LacZ/pr Ren, depositado en la Colección Española de Cultivos Tipo como CECT 5846, que posee un sitio único de restricción para la enzima NcoI, que se ha introducido por mutagénesis dirigida en la posición 2.593 en la secuencia de ADN, y el gen LacZ está clonado entre los sitios de restricción Apal-Ncol en las posiciones 5' y 3', respectivamente, sustituyendo el fragmento del gen pol que codifica la proteasa.
4. Clon viral recombinante de acuerdo con la reivindicación 1, caracterizado porque dicho clon es el clon IP HIV NL LacZ/pol Ren, depositado en la Colección Española de Cultivos Tipo como CECT 5847, que posee el gen LacZ clonado entre los sitios de restricción ApaI-Agel en las posiciones 5' y 3' respectivamente, sustituyendo el fragmento del gen pol que codifica la transcriptasa inversa.
5. Clon viral recombinante de acuerdo con la reivindicación 1, caracterizado porque dicho clon es el clon IP HIV NL LacZ/gag-pr Ren, depositado en la Colección Española de Cultivos Tipo como CECT 5848, que posee sitios únicos de restricción para las enzimas Narl y Kspl, introducida esta última por mutagénesis dirigida, en las posiciones 637 y 4.498, respectivamente, en la secuencia de ADN, y el gen Lacz está clonado entre los sitios de restricción Apal-Ncol en las posiciones 5' y 3', respectivamente, sustituyendo el fragmento del gen pol que codifica la proteasa.
6. Clon viral recombinante de acuerdo con la reivindicación 1, caracterizado porque dicho clon es el clon IP HIV NL LacZ/env Ren, depositado en la Colección Española de Cultivos Tipo como CECT 5844, que posee un sitio único de restricción, introducido por mutagénesis dirigida en la posición 6.112 de la secuencia de ADN y el gen LacZ está clonado en los sitios de restricción Xbal-Notl en las posiciones 5' y 3' respectivamente, sustituyendo al gen env.
7. El uso de clones virales recombinantes definidos en cualquiera de las reivindicaciones 1 a 6, en métodos analíticos in vitro para la determinación de resistencias fenotípicas a fármacos antirretrovirales para el tratamiento de infección por VIH.
8. El uso de clones virales recombinantes definidos en cualquiera de las reivindicaciones 1 a 6, en métodos analíticos in vitro para la determinación de la capacidad replicativa de virus recombinantes que portan secuencias gag, pol y/o env de pacientes con infección por VIH.
9. El uso de clones virales recombinantes definidos en la reivindicación 6, en métodos analíticos in vitro para la caracterización del tropismo viral en la infección por VIH.
10. El uso de clones virales recombinantes definidos en cualquiera de las reivindicaciones 1 a 6, en métodos analíticos in vitro para la detección de anticuerpos neutralizantes contra el VIH en suero de pacientes seropositivos
para el VIH y de sujetos no infectados, sometidos a vacunación.
11. El uso de clones virales recombinantes definidos en cualquiera de las reivindicaciones 1 a 6, en métodos analíticos in vitro para la selección y caracterización de compuestos con actividad antiviral contra el VIH.
Patentes similares o relacionadas:
Integración estable de los vectores de transferencia lentivirales SIN, del 20 de Mayo de 2020, de MOLMED SPA: Un sistema para la integracion estable de un vector de transferencia lentiviral autoinactivable (SIN) en una linea celular de empaquetamiento en donde […]
Polipéptidos para la ingeniería de proteínas integrasas quiméricas y su uso en terapia génica, del 12 de Febrero de 2020, de INSERM (INSTITUT NATIONAL DE LA SANTE ET DE LA RECHERCHE MEDICALE): Un polipéptido que consiste en la secuencia de aminoácidos seleccionada del grupo consistente en la SEQ ID NO:2 a la SEQ ID NO:12.
Aislador para mejorar vectores de transferencia génica, del 1 de Enero de 2020, de FUNDACIÓN PÚBLICA ANDALUZA PROGRESO Y SALUD: Molécula de ácido nucleico que comprende: a. la SEQ ID No 1 y la SEQ ID No 2, o una secuencia complementaria de las mismas; o b. una molécula […]
Vector retroviral que tiene actividad inmunoestimuladora, del 25 de Diciembre de 2019, de Tocagen Inc: Un vector retroviral gamma competente para la replicación recombinante que comprende: una proteína retroviral GAG; una proteína retroviral POL; una cubierta […]
Compuestos y métodos para incrementar la transferencia génica viral en células hematopoyéticas humanas, del 6 de Noviembre de 2019, de UNIVERSITE DE MONTREAL: Un método para transducir un vector viral en células, y dicho método comprende poner en contacto dichas células in vitro con un compuesto de […]
Vector dual para la inhibición del virus de la inmunodeficiencia humana, del 16 de Octubre de 2019, de Calimmune Inc: Una célula hospedadora preparada transduciendo una célula hematopoyética con un vector de expresión lentiviral, comprendiendo el vector de expresión lentiviral una primera […]
Vectores lentivirales pseudotipados, del 16 de Octubre de 2019, de Sirion Biotech GmbH: Partícula de vector lentiviral pseudotipada con (a) una proteína de fusión de glicoproteína de la envuelta del virus de la estomatitis vesicular (VSV-G) […]
Purificación de virus, del 16 de Octubre de 2019, de Oxford BioMedica (UK) Limited: Un proceso para producir una formulación de vector retroviral adecuada para la administración a un paciente, que comprende una etapa de esterilización por filtrado y una […]