Métodos y sistemas para la selección de portadores universales.
Un método que comprende:
a) usar un análisis genético combinado para analizar a una posible madre o a un posible padre de un niño potencial para determinar la presencia de una pluralidad de variantes genéticas causales correspondientes cada una a al menos una enfermedad genética mendeliana rara y la presencia de al menos un marcador informativo de ascendencia (AIM);
y
b) predecir una probabilidad de un fenotipo del niño potencial con respecto a la al menos una enfermedad genética mendeliana rara basándose al menos en parte, en la presencia de la pluralidad de variantes genéticas causales y la presencia del al menos un AIM, en donde dicha predicción comprende realizar un análisis totalmente probabilístico en los datos recogidos sobre dichas variantes genéticas causales, en donde la información obtenida de la presencia de al menos un AIM de la posible madre o el posible padre se usa para reducir la probabilidad de clasificación errónea de dichas variantes genéticas causales en el análisis genético combinado.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2009/003104.
Solicitante: Counsyl, Inc.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 180 KIMBALL WAY SOUTH SAN FRANCISCO, CA 94080 ESTADOS UNIDOS DE AMERICA.
Inventor/es: SRINIVASAN,BALAJI S, SRINIVASAN,BALAJI K, EVANS,ERIC, SRINIVASAN,RAMJI, BALAKRISHNAN,KUMARANAYAGAM.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- F41H1/02 MECANICA; ILUMINACION; CALEFACCION; ARMAMENTO; VOLADURA. › F41 ARMAS. › F41H BLINDAJE; TORRETAS ACORAZADAS; VEHICULOS BLINDADOS O ARMADOS; MEDIOS DE ATAQUE O DE DEFENSA, p. ej. ENMASCARAMIENTO, EN GENERAL. › F41H 1/00 Equipo de protección individual (escudos individuales F41H 5/08; contra la guerra química A62B). › Trajes blindados o a prueba de misiles o proyectiles; Tejidos de protección compuestos.
PDF original: ES-2528028_T3.pdf
Fragmento de la descripción:
Métodos y sistemas para la selección de portadores universales Antecedentes de la invención
Los análisis genéticos de padres potenciales se pueden usar para predecir la probabilidad de que la descendencia de una pareja tenga determinadas enfermedades genéticas. Personas para las cuales este ensayo es atractivo incluyen aquellos cuyas enfermedades genéticas se llevan en la familia o los pertenecientes a grupos étnicos que tienen una alta incidencia de enfermedades genéticas. Los resultados de estos análisis pueden proporcionar a una pareja información que pueden usar para tomar decisiones acerca de convertirse en padres. Por ejemplo, una pareja puede decidir hacer preparaciones para el cuidado especial que podría ser necesario para criar a un niño con necesidades especiales, o la pareja puede explorar opciones para la reproducción asistida. El documento W27/53752 describe métodos basados en ordenador y sistemas para facilitar la evaluación de resultados de análisis de selección genética.
Muchas enfermedades genéticas son raras en una población, por ejemplo, con frecuencias de menos de 1 en 1. Sin embargo, si una enfermedad genética está causada por un único alelo recesivo de un gen y ambos padres potenciales son portadores del alelo recesivo, entonces la probabilidad de que un niño de la pareja tenga la enfermedad es probablemente del 25 %.
La incidencia de alelos para ciertas enfermedades genéticas es diferente entre diferentes poblaciones. Por ejemplo, en personas con ascendencia judía asquenazí, la frecuencia portadora de la enfermedad de Tay-Sachs es de 1:3; para la enfermedad de Canavan es 1:4; para la enfermedad de Niemann-Pick tipo A es 1:9; para la anemia de Fanconi tipo C es 1:89; para el síndrome de Bloom es 1:1; para la enfermedad de Gaucher tipo 1 es 1:12. En las personas de ascendencia del sudeste asiático, la frecuencia portadora de alfa-talasemia es tan alta como 1:2. En los caucásicos, la frecuencia portadora de fibrosis quística es de 1:25.
Aunque estas enfermedades pueden ser raras individualmente, hay un número suficiente de ellas por lo que la probabilidad de que cualquier individuo sea portador de al menos una es significativamente mayor. Por ejemplo, se ha estimado que el 7 % de la población judía asquenazí tiene al menos un alelo causante de enfermedad. Las estimaciones de carga genética indican que todo ser humano porta de aproximadamente 8 a 3 alelos recesivos deletéreos.
La selección de portadores puede disminuir la incidencia de enfermedades genéticas en una población. Por ejemplo, como resultado de selección de portadores, la incidencia de la enfermedad de Tay Sachs entre la población judía asquenazí ha disminuido en los últimos años. Otro ejemplo de una enfermedad genética mendeliana es la fibrosis quística (CF). La fibrosis quística es a menudo fatal, debilitante e incurable, y costosa de tratar. CF se puede caracterizar por herencia autosómica recesiva y portada por individuos asintomáticos causada por cientos de mutaciones diferentes, cada una de las cuales varía en frecuencia entre los grupos étnicos. El Colegio Americano de Genética Médica (ACMG) recomienda la selección de portadores por análisis genético para todos los padres potenciales para varias enfermedades mendelianas. Desde 1998, se ha recomendado por el ACMG el cribado de toda la población panétnica para el estado portador de fibrosis quística. La lista de enfermedades que el ACMG recomienda ensayar se expande continuamente como una función de los nuevos descubrimientos relacionados con enfermedades genéticas. La selección de portadores se ha adoptado porque los beneficios para la salud son mayores que los costes financieros de ensayar por un margen definitivo.
Actualmente, la selección de los padres potenciales para el estado portador es selectiva. Está indicado para parejas pertenecientes a las poblaciones en riesgo aumentado de afecciones particulares. Hay una necesidad en la técnica de ensayo universal para una amplia diversidad de afecciones genéticas para individuos de cualquier ascendencia.
Sumario de la invención
El alcance de la presente invención se define por las reivindicaciones adjuntas 1 a 19. En un aspecto, se describe un método en este documento que comprende: ensayar un subconjunto de parientes biológicos de un niño o posible niño para determinar la presencia de una pluralidad de variantes genéticas causales correspondientes a al menos una enfermedad genética rara y la presencia de al menos un marcador informativo de ascendencia (AIM); y predecir una probabilidad de un fenotipo del niño o posible niño del subconjunto de parientes biológicos con respecto a la al menos una enfermedad genética rara basándose al menos en parte en la presencia de la pluralidad de variantes genéticas causales y la presencia del al menos un AIM. En algunos casos, la predicción comprende realizar un análisis totalmente probabilístico en los datos recogidos sobre dichas variantes genéticas causales. En algunos casos, la predicción se basa además en información fenotípica sobre al menos un miembro del subconjunto de parientes biológicos. El método puede comprender además la prestación de servicios de asesoramiento genético a al menos un miembro del subconjunto de parientes biológicos. El método puede comprender además la entrega de la probabilidad del fenotipo del niño a un servicio médico de referencia.
En un aspecto, un medio legible por ordenador comprende: lógica configurada para predecir una probabilidad de un fenotipo de un niño o posible niño a partir de un subconjunto de parientes biológicos con respecto a al menos una enfermedad genética rara basándose al menos en parte en los resultados de un ensayo del subconjunto de parientes biológicos para la presencia de una pluralidad de variantes genéticas causales y al menos un marcador informativo de ascendencia (AIM). En algunos casos, la lógica realiza un análisis totalmente probabilístico. En algunos casos, el medio legible por ordenador proporciona una salida en forma de un informe que detalla la presencia del al menos un AIM y la presencia de cualquiera de la pluralidad de variantes genéticas causales en cualquier miembro del subconjunto de parientes biológicos.
En un aspecto, un medio legible por ordenador comprende: lógica configurada para realizar un análisis totalmente probabilístico en los datos correspondientes a una pluralidad de variantes genéticas causales de un hombre y una mujer para predecir una probabilidad de un fenotipo de un niño, donde el hombre y la mujer son padres potenciales del niño. En algunos casos, las variantes genéticas causales de cada uno del hombre y la mujer comprenden uno o más marcadores informativos de ascendencia (AIM), una o más variantes genéticas causales correspondientes a una enfermedad genética rara, una o más variantes genéticas causales correspondientes a un rasgo de la personalidad, o ambos. En algunos casos, el análisis totalmente probabilístico incorpora una pluralidad de fuentes de incertidumbre estadística en la probabilidad. Un medio legible por ordenador en este documento puede comprender además lógica para recibir la entrada de una batería de fenotipos y la asignación de una función de ponderación a la pluralidad de variantes genéticas causales basad en dicha entrada. En algunos casos, la entrada de la batería fenotipos comprende: altura, peso, y la historia de la enfermedad familiar. En algunos casos, el medio legible por ordenador proporciona una salida en forma de un informe que detalla una distribución de probabilidad sobre los riesgos o fenotipos del niño.
En un aspecto, se describe un sistema en el presente documento para predecir un fenotipo de un niño que comprende: un dispositivo de detección de ácido nucleico configurado para detectar una pluralidad de variantes genéticas causales correspondientes a al menos una enfermedad genética rara y al menos un marcador informativo de ascendencia (AIM), donde el dispositivo está en contacto con una muestra de un pariente biológico de un niño o posible niño; un lector configurado para leer los datos de los dispositivos; e instrucciones legibles por ordenador, donde las instrucciones cuando se ejecutan utilizan los datos desde el lector correspondientes a la pluralidad de variantes genéticas causales y los datos del al menos un AIM para predecir una probabilidad de un fenotipo del niño con respecto a la al menos una enfermedad genética rara. En algunos casos, el pariente biológico es una madre potencial o padre potencial del niño o posible niño. En algunos casos, el dispositivo de detección de ácido nucleico comprende una pluralidad de sondas de ácido nucleico que se unen selectivamente a la pluralidad de variantes genéticas causales y el al menos... [Seguir leyendo]
Reivindicaciones:
1. Un método que comprende:
a) usar un análisis genético combinado para analizar a una posible madre o a un posible padre de un niño potencial para determinar la presencia de una pluralidad de variantes genéticas causales correspondientes cada una a al menos una enfermedad genética mendeliana rara y la presencia de al menos un marcador informativo de ascendencia (AIM); y
b) predecir una probabilidad de un fenotipo del niño potencial con respecto a la al menos una enfermedad genética mendeliana rara basándose al menos en parte, en la presencia de la pluralidad de variantes genéticas causales y la presencia del al menos un AIM, en donde dicha predicción comprende realizar un análisis totalmente probabilístico en los datos recogidos sobre dichas variantes genéticas causales, en donde la información obtenida de la presencia de al menos un AIM de la posible madre o el posible padre se usa para reducir la probabilidad de clasificación errónea de dichas variantes genéticas causales en el análisis genético combinado.
2. El método de cualquiera de las reivindicaciones anteriores, en el que la predicción en la etapa b) se basa adicionalmente en información fenotípica sobre la posible madre o el posible padre.
3. El método de cualquiera de las reivindicaciones anteriores que comprende analizar a una posible madre y a un posible padre del niño potencial.
4. El método de cualquiera de las reivindicaciones anteriores, en el que una pluralidad de las enfermedades genéticas tienen, cada una, una frecuencia de menos de 1 en 1 en seres humanos.
5. El método de cualquiera de las reivindicaciones anteriores, en el que la pluralidad de enfermedades genéticas raras es de más de 85 enfermedades genéticas mendelianas raras.
6. El método de la reivindicación 5, en el que la pluralidad de las enfermedades se seleccionan entre fibrosis quística, Tay Sachs, deficiencia en 21-hidroxilasa, hiperinsulinismo relacionado con ABCC8, ARSACS, acondroplasia, acromatopsia, adenosina monofosfato desaminasa 1, agenesia del cuerpo calloso con neuronopatía, alcaptonuria, deficiencia en alfa-1-antitripsina, alfa-manosidosis, alfa-sarcoglicanopatía, alfa-talasemia, receptor de angiotensina II, Tipo 1, argininosuccinicaciduria, aspartilglicosaminuria, ataxia con deficiencia de vitamina E, ataxia- telangiectasia, síndrome de poliendocrinopatía autoinmune tipo 1, síndrome de Bardet-Biedl, distrofia macular viteliforme de Best, beta-sarcoglicanopatía, beta-talasemia, deficiencia en biotinidasa, síndrome de Blau, síndrome de Bloom, trastornos relacionados con CFTR, lipofuscinosis ceroide neuronal relacionada con CLN3, lipofuscinosis ceroide neuronal relacionada con CLN5, lipofuscinosis ceroide neuronal relacionada con CLN8, enfermedad de Canavan, deficiencia en carnitina palmitoiltransferasa IA, deficiencia en carnitina palmitoiltransferasa II, hipoplasia de cartílago piloso, malformación cavernosa cerebral, coroideremia, síndrome de Cohén, cataratas congénitas, dismorfia facial y neuropatía, enfermedad congénita de glicosilación, trastorno congénito de glicosilación Ib, nefrosis congénita finlandesa, cistinosis, DFNA 9 (COCFI), distonía primaria de aparición temprana (DYTI), epidermólisis hullosa juntural tipo Flerlitz-Pearson, anemia de Fanconi relacionada con FANCC, craneosinostosis relacionada con FGFR1, craneosinostosis relacionada con FGFR2, craneosinostosis relacionada con FGFR3, trombofilia de Leiden de Factor V, trombofilia de mutación R2 de Factor V, deficiencia en Factor XI, deficiencia en Factor XIII, disautonomía familiar, hipercolesterolemia familiar Tipo B, fiebre mediterránea familiar, trastornos de almacenamiento de ácido siálico libre, demencia frontotemporal con Parkinsonismo-17, deficiencia en fumarasa, pérdida de audición y sordera no sindrómica DFNA3 relacionada con GJB2, pérdida de audición y sordera no sindrómica DFNB1 relacionada con GJB2, miopatías relacionadas con GNE, galactosemia, enfermedad de Gaucher, deficiencia en glucosa-6-fosfato deshidrogenasa, glutaricacidemia Tipo 1, enfermedad de almacenamiento de glucógeno Tipo 1a, enfermedad de almacenamiento de glucógeno Tipo II, enfermedad de almacenamiento de glucógeno Tipo III, enfermedad de almacenamiento de glucógeno Tipo V, síndrome de Gracile, hemocromatosis hereditaria asociada a PIFE, beta-talasemia de Hemoglobina S, intolerancia hereditaria a la fructosa, pancreatitis hereditaria, timina-uraciluria hereditaria, deficiencia en hexosaminidasa A, displasia ectodérmica hidrótica 2, homicistinuria causada por deficiencia en cistationina beta-sintasa, parálisis periódica hipercalémica Tipo 1, síndrome de hiperornitinemia-hiperamonemia-homocitrulinuria, hiperoxaluña primaria Tipo 1, hiperoxaluña primaria Tipo 2, hipocondroplasia, parálisis periódica hipocalémica Tipo 1, parálisis periódica hipocalémica Tipo 2, hipofosfatasia, acidemias isovaléñcas, enfermedad de Krabbe, LGMD2I, tipo franco-canadiense, deficiencia en 3- hidroxiacil de cadena larga-CoA deshidrogenasa, deficiencia en MTHFR, variante termolábil de MTHFR, pérdida de audición y sordera relacionada con MTTS1, poliposis asociada a MYH, enfermedad urinaria de jarabe de arce Tipo 1A, enfermedad urinaria de jarabe de arce Tipo 1B, deficiencia en acil de cadena media-Coenzima A deshidrogenasa, leucoencefalopatía megaloencefálica con quistes subcorticales, leucodistrofia metacromática, cardiomiopatía mitocondrial, síndrome de Leigh asociada a ADN mitocondñal y NARP, mucolipidosis IV, mucopolisacañdosis tipo I, mucopolisacañdosis Tipo NIA, mucopolisacañdosis Tipo Vil, neoplasia endocrina múltiple Tipo 2, enfermedad de músculo-ojo-cerebro, miopatía nemalínica, enfermedad Niemann-Pick debida a deficiencia en esfingomielinasa, enfermedad de Niemann-Pick Tipo C1, síndrome de rotura de Nijmegen, lipofuscinosis ceroide neuronal relacionada con PPT1, deficiencia en hormona de la pituitaria relacionada con PROP1, Síndrome de
Pallister-Hall, paramiotonía congénita, síndrome de Pendred, deficiencia en la enzima bifuncional peroxisomal, deficiencia en fenilalanina hidroxilasa, inhibidor I del activador del plasminógeno, enfermedad renal poliquística, autosómica recesiva, trombofilia de protrombina G221A, picnodisostosis, retinitis pigmentosa, autosómica recesiva, Tipo Botnia, síndrome de Rett, condrodisplasia punteada rizomélica Tipo 1, deficiencia en acil de cadena corta-CoA deshidrogenasa, síndrome de Shwachman-Diamond, síndrome de Sjogren-Larsson, síndrome de Smith- Lemli-Opitz, paraplejia espástica 13, osteocondrodisplasia relacionada con transportador de sulfato, hemocromatosis hereditaria relacionada con TFR2, lipofuscinosis ceroide neuronal relacionada con TPP1, displasia tanatofórica, amiloidosis de transtiretina, deficiencia en proteína trifuncional, DRD deficiente en tirosina hidroxilasa, tirosinemia Tipo I, enfermedad de Wilson, retinosquisis juvenil ligada a X y espectro de síndrome de Zellweger.
7. El método de cualquiera de las reivindicaciones anteriores, en el que la pluralidad de variantes genéticas causales corresponden a una o más enfermedades genéticas para las cuales la población de Asia oriental está en riesgo aumentado, una o más enfermedades genéticas para las cuales la población de África subsahariana está en riesgo aumentado y una o más enfermedades genéticas para las cuales la población de Eurasia occidental está en riesgo aumentado.
8. El método de la reivindicación 7 en el que:
(i) el riesgo aumentado es al menos 1 veces en comparación con otras poblaciones, o
(ii) la población de Eurasia occidental se selecciona entre las subpoblaciones europea, asiática occidental/central, asiática meridional, y norteafricana, o
(iii) la población de Asia oriental se selecciona entre las subpoblaciones china, japonesa y coreana.
9. El método de cualquiera las reivindicaciones 1-6, en el que las variantes genéticas causales corresponden a una o más enfermedades genéticas para las cuales la población de nativos americanos están en riesgo aumentado o una o más enfermedades para las cuales la población de judíos asquenazíes están en riesgo aumentado.
1. El método de cualquiera de las reivindicaciones anteriores, en el que al menos un AIM no es una variante genética causal.
11. El método de cualquiera de las reivindicaciones anteriores, en el que los AIM incluyen al menos un AIM que distingue poblaciones africanas y europeas, al menos un AIM que distingue poblaciones africanas y asiáticas y al menos un AIM que distingue poblaciones europeas y asiáticas.
12. El método de la reivindicación 11, en el que los AIM incluyen al menos un AIM que distingue poblaciones africanas y americanas, poblaciones europeas y americanas, poblaciones asiáticas y americanas, poblaciones noreuropeas y sureuropeas, poblaciones noreuropeas y judías asquenazíes, poblaciones sureuropeas y judías asquenazíes, poblaciones irlandesas e inglesas, poblaciones hispanas y caucásicas, poblaciones chinas y japonesas, o poblaciones surasiáticas, centroasiáticas y asiáticas orientales.
13. El método de cualquiera de las reivindicaciones anteriores, en el que los AIM se seleccionan entre AIM de la Figura 3.
14. El método de la reivindicación 1, en el que el ensayo comprende el uso de una serie de ácidos nucleicos, secuenciación por hibridación, secuenciación por ligamiento, secuenciación por extensión, secuenciación de Sanger, secuenciación de Maxam Gilbert o pirosecuenciación.
15. Un medio legible por ordenador que comprende un código informático que cuando se ejecuta predice una probabilidad de un fenotipo de un niño potencial, a partir de la posible madre o del posible padre, con respecto a al menos una enfermedad genética mendeliana rara, basada al menos en parte en los resultados de un análisis de la posible madre o del posible padre para la presencia de una pluralidad de variantes genéticas causales y al menos un marcador informativo de ascendencia (AIM),
en el que la probabilidad de un fenotipo del niño potencial se calcula de acuerdo con el método de una cualquiera de las reivindicaciones 1 a 13.
16. Un sistema para predecir un fenotipo de un niño que comprende:
un dispositivo de detección de ácido nucleico combinado configurado para detectar una pluralidad de variantes genéticas causales correspondientes a al menos una enfermedad genética mendeliana rara y al menos un marcador informativo de ascendencia (AIM), en donde el dispositivo está en contacto con una muestra de una posible madre o de un posible padre de un niño potencial; un lector configurado para leer los datos de los dispositivos; y un medio legible por ordenador de acuerdo con la reivindicación 15.
17. Un sistema para indicar si un sujeto es portador de una enfermedad genética mendeliana rara que comprende: un lector configurado para leer los datos de un dispositivo de detección de ácido nucleico combinado configurado
para detectar una pluralidad de variantes genéticas causales correspondientes a al menos una enfermedad genética mendeliana rara y al menos un marcador informativo de ascendencia (AIM), y un medio legible por ordenador de acuerdo con la reivindicación 15.
18. Un método que comprende:
recibir una muestra de un usuario;
analizar la muestra con un dispositivo de detección de ácido nucleico combinado configurado para analizar una pluralidad de variantes genéticas causales de enfermedades genéticas mendelianas raras y al menos un 1 marcador informativo de ascendencia (AIM);
calcular una pluralidad de probabilidades para los posibles genotipos del usuario en cada localización de la pluralidad de variantes genéticas causales basándose en los resultados de la etapa de análisis respecto a la pluralidad de variantes genéticas causales y el al menos un AIM,
en donde dicho cálculo comprende realizar un análisis totalmente probabilístico en los datos recogidos sobre 15 dichas variantes genéticas causales, en donde la información obtenida del al menos un AIM respecto a la ascendencia del usuario se usa para reducir la probabilidad de clasificación errónea de dichas variantes genéticas causales en el dispositivo de detección de ácido nucleico combinado; y entregar al usuario la pluralidad de probabilidades correspondientes al usuario que es portador.
19. El método de cualquiera de las reivindicaciones 1-14, en el que al menos dos de las enfermedades genéticas
mendelianas raras ocurren a frecuencias que difieren en al menos 1 veces en al menos dos poblaciones distintas, en donde las al menos dos poblaciones distintas se diferencian en al menos un AIM.
Patentes similares o relacionadas:
Unidad de prenda protectora y su uso, del 3 de Junio de 2020, de BLUCHER GMBH: Unidad de prenda protectora textil con protección frente a esquirlas y fragmentos y/o con función protectora balística, preferentemente con función protectora […]
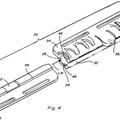 Aparato y método de ensamblaje y liberación de prenda, del 25 de Marzo de 2020, de FirstSpear, LLC: Un aparato de ensamblaje y liberación para una prenda, que comprende:
un clip con forma de C que define un canal y una ranura […]
Aparato y método de ensamblaje y liberación de prenda, del 25 de Marzo de 2020, de FirstSpear, LLC: Un aparato de ensamblaje y liberación para una prenda, que comprende:
un clip con forma de C que define un canal y una ranura […]
Prenda de vestir textil con un equipamiento de protección balística, del 4 de Marzo de 2020, de HEXONIA GMBH: Prenda de vestir textil con un equipamiento de protección balística con una pieza de torso y piezas de brazo, en la que la pieza de torso es […]
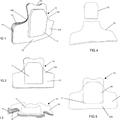 Elemento de protección balística para chaleco antibalas, del 25 de Septiembre de 2019, de Paul Boye Technologies: Elemento de protección balística destinado a la protección del torso y/o de la espalda de un individuo, dicho elemento :
- que […]
Elemento de protección balística para chaleco antibalas, del 25 de Septiembre de 2019, de Paul Boye Technologies: Elemento de protección balística destinado a la protección del torso y/o de la espalda de un individuo, dicho elemento :
- que […]
Dispositivo de absorción de choques, del 28 de Agosto de 2019, de SAES GETTERS S.P.A.: Dispositivo de absorción de choques, que comprende una pluralidad de elementos (11, 11', ..., 11n, 12, 12', ..., 12n) fabricados de un material […]
Cinta de fibra híbrida unidireccional y laminados compuestos, del 15 de Abril de 2019, de HONEYWELL INTERNATIONAL INC.: Un material con resistencia balística que comprende al menos una capa híbrida, cuya capa híbrida comprende una pluralidad de fibras o una […]
Arnés, del 4 de Abril de 2019, de THALES HOLDINGS UK PLC: Un arnés , que comprende: una correa para rodear al menos parcialmente la cintura de un usuario, comprendiendo la correa al menos un cable; […]
Casco con una capa intermedia de fricción que disminuye el material, del 20 de Marzo de 2019, de Mips AB: Un casco que comprende: una capa externa y una capa interna , en el que las capas externa e interna son móviles entre sí; y una […]