Método para preparar una lámina de fibrina sólida.
Un método para preparar una lámina de fibrina sólida, incluyendo el método:
extraer sangre de un paciente;
separar plasma de la sangre; y
concomitantemente coagular y centrifugar axialmente el plasma para formar la lámina de fibrina sólida, siendo adecuada la lámina de fibrina sólida para regenerar tejido corporal en un organismo vivo.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2003/020163.
Solicitante: Beretta, Roberto.
Nacionalidad solicitante: Italia.
Dirección: Via Rho, 8 20125 Milano ITALIA.
Inventor/es: GRIPPI, NICHOLAS A., BERETTA,ROBERTO.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61L24/10 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61L PROCEDIMIENTOS O APARATOS PARA ESTERILIZAR MATERIALES U OBJECTOS EN GENERAL; DESINFECCION, ESTERILIZACION O DESODORIZACION DEL AIRE; ASPECTOS QUIMICOS DE VENDAS, APOSITOS, COMPRESAS ABSORBENTES O ARTICULOS QUIRURGICOS; MATERIALES PARA VENDAS, APOSITOS, COMPRESAS ABSORBENTES O ARTICULOS QUIRURGICOS (conservación de cuerpos o desinfección caracterizada por los agentes empleados A01N; conservación, p. ej. esterilización de alimentos o productos alimenticios A23; preparaciones de uso medico, dental o para el aseo A61K). › A61L 24/00 Adhesivos o cementos quirúrgicos; Adhesivos para dispositivos de colostomía (adhesivos conductores de la electricidad que se utilizan en terapia o examen en vivo A61K 50/00). › Polipéptidos; Proteínas.
PDF original: ES-2524444_T3.pdf
Fragmento de la descripción:
Método para preparar una lámina de fibrina sólida Antecedentes de la invención
La presente invención se refiere a métodos para preparar una lámina de fibrina sólida o cola de fibrina autóloga.
Es sabido que la cola de fibrina es un hemoderivado en gran parte que se usa como un adhesivo quirúrgico tópico o un agente hemostático. Hay disponibles en el mercado varios kits que contienen fibrinógeno concentrado de donantes, asociado a un activador proteico de origen humano o animal, tal como trombina o batroxobina, para obtener cola de fibrina heteróloga.
Tales kits conocidos implican el uso de material de origen humano o animal, que, debido a su origen, podría dar lugar a posible contaminación viral y a graves riesgos para el receptor de la cola de fibrina. Las autoridades se han visto obligadas en el pasado a quitar del comercio o incluso prohibir los hemoderivados obtenidos usando material de origen humano o animal. Además, se conocen en la literatura casos de rechazo resultantes de reimplantar fibrina producida usando proteínas humanas o animales en pacientes. De hecho, tales casos son debidos al origen heterólogo, con respecto al organismo receptor, de la proteína sellante reimplantada o algunos de los componentes usados para prepararla.
La cola de fibrina autóloga, es decir, cola de fibrina obtenida autológicamente a partir de la propia sangre del paciente, es más fiable con respecto a los riesgos de rechazo y/o infección. Ya se han descrito varios procedimientos para obtener cola de fibrina autóloga extemporánea, pero no hay disponible en el mercado kit preparado para uso aunque se puede hallaren la literatura de patentes algunas referencias relevantes.
La Patente de Estados Unidos número 5.733.545 describe un concentrado de plasma-capa leucocitaria a combinar con un activador fibrinógeno para formar un sellante de heridas de cola de plaquetas. El método descrito en esta patente permite procesar la sangre del paciente con el fin de obtener cola de fibrina autóloga, pero los métodos utilizan trombina o batroxobina como el activador fibrinógeno. Estos activadores son de naturaleza humana o animal y por lo tanto siguen implicando el riesgo de rechazo y/o infecciones virales para el paciente.
La Patente de Estados Unidos número 6.368.298 describe la preparación de cola de fibrina autóloga tratando plasma separado con un activador de coagulación de calcio (cloruro de calcio) en un kit preparado para el uso. La Patente de Estados Unidos número 5.853.6 describe un método para la separación rápida, por centrifugación axial, de suero y plasma usando un tubo de muestra cilindrico que tiene nervios internos que se extienden longitudinalmente. La publicación no potente C. A. Estey, R. A. Felder, Clinical Chemistry 1996, 42(3), 42-49 se refiere a pruebas clínicas realizadas usando separación axial y describe las mejoras de la producción y la variedad de análisis sobre los métodos de separación convencionales por centrifugación.
La Patente de Estados Unidos número 5.555.7 describe un método y un aparato para hacer plasma concentrado a usar como un sellante de tejidos. El método consiste en separar plasma de sangre entera y extraer agua de dicho plasma poniéndolo en contacto con un concentrador para obtener plasma concentrado que a continuación puede ser coagulado con una solución conteniendo trombina y calcio. El aparato incluye un primer separador centrífugo en una primera cámara, un concentrador (por ejemplo, dextranómero o polacrilamida) incluido en una segunda cámara que comunica con la primera cámara, y un segundo separador. El método descrito en esta referencia requiere un largo tiempo para obtener el concentrado de plasma necesario para la posterior preparación de cola de fibrina autóloga y el aparato es caro y no desechable. El método no describe el uso de un activador de coagulación de calcio, y requiere un paso de preconcentración.
Muchos métodos y sistemas requieren la transferencia de un fluido de un recipiente a otro. Por ejemplo, muchos dispositivos químicos y médicos requieren la transferencia de un volumen necesario de líquido a reaccionar secuencialmente con varios reactivos y alícuotas volumétricas específicas. Una práctica común es quitar cierres en dos recipientes y pipetar líquido de un recipiente al otro. Sin embargo, esta práctica expone la muestra a contaminantes medioambientales. Por ejemplo, se usa esta técnica para transferir plasma que ha sido separado de glóbulos rojos en una muestra de sangre. Sin embargo, se precisa una técnica especial para extraer el plasma en el menisco de interfaz. Con frecuencia, los glóbulos rojos de fracción inferior, de alta densidad, indeseables contaminan la muestra aspirada. Para evitar este problema, la pipeta se mantiene frecuentemente a una distancia segura del menisco (es decir, el separador entre el plasma y los glóbulos rojos), dando lugar por ello a una transferencia incompleta de la muestra. La transferencia incompleta de la fracción deseable da lugar a rendimiento de volumen inferior al óptimo y relaciones no estequiométricas de los reactivos de la muestra y los del segundo recipiente. Esta segunda condición puede ser una fuente importante de variación del rendimiento del producto. Éste es el caso de muchas reacciones enzimáticas en las que las tasas de reacción son un máximo en algunas relaciones estequiométricas y disminuyen rápidamente a relaciones más altas o más bajas.
El cuidado de las heridas es una de las cuestiones más importantes en medicina, especialmente con respecto a
úlceras crónicas, fístulas, etc. Esta cuestión es Importante no solamente a causa del alto costo de la gestión, sino también a causa de la baja tasa de éxito. Otros problemas asociados con el cuidado de heridas y quemaduras incluyen la pérdida de líquidos y la posibilidad de que se produzcan Infecciones. Se ha usado membranas sintéticas o de origen animal para separar las cavidades óseas de los tejidos blandos en el proceso de reosificación.
Un tratamiento para el cuidado de heridas puede Incluir aplicar tejidos biológicos o esponjas (generalmente a base de proteínas) de origen animal, por ejemplo, colágeno, fibrina, albúmina al lugar de la herida. Sin embargo, las respuestas alérgicas e inmunológlcas son comunes en estas aplicaciones.
El cincuenta por ciento de estos casos no se resuelven con una sola aplicación. Más del veinte por ciento puede no resolverse ni siquiera después de dos aplicaciones.
Otro tratamiento incluye trasplante de piel, que se realiza en los casos más difíciles. Sin embargo, el trasplante de piel es caro, y puede costar alrededor de $6-7 por aplicación. Se usa una malla de colágeno de caballo modificado para soportar el nuevo tejido autólogo. La aplicación es un proceso difícil que puede durar hasta 2 días para cultivo de tejido dérmico, con la posibilidad de contaminar la muestra, en relación con las dimensiones.
En general, se desean métodos y sistemas para preparar cola de fibrina autóloga o una fibrina sólida que sea capaz de regenerar tejido en un organismo vivo.
Descripción detallada de los dibujos
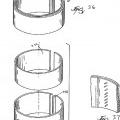
La figura 1 es una vista en perspectiva de una primera realización comparativa.
La figura 2 es una vista en sección transversal de un recipiente primario de la primera realización comparativa representada en la figura 1.
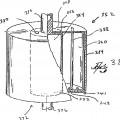
La figura 3 es una vista en sección transversal de una realización comparativa diferente del recipiente primario de la figura 2.
La figura 4 es una vista en sección transversal de una realización comparativa diferente del recipiente primario de la figura 2.
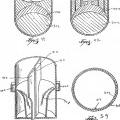
La figura 5 es una vista en sección transversal parcial ampliada de una porción de la primera realización comparativa de la figura 1 que ¡lustra un primer extremo de un dispositivo de transferencia comenzando a perforar un recipiente primario sellado.
La figura 6 es una vista similar a la expuesta en la figura 5 que ilustra el primer extremo del dispositivo de transferencia perforando completamente el recipiente primario sellado y un segundo extremo del dispositivo de transferencia perforando completamente un recipiente primario secundario sellado.
La figura 7 es una vista similar a la figura 2 que representa el tubo primario y su contenido invertido.
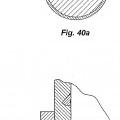
La figura 8 es una vista en planta superior de la primera realización comparativa representada en la figura 1.
La figura 9 es una vista en sección transversal parcial de la figura 8 que representa el recipiente primario, el recipiente secundario y el dispositivo de transferencia enganchados, y siendo transferido el contenido del primer recipiente al segundo recipiente.
La figura 1 es una vista en planta superior de... [Seguir leyendo]
Reivindicaciones:
1. Un método para preparar una lámina de fibrina sólida, incluyendo el método: extraer sangre de un paciente;
separar plasma de la sangre; y
concomitantemente coagular y centrifugar axialmente el plasma para formar la lámina de fibrina sólida, siendo adecuada la lámina de fibrina sólida para regenerar tejido corporal en un organismo vivo.
2. El método para preparar una lámina de fibrina sólida según la reivindicación 1, donde se usa un dispositivo para preparar una lámina de fibrina sólida, incluyendo el dispositivo:
una cámara primaria;
una cámara secundaria conteniendo un coagulador; y
un medio que separa la cámara primaria de la cámara secundaria, usándose el dispositivo en centrifugación axial.
3. El método para preparar una lámina de fibrina sólida según las reivindicaciones 1 o 2, donde el plasma separado de la sangre contiene calcio endógeno y el método incluye además:
poner el plasma en contacto con un anticoagulante; y
poner el plasma en contacto con un coagulador incluyendo una especie catiónica que tiene una afinidad igual o más alta al anticoagulante que al calcio endógeno.
4. El método para preparar una lámina de fibrina sólida según la reivindicación 3, donde la especie catiónica incluye al menos uno de magnesio, manganeso, zinc y una combinación de los mismos.
5. El método para preparar una lámina de fibrina sólida según la reivindicación 3, donde la especie catiónica incluye calcio.
6. El método para preparar una lámina de fibrina sólida según la reivindicación 3, donde la especie catiónica incluye al menos uno de cloruro de calcio, fluoruro de calcio, carbonato de calcio, gluconato de calcio, fumarato de calcio, piruvato de calcio, y una combinación de los mismos.
7. El método para preparar una lámina de fibrina sólida según las reivindicaciones 1 o 2, donde la lámina de fibrina sólida incluye además un agente mejorador terapéutico.
8. El método para preparar una lámina de fibrina sólida según la reivindicación 7, donde el agente mejorador terapéutico incluye al menos uno de un antibiótico, analgésico, terapéutico contra el cáncer, factor de crecimiento de plaquetas, proteína morfogénica ósea, célula madre, material de injerto óseo, injerto de tejido blando, material de cultivo de células, inmunosupresor, y una combinación de los mismos.
9. El método para preparar una lámina de fibrina sólida según la reivindicación 7, donde el agente mejorador terapéutico incluye un antibiótico, y el antibiótico incluye al menos uno de ampicilina, eritromicina, tobramicina y una combinación de las mismas.
1. El método para preparar una lámina de fibrina sólida según la reivindicación 7, donde el agente mejorador terapéutico incluye un analgésico, y el analgésico incluye al menos uno de aspirina, codeína y una combinación de
las mismas.
11. El método para preparar una lámina de fibrina sólida según la reivindicación 7, donde el agente mejorador terapéutico incluye material de injerto óseo, y el material de injerto óseo incluye al menos uno de hueso autólogo, aloinjerto de cadáver, homoinjerto de cadáver, hueso de origen animal, injerto óseo sintético, compuesto ortobiológico, proteína morfogénica ósea (BMP), proteína morfogénica ósea humana recombinante (rhBMP), y una combinación de los mismos.
12. El método para preparar una lámina de fibrina sólida según la reivindicación 7, donde el agente mejorador terapéutico incluye al menos uno de piel, materiales de injerto cutáneo, injerto gingival, colágeno, un injerto bioabsorbible, un injerto vascular, un factor de crecimiento derivado de plaquetas, Factor 4 de plaqueta (PF4), tromboglobulina, trombospondina, y una combinación de los mismos.
13. El método para preparar una lámina de fibrina sólida según la reivindicación 7, donde el agente mejorador
terapéutico incluye al menos uno de un inmunosupresor para trasplantes de órganos y un inmunosupresor cutáneo.
14. El método para preparar una lámina de fibrina sólida según la reivindicación 7, donde la membrana de fibrina sólida incluye células vivas para expresión de moléculas deseadas, terapia génica y terapia celular.
15. El método para preparar una lámina de fibrina sólida según la reivindicación 7, donde la lámina de fibrina sólida se ha de usar para regenerar tejido en un organismo vivo.
Patentes similares o relacionadas:
Parche adhesivo de tejidos basado en fibrinógeno mejorado, del 3 de Julio de 2019, de Sealantium Medical Ltd: Un parche adhesivo de tejidos basado en fibrinógeno, en donde dicho parche adhesivo comprende: un refuerzo preparado a partir de una película preparada a partir […]
Material sellante seco de acción rápida y métodos para su uso y fabricación, del 3 de Mayo de 2019, de BAXTER INTERNATIONAL INC.: Composición seca para conseguir la hemostasis o la contención de otro fluido en un contexto in vivo de matriz para aplicar a un vertebrado con el fin de facilitar la contención […]
Colágeno modificado, del 24 de Abril de 2019, de Innocoll Pharmaceuticals Limited: Un colágeno maduro que se puede obtener proporcionando colágeno aislado, congelando el colágeno aislado, deshidratando el colágeno congelado y madurando el […]
Composiciones proteicas de fase reversible biocompatible y métodos para prepararlas y usarlas, del 8 de Marzo de 2019, de BAXTER INTERNATIONAL INC.: Una composición de fase reversible biocompatible que pasa de un primer estado fluido a un segundo estado no fluido, en la que dicha composición […]
Adhesivo de fibrina de un componente que comprende un inhibidor de la polimerización, del 4 de Marzo de 2019, de OMRIX BIOPHARMACEUTICALS LTD.: Una formulación de sellante líquida que comprende monómeros de fibrina a una concentración del 1 al 13% (p/v) y un péptido GPRP; en la que el […]
Métodos para obtener hidrogeles liofilizados superabsorbentes para aplicaciones médicas, del 14 de Febrero de 2019, de INCEPT LLC: Un método para obtener hidrogel superabsorbente, que comprende: formar una mezcla combinando componentes precursores para iniciar la reticulación […]
NOVEDOSOS AGENTES RETICULANTES DE ÁCIDO FÍTICO, del 14 de Diciembre de 2018, de CONSEJO SUPERIOR DE INVESTIGACIONES CIENTIFICAS (CSIC): Novedosos agentes reticulantes de ácido fítico. La presente invención describe membranas novedosas, estables y biodegradables de proteínas y/o polisacáridos, particularmente […]
Adhesivo biológico libre de trombina y su utilización como medicamento, del 4 de Octubre de 2018, de LABORATOIRE FRANCAIS DU FRACTIONNEMENT ET DES BIOTECHNOLOGIES SOCIETE ANONYME: Adhesivo biológico líquido monocompuesto, estable, es decir que no forma fibrina, durante 24 horas a 37°C, para uso terapéutico por aplicación local, libre de trombina, […]