Método para evaluar la eficacia de los medios de cultivo embrionario, empleados en procesos de fecundación y cultivo in vitro, basado en la capacidad de los embriones para unir factores de crecimiento epidérmico.
La presente invención contempla un método para evaluar la eficacia de los medios de cultivo embrionario,
empleados en procesos de fecundación y cultivo in vitro, basado en la capacidad de los embriones para unir factores de crecimiento epidérmico, caracterizado porque comprende las siguientes etapas: a) Obtención de embriones no humanos por fecundación in vitro o in vivo, b) Desarrollo de los embriones hasta el estadio de blastocisto, c) Cultivo de los embriones obtenidos en a) y b) en un medio de cultivo con factores de crecimiento epidérmico conjugados a fluorocromo y d) Medición de la cantidad de factor de crecimiento conjugado a fluorocromo, unida a la superficie de los embriones cultivados en c), donde una intensidad de fluorescencia más elevada, se relaciona con unas condiciones de cultivo óptimas.
Tipo: Patente de Invención. Resumen de patente/invención. Número de Solicitud: P201231895.
Solicitante: UNIVERSIDAD DE EXTREMADURA.
Nacionalidad solicitante: España.
Inventor/es: ÁLVAREZ MIGUEL,Ignacio Santiago, PERIANES CARRASCO,Mario Javier, MARTÍN ROMERO,Francisco Javier.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K38/18 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 38/00 Preparaciones medicinales que contienen péptidos (péptidos que contienen ciclos beta-lactama A61K 31/00; dipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina 2,5-dionas, A61K 31/00; péptidos basados en la ergolina A61K 31/48; que contienen compuestos macromoleculares que tienen unidades aminoácido repartidas estadísticamente A61K 31/74; preparaciones medicinales que contienen antígenos o anticuerpos A61K 39/00; preparaciones medicinales caracterizadas por los ingredientes no activos, p. ej. péptidos como soportes de fármacos, A61K 47/00). › Factores de crecimiento; Reguladores de crecimiento.
- C12N5/073 QUIMICA; METALURGIA. › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 5/00 Células no diferenciadas humanas, animales o vegetales, p. ej. líneas celulares; Tejidos; Su cultivo o conservación; Medios de cultivo para este fin (reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00). › Células o tejidos embrionarios; Células o tejidos fetales.
Fragmento de la descripción:
Método para evaluar la eficacia de los medios de cultivo embrionario, empleados en procesos de fecundación y cultivo in vitro, basado en la capacidad de los embriones para unir factores de crecimiento epidérmico.
Campo de la invención Esta invención pertenece, de forma general, al campo de la mejora industrial de los medios de cultivo embrionario. De forma particular, la presente invención se refiere a un nuevo método para evaluar la eficacia de los medios de cultivo embrionario, basado en la medición de la capacidad de embriones no humanos para unir los factores de crecimiento epidérmico (EGF: Epidermal Growth Factors) después del cultivo.
Antecedentes de la invención De cara a mejorar la selección embrionaria, conseguir embriones en el último estadio de desarrollo preimplantacional (Blastocisto) , que es cuando ya se ha superado el posible bloqueo del desarrollo, ha sido un objetivo prioritario desde que surgieron las técnicas de reproducción asistida. Sin embargo, conseguir completar esta etapa del desarrollo no proporciona garantías sobre el éxito del proceso reproductivo, ya que las condiciones en las que se produce el cultivo de los embriones obtenidos por fecundación in vitro, influyen en su desarrollo y pueden comprometer su viabilidad (Grossman, M., Marina, F., Martín, P., Pons, M.C., Alcolea, R. , 1998. Cocultivo hoy = Medios secuenciales Mañana? Asebir 3, 4.) y producir alteraciones génicas (Doherty, A.S., Mann, M.R., Tremblay, K.D., Bartolomei, M.S., Schultz, R.M., 2000. Differential effects of culture on imprinted H19 expression in the preimplantation mouse embr y o. Biol Reprod 62, 1526-1535 ) o afectar a algunos de los procesos fundamentales de desarrollo embrionario, como la proliferación, diferenciación celular y apoptosis (Fong, B., Watson, P.H., Watson, A.J., 2007. Mouse preimplantation embr y o responses to culture medium osmolarity include increased expression of CCM2 and p38 MAPK activation. BMC Dev Biol 7, 2. ) ; (Ho, Y., Doherty, A.S., Schultz, R.M., 1994. Mouse preimplantation embr y o development in vitro: effect of sodium concentration in culture media on RNA synthesis and accumulation and gene expression. Mol Reprod Dev 38, 131-141 ) ; (Scheil, V., Zurn, A., Kohler, H.R., Triebskorn, R. 2010. Embr y o development, stress protein (Hsp70) responses, and histopathology in zebrafish (Danio rerio) following exposure to nickel chloride, chlorpyrifos, and binar y mixtures of them. Environ Toxicol 25, 83-93 ) ; (Warzych, E., Wrenzycki, C., Peippo, J., Lechniak, D., 2007. Maturation medium supplements affect transcript level of apoptosis and cell survival related genes in bovine blastocysts produced in vitro. Mol Reprod Dev 74, 280-289. ) . Todos estos procesos influyen netamente en la viabilidad embrionaria, por lo que las condiciones en las que se desarrolla el cultivo embrionario podrían ser el motivo de algunos de los fallos de implantación que han sido tradicionalmente diagnosticados como de origen desconocido.
Tradicionalmente, se han tomado los criterios de valoración morfológicos así como las tasas de desarrollo embrionario, supervivencia o el grado de fragmentación celular como valores indicativos de la calidad de los medios de cultivo. Sin embargo, las condiciones en las que se desarrolla el embrión durante su fase preimplantacional (desde la formación del cigoto hasta el estadio de blastocisto) , cuando está sujeto a un cultivo in vitro prolongado, pueden también tener efectos imperceptibles y pasar desapercibidos (Feil, D., Lane, M., Roberts, C.T., Kelley, R.L., Edwards, L.J., Thompson, J.G., Kind, K.L., 2006. Effect of culturing mouse embr y os under different oxygen concentrations on subsequent fetal and placental development. J Physiol 572, 87-96. ) ; (Zander, D.L., Thompson, J.G., Lane, M., 2006. Perturbations in mouse embr y o development and viability caused by ammonium are more severe after exposure at the cleavage stages. Biol Reprod 74, 288-294.) .
En este sentido para que un medio de cultivo sea eficaz, debe tener una composición que simule el ambiente en el que el embrión se desarrolla naturalmente. Se ha podido comprobar como la suplementación del medio de cultivo con los nutrientes y metabolitos adecuados mejora la calidad de los embriones cultivados (Dirnfeld, M., Goldman, S., Gonen, Y., Koifman, M., Calderon, I., Abramovici, H., 1997. A simplified coculture system with luteinized granulosa cells improves embr y o quality and implantation rates: a controlled study. Fertil Steril 67, 120-122.) . Por otra parte, los factores de crecimiento son un elemento importante en la composición de los medios de cultivo, mejorando considerablemente el desarrollo de los embriones preimplantacionales que han sido cultivados in vitro (Dorado, M., Marqués de Olivera, N., Lorenzo, C., Vazquez, G., Marco, Y., 2006. Evolución de los medios de cultivo embrionario en técnicas de reproducción asistida. . Revista Iberoamericana de Fertilidad 23, 6) . Algunos autores sugieren que las deficiencias demostradas por algunos de los embriones desarrollados in vitro, son la consecuencia de dos elementos fundamentales: Primero, la ausencia de los factores de crecimiento, que en condiciones fisiológicas son secretados al tracto reproductivo. Y segundo, la dilución de aquellos factores de crecimiento que son liberados por los embriones, en el medio de cultivo (Paria, B.C., Dey, S.K., 1990. Preimplantation embr y o development in vitro: cooperative interactions among embr y os and role of growth factors. Proc Natl Acad Sci U S A 87, 4756-4760) . Son muchos los trabajos que apoyan esta premisa y evidencian el papel fundamental de los factores de crecimiento epidérmico en el desarrollo embrionario preimplantacional (Song, H., Lim, H., Das, S.K., Paria, B.C., Dey, S.K., 2000. Dysregulation of EGF family of growth factors and COX-2 in the uterus during the preattachment and attachment reactions of the blastocyst with the luminal epithelium correlates with implantation failure in LIF-deficient mice. Mol Endocrinol 14, 1147-1161 ) ; (Lim, H.J., Dey, S.K., 2009. HB-EGF: a unique mediator of embr y o-uterine interactions during implantation. Exp Cell Res 315, 619-626 ) ; Wang, X., Wang, H., Matsumoto, H., Roy, S.K., Das, S.K., Paria, B.C., 2002. Dual source and target of heparin-binding EGF-like growth factor during the onset of implantation in the hamster. Development 129, 4125-4134.
Por otra parte, y confirmando la importancia de dichos factores, cualquier deficiencia en la capacidad embrionaria para interactuar con estos factores de crecimiento, produce fallos tanto en el desarrollo embrionario como en el proceso de implantación (Stewart, C.L., Kaspar, P., Brunet, L.J., Bhatt, H., Gadi, I., Kontgen, F., Abbondanzo, S.J., 1992. Blastocyst implantation depends on maternal expression of leukaemia inhibitor y factor. Nature 359, 76-79) ; (Schneider, M.R., Wolf, E., 2008. The epidermal growth factor receptor and its ligands in female reproduction: insights from rodent models. Cytokine Growth Factor Rev 19, 173-181 ) ; (Threadgill, D.W., Dlugosz, A.A., Hansen, L.A., Tennenbaum, T., Lichti, U., Yee, D., LaMantia, C., Mourton, T., Herrup, K., Harris, R.C., et al., 1995. Targeted disruption of mouse EGF receptor: effect of genetic background on mutant phenotype. Science 269, 230-234) ; (Chobotova, K., Karpovich, N., Carver, J., Manek, S., Gullick, W.J., Barlow, D.H., Mardon, H.J., 2005. Heparin-binding epidermal growth factor and its receptors mediate decidualization and potentiate survival of human endometrial stromal cells. J Clin Endocrinol Metab 90, 913-919 ) ; (Chobotova, K., Spyropoulou, I., Carver, J., Manek, S., Heath, J.K., Gullick, W.J., Barlow, D.H., Sargent, I.L., Mardon, H.J., 2002. Heparin-binding epidermal growth factor and its receptor ErbB4 mediate implantation of the human blastocyst. Mech Dev 119, 137-144 ) ; (Johnson, D.C., Chatterjee, S., 1993. Embr y o implantation in the rat uterus induced by epidermal growth factor. J Reprod Fertil 99, 557-559) . Por esta razón, la posibilidad de medir la capacidad de los embriones cultivados in vitro para unir factores de crecimiento, supondría una herramienta muy útil para evaluar la calidad del ambiente en el que se ha desarrollado y por ende de la eficacia del medio de cultivo.
El campo de la biotecnología aporta ciertas herramientas que pueden ser combinadas con este objetivo. A día de hoy, existen una gran cantidad de factores de crecimiento conjugados (ligando-fluorocromo) que se encuentran disponibles de forma comercial y permiten detectar un amplio rango de procesos moleculares, relacionados con la señalización celular y la unión ligando-receptor (Iwashita, S., Kobayashi, M., 1992. Signal transduction system for growth factor receptors associated with tyrosine kinase activity: epidermal growth factor receptor signalling and its regulation. Cell Signal 4, 123-132.)...
Reivindicaciones:
1. Método para evaluar la eficacia de los medios de cultivo embrionario, empleados en procesos de fecundación y cultivo in vitro, que se basa en la medición de la calidad de los embriones cultivados, en función de su capacidad para unir factores de crecimiento, caracterizado porque comprende las siguientes etapas:
a) Obtención de embriones no humanos por fecundación in vitro o in vivo.
b) Desarrollo de los embriones hasta el estadio de blastocisto.
c) Cultivo de los embriones obtenidos en a) y b) en un medio de cultivo con factores de crecimiento epidérmico conjugados a fluorocromo.
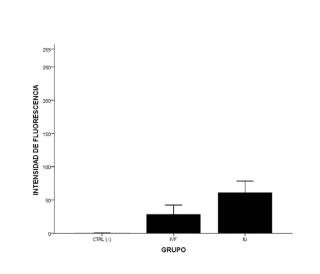
d) Medición de la cantidad de factor de crecimiento conjugado a fluorocromo, unida a la superficie de los embriones cultivados en c) , donde una intensidad de fluorescencia más elevada, se relaciona con unas condiciones de cultivo óptimas.
2. Método según la reivindicación 1, caracterizado porque los factores de crecimiento conjugados se seleccionan entre la familia de ligandos EGF. Tales como EGF (Epidermal growth factor) , TGFa (Transforming growth factor a) , AR (Amphiregulin) , EGF-HB (Heparin Binding EGF-like growth factor) , BTC (Betacellulin) o EPR (Epiregulin) .
3. Método según la reivindicación 2, caracterizado por que la concentración de factores de crecimiento en el medio de cultivo está comprendida entre 1 y 5μg/ml.
4. Método de acuerdo con las reivindicaciones anteriores, caracterizado por que la etapa 1.d) , se lleva a cabo utilizando microscopía de fluorescencia.
5. Método de acuerdo con las reivindicaciones anteriores, caracterizada por que la medición de la fluorescencia en la superficie embrionaria, se lleva a cabo sobre imágenes capturadas a través de una cámara fotográfica acoplada al microscopio de fluorescencia.
6. Método de acuerdo con las reivindicaciones anteriores, caracterizado por que la intensidad de fluorescencia se medirá en una escala de intensidad estándar de 255 niveles, en un rango comprendido entre 10 y 100 unidades de nivel, con un software de análisis de imagen.
FIGURA 1
Patentes similares o relacionadas:
Neuregulina para tratar la insuficiencia cardíaca, del 29 de Julio de 2020, de Zensun (Shanghai) Science & Technology, Co., Ltd: Neuregulina para usar en un método para tratar la insuficiencia cardíaca crónica en un paciente, donde el paciente tiene un nivel plasmático de NT-proBNP […]
Dispositivo médico que tiene un revestimiento que comprende ACCS, del 15 de Julio de 2020, de Noveome Biotherapeutics, Inc: Un dispositivo médico implantable que tiene un revestimiento en su superficie, útil para la implantación quirúrgica en el cuerpo de un sujeto, […]
Composiciones que comprenden cócteles de fagos antibacterianos y usos de las mismas para el tratamiento de infecciones bacterianas, del 24 de Junio de 2020, de Tecnifar-Indústria Técnica Farmacêutica, S.A: Una composicion que comprende: una primera y una segunda cepa purificada de bacteriofago, cada una de dichas cepas que tiene un genoma que comprende […]
Trampas de GDF, del 3 de Junio de 2020, de ACCELERON PHARMA, INC: Un polipéptido aislado que comprende la secuencia de aminoácidos de SEQ ID NO: 28.
Combinacion de peptidos tolerogenos con TFG-â para inducir y mantener la tolerancia oral en mamiferos jovenes, del 3 de Junio de 2020, de SOCIETE DES PRODUITS NESTLE S.A.: Una composición nutricional - que contiene al menos un péptido de cinco hasta doce aminoácidos de longitud e incluye una secuencia elegida entre […]
Formulaciones con oxidación reducida, del 3 de Junio de 2020, de F. HOFFMANN-LA ROCHE AG: Una formulación líquida que comprende un anticuerpo y un compuesto que previene la oxidación del anticuerpo en la formulación líquida, en la que el compuesto es […]
Modulación de la actividad del factor de crecimiento epidérmico de unión a heparina para la curación de la membrana timpánica, del 6 de Mayo de 2020, de THE BOARD OF TRUSTEES OF THE LELAND STANFORD JUNIOR UNIVERSITY: Un agente que proporciona actividad de factor de crecimiento epidérmico de unión a heparina (HB-EGF) para su uso en el tratamiento de una perforación crónica de la membrana […]
Composiciones para lograr niveles plasmáticos deseados del factor 2 de crecimiento glial, del 6 de Mayo de 2020, de ACORDA THERAPEUTICS, INC: Factor de crecimiento glial 2 (GGF2) para su uso en la promocion de la remielinizacion celular en un paciente, donde el GGF2 se administra al paciente en una cantidad de […]