MÉTODO DE DIAGNÓSTICO Y/O PRONÓSTICO DE ENFERMEDADES NEURODEGENERATIVAS.
Método de diagnóstico y/o pronóstico de enfermedades neurodegenerativas.
La presente invención se refiere al uso del ADN mitocondrial como biomarcador cuantitativo de enfermedades neurodegenerativas, preferiblemente de la enfermedad de Alzheimer, así como a un método y a un kit diagnóstico y/o pronóstico de dichas enfermedades mediante el uso de dicho biomarcador.
Tipo: Patente de Invención. Resumen de patente/invención. Número de Solicitud: P201231807.
Solicitante: CONSEJO SUPERIOR DE INVESTIGACIONES CIENTIFICAS (CSIC).
Nacionalidad solicitante: España.
Inventor/es: TRULLAS OLIVA,RAMON, FIGUEIRÓ SILVA,Joana, MIHAYLOVICH PODLESNIY,Petar.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C12Q1/68 QUIMICA; METALURGIA. › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12Q PROCESOS DE MEDIDA, INVESTIGACION O ANALISIS EN LOS QUE INTERVIENEN ENZIMAS, ÁCIDOS NUCLEICOS O MICROORGANISMOS (ensayos inmunológicos G01N 33/53 ); COMPOSICIONES O PAPELES REACTIVOS PARA ESTE FIN; PROCESOS PARA PREPARAR ESTAS COMPOSICIONES; PROCESOS DE CONTROL SENSIBLES A LAS CONDICIONES DEL MEDIO EN LOS PROCESOS MICROBIOLOGICOS O ENZIMOLOGICOS. › C12Q 1/00 Procesos de medida, investigación o análisis en los que intervienen enzimas, ácidos nucleicos o microorganismos (aparatos de medida, investigación o análisis con medios de medida o detección de las condiciones del medio, p. ej. contadores de colonias, C12M 1/34 ); Composiciones para este fin; Procesos para preparar estas composiciones. › en los que intervienen ácidos nucleicos.
PDF original: ES-2482866_A1.pdf
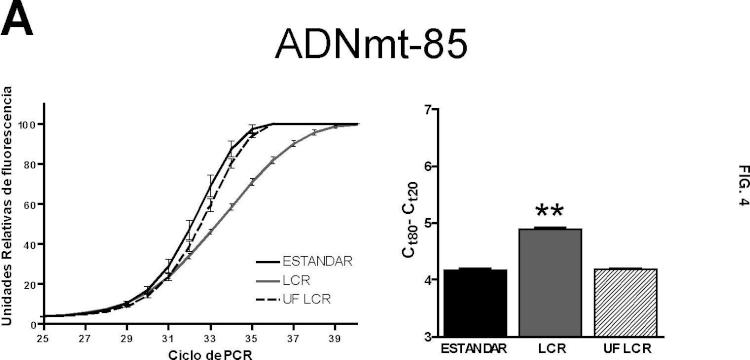
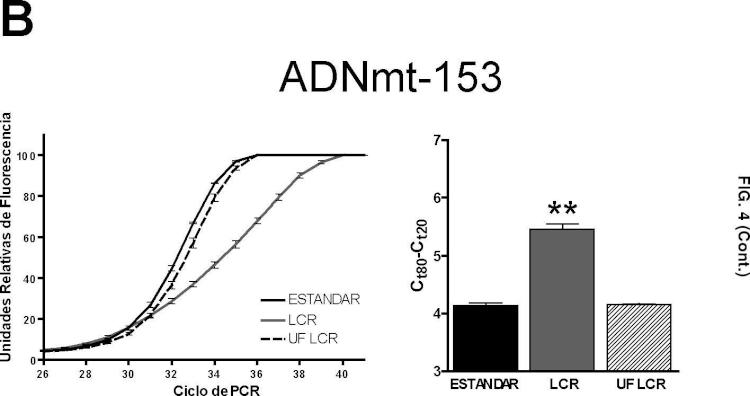
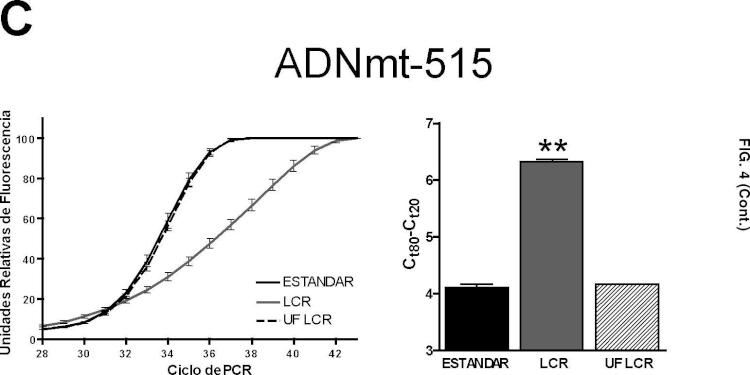
Fragmento de la descripción:
Método de diagnóstico y/o pronóstico de enfermedades neurodegenerativas.
La presente invención se encuadra en el campo de las enfermedades neurodegenerativas, concretamente dentro de los métodos de diagnóstico y/o pronóstico de este tipo de enfermedades, preferiblemente Alzheimer, que se basan en la cuantificación de biomarcadores en muestras biológicas aisladas.
ESTADO DE LA TÉCNICA
Recientes evidencias indican que la enfermedad de Alzheimer (EA) es precedida por una larga fase preclínica con cambios bioquímicos anormales, estructurales y funcionales en el cerebro. Estos cambios sugieren que el proceso fisiopatológico de la neurodegeneración de la EA se inicia mucho antes de la aparición de síntomas clínicos de demencia. Por lo tanto, la identificación de nuevos biomarcadores que preceden a la aparición de síntomas clínicos de la enfermedad es esencial para avanzar en el conocimiento de la EA y poder desarrollar posibles métodos diagnósticos y/o pronósticos y tratamientos terapéuticos tempranos y eficientes.
En la actualidad se conocen dos biomarcadores utilizados en procedimientos en forma de kit diagnóstico que utilizan ensayos con anticuerpos para detectar los niveles de proteínas p-amiloide (AP) y de tau total (t-tau) y tau fosforilado (f-tau) para diagnosticar la EA en un estado pre-clínico, antes de que se manifiesten los síntomas clínicos de demencia. Una acumulación de Ap en cerebro o una baja concentración de Ap^ en líquido cefalorraquídeo (LCR) o un aumentado nivel de t-tau y f-tau en LCR (Jack, C. R. et al., 2010, Lancet Neurol. 9, 119-128) indican un diagnóstico positivo de la EA. Utilizados en combinación, estos dos biomarcadores respaldan un buen valor predictivo de un diagnóstico negativo de la EA. Aun así, el diagnóstico de la EA es todavía probabilístico y requiere la presencia de síntomas clínicos. Además, la relación entre los niveles de proteínas en cerebro y en LCR en la EA no es sencilla debida a que los niveles de proteínas en LCR como tau total y fosforilado se correlacionan positivamente, mientras que los niveles de Ap se correlacionan negativamente con una acumulación en cerebro y una baja concentración en LCR. La razón por la cual se asocia la acumulación de Ap en cerebro con bajas concentraciones de Ap!_42 en LCR no está clara, aunque puede ser debido a una disminución de la liberación de APí-42 desde el cerebro al LCR (Mawuenyega, K.G. et al. 2010, Science. 330, 1774). Por el contrario, se considera que una alta concentración de tau total en el LCR refleja una lesión neuronal asociada con la acumulación de tau en el cerebro. Sin embargo, otras tau-patías en las cuales hay una alta acumulación de tau en los ovillos neurofibrilares en cerebro, no muestran un aumento correspondiente de tau total en el LCR (Bian, H. etal. 2008, Neurology. 70, 1827-1835).
Existe la hipótesis de que la disfunción mitocondrial está involucrada en la fisiopatología de la EA, pero si ésta precede o es una consecuencia del proceso neurodegenerativo todavía no está claro. Además, la EA se asocia con alteraciones en la bioenergética y función mitocondrial, dado que las neuronas son altamente dependientes de la energía aeróbica proporcionada por las mitocondrias (Swerdlow, R.H. etal. J. Alsheimers. Dis., 2010, 293-310).
En el estado de la técnica se describe además, que pacientes que sufren de la EA tienen en el cerebro una mayor incidencia de mutaciones localizadas en la región control (CR) del ADN mitocondrial dentro de los elementos que se sabe están involucrados en la transcripción de la cadena-L y la replicación de la cadena-H (W02007011322A2). Para ello, el documento W02007011322A2 aporta métodos y sistemas analíticos para el diagnóstico pre- o postsintomático de trastornos neurodegenerativos asociados con la formación de depósitos de p- amiloide y/o fibrillas de p-amiloide, mediante la cuantificación o detección de dichas mutaciones en el ADN mitocondrial en tejido o células de un individuo. Otro método está descrito en el
documento WO9409162A1 para diagnosticar o pronosticar una predisposición a la EA que comprende la detección de mutaciones o inserciones en el ADN mitocondrial.
Otros estudios asocian polimorfismos con la EA. Están descritos 138 polimorfismos asociados con dicha enfermedad ("Alzheimer's Disease Neuroimaging Initiative"). Lakatos et al. aportan, en su estudio sobre el papel de los haplogrupos mitocondriales procedentes de 138 polimorfismos mitocondriales en 358 individuos de raza caucásica, 5 polimorfismos más a los ya descritos, que se pueden asociar con EA (Lakatos A. et al. Neurobiol Aging, 2010, 31(8): 1355-1363). Por otro lado, un estudio de 138 polimorfismos de nucleótido único realizado en 3.250 pacientes con EA y 1.221 controles, concluye que no hay ninguna evidencia consistente de asociación entre las variaciones del ADN mitocondrial y la EA.
En resumen, hasta el momento, se han descrito métodos diagnósticos y/o pronósticos de la EA en los cuales se miden los niveles de biomarcadores como p-amiloide y tau total y fosforilado, así como mutaciones o polimorfismos en el ADN mitocondrial. También se sabe que el LCR está en contacto directo con el parénquima cerebral, por lo que se considera que es el mejor fluido para identificar posibles alteraciones del metabolismo cerebral. Sin embargo, estos métodos tienen el inconveniente de que el diagnóstico y/o pronóstico se realiza en muestras biológicas de tejido o LCR, lo cual requiere la obtención de dichas muestras a través de un procedimiento invasivo en el paciente, además de ser métodos poco fiables para el diagnóstico y/o prevención precoz de la enfermedad. Por lo tanto, existe la necesidad de desarrollar otros métodos de diagnóstico y/o pronóstico precoces de la EA que puedan emplear muestras biológicas cuya obtención no implique realizar un método invasivo en el paciente. Además, sería deseable que estos procedimientos fueran más sencillos de realizar, más sensibles, más específicos, más reproducibles entre los laboratorios y con menor variabilidad que la medida de niveles de proteínas con anticuerpos que se utiliza en los kits actualmente disponibles para el diagnóstico de la enfermedad de EA.
DESCRIPCIÓN DE LA INVENCIÓN
La presente invención se refiere en un primer aspecto al uso del ADN mitocondrial como biomarcador cuantitativo para el diagnóstico y/o pronóstico de enfermedades neurodegenerativas, preferiblemente de la EA.
En un segundo aspecto, la presente invención se refiere a un método diagnóstico y/o pronóstico in vitro de una enfermedad neurodegenerativa, preferiblemente de la EA, basado en la cuantificación del ADN mitocondrial en una muestra biológica aislada de un sujeto.
En un tercer aspecto, la presente invención se refiere a un kit para el diagnóstico y/o pronóstico de una enfermedad neurodegenerativa, preferiblemente de la EA, caracterizado porque comprende al menos un conjunto de cebadores o sondas para la cuantificación del ADN mitocondrial.
En un cuarto aspecto, la presente invención se refiere a un uso del kit que comprende cebadores y/o sondas específicos para el ADN mitocondrial, para el diagnóstico y/o pronóstico de una enfermedad neurodegenerativa, preferiblemente de la EA.
DESCRIPCIÓN DETALLADA DE LA INVENCIÓN
La presente invención propone el uso del ADN mitocondrial como biomarcador cuantitativo para el diagnóstico y/o pronóstico precoz de una enfermedad neurodegenerativa, preferiblemente de la EA, y por tanto proporciona un método mejorado de diagnóstico y/o pronóstico de una enfermedad neurodegenerativa, preferiblemente de la EA, basado en el uso de dicho biomarcador.
El método descrito en la presente invención aporta la ventaja de que permite llevar a cabo un
diagnóstico y/o pronóstico precoz de la enfermedad neurodegenerativa, es decir, antes de que se manifiesten los síntomas clínicos asociados a dicha enfermedad. Esto permite administrar al paciente tratamientos terapéuticos y/o profilácticos tempranos y eficientes.
Además, dicho método puede llevarse a cabo en una amplia variedad de muestras biológicas sin que su fiabilidad y reproducibilidad se vean alteradas, entre ellas, por ejemplo aunque sin limitarnos, sangre, suero o plasma del sujeto en estudio. Así, el método de la invención no requiere necesariamente la realización de un procedimiento invasivo en el paciente como ocurre con otros métodos de diagnóstico conocidos hasta la fecha que necesitan de la obtención de tejido cerebral o líquido cefalorraquídeo. Además, este procedimiento es sencillo de realizar, ya que la cuantificación del ADN mitocondrial puede realizarse mediante técnicas ampliamente utilizadas de cuantificación de... [Seguir leyendo]
Reivindicaciones:
1. Uso del ADN mitocondrial como biomarcador cuantitativo para el diagnóstico y/o pronóstico de la enfermedad de Alzheimer.
2. Uso según la reivindicación 1, donde el ADN mitocondrial es extracelular.
3. Un método para el diagnóstico y/o pronóstico in vitro de la enfermedad de Alzheimer que comprende las siguientes etapas:
a) cuantificar el ADN mitocondrial en una muestra biológica aislada de un sujeto; y
b) comparar el valor obtenido en la etapa (a) con un valor estándar.
4. El método según la reivindicación 3, que además comprende:
c) asignar al sujeto del paso (a) al grupo de pacientes con predisposición a padecer la enfermedad de Alzheimer o al grupo de pacientes que padecen la enfermedad de Alzheimer cuando el valor obtenido en la etapa (a) es significativamente menor que el valor estándar.
5. El método según cualquiera de las reivindicaciones 3 ó 4, donde la muestra biológica aislada se selecciona de la lista que consiste en: saliva, sudor, lágrimas, orina, líquido cefalorraquídeo, sangre, suero y plasma sanguíneo.
6. El método según la reivindicación 5, donde la muestra biológica aislada es líquido cefalorraquídeo.
7. El método según la reivindicación 5, donde la muestra biológica aislada es sangre, suero o plasma sanguíneo.
8. El método según la reivindicación 7, donde la muestra biológica aislada es suero.
9. El método según cualquiera de las reivindicaciones 3 a 8, donde la etapa (a) se lleva a cabo mediante PCR, PCR cuantitativa, PCR digital en gotas o Southern Blot.
10. El método según la reivindicación 9, donde la etapa (a) se lleva a cabo mediante PCR cuantitativa o PCR digital en gotas.
11. El método según cualquiera de las reivindicaciones 9 ó 10, donde la etapa (a) se lleva a cabo mediante PCR digital en gotas.
12. El método según cualquiera de las reivindicaciones 3 a 11, donde el ADN mitocondrial es extracelular.
13. El método según cualquiera de las reivindicaciones 3 a 12, donde el sujeto es un humano.
14. Un kit para el diagnóstico y/o pronóstico de la enfermedad de Alzheimer que comprende al menos uno de los siguientes conjuntos de cebadores o sondas:
| a) | SEQ | ID | NO: 1 y SEQ | ID | NO: 4, |
| b) | SEQ | ID | NO: 1 y SEQ | ID | NO: 2 y opcionalmente SEQ ID NO:8, |
| c) | SEQ | ID | NO: 3 y SEQ | ID | NO: 4, |
| d) | SEQ | ID | NO: 6 y SEQ | ID | NO: 7 y opcionalmente SEQ ID NO: 5,o |
| e) | SEQ | ID | NO: 9 y SEQ | ID | NO: 10. |
15. El kit según la reivindicación 14 que comprende los cebadores SEQ ID NO: 3 y SEQ ID
NO: 4 o SEQ ID NO: 9 y SEQ ID NO: 10.
16. Uso de un kit que comprende cebadores y/o sondas específicos para el ADN mitocondrial, para el diagnóstico y/o pronóstico de la enfermedad de Alzheimer.
17. Uso según la reivindicación 16, donde el kit es el kit según cualquiera de las reivindicaciones 14 ó 15.
Patentes similares o relacionadas:
Método para analizar ácido nucleico molde, método para analizar sustancia objetivo, kit de análisis para ácido nucleico molde o sustancia objetivo y analizador para ácido nucleico molde o sustancia objetivo, del 29 de Julio de 2020, de Kabushiki Kaisha DNAFORM: Un método para analizar un ácido nucleico molde, que comprende las etapas de: fraccionar una muestra que comprende un ácido nucleico molde […]
MÉTODOS PARA EL DIAGNÓSTICO DE ENFERMOS ATÓPICOS SENSIBLES A COMPONENTES ALERGÉNICOS DEL POLEN DE OLEA EUROPAEA (OLIVO), del 23 de Julio de 2020, de SERVICIO ANDALUZ DE SALUD: Biomarcadores y método para el diagnostico, estratificación, seguimiento y pronostico de la evolución de la enfermedad alérgica a polen del olivo, kit […]
Detección de interacciones proteína a proteína, del 15 de Julio de 2020, de THE GOVERNING COUNCIL OF THE UNIVERSITY OF TORONTO: Un método para medir cuantitativamente la fuerza y la afinidad de una interacción entre una primera proteína de membrana o parte de la misma y una […]
Secuenciación dirigida y filtrado de UID, del 15 de Julio de 2020, de F. HOFFMANN-LA ROCHE AG: Un procedimiento para generar una biblioteca de polinucleótidos que comprende: (a) generar una primera secuencia del complemento (CS) de un polinucleótido diana a partir […]
Métodos para la recopilación, estabilización y conservación de muestras, del 8 de Julio de 2020, de Drawbridge Health, Inc: Un método para estabilizar uno o más componentes biológicos de una muestra biológica de un sujeto, comprendiendo el método obtener un […]
Evento de maíz DP-004114-3 y métodos para la detección del mismo, del 1 de Julio de 2020, de PIONEER HI-BRED INTERNATIONAL, INC.: Un amplicón que consiste en la secuencia de ácido nucleico de la SEQ ID NO: 32 o el complemento de longitud completa del mismo.
Composiciones para modular la expresión de SOD-1, del 24 de Junio de 2020, de Biogen MA Inc: Un compuesto antisentido según la siguiente fórmula: mCes Aeo Ges Geo Aes Tds Ads mCds Ads Tds Tds Tds mCds Tds Ads mCeo Aes Geo mCes Te (secuencia […]
Aislamiento de ácidos nucleicos, del 24 de Junio de 2020, de REVOLUGEN LIMITED: Un método de aislamiento de ácidos nucleicos que comprenden ADN de material biológico, comprendiendo el método las etapas que consisten en: (i) efectuar un lisado […]