Dispositivo médico de acceso endoluminal.
Un dispositivo médico de acceso endoluminal (1), concebido para administración endoluminal a un sitio diana extravascular (5) en un sitio de la vasculatura (4),
tal como un sitio de la microvasculatura, de una vasculatura del cuerpo humano o animal, en el que dicho dispositivo (1) comprende
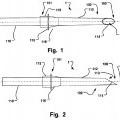
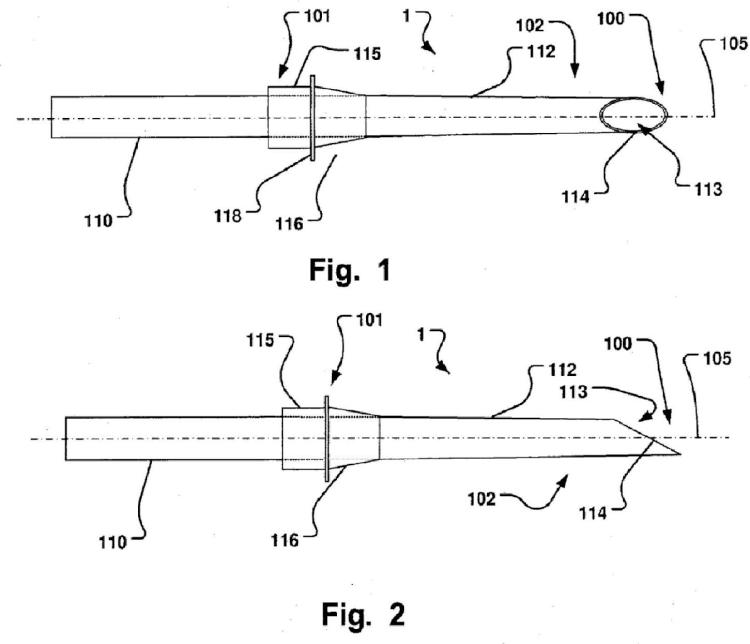
un cuerpo hueco (112) que está dispuesto alrededor de un canal continuo (113) que termina en una abertura en un extremo distal (100) de dicho dispositivo; en el que dicho cuerpo hueco (112) comprende una porción distal alargada desprendible (102) que está concebida para extenderse a través de una pared del tejido (200) de dicha vasculatura en dicho sitio de la vasculatura (4) en dicho cuerpo y concebida para proporcionar comunicación con dicho sitio diana extravascular (5) a través de dicho canal (113) y concebida para yuxtaponerse al menos parcialmente con dicha pared del tejido (200), y una porción proximal (110), que se une proximalmente con dicha porción distal (102) en una sección de conexión proximal (101); y
una sección de separación hueca (115) que está dispuesta en dicho cuerpo hueco (112) para la separación controlada de dicha porción distal (102) de dicha porción proximal (110) de dicho cuerpo hueco (112) en dicha sección de conexión proximal (101).
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP2009/054273.
Solicitante: SmartWise Sweden AB.
Nacionalidad solicitante: Suecia.
Dirección: P.O. Box 55963 10216 Stockholm SUECIA.
Inventor/es: JONSSON, STEFAN, HOLMIN,STAFFAN, LUNDBERG,JOHAN.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61B17/34 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61B DIAGNOSTICO; CIRUGIA; IDENTIFICACION (análisis de material biológico G01N, p.ej. G01N 33/48). › A61B 17/00 Instrumentos, dispositivos o procedimientos quirúrgicos, p. ej. torniquetes (A61B 18/00 tiene prioridad; dispositivos anticonceptivos, pesarios, dispositivos para su introducción A61F 6/00; cirugía ocular A61F 9/007; cirugía otorrina A61F 11/00). › Trócares; Agujas de punción.
- A61B18/18 A61B […] › A61B 18/00 Instrumentos, dispositivos o procedimientos quirúrgicos para transferir formas de energía no mecánica hacia o desde el cuerpo (cirugía ocular A61F 9/007; cirugía otorrina A61F 11/00). › aplicando radiación electromagnética, p. ej. microondas (radioterapia A61N 5/00).
- A61M25/00 A61 […] › A61M DISPOSITIVOS PARA INTRODUCIR AGENTES EN EL CUERPO O PARA DEPOSITARLOS SOBRE EL MISMO (introducción de remedios en o sobre el cuerpo de animales A61D 7/00; medios para la inserción de tampones A61F 13/26; dispositivos para la administración vía oral de alimentos o medicinas A61J; recipientes para la recogida, almacenamiento o administración de sangre o de fluidos médicos A61J 1/05 ); DISPOSITIVOS PARA HACER CIRCULAR LOS AGENTES POR EL CUERPO O PARA SU EXTRACCION (cirugía A61B; aspectos químicos de los artículos quirúrgicos A61L; magnetoterapia utilizando elementos magnéticos colocados dentro del cuerpo A61N 2/10 ); DISPOSITIVOS PARA INDUCIR UN ESTADO DE SUEÑO O LETARGIA O PARA PONERLE FIN. › Catéteres; Sondas huecas (para medida o examen A61B).
- A61M25/06 A61M […] › A61M 25/00 Catéteres; Sondas huecas (para medida o examen A61B). › Agujas con una guía para pinchar el cuerpo o similares (A61M 25/088 tiene prioridad).
- A61N1/05 A61 […] › A61N ELECTROTERAPIA; MAGNETOTERAPIA; RADIOTERAPIA; TERAPIA POR ULTRASONIDOS (medida de corrientes bioeléctricas A61B; instrumentos quirúrgicos, dispositivos o métodos para transferir formas no mecánicas de energía hacia o desde el cuerpo A61B 18/00; aparatos de anestesia en general A61M; lámparas incandescentes H01K; radiadores de infrarrojos utilizados como calefactores H05B). › A61N 1/00 Electroterapia; Circuitos correspondientes (A61N 2/00 tiene prioridad; preparaciones conductoras de la electricidad que se utilizan en terapia o en examen in vivo A61K 50/00). › para implantar o para introducir en el cuerpo, p. ej. electrodo cardiaco (A61N 1/06 tiene prioridad).
PDF original: ES-2553112_T3.pdf


Patentes similares o relacionadas:
Dispositivo de administración de un solo uso que tiene un elemento de cebado, del 29 de Julio de 2020, de BECTON, DICKINSON AND COMPANY: Un dispositivo de administración de un solo uso que comprende: un recipiente de líquido deformable manualmente que define una cámara interior , […]
Administración intravascular de composiciones de nanopartículas y usos de las mismas, del 29 de Julio de 2020, de ABRAXIS BIOSCIENCE, LLC: Una composición que comprende nanopartículas que comprenden rapamicina y albúmina para su uso en un procedimiento para inhibir la remodelación […]
 Válvula de catéter, del 29 de Julio de 2020, de Profiform AG: Válvula de catéter, en particular, una válvula de catéter de cierre automático para su uso en urología, geriatría, entre otros, que comprende entre otras piezas, […]
Válvula de catéter, del 29 de Julio de 2020, de Profiform AG: Válvula de catéter, en particular, una válvula de catéter de cierre automático para su uso en urología, geriatría, entre otros, que comprende entre otras piezas, […]
Kit de tratamiento, dispositivo de medición y uso asociados, del 22 de Julio de 2020, de Perouse Medical: Kit de tratamiento que comprende: - una guía que consta de un extremo distal y un extremo proximal , - un dispositivo de determinación […]
Catéter integrado con caminos de fluido independientes, del 15 de Julio de 2020, de BECTON, DICKINSON AND COMPANY: Un sistema de catéter que comprende: un adaptador de catéter que comprende un conectador de catéter que define una cámara que se extiende […]
DISPOSITIVO PARA PROTEGER DE LA HUMEDAD UNA HERIDA, del 9 de Julio de 2020, de GARCIA GONZALEZ, Maria Pilar: Dispositivo (D) para proteger de la humedad una herida del cuerpo de un paciente que comprende una parte de base para ser conectada al cuerpo del paciente, […]
Catéter de múltiples luces con características de flujo potenciadas, del 1 de Julio de 2020, de C.R. BARD, INC.: Método para formar un tubo de catéter, comprendiendo el método: proporcionar una estructura de refuerzo que incluye partes de refuerzo […]
Alambre guía con tubo autohumectante, del 24 de Junio de 2020, de St. Jude Medical Coordination Center BVBA: Un alambre guía para medir la presión biológica, que comprende: un tubo que se extiende a lo largo de un eje longitudinal del alambre guía, teniendo […]