MATERIALES Y PROCEDIMIENTOS PARA LA ESTIMULACIÓN DEL SISTEMA INMUNITARIO.
Compuesto aislado que presenta la estructura química siguiente (I) o una sal farmacéuticamente aceptable del mismo: **Fórmula**
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2005/024410.
Solicitante: VARIETY CHILDREN'S HOSPITAL D/B/A/ MIAMI CHILDREN'S HOSPITAL.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 3100 S.W. 62ND AVENUE MIAMI, FLORIDA 33155 ESTADOS UNIDOS DE AMERICA.
Inventor/es: NAIR,P.K. Raveendran, MELNICK,Steven,J, RAMACHANDRAN,Cheppail.
Fecha de Publicación: .
Fecha Solicitud PCT: 11 de Julio de 2005.
Clasificación Internacional de Patentes:
- C08B37/00M2
Clasificación PCT:
- A61K31/716 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › Glucanos.
- C08B37/00 QUIMICA; METALURGIA. › C08 COMPUESTOS MACROMOLECULARES ORGANICOS; SU PREPARACION O PRODUCCION QUIMICA; COMPOSICIONES BASADAS EN COMPUESTOS MACROMOLECULARES. › C08B POLISACARIDOS; SUS DERIVADOS (polisacáridos que contienen menos de seis radicales sacáridos unidos entre sí por enlaces glucosídicos C07H; procesos de fermentación o procesos que utilizan enzimas C12P 19/00; producción de celulosa D21). › Preparación de polisacáridos no previstos en los grupos C08B 1/00 - C08B 35/00; Sus derivados (celulosa D21).
Clasificación antigua:
- A61K31/716 A61K 31/00 […] › Glucanos.
- C08B37/00 C08B […] › Preparación de polisacáridos no previstos en los grupos C08B 1/00 - C08B 35/00; Sus derivados (celulosa D21).
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Eslovenia, Finlandia, Rumania, Chipre, Lituania, Letonia.
PDF original: ES-2360862_T3.pdf
Fragmento de la descripción:
Antecedentes de la invención
La posibilidad de bioterrorismo, la epidemia del síndrome respiratorio agudo grave (SARS) y el virus de la gripe aviar, la continuada propagación del VIH/SIDA, y la aparición de cepas patógenas resistentes a las medicaciones actuales apremian a los investigadores a buscar nuevas medidas de protección que comprenden las estrategias de biodefensa contra estas amenazas. La activación inmunitaria es una estrategia eficaz así como protectora para las estrategias de biodefensa destinadas a las enfermedades infecciosas emergentes (Hackett, C. J., J. Allergy and Clin. Immunol., 2003, 112:686-694). Aunque el sistema inmunitario humano presenta una red de detección microbiana amplia y mecanismos de defensa del hospedador, la evasión de patógenos de la vigilancia inmunitaria y del sistema de destrucción es la norma. La situación no es diferente para el cáncer ya que la mayoría de las células tumorales no se detectan y escapan a la vigilancia inmunitaria (Wajchman, H. J. et al., Cancer Res., 2004, 64:1171-1180).
Son los componentes del sistema inmunitario innato los que detectan los patógenos o los no autointrusos, con ayuda de los receptores específicos, y responden inmediatamente por activación de las células inmunitarias competentes, síntesis de citocinas y quimiocinas y liberación de mediadores inflamatorios para eliminar o contener a los intrusos. La activación inmunitaria innata también activa y allana el camino a la respuesta inmunitaria adaptativa por los linfocitos T y B específicos para el antígeno. Las células destructoras naturales (NK) desempeñan una función decisiva en la defensa inmunitaria innata contra las células infectadas por virus y malignas en virtud de su capacidad para reconocer y destruir células anormales, pendiente el desarrollo de inmunidad adaptativa (Smith, H. R. et al., Proc. Natl. Acad. Sci. USA, 2002, 99:8826-8831; Moser, J. M. et al., Curr. Opin, Immunol., 2002, 14:509-516).
Varios compuestos activan el sistema inmunitario, tales como los lipopolisacáridos (LPS) microbianos, los oligonucleótidos del ARN bicatenario y ADN que contienen motivos CpG no metilados se han descrito al principio (Hackett, C. J., J. Allergy and Clin. Immunol., 2003, 112:686-694; Kandimalla, E. R. et al., Proc. Natl. Acad. Sci., USA, 2003, 100:14303-14308). Se informa de que la estimulación de múltiples receptores presenta efecto sinérgico en la producción de citocina (Gao, J. J. et al., J. Immunol., 2001, 166:6855-6860). La cascada de activación del complemento es otra parte integral del sistema inmunitario innato en el que los patógenos celulares, tales como las bacterias intracelulares, están recubiertos con componentes de complemento (opsonización) y experimentan fácilmente fagocitosis. Por tanto, la activación del complemento desempeña una función importante en la destrucción microbiana y es esencial para el transporte y la eliminación de complejos inmunitarios.
El tipo de respuesta inmunitaria adaptativa (conocida también como la respuesta inmunitaria específica o adquirida) que se genera a la infección u otra prueba de provocación antigénica puede generalmente distinguirse por el subconjunto de linfocitos T cooperadores (Th) implicados en la respuesta. La respuesta de Th1 (la respuesta celular
o mediada por células) es responsable de las funciones clásicas mediadas por las células tal como la hipersensibilidad de tipo retardado y la activación de los linfocitos T citotóxicos (LTC), mientras que la respuesta de Th2 (respuesta humoral) funciona con más eficacia como cooperador para la activación de linfocitos B. El tipo de respuesta inmunitaria a un antígeno se determina generalmente por las citocinas producidas por las células que responden al antígeno. Las diferencias en las citocinas segregadas por los linfocitos Th1 y Th2 se cree que reflejan diferentes funciones biológicas de estos dos subconjuntos.
Resulta evidente que las citocinas desempeñan funciones cruciales en la regulación de varios aspectos de las respuestas inmunitarias. Entre las citocinas, la interleucina (IL)-12 desempeña una función central en la coordinación innata y en la inmunidad adaptativa mediada por las células (Watford, W. T. et al., Cytokine Growth Factor Rev., 2003, 14:361-368). Se ha demostrado la protección profiláctica así como después de la exposición por estimulación inmunitaria (Walker, P. S. et al., Proc. Natl. Acad. Sci., USA, 1999, 96:6970-6975; Juffermans, N. P. et al., Infect. Immunol., 2002, 70:147-152). Habitualmente, estas medidas protectoras se correlacionan con la síntesis de IL-12 y del interferón (IFN)-γ, las citocinas de la ruta de Th1 de la diferenciación de los linfocitos T asociada con el sistema inmunitario adaptable (Gramzinski, A. M. et al., Infect. Immunol., 2001, 69:1643-1649).
El subconjunto Th1 puede ser particularmente adecuado para responder a las infecciones víricas y a patógenos intracelulares porque segrega IL-2 e IFN-gamma, que activan los LTC. El subconjunto Th2 puede ser más adecuado para responder a las bacterias vivas y a los parásitos helmínticos y puede mediar en reacciones alérgicas, ya que IL4 e IL-5 son conocidos porque provocan la producción de IgE y la activación de eosinófilos, respectivamente. En general, los linfocitos Th1 y Th2 segregan distintos modelos de citocinas y, por lo tanto, un tipo de respuesta puede modelar la actividad del otro tipo de respuesta. Un cambio en el equilibrio Th1/Th2 puede producir una respuesta alérgica, por ejemplo, o, alternativamente, un aumento de la respuesta de LTC.
La inmunización de un animal hospedador contra un antígeno específico ha sido realizada tradicionalmente por vacunación repetida del hospedador con una forma inmunógena del antígeno. Aunque la mayoría de las vacunas actuales producen respuestas humorales eficaces (anticuerpo, o “tipo Th2”), no pueden provocar respuestas celulares (en particular, el complejo de histocompatibilidad mayor (CMH) LTC restringido de Clase I o respuestas de “tipo Th1”) que están generalmente ausentes o son débiles. Para muchas enfermedades infecciosas, tales como la tuberculosis y la malaria, las respuestas de tipo Th2 son de poco valor protector contra la infección. Además, las respuestas del anticuerpo son inapropiadas en determinadas indicaciones, más en particular en alergia en la que una respuesta del anticuerpo puede producir un choque anafiláctico. Las vacunas propuestas que utilizan péptidos pequeños derivados del antígeno diana y otros agentes antigénicos utilizados actualmente han impedido la utilización de partículas víricas intactas potencialmente ineficaces, hacen que no siempre produzcan la respuesta inmunitaria necesaria para conseguir un efecto terapéutico. La falta de una vacuna de virus de inmunodeficiencia humana (VIH) terapéuticamente eficaz es un ejemplo desafortunado de esta insuficiencia.
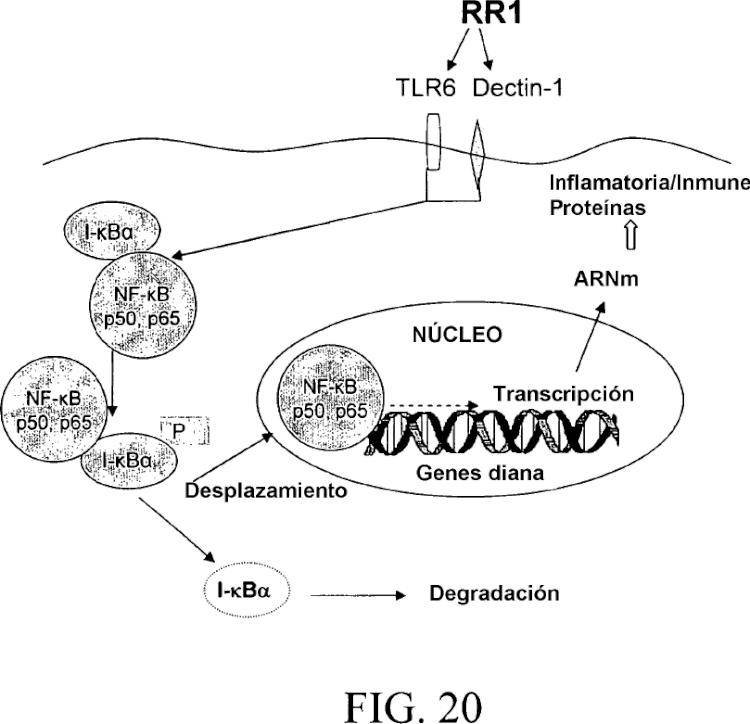
La inmunidad innata mediada por macrófagos, neutrófilos y células destructoras naturales (NK) es la primera línea del mecanismo de defensa del hospedador contra la invasión microbiana. El sistema inmunitario innato se dirige a los modelos moleculares asociados a patógenos conservados estructuralmente (PAMP) mediante receptores codificados específicos de la línea germinal denominados receptores de reconocimiento del modelo (PRR) (Aderem,
A. y Ulevitch, R. J., Nature, 2000, 406:782-787). El aumento del sistema inmunitario con estimuladores inmunitarios naturales así como sintéticos ofrece una ventaja distinta sobre las terapias convencionales especialmente con el sistema inmunitario debilitado y resistencia a antibióticos.
Varias investigaciones preclínicas y clínicas han indicado la utilidad de los β-glucanos, una clase de modificadores de la respuesta biológica (MRB), para la aceleración de la cicatrización de heridas y contra la orquestación del síndrome de la respuesta inflamatoria generalizada y el choque séptico (Ross, G. D. et al., Immunopharmacology, 1999, 42:61-74; Williams, D. L., Mediators Inflamm., 1997, 6:247-250; Hetland, G., Curr. Med. Chem., 2003, 2:135146). Los β-glucanos son potentes estimuladores del sistema inmunitario innato en los invertebrados, mientras que en los mamíferos son potentes activadores del sistema de complemento. Estos polímeros tienen potencial terapéutico debido a sus efectos sobre el sistema inmunitario que pueden incluir actividades antitumorales y antiinfecciosas, así como la protección contra infecciones por hongos, bacterias, virus y protozoos. Los β-glucanos solubles y en partículas interactúan con receptores afines en los macrófagos que estimulan la síntesis... [Seguir leyendo]
Reivindicaciones:
1. Compuesto aislado que presenta la estructura química siguiente (I) o una sal farmacéuticamente aceptable del mismo:
2. Composición farmacéutica que comprende un compuesto aislado que presenta la estructura química siguiente (I)
**(Ver fórmula)**
o una sal farmacéuticamente aceptable del mismo; y un vehículo farmacéuticamente aceptable:
**(Ver fórmula)**
3. Composición farmacéutica según la reivindicación 2, que comprende además un facilitador inmunomodulador. 15
4. Composición farmacéutica según la reivindicación 2 ó 3, que comprende además un antígeno.
5. Composición farmacéutica según la reivindicación 2 ó 3, que comprende además un adyuvante.
7. Composición farmacéutica según cualquiera de las reivindicaciones 2 a 6, que comprende además un agente anticanceroso. 9. Composición farmacéutica según cualquiera de las reivindicaciones 2 a 8, que comprende además un agente quimioterapéutico. 30 10. Composición farmacéutica según cualquiera de las reivindicaciones 2 a 9, que comprende además un inmunomodulador seleccionado de entre el grupo constituido por el factor de necrosis tumoral (TNF), interferón, factor de crecimiento nervioso (NGF), factor de crecimiento plaquetario (PDGF) y activador de plasminógeno tisular. 11. Composición farmacéutica según cualquiera de las reivindicaciones 2 a 10, que comprende además un modificador de la respuesta biológica seleccionado de entre el grupo constituido por linfocina, interleucina y factor de crecimiento. 12. Procedimiento para la estimulación de una respuesta inmunitaria, que comprende administrar una cantidad eficaz del compuesto aislado según la reivindicación 1 a células in vitro. 13. Utilización de un compuesto según la reivindicación 1, en la preparación de un medicamento para estimular un sistema inmunitario en un paciente. 14. Utilización según la reivindicación 13, en la que el sistema inmunitario del paciente se estimula por activación de los macrófagos. 15. Utilización según la reivindicación 13 ó 14, en la que el sistema inmunitario del paciente se estimula por una o más de las maneras siguientes: (a) aumento en la activación de las células destructoras naturales (NK); (b) aumento en la síntesis del factor de necrosis tumoral (TNF)-alfa eN macrófagos; (c) aumento en la síntesis de la proteína quimiotáctica de macrófagos (MCP)-1; (d) activación de NF-κB; (e) aumento en la producción de citocina Th1; y (f) aumento en la cantidad de C3a des Arg de la ruta de activación del complemento alternativa. 16. Utilización según cualquiera de las reivindicaciones 13 a 15, en la que el paciente padece un trastorno de proliferación celular. 17. Utilización según la reivindicación 16, en la que el trastorno de proliferación celular es el cáncer. 18. Utilización según cualquiera de las reivindicaciones 13 a 17, en la que el paciente padece una infección. 19. Procedimiento para la obtención de RR1 del material de la planta Tinospora cordifolia, que comprende: (a) proporcionar material de la planta Tinospora cordifolia; y (b) extraer el compuesto según la reivindicación 1. 20. Procedimiento según la reivindicación 19, que comprende además mezclar el compuesto extraído con un vehículo farmacéuticamente aceptable para formar una composición farmacéutica. 20 6. Composición farmacéutica según la reivindicación 2 ó 3, que comprende además un antígeno y un adyuvante.
25 8. Composición farmacéutica según cualquiera de las reivindicaciones 2 a 7, que comprende además un agente citotóxico.
Patentes similares o relacionadas:
USO DE POLI-ALFA-1,4-GLUCANOS LINEALES COMO ALMIDON RESISTENTE, del 22 de Febrero de 2010, de BAYER CROPSCIENCE AG: Uso de poli-alfa-1,4-D-glucanos lineales insolubles en agua como almidón resistente (RS), caracterizado porque los poli-alfa-1,4-D-glucanos no están […]
Separación de contaminantes de polisacárido de Streptococcus pneumoniae por manipulación del pH, del 17 de Junio de 2020, de WYETH LLC: Un procedimiento de reducción del contenido de proteínas y preservar el contenido de polisacárido capsular en un caldo de lisado celular complejo de Streptococcus pneumoniae, […]
Compuestos y sus efectos sobre el control del apetito y la sensibilidad a la insulina, del 10 de Junio de 2020, de IMPERIAL COLLEGE INNOVATIONS LIMITED: Un éster de propionato de inulina para su uso en la terapia para la reducción del apetito, ingesta de alimentos y/o ingesta de calorías y/o para mejorar […]
Evaluación de preparaciones de heparina, del 10 de Junio de 2020, de MOMENTA PHARMACEUTICALS, INC: Un procedimiento para identificar si se utilizó un procedimiento que incluye oxidación u oxidación seguido de tratamiento con un ácido para elaborar […]
Preparación de poli(ésteres de alfa-1,3-glucano) usando anhídridos orgánicos cíclicos, del 3 de Junio de 2020, de DuPont Industrial Biosciences USA, LLC: Una composición que comprende un compuesto de poli(éster de alfa-1,3-glucano) representado por la estructura **(Ver fórmula)** en donde (i) n es al menos […]
Composiciones detergentes, del 3 de Junio de 2020, de DuPont Industrial Biosciences USA, LLC: Una composición que comprende un derivado de polisacárido, en donde el derivado de polisacárido comprende un polisacárido sustituido con: a) uno o más grupos de poliamina; […]
 Método de desacetilación de biopolímeros, del 27 de Mayo de 2020, de GALDERMA S.A.: Un método para la desacetilación al menos parcial de un glucosaminoglucano que comprende grupos acetilo, que comprende:
a1) proporcionar un glucosaminoglucano que comprende […]
Método de desacetilación de biopolímeros, del 27 de Mayo de 2020, de GALDERMA S.A.: Un método para la desacetilación al menos parcial de un glucosaminoglucano que comprende grupos acetilo, que comprende:
a1) proporcionar un glucosaminoglucano que comprende […]
Reticulante de carbohidratos, del 6 de Mayo de 2020, de GALDERMA S.A.: Un producto de hidrogel que comprende moléculas de glucosaminoglucano como el polímero hinchable, en donde las moléculas de glucosaminoglucano se reticulan covalentemente […]