Inhibidores de la dipeptidil peptidasa.
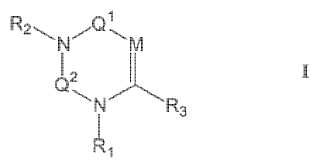
Compuesto que comprende: (Ver fórmula) en la que M es CR4; R2 es hidrógeno o se selecciona de entre el grupo constituido por alquilo(C1 - 10),
cicloalquilo(C3 - 12), cicloalquilo (C3 - 12)alquilo(C1 - 5), heterocicloalquil(C3 - 12)alquil(C1 - 5), heterocicloalquil(C3 - 12), arilalquilo(C1 - 10), heteroarilalquilo (C1 - 5), bicicloaril(C9 - 12), heterobicicloaril(C4 - 12), heterobicicloaril(C4 - 12)alquil(C1 - 5), carbonilalquil(C1 - 3), tiocarbonilalquil( C1 - 3), sulfonilalquil(C1 - 3), sulfinilalquil(C1 - 3), iminoalquil(C1 - 3), amino, arilo, heteroarilo, hidroxi, alcoxi, ariloxi, heteroariloxi, grupo carbonilo, grupo imino, grupo sulfonilo y grupo sulfinilo, cada uno sustituido o no sustituido; R3 comprende la fórmula, (Ver fórmula) siendo seleccionados R10 y R11 cada uno independientemente de entre el grupo constituido por hidrógeno, perhaloalquil (C1 - 10), amino, alquilo(C1 - 10), cicloalquilo(C3 - 12), heterocicloalquilo(C3 - 12), arilalquilo(C1 - 10), heteroarilalquilo(C1 - 5), bicicloarilo(C9 - 12), heterobicicloarilo(C4 - 12), carbonilalquilo(C1 - 3), tiocarbonilalquilo(C1 - 3), arilo, heteroarilo, hidroxi, alcoxi, ariloxi, heteroariloxi, grupo carbonilo, grupo sulfonilo y grupo sulfinilo, sustituido o no sustituido cada uno, o R10 y R11 se consideran conjuntamente para formar un anillo de 4, 5, 6 ó 7 miembros, cada uno sustituido o no sustituido; R4 es hidrógeno o se selecciona de entre el grupo constituido por halo, perhaloalquil(C1 - 10), amino, amino, ciano, tio, alquilo (C1 - 10), cicloalquilo, heterocicloalquilo, arilalquilo, heteroarilalquilo, arilo, heteroarilo, carbonilalquilo (C1 - 3), tiocarbonilalquilo(C1 - 3), sulfonilalquilo(C1 - 3), sulfinilalquilo(C1 - 3), iminoalquilo(C1 - 3), hidroxi, alcoxi, ariloxi, heteroariloxi, grupo carbonilo, grupo imino, grupo sulfonilo y grupo sulfinilo, sustituido o no sustituido cada uno; y -L-X considerados conjuntamente se seleccionan de entre el grupo constituido por -(CH2)-(2-ciano)fenilo; -(CH2)-( 3-ciano)fenilo; -(CH2)-(2-hidroxi)fenilo; -(CH2)-(3-hidroxi)-fenilo; -(CH2)-(2-alquenil)fenilo; -(CH2)-(3-alquenil)fenilo; -(CH2)-(2-alquinil)fenilo; -(CH2)-(3-alquinil)fenilo; -(CH2)-(2-metoxi)fenilo; -(CH2)-(3-metoxi)fenilo; -(CH2)-( 2-nitro)fenilo; -(CH2)-(3-nitro)fenilo; -(CH2)-(2-carboxi)fenilo; -(CH2)-(3-carboxi)fenilo; -(CH2)-(2-carboxamido)-fenilo; -(CH2)-(3-carboxamido)fenilo; -(CH2)-(2-sulfonamido)fenilo; -(CH2)-(3-sulfonamido)-fenilo; -(CH2)-(2-tetrazolil) fenilo; -(CH2)-(3-tetrazolil)fenilo; -(CH2)-(2-aminometil)fenilo; -(CH2)-(3-aminometil)fenilo; -(CH2)-(2-hidroximetil) fenilo; -(CH2)-(3-hidroximetil)fenilo; -(CH2)-(2-fenil)fenilo; -(CH2)-(3-fenil)fenilo; -(CH2)-(2-halo)fenilo; -(CH2)-(3-halo)fenilo; -(CH2)-(2-CONH2)fenilo; -(CH2)-(3-CONH2)fenilo; -(CH2)-(2-CONH(alquil(C1 - 7))fenilo; -(CH2)-(3-CONH(alquil(C1 - 7))fenilo; -(CH2)-(2-CO2(alquil(C1 - 7))fenilo; -(CH2)-(3-CO2alquil (C1 - 7))fenilo; -(CH2)-( 2-NH2)fenilo; -(CH2)-(3-NH2)fenilo; -(CH2)-(2-alquil(C3 - 7))fenilo; -(CH2)-(3-alquil(C3 - 7))fenilo; -(CH2)-(2-cicloalquil( C3 - 7))fenilo; -(CH2)-(3-cicloalquil(C3 - 7))-fenilo; -(CH2)-(2-aril)fenilo; -(CH2)-(3-aril)fenilo; -(CH2)-(2-heteroaril) fenilo; -(CH2)-(3-heteroaril)fenilo; -(CH2)-2-bromo-5-fluorofenilo; -(CH2)-2-cloro-5-fluorofenilo; -(CH2)-2-ciano-5- fluorofenilo; -(CH2)-2,5-diclorofenilo; -(CH2)-2,5-difluorofenilo; -(CH2)-2,5-dibromofenilo; -(CH2)-2-bromo-3,5- difluorofenilo; -(CH2)-2-cloro-3,5-difluorofenilo; -(CH2)-2,3,5-trifluorofenilo; -(CH2)-2,3,5,6-tetrafluorofenilo; -(CH2)-2-bromo-3,5,6-trifluorofenilo; -(CH2)-2-cloro-3,5,6-trifluorofenilo; -(CH2)-2-ciano-3,5-difluorofenilo; -(CH2)-2-ciano-3,5,6-trifluorofenilo; -(CH2)-(2-heterocicloalquil)fenilo; y -(CH2)-(3-heterocicloalquil)fenilo, cada uno sustituido o no sustituido.
Tipo: Patente Europea. Resumen de patente/invención. Número de Solicitud: E04258153.
Solicitante: TAKEDA PHARMACEUTICAL COMPANY LIMITED.
Nacionalidad solicitante: Japón.
Dirección: 1-1, DOSHOMACHI 4-CHOME CHUO-KU OSAKA-SHI OSAKA 541-0045 JAPON.
Inventor/es: STAFFORD, JEFFREY A., FENG,JUN, GWALTNEY,II,STEPHEN,L, ZHANG,ZHIYUAN, ELDER,BRUCE J, ISBESTER,PAUL K, PALMER,GRANT J, SALSBURY,JONATHON S, ULYSEE,LUCKNER G.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K31/506 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › no condensadas y conteniendo otros heterociclos.
- A61P3/10 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › A61P 3/00 Medicamentos para el tratamiento de trastornos del metabolismo (de la sangre o de fluido extracelular A61P 7/00). › para la hiperglucemia, p.ej. antidiabéticos.
- A61P35/00 A61P […] › Agentes antineoplásicos.
- C07D401/04 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07D COMPUESTOS HETEROCICLICOS (Compuestos macromoleculares C08). › C07D 401/00 Compuestos heterocíclicos que contienen dos o más heterociclos, que tienen átomos de nitrógeno como únicos heteroátomos del ciclo, siendo al menos un ciclo de seis miembros con solamente un átomo de nitrógeno. › directamente unidos por un enlace entre dos miembros cíclicos.
- C07D401/12 C07D 401/00 […] › unidos por una cadena que contiene heteroátomos como enlaces de cadena.
- C07D401/14 C07D 401/00 […] › que contienen tres o más heterociclos.
PDF original: ES-2310704_T3.pdf
Fragmento de la descripción:
Inhibidores de la dipeptidil peptidasa La invención se refiere a compuestos que pueden usarse para inhibir las dipeptidil peptidasas así como a las composiciones de materia y a los kits que comprenden estos compuestos. La presente invención se refiere asimismo a los procedimientos para inhibir las dipeptidil peptidasas así como a los procedimientos de tratamiento que usan compuestos según la presente invención.
La dipeptidil peptidasa IV (nomenclatura de enzimas IUBMB EC.3.4.14.5) es una proteína membranaria de tipo II que ha sido citada en la bibliografía por una amplia variedad de denominaciones que incluyen DPP4, DP4, DAP-IV, FAPß, proteína 2 acomplejante de la adenosina desaminasa, proteína de unión a la adenosina desaminasa (ADAbp) , dipeptidilaminopeptidasa IV; Xaa-Pro-dipeptidilaminopeptidasa; Gly-Pro naftilamidasa; posprolina dipeptidil aminopeptidasa IV; linfocito antígeno CD26; glucoproteína GP110; dipepditil peptidasa IV; glicilprolina aminopeptidasa; glicilprolina aminopeptidasa; X-prolil-dipeptidil aminopeptidasa; pep X; leucocito antígeno CD26; glicilprolil dipeptidilaminopeptidasa; dipeptidil-péptido hidrolasa; glicilpropil aminopeptidasa; dipeptidilaminopeptidasa IV; DPP IV/CD26; amino acil-prolil dipeptidil aminopeptidasa; molécula Tp103 activadora de linfocitos T; X-PDAP. La dipeptidil peptidasa IV se cita en la presente memoria descriptiva como "DPP-IV".
La DPP-IV es una serina aminodipeptidasa no clásica que elimina dipéptidos Xaa-Pro del terminal amino (terminal N) de polipéptidos y proteínas. La DPP-IV dependiente de la liberación lenta de los dipéptidos de tipo X-Gly o X-Ser ha sido también descrita para algunos péptidos naturales.
La DPP-IV se expresa de manera constitutiva en las células epiteliales y endoteliales de una variedad de tejidos diferentes (intestino, hígado, pulmón, riñón y placenta) y se encuentra también en los fluidos corporales. La DPP-IV se expresa también en los linfocitos T circulantes y se ha demostrado que es sinónimo del antígeno de la superficie celular, CD-26. La DPP-IV ha estado implicada en numerosas enfermedades, algunas de las cuales se exponen a continuación.
La DPP-IV es responsable de la escisión metabólica de determinados péptidos endógenos (GLP-1 (7-36) , glucagón) in vivo y ha demostrado actividad proteolítica frente a una variedad de otros péptidos (GHRH, NPY, GLP2, VIP) in vitro.
GLP-1 (7-36) es un péptido de 29 aminoácidos obtenido por tratamiento después de la traducción del proglucagón en el intestino delgado. GLP-1 (7-36) presenta múltiples acciones in vivo incluyendo la estimulación de la secreción de insulina, la inhibición de la secreción de glucagón, la estimulación de la saciedad y la reducción del vacío gástrico. Basándose en su perfil fisiológico, las acciones de GLP-1 (7-36) se cree que son beneficiosas en la prevención y el tratamiento de la diabetes de tipo II y potencialmente en la obesidad. Por ejemplo, la administración exógena de GLP-1 (7-36) (infusión continua) en pacientes diabéticos se ha descubierto que es eficaz en esta población de pacientes. Desgraciadamente, GLP-1 (7-36) se degrada rápidamente in vivo y se ha demostrado que tiene una vida media corta in vivo (t1/2=1, 5 minutos) .
Basándose en un estudio de ratones modificados genéticamente alimentados con DPP-IV y en estudios in vivo/in vitro con inhibidores selectivos de DPP-IV, se ha demostrado que DPP-IV es la enzima degradadora primaria de 45 GLP-1 (7-36) in vivo. GLP-1 (7-36) es degradado por DPP-IV eficazmente a GLP-1 (9-36) , que se ha especulado que actúa como antagonista fisiológico para GLP-1 (7-36) . La inhibición de DDP-IV in vivo se cree por consiguiente que es útil para potenciar los niveles endógenos de GLP-1 (7-36) y atenuar la formación de su antagonista GLP-1 (9-36) . Por lo tanto, se cree que los inhibidores de DPP-IV son agentes útiles para la prevención, retardo de la evolución y/o tratamiento de enfermedades mediadas por DPP-IV, en particular la diabetes y más específicamente, la diabetes mellitus de tipo 2, la dislipidemia diabética, enfermedades de tolerancia a la glucosa alterada (IGT) , enfermedades de glucosa en el plasma alterada en ayunas (IFG) , acidosis metabólica, cetosis, regulación del apetito y obesidad.
La expresión de DPP-IV aumenta en los linfocitos T durante la estimulación mitógena o antígena (Mattem, T., et al., Scand. J. Immunol., 1991, 33, 737) . Se ha comunicado que los inhibidores de DDP-IV y los anticuerpos contra DDP55 IV suprimen la proliferación de linfocitos T estimulados por mitógenos y estimulados por antígenos en función de la dosis (Schon, E., et al., Biol. Chem., 1991, 372, 305) . Otras diversas funciones de los linfocitos T tales como la producción de citocina, la proliferación de células mediada por IL-2 y la actividad cooperadora de los linfocitos B se han demostrado que dependen de la actividad de DPP-IV (Schon, E., et al., Scand. J. Immunol., 1989, 29, 127) . Los inhibidores de DDP-IV, basados en boroProlina, (Flentke, G. R., et al., Proc. Natl. Acad. Sci. USA, 1991, 88, 1556) aunque inestable, resultaron ineficaces en la inhibición de la proliferación de linfocitos inducida por antígenos y en la producción de IL-2 en linfocitos T cooperadores CD4+ murinos. Dichos inhibidores de ácido bórico se ha demostrado que tienen un efecto in vivo en ratones que origina la supresión de la producción de anticuerpos provocada por la prueba de provocación inmunitaria (Kubota, T. et al., Clin. Exp. Immun., 1992, 89, 192) . La función de DPP-IV en la regulación de la actividad de los linfocitos T puede atribuirse también, en parte, a su asociación en 65 la superficie celular con la fosfatasa transmembranaria, CD45. Los inhibidores de DDP-IV o los ligandos de zonas no activas pueden destruir posiblemente la asociación CD45-DPP-IV. Se sabe que CD45 es un componente integral
del aparato de señalización de los linfocitos T. Se ha publicado que DPP-IV es esencial para la penetración e infección de los virus VIH-1 y VIH-2 en los linfocitos T CD4+ (Wakselman, M., Nguyen, C., Mazaleyrat, J. P, Callebaut, C., Krust, B., Hovanessian, A.G., Inhibition of HIV-1 infection of CD 26+ but not CD 26-cells by a potent cyclopeptidic inhibitor of the DPP-IV activity of CD 26. Resumen P.44 del 24º simposio europeo de péptidos 1996) .
Además, se ha demostrado que DPP-IV se asocia con la enzima adenosina desaminasa (ADA) en la superficie de los linfocitos T (Kameoka, J., et al., Science, 193, 26466) . La insuficiencia de ADA produce la enfermedad de la inmunodeficiencia combinada grave (SCID) en seres humanos. Esta interacción ADA-CD26 puede proporcionar claves para la patofisiología de SCID. Ello obedece a que los inhibidores de DPP-IV pueden ser inmunosupresores útiles (o fármacos supresores de la liberación de citocina) para el tratamiento de entre otras cosas: el rechazo del trasplante de órganos; las enfermedades autoinmunitarias tales como la enfermedad inflamatoria del intestino, la esclerosis múltiple y la artritis reumatoide; y el tratamiento del SIDA.
Se ha demostrado que la célula DPP-IV endotelial pulmonar es una molécula de adhesión para la mama de rata con metástasis pulmonar y células de carcinoma de próstata (Johnson, R. C., et al., J. Cell. Biol., 1993, 121, 1423) .
Es conocido que la DPP-IV se une a la fibronectina y a algunas células tumorales metastásicas son conocidas por transportar grandes cantidades de fibronectina en su superficie. Los potentes inhibidores de DPP-IV pueden ser útiles como fármacos para impedir la metástasis, por ejemplo, de tumores de mama y de próstata a los pulmones.
Se han descubierto también altos niveles de expresión de DPP-IV en células de fibroblasto de piel humana en pacientes con psoriasis, artritis reumatoide (RA) y liquen plano (Raynaud, F., et al., J. Cell. Physiol., 1992, 151, 378) . Por consiguiente, los inhibidores de DPP-IV pueden ser útiles como agentes para tratar enfermedades dermatológicas tales como la psoriasis y el liquen plano.
Se ha descubierto gran actividad de DPP-IV en homogeneizados de tejido de pacientes con hipertrofia de próstata benigna y en prostatosomas. Existen orgánulos obtenidos de la próstata importantes para el aumento de motilidad hacia adelante del esperma (Vanhoof, G., et al., Eur. J. Clin. Chem. Clin. Biochem., 1992, 30, 333) . Los inhibidores de DPP-IV pueden también actuar para suprimir la motilidad del esperma y por consiguiente actuar como agente anticonceptivo masculino. Por el contrario, los inhibidores de DPP-IV han estado implicados como nuevos para el tratamiento de la infecundidad y particularmente la infecundidad femenina humana debida al síndrome poliquístico del ovario (PCOS, síndrome de Stein-Leventhal) que... [Seguir leyendo]
Reivindicaciones:
1. Compuesto seleccionado de entre el grupo constituido por:
2. {6-[3-amino-piperidin-1-il]-3-metil-2, 4-dioxo-3, 4-dihidro-2H-pirimidin-1-ilmetil}-benzonitrilo; y 2-[6- (3-amino-piperidin-1-il) -3-metil-2, 4-dioxo-3, 4-dihidro-2H-pirimidin-1-ilmetil]-4-fluoro-benzonitrilo.
2. Compuesto seleccionado de entre el grupo constituido por:
2. {6-[3 (R) -amino-piperidin-1-il]-3-metil-2, 4-dioxo-3, 4-dihidro-2H-pirimidin-1-ilmetil}-benzonitrilo; y 2-[6- (3 (R) -amino-piperidin-1-il) -3-metil-2, 4-dioxo-3, 4-dihidro-2H-pirimidin-1-ilmetil]-4-fluoro-benzonitrilo.
3. Compuesto según cualquiera de las reivindicaciones 1 a 2, en el que el compuesto está en forma de sal farmacéuticamente aceptable.
4. Compuesto según cualquiera de las reivindicaciones 1 a 3, en el que el compuesto está presente en una mezcla de estereoisómeros.
5. Compuesto según cualquiera de las reivindicaciones 1 a 3, en el que el compuesto comprende un solo estereoisómero.
6. Compuesto según la reivindicación 1, constituido por 2-{6-[3 (R) -amino-piperidin-1-il]-3-metil-2, 4-dioxo-3, 4-dihidro2.
2. pirimidin-1-ilmetil}-benzonitrilo.
7. Compuesto según la reivindicación 1, constituido por una sal benzoato de 2-{6-[3 (R) -amino-piperidin-1-il]-3-metil2, 4-dioxo-3, 4-dihidro-2H-pirimidin-1-ilmetil}-benzonitrilo.
8. Compuesto según la reivindicación 1, constituido por 2-[6- (3-amino-piperidin-1-il) -3-metil-2, 4-dioxo-3, 4-dihidro-2Hpirimidin-1-ilmetil]-4-fluoro-benzonitrilo.
9. Compuesto según la reivindicación 1, constituido por una sal succinato de 2-[6- (3-amino-piperidin-1-il) -3-metil-2, 4dioxo-3, 4-dihidro-2H-pirimidin-1-ilmetil]-4-fluoro-benzonitrilo.
3.
10. Composición farmacéutica que comprende, como ingrediente activo, un compuesto según cualquiera de las reivindicaciones 1 a 9.
11. Composición farmacéutica según la reivindicación 10, en la que la composición es una formulación sólida adaptada para la administración oral.
12. Composición farmacéutica según la reivindicación 11, en la que la composición es un comprimido.
13. Composición farmacéutica según la reivindicación 11, en la que la composición es una formulación líquida 45 adaptada para la administración oral.
14. Composición farmacéutica según la reivindicación 10, en la que la composición es una formulación líquida adaptada para la administración parenteral.
15. Composición farmacéutica que comprende un compuesto según cualquiera de las reivindicaciones 1 a 9, en la que la composición está adaptada para la administración por una vía seleccionada de entre el grupo constituido por las vías oral, parenteral, intraperitoneal, intravenosa, intraarterial, transdérmica, sublingual, intramuscular, rectal, transbucal, intranasal, liposomal, por inhalación, vaginal, intraocular, por suministro local (por ejemplo mediante catéter o endoprótesis vascular) , subcutánea, intradiposa intrarticular, y intratecal.
5.
16. Kit que comprende:
un compuesto según cualquiera de las reivindicaciones 1 a 9; e instrucciones que comprenden una o más formas de información seleccionadas de entre el grupo constituido por indicar un estado patológico para el que se debe administrar el compuesto, información sobre el almacenamiento del compuesto, información de la dosificación de instrucciones con respecto a cómo administrar el compuesto.
17. Kit según la reivindicación 16, en el que el kit comprende el compuesto en una forma de dosis múltiple. 6.
18. Artículo de preparación que comprende:
un compuesto según cualquiera de las reivindicaciones 1 a 9; y materiales de embalaje.
19. Artículo de preparación según la reivindicación 18, en el que el material de embalaje comprende un recipiente para alojar el compuesto.
20. Artículo de preparación según la reivindicación 19, en el que el recipiente comprende una etiqueta que indica uno o más elementos de entre el grupo constituido por un estado patológico para el que se administra el 10 compuesto, información sobre el almacenamiento, información sobre la dosificación e instrucciones con respecto a cómo administrar la composición.
21. Artículo de preparación según la reivindicación 18, en el que el artículo de preparación comprende el compuesto en una forma de dosis múltiple. 1.
22. Procedimiento para producir una pirimidin-diona de fórmula:
** (Ver fórmula) **
que comprende:
(i) mezclar la 6-cloro-1H-pirimidina-2, 4-diona con un haluro de arilo de fórmula
** (Ver fórmula) **
en la que Hal es Br, Cl o I, en condiciones suficientes para producir un compuesto de fórmula
** (Ver fórmula) **
(ii) alquilar el producto anterior con un haluro de metilo en condiciones suficientes para formar un compuesto de fórmula
** (Ver fórmula) **
y (iii) condensar el producto anterior con un compuesto de fórmula
** (Ver fórmula) **
23. Procedimiento para producir una pirimidin-diona según la reivindicación 22, que comprende además la formación de la sal de adición de ácido.
24. Procedimiento según la reivindicación 23, en el que la sal de adición de ácido es la sal benzoato.
25. Compuesto según cualquiera de las reivindicaciones 1 a 9, para uso como medicamento.
.
26. Uso de un compuesto según cualquiera de las reivindicaciones 1 a 9, en la preparación de un medicamento para tratar el cáncer.
27. Uso de un compuesto según cualquiera de las reivindicaciones 1 a 9, en la preparación de un medicamento 10 para tratar la diabetes tipo I o tipo II.
28. Uso de un compuesto según cualquiera de las reivindicaciones 1 a 9, en la preparación de un medicamento para tratar trastornos autoinmunitarios.
29. Uso de un compuesto según cualquiera de las reivindicaciones 1 a 9, en la preparación de un medicamento para tratar una enfermedad caracterizada porque presenta la activación o concentración inadecuada de linfocitos o de células hematopoyéticas.
30. Uso de un compuesto según cualquiera de las reivindicaciones 1 a 9, en la preparación de un medicamento 20 para tratar la infección por el VIH.
31. Uso de un compuesto según cualquiera de las reivindicaciones 1 a 9, en la preparación de un medicamento para tratar una enfermedad caracterizada porque presenta síntomas de inmunodeficiencia.
Patentes similares o relacionadas:
Compuestos heterocíclicos que activan AMPK y métodos de uso de los mismos, del 29 de Julio de 2020, de RIGEL PHARMACEUTICALS, INC.: Un compuesto que es N-((cis)-1-(4-cianobencil)-3-fluoropiperidin-4-il)-6-(4-(4-metoxibenzoil)piperidin-1-carbonil)nicotinamida; N-((3S,4S)-1-(4-cianobencil)-3-fluoropiperidin-4-il)-6-(4-(4-metoxibenzoil)piperidin-1-carbonil)nicotinamida; […]
Derivados de piperidina 1,4 sustituidos, del 29 de Julio de 2020, de 89Bio Ltd: Un compuesto de acuerdo con la Fórmula I: **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en donde: A se selecciona de […]
Compuestos y procedimientos de uso, del 29 de Julio de 2020, de Medivation Technologies LLC: Un compuesto de fórmula (Aa-1): **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en la que: A representa H, halógeno, amino, […]
Ureas asimétricas p-sustituidas y usos médicos de las mismas, del 22 de Julio de 2020, de Helsinn Healthcare SA: Un compuesto de Fórmula I: **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en donde: una línea discontinua indica un enlace opcional; X es CH; […]
Ureas cíclicas como inhibidores de ROCK, del 22 de Julio de 2020, de BRISTOL-MYERS SQUIBB COMPANY: Un compuesto de acuerdo con la Fórmula (I): **(Ver fórmula)** o un enantiómero, un diastereómero, un estereoisómero, un tautómero, una sal farmacéuticamente aceptable […]
Inhibidores de btk de tipo nicotinimida sustituida y su preparación y uso en el tratamiento del cáncer, la inflamación y las enfermedades autoinmunitarias, del 15 de Julio de 2020, de Guangzhou InnoCare Pharma Tech Co., Ltd: Un compuesto seleccionado del grupo que consiste en: 6-(1-acriloilpiperidin-4-il)-2-(4-fenoxifenil)nicotinamida; **(Ver fórmula)** 6-(4-acriloilpiperazin-1-il)-2-(4-fenoxifenil)nicotinamida; […]
Formas en estado sólido de sales de Nilotinib, del 15 de Julio de 2020, de PLIVA HRVATSKA D.O.O: Una forma cristalina de fumarato de Nilotinib designada como Forma III, caracterizada por datos seleccionados de uno o más de los siguientes: a. un patrón de […]
Inhibidores de Bcl-2/Bcl-xL y su uso en el tratamiento de cáncer, del 15 de Julio de 2020, de THE REGENTS OF THE UNIVERSITY OF MICHIGAN: Compuesto que tiene una estructura **(Ver fórmula)**