Inhibidores de azaindol de las cinasas Aurora.
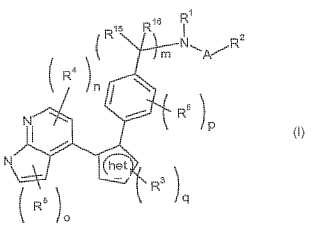
Un compuesto de fórmula (I):**Fórmula**
o una sal farmacéuticamente aceptable del mismo,
en la que:**Fórmula**
representa un fragmento de un anillo heteroaromático de 5 miembros;
A es >C≥Y o >S(O)x en la que Y es O, S o N-R1; en la que x es 1 ó 2;
R1 es independientemente H, alquilo C1-C3 o ciclopropilo;
R2 es H, alquilo C1-C6, haloalquilo C1-C6, cicloalquilo C3-C6, alcoxi C1-C6, hidroxialquilo C1-C6, aminoalquilo C1-C6,alcoximetilo C1-C6, hidroxi, -(CH2)10 y-Ar-(R7)z, o NR8R9, con la condición de que cuando A sea S(O)x, R2 no sea H; enla que y es 0, 1 ó 2; y z es un número entero no negativo no mayor que el número de posiciones disponibles en el Arpara sustitución;
Ar es fenilo o heteroarilo;
R3 es independientemente H, alquilo C1-C6, alquenilo C2-C6, haloalquilo C1-C6, hidroxialquilo C1-C6, aminoalquilo C1-C6, alquilamino C1-C6 alquilo C1-C6, dialquilamino C1-C6 alquilo C1-C6, -(CH2)w-R10; en la que w es 1 ó 2;
R4 es independientemente alquilo C1-C6, halo, haloalquilo C1-C6 o Ar-(R7)z;
R5 es independientemente alquilo C1-C6, halo, haloalquilo C1-C6-, Ar-(R7)z, -(CH2)aNR13R14, -Ar-(CH2)aNR13R14, -A'-NR1-(CH2)b-A'', -CH2CH2C(O)-A''' o -Ar'-(C(O)(CH2)aNR13R14)c;
en la que A' es C(O) o CH2; A" es H, NR13R14, tioalquilo C1-C6, alcoxi C1-C6, -SO2CH3 u -OH; A'" es -OH, alcoxi C1-C6o -NR13R14; y Ar' es un anillo heterocicloalquilo de 5 ó 6 miembros;
en la que a es independientemente 0, 1 ó 2; b es 1, 2 ó 3, con la condición de que cuando b sea 1, A" sea H; y c sea0 ó 1;
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2006/062289.
Solicitante: GLAXOSMITHKLINE LLC.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: ONE FRANKLIN PLAZA 200 NORTH 16TH STREET PHILADELPHIA, PA 19102 ESTADOS UNIDOS DE AMERICA.
Inventor/es: DHANAK, DASHYANT, ADAMS, JERRY LEROY, NEWLANDER, KENNETH ALLEN, TANG,JUN, AXTEN,JEFFREY,MICHAEL, SILVA,Domingos,J, ADAMS,NICHOLAS D, CHAUDHARI,AMITA M, HAMAJIMA,TOSHIHIRO, PARRISH,CYNTHIA A, SARPONG,MARTHA A.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K31/00 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › Preparaciones medicinales que contienen ingredientes orgánicos activos.
- A61K31/335 A61K […] › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › que tienen el oxígeno como único heteroátomo de un ciclo, p. ej. fungicromina.
- A61K31/437 A61K 31/00 […] › conteniendo el sistema heterocíclico un ciclo de cinco eslabones teniendo el nitrógeno como heteroátomo del ciclo, p. ej. indolicina, beta-carbolina.
PDF original: ES-2408318_T3.pdf
Fragmento de la descripción:
Inhibidores de azaindol de las cinasas Aurora
Antecedentes de la invención La presente invención se refiere a compuestos de azaindol, a composiciones y medicamentos del mismo, así como a los usos del mismo. Estos azaindoles inhiben la cinasa Aurora.
Las cinasas de proteínas catalizan la fosforilación de las cadenas laterales de los aminoácidos hidroxílicos en proteínas mediante la transferencia del γ-fosfato del ATP-Mg2+ para formar un éster monofosfato de serina, treonina o tirosina. Algunos estudios han demostrado que las cinasas de proteínas son reguladores clave de muchas funciones celulares, incluyendo la transducción de señales, la regulación de la transcripción, la motilidad celular y la división celular. También se ha demostrado que varios oncogenes codifican para cinasas de proteínas, lo que sugiere que las cinasas pueden jugar un papel en la oncogénesis.
La familia de enzimas de cinasas de proteínas se clasifica típicamente en dos subfamilias principales: las tirosina cinasas de proteínas y las serina/treonina cinasas de proteínas, en base al residuo de aminoácido que fosforilan. La actividad aberrante de las serina/treonina cinasas de proteínas se ha implicado o es sospechosa en varias patologías tales como artritis reumatoide, psoriasis, choque séptico, pérdida ósea, cánceres y otras enfermedades proliferativas. Las tirosina cinasas juegan un papel igualmente importante en la regulación celular. Estas cinasas incluyen varios receptores para moléculas tales como factores de crecimiento y hormonas, incluyendo el receptor del factor de crecimiento epidérmico, el receptor de insulina y el receptor del factor de crecimiento derivado de plaquetas. Algunos estudios han indicado que muchas tirosina cinasas son proteínas transmembranales con sus dominios de receptor ubicados en el exterior de la célula y sus dominios de cinasa en el interior. Por consiguiente, ambas subfamilias de cinasas y sus vías de transducción de señales son objetivos importantes para el diseño de fármacos.
Desde su descubrimiento en 1997, la familia Aurora de cinasas de serina/treonina de mamíferos se ha relacionado estrechamente con la oncogénesis. Los tres miembros de la familia conocidos en mamíferos, Aurora-A ("2") , B ("1") y C ("3") , son proteínas con una gran homología, responsables de la segregación cromosómica, de la función del huso mitótico y de la citocinesis. La expresión de Aurora es baja o indetectable en las células en reposo, con un pico de expresión y actividad durante las fases G2 y mitóticas en células en división. En las células de mamíferos, los sustratos propuestos para las cinasas Aurora A y B incluyen histona H3, CENP-A, cadena ligera reguladora de la miosina II, fosfatasa de proteína 1, TPX2, INCENP, p53 y survivina, muchos de los cuales son necesarios para la división celular.
Se ha informado de que las cinasas Aurora se sobreexpresan en una amplia variedad de tumores humanos. Se ha detectado una elevada expresión de Aurora A en cáncer colorrectal, de ovario y pancreático, y en adenocarcinomas invasivos de los conductos mamarios. También se ha informado de unos elevados niveles de Aurora A en líneas celulares tumorales renales, cervicales, de neuroblastoma, de melanoma, de linfoma, pancreáticas y prostáticas. Se observa una amplificación/sobreexpresión de Aurora A en cánceres de vejiga en seres humanos, y la amplificación de Aurora A está asociada con aneuploidía y un comportamiento clínico agresivo. Además, la amplificación del locus Aurora A (20q13) se correlaciona con un mal pronóstico en pacientes con cáncer de mama negativo en los nódulos. Además, se informa de que una variante alélica, con isoleucina en la posición del aminoácido 31, es un gen con una susceptibilidad tumoral de baja penetrancia y muestra un mayor potencial de transformación que la variante de fenilalanina-31, y está asociada con un aumento en el riesgo de enfermedad avanzada y metastásica. Al igual que la Aurora A, la Aurora B también es muy expresada en múltiples líneas celulares tumorales humanas, incluyendo células leucémicas. Los niveles de Aurora B aumentan en función de la etapa de Duke en cánceres colorrectales primarios. La Aurora C, que normalmente sólo se encuentra en células germinales, también se sobreexpresa en un elevado porcentaje de cánceres colorrectales primarios y en varias líneas celulares tumorales, incluyendo adenocarcinoma cervical y células de carcinoma de mama.
Se ha sugerido que in vitro, un inhibidor de la actividad de la cinasa Aurora altera la mitosis causando defectos en el ciclo celular y una posible muerte celular. Por lo tanto, in vivo, un inhibidor de la cinasa Aurora debería ralentizar el crecimiento tumoral e inducir su regresión. Por ejemplo, Hauf y col. describen un inhibidor de la Aurora B, Hesperadina, que causa defectos en la segregación cromosómica y un bloqueo en la citocinesis, dando así como resultado una poliploidía [Hauf, S y col. JCB 161 (2) , 281 -294 (2003) ]. Ditchfield y col. han descrito un inhibidor equipotente de Aurora A y B (ZM447439) que causa defectos en la alineación cromosómica, en la segregación cromosómica y en la citocinesis [Ditchfield, C. y col., JCB 161 (2) , 267 -280 (2003) ]. Adicionalmente, los autores muestran que las células en proliferación, pero no las células con el ciclo detenido, son sensibles al inhibidor. Recientemente se informó de la eficacia de un potente inhibidor de Aurora A y B en modelos de xenoinjerto de ratón y de rata [Harrington, E. A. y col., Nature Medicine 10 (3) , 262 -267, (2004) ]. Estos resultados demuestran que la inhibición de las cinasas Aurora puede proporcionar una ventana terapéutica para el tratamiento de trastornos proliferativos tales como el cáncer (véase Nature, Cancer Reviews, Vol. 4, págs. 927 -936, diciembre de 2004, para una revisión de N. Keen y S Taylor) .
En vistas de las enseñanzas de la técnica, hay una necesidad del descubrimiento de inhibidores de la actividad cinasa, en particular, de compuestos que inhiban la actividad de las cinasas Aurora.
Resumen de la invención En un primer aspecto, la presente invención es un compuesto de fórmula (I) :
o una sal farmacéuticamente aceptable del mismo, en la que:
representa un fragmento de un anillo heteroaromático de 5 miembros; A es >C=Y o >S (O) xen la que Y es O, S o N-R1; en la que x es 1 ó 2; R1 es independientemente H, alquilo C1-C3 o ciclopropilo; R2 es H, alquilo C1-C6, haloalquilo C1-C6, cicloalquilo C3-C6, alcoxi C1-C6, hidroxialquilo C1-C6, aminoalquilo C1-C6, alcoximetilo C1-C6, hidroxi, - (CH2) y-Ar- (R7) z, o NR8R9, con la condición de que cuando A es S (O) x, R2 no sea H; en la que y es 0, 1 ó 2; y z es un número entero no negativo no mayor que el número de posiciones disponibles en el Ar para sustitución; Ar es fenilo o heteroarilo; R3 es independientemente H, alquilo C1-C6, alquenilo C2-C6, haloalquilo C1-C6, hidroxialquilo C1-C6, aminoalquilo C1- C6, alquilamino C1-C6 alquilo C1-C6, dialquilamino C1-C6 alquilo C1-C6, - (CH2) w-R10; en la que w es 1 ó 2; R4 es independientemente alquilo C1-C6, halo, haloalquilo C1-C6 o Ar- (R7) z; R5 es independientemente alquilo C1-C6, halo, haloalquilo C1-C6-, Ar- (R7) z, - (CH2) aNR13R14, -Ar- (CH2) aNR13R14, -A’NR1- (CH2) b-A", -CH2CH2C (O) -A"’ o -Ar’- (C (O) (CH2) aNR13R14) c; en la que A’ es C (O) o CH2; A" es H, NR13R14, tioalquilo C1-C6, alcoxi C1-C6, -SO2CH3 u -OH; A’" es -OH, alcoxi C1-C6 o -NR13R14; y Ar’ es un anillo heterocicloalquilo de 5 ó 6 miembros; en la que a es independientemente 0, 1 ó 2; b es 1, 2 ó 3, con la condición de que cuando b es 1, A" es H; y c es 0 ó 1; R6 y cada R7 son cada uno independientemente halo, ciano, nitro, alquilo C1-C6, COOH, alquilcarbonilo C1-C6, alquilcarbonilo C1-C6 alquilo C1-C6, amino, alquilamino C1-C6, dialquilamino C1-C6, aminoalquilo C1-C6, alquilamino C1-C6 alquilo C1-C6, dialquilamino-C1-C6 alquilo C1-C6, OH, haloalquilo C1-C6, hidroxialquilo C1-C6, alcoxi C1-C6, alcoxi C1-C6 alquilo C1-C6, heteroarilo o fenilo; R8 es H o alquilo C1-C6; R9 es H, alquilo C1-C6, haloalquilo C1-C6, cicloalquilo C3-C6, alcoxi C1-C6, - (CH2) y-Ar- (R7) z; o R8 y R9, junto con el átomo de nitrógeno al que están unidos, forman un anillo heterocicloalquilo de 5 ó 6 miembros opcionalmente sustituido con alquilo C1-C6, halo, amino, ciano, alcoxi C1-C6 u OH; R10 es heterocicloalquilo, Ar- (R7) z, COOH o C (O) -NR11R12 R11 es H o alquilo C1-C3; R12 es H, alquilo C1-C6, haloalquilo C1-C3, o hidroxialquilo C1-C3; o R11 y R12, junto con el átomo de nitrógeno al que están unidos forman un anillo heterocicloalquilo de 5 ó 6 miembros opcionalmente sustituido con alquilo C1-C6, halo, amino, ciano, alcoxi C1-C6 o hidroxi;... [Seguir leyendo]
Reivindicaciones:
1. Un compuesto de fórmula (I) :
o una sal farmacéuticamente aceptable del mismo, en la que:
representa un fragmento de un anillo heteroaromático de 5 miembros; A es >C=Y o >S (O) xen la que Y es O, S o N-R1; en la que x es 1 ó 2; R1 es independientemente H, alquilo C1-C3 o ciclopropilo; R2 es H, alquilo C1-C6, haloalquilo C1-C6, cicloalquilo C3-C6, alcoxi C1-C6, hidroxialquilo C1-C6, aminoalquilo C1-C6,
alcoximetilo C1-C6, hidroxi, - (CH2) y-Ar- (R7) z, o NR8R9, con la condición de que cuando A sea S (O) x, R2 no sea H; en la que y es 0, 1 ó 2; y z es un número entero no negativo no mayor que el número de posiciones disponibles en el Ar para sustitución; Ar es fenilo o heteroarilo; R3 es independientemente H, alquilo C1-C6, alquenilo C2-C6, haloalquilo C1-C6, hidroxialquilo C1-C6, aminoalquilo C1
C6, alquilamino C1-C6 alquilo C1-C6, dialquilamino C1-C6 alquilo C1-C6, - (CH2) w-R10; en la que w es 1 ó 2; R4 es independientemente alquilo C1-C6, halo, haloalquilo C1-C6 o Ar- (R7) z; R5 es independientemente alquilo C1-C6, halo, haloalquilo C1-C6-, Ar- (R7) z, - (CH2) aNR13R14, -Ar- (CH2) aNR13R14, -A’NR1- (CH2) b-A'', -CH2CH2C (O) -A''' o -Ar’- (C (O) (CH2) aNR13R14) c; en la que A’ es C (O) o CH2; A" es H, NR13R14, tioalquilo C1-C6, alcoxi C1-C6, -SO2CH3 u -OH; A’" es -OH, alcoxi C1-C6
o -NR13R14; y Ar’ es un anillo heterocicloalquilo de 5 ó 6 miembros; en la que a es independientemente 0, 1 ó 2; b es 1, 2 ó 3, con la condición de que cuando b sea 1, A" sea H; y c sea 0 ó 1; R6 y cada R7 son cada uno independientemente halo, ciano, nitro, alquilo C1-C6, COOH, alquilcarbonilo C1-C6, alquilcarbonilo C1-C6 alquilo C1-C6, amino, alquilamino C1-C6, dialquilamino C1-C6, aminoalquilo C1-C6, alquilamino C1-C6 alquilo C1-C6, dialquilamino-C1-C6 alquilo C1-C6-, OH, haloalquilo C1-C6, hidroxialquilo C1-C6, alcoxi C1-C6, alcoxi C1-C6 alquilo C1-C6, heteroarilo o fenilo; R8 es H o alquilo C1-C6; R9 es H, alquilo C1-C6, haloalquilo C1-C6, cicloalquilo C3-C6, alcoxi C1-C6, - (CH2) y-Ar- (R7) z; o R8 y R9, junto con el átomo de nitrógeno al que están unidos, forman un anillo heterocicloalquilo de 5 ó 6 miembros opcionalmente sustituido con alquilo C1-C6, halo, amino, ciano, alcoxi C1-C6 u OH; R10 es heterocicloalquilo, Ar- (R7) z, COOH o C (O) -NR11R12 R11 es H o alquilo C1-C3; R12 es H, alquilo C1-C6, haloalquilo C1-C3, o hidroxialquilo C1-C3; o R11 y R12, junto con el átomo de nitrógeno al que están unidos forman un anillo heterocicloalquilo de 5 ó 6 miembros opcionalmente sustituido con alquilo C1-C6, halo,
amino, ciano, alcoxi C1-C6 o hidroxi; R13 es H, alquilo C1-C6 o hidroxialquilo C1-C6; R14 es H, alquilo C1-C6, haloalquilo C1-C6, hidroxialquilo C1-C6, alquilamino C1-C6 o SO2CH3; o R13 y R14, junto con el átomo de nitrógeno al que están unidos, forman un anillo heterocicloalquilo de 5 ó 6 miembros opcionalmente sustituido con alquilo C1-C6, halo, amino, ciano, alcoxi C1-C6, hidroxialquilo C1-C6 u OH; y
R15 y R16 son cada uno independientemente H, alquilo C1-C6 o halo, o R15 y R16, junto con el átomo de carbono al que están unidos forman ciclopropilo, C=O, C=S o C=NR1; m es 0 ó 1;
n, o y q son cada uno independientemente 0, 1 ó 2; y p es 0, 1, 2, 3 ó 4.
2. El compuesto de fórmula (I) de la Reivindicación 1 o una sal farmacéuticamente aceptable del mismo en el que m es 0.
3. El compuesto de fórmula (I) de la Reivindicación 2 o una sal farmacéuticamente aceptable del mismo en el que n es 0; p es 0, 1 ó 2, y cada R6 es independientemente halo, ciano, nitro, alquilo C1-C6, alquilcarbonilo C1-C6, amino, alquilamino C1-C6, dialquilamino C1-C6, aminoalquilo C1-C6, OH, haloalquilo C1-C6 o alcoxi C1-C6.
4. El compuesto de fórmula (I) de la Reivindicación 3 o una sal farmacéuticamente aceptable del mismo en el que p es 0 y
es 5. El compuesto de fórmula (I) de la Reivindicación 4 o una sal farmacéuticamente aceptable del mismo en el que q es 0 ó 1, y R3 es alquilo C1-C6, alquenilo C2-C6, haloalquilo C1-C6, hidroxialquilo C1-C6, aminoalquilo C1-C6,
alquilamino C1-C6 alquilo C1-C6, dialquilamino C1-C6 alquilo C1-C6, - (CH2) w-R10 en la que w es 1 ó 2, R10 es heterocicloalquilo, Ar- (R7) z, COOH o C (O) -NR11R12 en la que R11 es H o alquilo C1-C3; R12 es H, alquilo C1-C6, haloalquilo C1-C3 o hidroxialquilo C1-C3; o R11 y R12, junto con el átomo de nitrógeno al que están unidos forman un anillo de heterocicloalquilo de 5 ó 6 miembros opcionalmente sustituido con alquilo C1-C6, halo, amino, ciano, alcoxi C1-C6 o hidroxi; y
6. El compuesto de fórmula (I) de la Reivindicación 5 o una sal farmacéuticamente aceptable del mismo en el que:
es
7. El compuesto de fórmula (I) de la Reivindicación 6 o una sal farmacéuticamente aceptable del mismo en el que R3 es alquilo C1-C6, alquenilo C2-C6, haloalquilo C1-C6, hidroxialquilo C1-C6, aminoalquilo C1-C6, alquilamino C1-C6 alquilo C1-C6, dialquilamino C1-C6 alquilo C1-C6, - (CHz) w-R10 en la que w es 1 ó 2, R10 es heterocicloalquilo, Ar- (R7) z, C OOH o C (O) -NR11R12 en la que R11 es H o alquilo C1-C3; R12 es H, alquilo C1-C6, haloalquilo C1-C3 o hidroxialquilo C1-C3-; o R11 y R12, junto con el átomo de nitrógeno al que están unidos forman un anillo de heterocicloalquilo de 5 o 6 miembros opcionalmente sustituido con alquilo C1-C6, halo, amino, ciano, alcoxi C1-C6 o hidroxi;
8. El compuesto de fórmula (I) de la Reivindicación 7 o una sal farmacéuticamente aceptable del mismo en el que R1 es H, R2 es alquilo C1-C6, fluoroalquilo C1-C6, fenilo, tienilmetilo, cicloalquilo C3-C6, halofenilo, cianofenilo, trifluorometilfenilo, bencilo, metoxi, etoxi, metoximetilo, N-metilpirrolilo o NR8R9, en la que R8 es H o alquilo C1-C6 y R9 es alquilo C1-C6, cicloalquilo C3-C6, fenilo, halofenilo, cianofenilo, tolilo, metoxifenilo, trifluorometilfenilo, bifenilo, bencilo, pirrolilo, piridinilo, tiazolilo, o tienilo, o R8 y R9, junto con el átomo de nitrógeno al que están unidos, forman un grupo morfolino, tiomorfolino, tiomorfolinil-1, 1-dióxido, pirrolidinilo, hidroxipirrolidinilo o piperidinilo; R3 es alquilo C1-C6, alquilamino C1-C6 alquilo C1-C6, trifluorometilo, 2, 2, 2-trifluoretilo, 1, 1, 1, 3, 3, 3-hexafluoroisopropilo, metoxibencilo, hidroxietilo, hidroxipropilo, ácido acético, acetamida, morfoliniloxoetilo, metoxifenilacetamida, hidroxietilacetamida o dihidroxipropilo; R4 es alquilo C1-C6, halo o dimetilaminometilfenilo; n es 0 ó 1; y R5 esacetanilido, dimetilaminometilfenilo, metilaminometilfenilo, morfolinometilfenilo, pirrolidinilmetilfenilo, etil (2hidroxietil) aminometilfenilo, 2-hidroxietil-1-piperacinilmetilfenilo, hidroxilmetilfenilo, 4-metil-1-piperacinilpirimidinilo, morfolinoetilaminometilo, hidroxietilaminometilo, dimetilaminometilo, dimetilaminoetilaminometilo, dimetilaminometilcarboniltetrahidropiridinilo, tetrahidropiridinilo, morfolinopiridinilo, morfolinocarboniltetrahidropiridinilo, metilsulfoniletilaminometilo, 4-metilpiperacinil-propilaminometilo, -CH2CH2C (O) - A’", en la que A’" es alcoxi C1-C2, OH o 4-metilpiperacinilo; o -C (O) NH (CH2) rNR13R14, en la que R13 y R14, junto con el nitrógeno al que están unidos, forman N-morfolino, N-tiomorfolino, piperacinilo, 4-metilpiperacinilo o -SCH3; en la que r es 2 ó 3.
9. Un compuesto seleccionado de entre el grupo que consiste en:
N’-{4-[4- (2-{3-[ (dimetilamino) metil]fenil}-1H-pirrolo[2, 3-b]piridin-4-il) -1-etil-1H-pirazol-3-il]fenil}-N, N-dimetilurea; N-{4-[4- (2-{3-[ (dimetilamino) metil]fenil}-1H-pirrolo[2, 3-b]piridin-4-il) -1-etil-1H-pirazol-3-il]fenil}-N’-fenilurea; N-{4-[4- (2-{3-[ (dimetilamino) metil]fenil}-1H-pirrolo[2, 3-b]piridin-4-il) -1-etil-1H-pirazol-3-il]fenil}-N’-etilurea; N’-[4- (1-etil-4-{2-[3- (4-morfolinilmetil) fenil]-1H-pirrolo[2, 3-b]piridin-4-il}-1H-pirazol-3-il) fenil]-N, N-dimetilurea; N’-{4-[4- (2-{4-[ (dimetilamino) metil]fenil}-1H-pirrolo[2, 3-b]piridin-4-il) -1-etil-1H-pirazol-3-il]fenil}-N, N-dimetilurea; N-{4-[4- (2-{4-[ (dimetilamino) metil]fenil}-1H-pirrolo[2, 3-b]piridin-4-il) -1-etil-1H-pirazol-3-il]fenil}-N’-etilurea; N’-[4- (1-etil-4-{2-[4- (1-pirrolidinilmetil) fenil]-1H-pirrolo[2, 3-b]piridin-4-il}-1H-pirazol-3-il) fenil]-N, N-dimetilurea; N’- (4-{1-etil-4-[2- (1, 2, 3, 6-tetrahidro-4-piridinil) -1H-pirrolo[2, 3-b]piridin-4-il]-1H-pirazol-3-il}fenil) -N, N-dimetilurea; N’-[4- (4-{2-[3- (dimetilamino) fenil]-1H-pirrolo[2, 3-b]piridin-4-il}-1-etil-1H-pirazol-3-il) fenil]-N, N-dimetilurea; N’-{4-[4- (2-{4-[ (dimetilamino) metil]fenil}-1H-pirrolo[2, 3-b]piridin-4-il) -1-metil-1H-pirazol-3-il]fenil}-N, N-dimetilurea; N’-{4-[4- (2-{4-[ (dimetilamino) metil]fenil}-1H-pirrolo[2, 3-b]piridin-4-il) -1- (1-metiletil) -1H-pirazol-3-il]fenil}-N, Ndimetilurea; N, N-dimetil-N’-[4- (1-metil-4-{2-[4- (1-pirrolidinilmetil) fenil]-1H-pirrolo[2, 3-b]piridin-4-il}-1H-pirazol-3-il) fenil]urea; N’- (4-{4-[2- (4-{[etil (2-hidroxietil) amino]metil}fenil) -1H-pirrolo[2, 3-b]piridin-4-il]-1-metil-1H-pirazol-3-il}fenil) -N, Ndimetilurea; N’-{4-[4- (2-{4-[ (dimetilamino) metil]fenil}-1H-pirrolo[2, 3-b]piridin-4-il) -1-etil-1H-pirazol-3-il]fenil}-N, N-dietilurea; N, N-dietil-N’-[4- (1-etil-4-{2-[4- (1-pirrolidinilmetil) fenil]-1H-pirrolo[2, 3-b]piridin-4-il}-1H-pirazol-3-il) fenil] urea; N’- (4-{1-etil-4-[2- (4-{[etil (2-hidroxietil) amino]metil}fenil) -1H-pirrolo[2, 3-b]piridin-4-il]-1H-pirazol-3-il}fenil) -N, Ndimetilurea; N’-{4-[4-[2- (4-{[etil (2-hidroxietil) amino]metil}fenil) -1H-pirrolo[2, 3-b]piridin-4-il]-1- (1-metiletil) -1H-pirazol-3-il]fenil}N, N-dimetilurea; N, N-dietil-N’- (4-{4-[2- (4-{[4- (2-hidroxietil) -1-piperacinil]metil}fenil) -1H-pirrolo[2, 3-b]piridin-4-il]-1-metil-1H-pirazol-3il}fenil) urea; N’-{4-[1-etil-4- (2-{3-[ (metilamino) metil]fenil}-1H-pirrolo[2, 3-b]piridin-4-il) -1H-pirazol-3-il]fenil}-N, N-dimetilurea; N’-{4-[4- (2-{4-[ (dimetilamino) metil]fenil}-1H-pirrolo[2, 3-b]piridin-4-il) -1- (1-metiletil) -1H-pirazol-3-il]fenil}-N, Ndietilurea; N’-{4-[4- (2-{4-[ (dimetilamino) metil]fenil}-1H-pirrolo[2, 3-b]piridin-4-il) -1-metil-1H-pirazol-3-il]fenil}-N, N-dietilurea; N’- (4-{4- (2-{3-[ (dimetilamino) metil]fenil}-1H-pirrolo[2, 3-b]piridin-4-il) -1-[2- (metilamino) etil]-1H-pirazol-3-il}fenil) N, N-dimetilurea; N’- (4-{4-{2-[3- (hidroximetil) fenil]-1H-pirrolo[2, 3-b]piridin-4-il}-1-[2- (metilamino) etil]-1H-pirazol-3-il}fenil) -N, Ndimetilurea; N’-{4-[1-[2- (dimetilamino) etil]-4- (2-{3-[ (dimetilamino) metil]fenil}-1H-pirrolo[2, 3-b]piridin-4-il) -1H-pirazol-3-il]fenil}N, N-dimetilurea; y N, N-dimetil-N’-[4- (1-metil-4-{2-[2- (4-metil-1-piperacinil) -5-pirimidinil]-1H-pirrolo[2, 3-b]piridin-4-il}-1H-pirazol-3il) fenil] urea; o una sal farmacéuticamente aceptable del mismo.
10. El compuesto de la Reivindicación 9, que es N’-{4-[4- (2-{3-[ (dimetilamino) metil]fenil}-1H-pirrolo[2, 3-b]piridin-4-il) 1-etil-1H-pirazol-3-il]fenil}-N, N-dimetilurea o una sal farmacéuticamente aceptable del mismo.
11. El compuesto de la Reivindicación 9, que es N’-{4-[4- (2-{3-[ (dimetilamino) metil]fenil}-1H-pirrolo[2, 3-b]piridin-4-il) 1-etil-1H-pirazol-3-il]fenil}-N, N-dimetilurea.
12. Un compuesto seleccionado del grupo que consiste en:
N’- (4-{4-[2- (4-{[etil (2-hidroxietil) amino]metil}fenil) -1H-pirrolo[2, 3-b]piridin-4-il]-1-metil-1H-pirazol-3-il}fenil) -N, Ndimetilurea; N’-{4-[4- (2-{4-[ (dimetilamino) metil]fenil}-1H-pirrolo[2, 3-b]piridin-4-il) -1-etil-1H-pirazol-3-il]fenil}-N, N-dimetilurea; N’-{4-[1-[2- (dimetilamino) etil]-4- (2-{3-[ (dimetilamino) metil]fenil}-1H-pirrolo[2, 3-b]piridin-4-il) -1H-pirazol-3-il]fenil}N, N-dimetilurea; N-{4-[4- (2-{3-[ (dimetilamino) metil]fenil}-1H-pirrolo[2, 3-b]piridin-4-il) -1-etil-1H-pirazol-3-il]fenil}-N’-etilurea; y N’-{4-[4- (2-{4-[ (dimetilamino) metil]fenil}-1H-pirrolo[2, 3-b]piridin-4-il) -1-metil-1H-pirazol-3-il]fenil}-N, N-dietilurea; o una sal farmacéuticamente aceptable del mismo.
13. Una composición farmacéutica que comprende a) un compuesto de fórmula (I) según se define en cualquiera de las Reivindicaciones 1 a 12, o una sal farmacéuticamente aceptable del mismo, y b) uno o más excipientes farmacéuticamente aceptables.
14. Una composición farmacéutica que comprende a) N’-{4-[4- (2-{3-[ (dimetilamino) metil]fenil}-1H-pirrolo[2, 3-b]piridin4-il) -1-etil-1H-pirazol-3-il]fenil}-N, N-dimetilurea, o una sal farmacéuticamente aceptable del mismo, y b) uno o más excipientes farmacéuticamente aceptables.
15. Un compuesto de fórmula (I) según se define en cualquiera de las Reivindicaciones 1 a 12, o una sal farmacéuticamente aceptable del mismo, para su uso en terapia.
16. Un compuesto de fórmula (I) según se define en cualquiera de las Reivindicaciones 1 a 12, o una sal farmacéuticamente aceptable del mismo, para su uso en el tratamiento del cáncer.
17. N’-{4-[4- (2-{3-
Patentes similares o relacionadas:
Uso de inhibidores de la PDE4 para la profilaxis y/o la terapia de la dislipoproteinemia y trastornos relacionados, del 27 de Mayo de 2020, de Albert-Ludwigs-Universität Freiburg: Inhibidor específico de la fosfodiesterasa 4 (PDE 4) para uso en el tratamiento profiláctico o terapéutico de la dislipoproteinemia, en donde el inhibidor […]
Métodos y composiciones para trastornos relacionados con la proliferación celular, del 27 de Mayo de 2020, de Agios Pharmaceuticals, Inc: Un método in vitro para diagnosticar a un sujeto que tiene un trastorno relacionado con la proliferación celular o que se sospecha que tiene un trastorno relacionado con […]
Un canal catiónico no selectivo en células neurales y compuestos que bloquean el canal para su uso en el tratamiento de la inflamación del cerebro, del 6 de Mayo de 2020, de UNIVERSITY OF MARYLAND, BALTIMORE: Un antagonista de SUR1 que bloquea el canal de NCCa-ATP para su uso en (a) la prevención o el tratamiento de la inflamación de las células neurales […]
Inhibidores de ERK y sus usos, del 8 de Abril de 2020, de Celgene CAR LLC: Un compuesto de fórmula VIII: **(Ver fórmula)** o una de sus sales farmacéuticamente aceptables, en donde: el anillo A se selecciona de **(Ver fórmula)** […]
Procedimiento de uso de inmunoconjugados anti-CD79b, del 8 de Abril de 2020, de F. HOFFMANN-LA ROCHE AG: Un inmunoconjugado que comprende un anticuerpo anti-CD79b unido a un agente citotóxico para su uso en un procedimiento para tratar un trastorno proliferativo […]
IMIPRAMINA PARA USO COMO INHIBIDOR DE LA SOBREXPRESIÓN DE LA FASCINA 1, del 2 de Abril de 2020, de FUNDACION UNIVERSITARIA SAN ANTONIO: La presente invención se refiere a imipramina para su uso como inhibidor de la sobreexpresión de la fascina 1, preferiblemente dicha sobreexpresión de la fascina 1 está asociada […]
Mutación novedosa del receptor de andrógenos, del 25 de Marzo de 2020, de NOVARTIS AG: Una composicion terapeutica para su uso en el tratamiento de un paciente que padece cancer de prostata o de mama, asociado con una mutacion del receptor de […]
Composiciones y métodos para la distribución de moléculas en células vivas, del 25 de Marzo de 2020, de THE TEXAS A & M UNIVERSITY SYSTEM: Un compuesto que tiene la fórmula: **(Ver fórmula)** En donde X es un resto de unión, Y es un residuo de aminoácido acoplado de forma covalente […]