HUELLA GENOMICA DE CANCER DE MAMA.
La presente invención se relaciona con métodos in vitro para determinar el pronóstico de un sujeto diagnosticado de cáncer de mama a desarrollar metástasis o para seleccionar el tratamiento adecuado para dicho sujeto.
En particular, la invención se refiere a una firma de genes cuya expresión está correlacionada con el pronóstico de un sujeto que ha sido diagnosticado de cáncer de mama
Tipo: Patente de Invención. Resumen de patente/invención. Número de Solicitud: P200802024.
Solicitante: CENTRO DE INVESTIGACIONES ENERGETICAS, MEDIOAMBIENTALES Y TECNOLOGICAS.
Nacionalidad solicitante: España.
Provincia: MADRID.
Inventor/es: MARTINEZ CRUZ,ANA BELEN, GARCIA ESCUDERO,RAMON, PARAMIO GONZALEZ,JESUS MARIA, SANTOS LAFUENTE,MIRENTXU.
Fecha de Solicitud: 2 de Julio de 2008.
Fecha de Publicación: .
Fecha de Concesión: 12 de Enero de 2011.
Clasificación Internacional de Patentes:
- C12Q1/68D4
Clasificación PCT:
- C12Q1/68 QUIMICA; METALURGIA. › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12Q PROCESOS DE MEDIDA, INVESTIGACION O ANALISIS EN LOS QUE INTERVIENEN ENZIMAS, ÁCIDOS NUCLEICOS O MICROORGANISMOS (ensayos inmunológicos G01N 33/53 ); COMPOSICIONES O PAPELES REACTIVOS PARA ESTE FIN; PROCESOS PARA PREPARAR ESTAS COMPOSICIONES; PROCESOS DE CONTROL SENSIBLES A LAS CONDICIONES DEL MEDIO EN LOS PROCESOS MICROBIOLOGICOS O ENZIMOLOGICOS. › C12Q 1/00 Procesos de medida, investigación o análisis en los que intervienen enzimas, ácidos nucleicos o microorganismos (aparatos de medida, investigación o análisis con medios de medida o detección de las condiciones del medio, p. ej. contadores de colonias, C12M 1/34 ); Composiciones para este fin; Procesos para preparar estas composiciones. › en los que intervienen ácidos nucleicos.
Fragmento de la descripción:
Huella genómica de cáncer de mama.
Campo de la invención
La presente invención se relaciona con métodos in vitro para determinar el pronóstico de un sujeto diagnosticado de cáncer de mama a desarrollar metástasis o para seleccionar el tratamiento adecuado para dicho sujeto.
Antecedentes de la invención
Mundialmente, el cáncer de mama es el segundo tipo más común de cáncer (10.4%; tras el cáncer de pulmón) y la quinta causa más común de muerte por cáncer (tras el cáncer de pulmón, cáncer de estómago, cáncer de hígado, y cáncer de colon). Entre las mujeres en el mundo, el cáncer de mama es la causa más común de muerte por cáncer. En 2005, el cáncer de mama produjo 502.000 muertes en el mundo (el 7% de las muertes por cáncer; casi el 1% de todas las muertes). El número de casos mundiales ha aumentado significativamente desde la década de 1970, un fenómeno del que se echa la culpa parcialmente a los estilos de vida modernos en el mundo occidental. Las mujeres de Norteamérica tienen la mayor incidencia de cáncer de mama en el mundo.
Debido a que la mama está compuesta de tejidos idénticos en hombres y mujeres, el cáncer de mama también se da en hombres. Las incidencias de cáncer de mama en hombres son aproximadamente 100 veces menores que en mujeres, pero se considera que los hombres con cáncer de mama tienen estadísticamente las mismas tasas de supervivencia que las mujeres.
El cáncer de mama se clasifica en fases según el sistema TNM. El pronóstico esta íntimamente unido a los resultados de la clasificación en fases, y la clasificación en fases también se usa para asignar pacientes a tratamientos tanto en ensayos clínicos como en la práctica médica. La información para clasificar en fases es como sigue:
• TX: El tumor primario no se puede evaluar. T0: No hay evidencia de tumor. Tis: Carcinoma in situ, no invasión. T1: El tumor es de 2 cm o menos. T2: El tumor es de más de 2 cm pero de menos de 5 cm. T3: El tumor es de más de 5 cm. T4: Tumor de cualquier tamaño que crece en la pared del pecho o piel, o cáncer de mama inflamatorio.
• NX: Los ganglios linfáticos cercanos no se pueden evaluar. N0: El cáncer no se ha extendido a los ganglios linfáticos regionales. N1: El cáncer se ha extendido a 1 a 3 ganglios linfáticos de la axila o a uno mamario interno. N2: El cáncer se ha extendido a 4 a 9 ganglios linfáticos de la axila o a múltiples ganglios mamarios internos. N3: Aplica uno de los siguientes:
• MX: La presencia de extensión distante (metástasis) no se puede evaluar. M0: No hay extensión distante. M1: Se ha producido la extensión a órganos distantes, que no incluyen el ganglio linfático supraclavicular.
El pilar principal del tratamiento de cáncer de mama es la cirugía cuando el tumor está localizado, con posible terapia adyuvante hormonal (con tamoxifeno o un inhibidor de aromatasa), quimioterapia, y/o radioterapia. En la actualidad, las recomendaciones de tratamiento después de la cirugía (terapia adyuvante) siguen un patrón. Este patrón está sujeto a cambio, ya que cada dos años, tiene lugar una conferencia mundial en St. Gallen, Suiza, para discutir los resultados reales de los estudios multicentros mundiales. Asimismo, dicho patrón también se revisa según el criterio consenso del National Institute of Health (NIH). Basándose en estos criterios, más del 85-90% de los pacientes que no presentan metástasis en nódulos linfáticos serían candidatos para recibir terapia sistémica adyuvante.
En la actualidad, no se ha identificado un set de predictores de prognosis satisfactorio basado únicamente en información clínica. Durante los últimos 30 años los oncólogos se han centrado en optimizar el desenlace de los pacientes de cáncer y es solo ahora que las nuevas tecnologías disponibles permiten investigar polimorfismos, niveles de expresión de genes y mutaciones de genes con el propósito de predecir el impacto de una terapia determinada en diferentes grupos de pacientes de cáncer para hacer quimioterapias a medida. Ensayos de PCR como Oncotype DX o ensayos de microarrays como MammaPrint pueden predecir el riesgo de recaída del cáncer de mama basada en la expresión de genes. En febrero de 2007, el ensayo MammaPrint se convirtió en el primer indicador de cáncer de mama en conseguir autorización oficial de la Food and Drug Administration.
Así, el documento WO02103320 describe un método para predecir el pronóstico de pacientes de cáncer de mama mediante el análisis de la expresión de un grupo de marcadores genéticos, en particular de 70 genes (Tabla 6, página 89). WO02103320 también describe un microarray para determinar el pronóstico de cáncer de mama a partir de una muestra de un paciente que comprende sondas para la detección de la expresión génica de dichos genes.
Por otra parte, el documento WO2005/083429 describe un método para la selección de una firma de marcadores genéticos para el pronóstico de cáncer de mama. Asimismo, dicho documento describe un método para determinar el pronóstico de pacientes con cáncer de mama mediante el análisis de la expresión de un grupo de genes seleccionados a partir de dicho método. En concreto, dicho documento se relaciona con el uso de marcadores genéticos para la predicción del pronóstico de cáncer de mama a partir de una firma característica formada por 76 marcadores genéticos. Dicho documento también describe un kit, tal como un microarray, para determinar el pronóstico de cáncer de mama a partir de una muestra de un paciente que comprende sondas para la detección de la expresión génica de dichos 76 genes.
Por tanto, existe la necesidad de desarrollar nuevos métodos que permitan identificar los genes más relevantes implicados en metástasis de forma que se puedan obtener firmas más fiables y basadas en un menor número de genes. Dichas firmas permitirán la predicción del pronóstico de un paciente que sufre cáncer de mama de forma más eficaz que los métodos descritos en el estado de la técnica. La identificación de nuevos factores de pronóstico servirá para guiar en la selección de los tratamientos más adecuados.
Compendio de la invención
En un primer aspecto, la presente invención se refiere a un método in vitro para determinar el pronóstico de un sujeto diagnosticado con cáncer de mama o para seleccionar el tratamiento de un sujeto diagnosticado con cáncer de mama que comprende determinar los niveles de expresión de los genes identificados en la Tabla 1 y en la Tabla 2 en una muestra de tejido tumoral procedente de dicho sujeto, en donde un aumento de la expresión de los genes identificados en la Tabla 1 y una disminución de la expresión de los genes identificados en la Tabla 2 con respecto a un valor de referencia es indicativo de un peor pronóstico o de que dicho sujeto tiene que ser tratado con quimioterapia.
En un segundo aspecto, la invención se refiere a un reactivo capaz de detectar los niveles de expresión de los genes de las Tablas 1 y 2.
En otro aspecto, la invención se refiere a un kit que comprende al menos un reactivo según la invención.
En otro aspecto, la invención se relaciona con el uso de un kit según la invención para el pronóstico de pacientes diagnosticados con cáncer de mama o para seleccionar el tratamiento de un sujeto diagnosticado con cáncer de mama.
Asimismo, la invención se refiere en otro aspecto, a un método para seleccionar marcadores genéticos para predecir la propensión a desarrollar metástasis de un tumor primario que comprende las siguientes etapas:
Reivindicaciones:
1. Un método in vitro para determinar el pronóstico de un sujeto diagnosticado con cáncer de mama o para seleccionar el tratamiento de un sujeto diagnosticado con cáncer de mama que comprende determinar los niveles de expresión de los genes identificados en la Tabla 1 y en la Tabla 2 conjuntamente en una muestra de tejido tumoral procedente de dicho sujeto, en donde un aumento de la expresión de los genes identificados en la Tabla 1 y una disminución de la expresión de los genes identificados en la Tabla 2 con respecto a un valor de referencia es indicativo de un peor pronóstico o de que dicho sujeto tiene que ser tratado con quimioterapia.
2. Método según la reivindicación 1, en donde la cuantificación de los niveles de expresión de los genes identificados en las Tablas 1 y 2 comprende la cuantificación del ARN mensajero (ARNm) de dichos genes, o un fragmento de dicho ARNm, el ADN complementario (ADNc) de dichos genes, o un fragmento de dicho ADNc, o sus mezclas.
3. Método según cualquiera de las reivindicaciones 1 a 2, en donde la cuantificación de los niveles de expresión de los genes identificados en las Tablas 1 y 2 se realiza mediante una reacción en cadena de la polimerasa (PCR) cuantitativa multiplex o un array de ADN o ARN.
4. Método según cualquiera de las reivindicaciones 1 a 3, donde la determinación de los niveles de expresión de los genes identificados en la Tabla 1 y la Tabla 2 se realiza mediante un array de ADN que comprende las sondas identificadas en las Tablas 3 y 4.
5. Método según cualquiera de las reivindicaciones 1 a 4, donde la determinación de dicho pronóstico comprende un análisis de regresión de riesgos proporcionales de dicho pronóstico en función de los niveles de expresión de los genes identificados en la Tabla 1 y en la Tabla 2.
6. Método según la reivindicación 5, donde dicho análisis de regresión de riesgos proporcionales es un análisis de tipo Cox.
7. Método según la reivindicación 6, donde en dicho análisis de tipo Cox se establece metástasis distal como variable pronóstico.
8. Método según la reivindicación 7, donde dicha metástasis distal es metástasis distal a 5 ó 10 años.
9. Método según cualquiera de las reivindicaciones 6 a 8, donde la determinación de dicho pronóstico se lleva a cabo aplicando la siguiente fórmula:
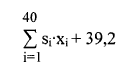
donde
en donde si dicho valor es mayor que cero entonces es indicativo de que dicho paciente presenta peor pronóstico o de que dicho paciente tiene que ser tratado con quimioterapia y donde si dicho valor es menor que cero es indicativo de que dicho paciente presenta buen pronóstico o de que dicho paciente no tiene que ser tratado con quimioterapia.
10. Método según la reivindicación 1, en donde la cuantificación de los niveles de expresión de los genes identificados en las Tablas 1 y 2 comprende la cuantificación de los niveles de proteína codificada por dichos genes o de una variante de la misma.
11. Método según la reivindicación 10, en donde la cuantificación de los niveles de proteína se realiza mediante western blot, ELISA o un array de proteínas.
12. Un reactivo capaz de detectar los niveles de expresión de los genes identificados en las Tablas 1 y 2.
13. Reactivo según la reivindicación 12, en donde el reactivo comprende
14. Reactivo según la reivindicación 13, en donde los ácidos nucleicos son sondas y/o cebadores de ADN, ADNc o ARN.
15. Un kit que comprende al menos un reactivo según cualquiera de las reivindicaciones 12 a 14.
16. Kit según la reivindicación 15, donde dicho kit es un array de ADN o ARN que comprende un conjunto de ácidos nucleicos, en donde dicho conjunto de ácidos nucleicos comprende las secuencias de nucleótidos de las sondas de las Tablas 1 y 2, o un fragmento de los mismos, o los productos de su transcripción.
17. Kit según la reivindicación 16, que comprende además, una molécula de ácido nucleico de uno o varios genes de expresión constitutiva.
18. Kit según la reivindicación 17 que comprende un conjunto de anticuerpos, en donde dicho conjunto de anticuerpos consiste en anticuerpos, o fragmentos de los mismos, capaces de unirse específicamente con las proteínas codificadas por los genes identificados en las Tablas 1 y 2 o cualquier variante de dichas proteínas.
19. Kit según la reivindicación 18, que comprende además, anticuerpos, o fragmentos de los mismos, capaces de unirse específicamente con las proteínas codificadas por uno o varios genes de expresión constitutiva.
20. Uso de un kit según cualquiera de las reivindicaciones 15 a 19 para el pronóstico de pacientes diagnosticados con cáncer de mama o para seleccionar el tratamiento de un sujeto diagnosticado con cáncer de mama.
21. Un método para seleccionar marcadores genéticos para predecir la propensión a desarrollar metástasis de un tumor primario que comprende las siguientes etapas:
22. Método según la reivindicación 21, donde dicho animal no humano es un animal en el que la expresión génica del gen Tp53 se encuentra inhibida.
23. Método según la reivindicación 22, donde dicho animal presenta inhibida, además, la expresión génica del gen pRb.
24. Método según cualquiera de las reivindicaciones 21 a 23, donde la muestra obtenida en la etapa (i) es una muestra de carcinomas epidérmicos.
25. Método según cualquiera de las reivindicaciones 21 a 24, donde dicha etapa iii) se lleva a cabo mediante un análisis de regresión de riesgos proporcionales.
26. Método según la reivindicación 25, donde dicho análisis de regresión es un análisis de tipo Cox.
27. Método según la reivindicación 26, donde dicho método de tipo Cox establece metástasis distal como variable pronóstico.
28. Método según la reivindicación 27, donde dicha metástasis distal es metástasis distal a 5 ó 10 años.
29. Método según cualquiera de las reivindicaciones 21 a 28, donde dichos tumores primarios analizados en la etapa iii) son tumores de cáncer de mama o de glioblastoma.
30. Método según cualquiera de las reivindicaciones 21 a 29, en donde la determinación de la expresión de dichos genes según la etapa iii) comprende la cuantificación del ARN mensajero (ARNm) de dichos genes, o un fragmento de dicho ARNm, el ADN complementario (ADNc), o un fragmento de dicho ADNc, o sus mezclas.
31. Método según la reivindicación 30, en donde la cuantificación de los niveles de expresión de los genes según la etapa iii) se realiza mediante una reacción en cadena de la polimerasa (PCR) cuantitativa multiplex o un array de ADN o ARN.
32. Método según cualquiera de las reivindicaciones 21 a 29, en donde la cuantificación de los niveles de expresión de los genes según la etapa iii) comprende la cuantificación de los niveles de proteína codificada por dichos genes.
33. Método según la reivindicación 32, en donde la cuantificación de los niveles de proteína se realiza mediante western blot, ELISA o un array de proteínas.
Patentes similares o relacionadas:
SECUENCIAS GENOMICAS DE CEBADORES Y SONDA PARA LA CUANTIFICACION DE ADENOVIRUS PORCINOS (PADV), del 30 de Junio de 2011, de UNIVERSIDAD DE BARCELONA: Secuencias genómicas de cebadores y sonda para la cuantificación de adenovirus porcinos (PAdV).La invención se refiere a un test sensible para la detección de […]
 MÉTODO Y SISTEMA PARA ANALIZAR REACCIONES USANDO UN SISTEMA DE INFORMACIÓN, del 4 de Mayo de 2011, de ABBOTT LABORATORIES: Un método de determinación de si una muestra de test contiene un ácido nucleico objetivo, comprendiendo el método: (a) poner en contacto […]
MÉTODO Y SISTEMA PARA ANALIZAR REACCIONES USANDO UN SISTEMA DE INFORMACIÓN, del 4 de Mayo de 2011, de ABBOTT LABORATORIES: Un método de determinación de si una muestra de test contiene un ácido nucleico objetivo, comprendiendo el método: (a) poner en contacto […]
 APARATO PARA LLEVAR A CABO LA PCR Y MONITORIZACIÓN DE LA REACCIÓN EN TIEMPO REAL DURANTE CICLOS DE TEMPERATURA, del 21 de Marzo de 2011, de UNIVERSITY OF UTAH RESEARCH FOUNDATION: Aparato para llevar a cabo la PCR y control de la reacción en tiempo real durante los ciclos de temperatura que comprende: una serie de recipientes […]
APARATO PARA LLEVAR A CABO LA PCR Y MONITORIZACIÓN DE LA REACCIÓN EN TIEMPO REAL DURANTE CICLOS DE TEMPERATURA, del 21 de Marzo de 2011, de UNIVERSITY OF UTAH RESEARCH FOUNDATION: Aparato para llevar a cabo la PCR y control de la reacción en tiempo real durante los ciclos de temperatura que comprende: una serie de recipientes […]
 MÉTODO PARA LA DETERMINACIÓN DEL GENOTIPO DE ANTÍGENOS DE CÉLULAS DE LA SANGRE Y KIT ADECUADO PARA LA DETERMINACIÓN DEL GENOTIPO DE ANTÍGENOS DE CÉLULAS DE LA SANGRE, del 24 de Febrero de 2011, de STICHTING SANQUIN BLOEDVOORZIENING: Método de determinación del genotipo de antígenos de células de la sangre que comprende someter al ADN de un individuo de una especie de mamífero a […]
MÉTODO PARA LA DETERMINACIÓN DEL GENOTIPO DE ANTÍGENOS DE CÉLULAS DE LA SANGRE Y KIT ADECUADO PARA LA DETERMINACIÓN DEL GENOTIPO DE ANTÍGENOS DE CÉLULAS DE LA SANGRE, del 24 de Febrero de 2011, de STICHTING SANQUIN BLOEDVOORZIENING: Método de determinación del genotipo de antígenos de células de la sangre que comprende someter al ADN de un individuo de una especie de mamífero a […]
 MÉTODOS PARA EL RÁPIDO ANÁLISIS FORENSE DE ADN MITOCONDRIAL Y CARATERIZACIÓN HETEROPLASMIA DE ADN MITOCONDRIAL, del 16 de Febrero de 2011, de IBIS BIOSCIENCES, INC: Un método forense que comprende los pasos de: (i) determinar una primera masa molecular de un primer producto de amplificación de un Cebador amplicón identificador […]
MÉTODOS PARA EL RÁPIDO ANÁLISIS FORENSE DE ADN MITOCONDRIAL Y CARATERIZACIÓN HETEROPLASMIA DE ADN MITOCONDRIAL, del 16 de Febrero de 2011, de IBIS BIOSCIENCES, INC: Un método forense que comprende los pasos de: (i) determinar una primera masa molecular de un primer producto de amplificación de un Cebador amplicón identificador […]
HUELLA GENOMICA PARA EL PRONOSTICO DE LA EVOLUCION DE ADENOCARCINOMA COLORECTAL, del 2 de Febrero de 2011, de UNIVERSIDAD AUTONOMA DE MADRID: La presente invención se relaciona con una huella genómica formada por un conjunto de 13 genes, cuya cuantificación de la expresión respecto a genes […]
CONJUNTO DE CEBADORES, SONDAS, PROCEDIMIENTO Y KIT PARA EL GENOTIPADODEL POLIMORFISMO GENETICO - 1131T/C DEL GEN APO A5, del 27 de Enero de 2011, de UNIVERSIDAD DE MALAGA: Conjunto de cebadores, sondas, procedimiento y kit para el genotipado del polimorfismo genético -1131T/C del gen APO A5.La presente invención se refiere […]
Método para analizar ácido nucleico molde, método para analizar sustancia objetivo, kit de análisis para ácido nucleico molde o sustancia objetivo y analizador para ácido nucleico molde o sustancia objetivo, del 29 de Julio de 2020, de Kabushiki Kaisha DNAFORM: Un método para analizar un ácido nucleico molde, que comprende las etapas de: fraccionar una muestra que comprende un ácido nucleico molde […]