HIDRATOS DE (RAC) -N-PIPERIDINIL-5-(4-CLOROFENIL)-1-(2,4-DICLOROFENIL)4,5-DIHIDRO-1H-PIRAZOL-3-CARBOXAMIDA.
Hidratos de (rac)-N-piperidinil-5-(4-clorofenil)-1-(2,4-diclorofenil)-4,
5-dihidro-1H-pirazol-3-carboxamida.
La presente invención se refiere a (rac)-N-piperidinil-5-(4-clorofenil)-1-(2,4-diclorofenil)-4,5-dihidro-1H-pirazol-3-carboxamida X H20, con X entre 0,7 y 0,3. Especialmente preferida es la (rac)-N-piperidinil-5-(4-clorofenil)-1-(2,4-diclorofenil)-4,5-dihidro-1H-pirazol-3-carboxamida monohidratada. También se describen métodos para su preparación y su uso como moduladores del receptor de cannabinoides
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP2006/006979.
Solicitante: LABORATORIOS DEL DR. ESTEVE, S.A..
Nacionalidad solicitante: España.
Inventor/es: BUSCHMANN,HELMUT H., BENET-BUCHHOLZ, JORDI, DR., TORRENS-JOVER, ANTONIO, SOLA,LLUIS.
Fecha de Publicación: .
Fecha de Concesión: 13 de Mayo de 2010.
Clasificación Internacional de Patentes:
- C07D231/06 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07D COMPUESTOS HETEROCICLICOS (Compuestos macromoleculares C08). › C07D 231/00 Compuestos heterocíclicos que contienen ciclos de diazol-1,2 o diazol-1,2 hidrogenado. › que tienen un enlace doble entre miembros cíclicos o entre miembros cíclicos y no cíclicos.
Clasificación PCT:
- A61K31/4155 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › no condensados y conteniendo otros heterociclos.
- C07D231/06 C07D 231/00 […] › que tienen un enlace doble entre miembros cíclicos o entre miembros cíclicos y no cíclicos.
Fragmento de la descripción:
Hidratos de (rac)-N-piperidinil-5-(4-clorofenil)-1-(2,4-diclorofenil)-4,5-dihidro-1H-pirazol-3-carboxamida.
La presente invención se refiere a hidratos de pirazolina sustituidos, métodos para su preparación, medicamentos que comprenden estos compuestos, además de su uso para la preparación de un medicamento para el tratamiento de seres humanos y animales.
Los cannabinoides son compuestos que se derivan de la planta Cannabis sativa que se conoce comúnmente como marihuana. El compuesto químico más activo de los cannabinoides naturales es el tetrahidrocannabinol (THC), particularmente el ?9-THC.
Estos cannabinoides naturales, además de sus análogos sintéticos, potencian sus efectos fisiológicos por medio de la unión a receptores acoplados a proteína G específicos, los denominados receptores de cannabinoides.
En la actualidad, se han identificado y clonado dos tipos diferenciados de receptores que se unen tanto a los cannabinoides naturales como a los sintéticos. Estos receptores, que se designan CB1 y CB2, participan en una variedad de procesos fisiológicos o patofisiológicos en seres humanos y animales, por ejemplo, procesos relacionados con el sistema nervioso central, el sistema inmunitario, el sistema cardiovascular, el sistema endocrino, el sistema respiratorio, el tracto gastrointestinal o con la reproducción, tal como se describe por ejemplo, en Hollister, Pharm. Rev. 38, 1986, 1-20; Reny y Singha, Prog. Drug. Res., 36, 71-114, 1991; Consroe y Sandyk, en Marijuana/Cannabinoids, Neurobiology and Neurophysiology, 459, Murphy L. y Barthe A. Eds., CRC Press, 1992.
Por tanto, los compuestos que tienen una alta afinidad de unión por estos receptores de cannabinoides y que son adecuados para modular estos receptores son útiles en la prevención y/o el tratamiento de trastornos relacionados con los receptores de cannabinoides.
En particular, el receptor CB1 participa en muchos trastornos diferentes relacionados con la ingestión de alimentos, tales como bulimia u obesidad, incluyendo obesidad asociada con la diabetes tipo II (diabetes no insulinodependiente) y por tanto, pueden utilizarse compuestos adecuados para regular este receptor en la profilaxis y/o el tratamiento de estos trastornos.
Por tanto, un objeto de la presente invención fue proporcionar compuestos novedosos para su uso como principios activos en medicamentos. En particular, estos principios activos deben ser adecuados para la modulación de los receptores de cannabinoides, más particularmente para la modulación de los receptores de cannabinoides 1 (CB1).
Se consiguió dicho objeto proporcionando los hidratos de piperidinil-pirazolina facilitados a continuación.
Se ha encontrado que estos compuestos tienen un alta afinidad por los receptores de cannabinoides, particularmente para el receptor CB1, y que actúan como moduladores, por ejemplo, antagonistas, agonistas inversos o agonistas de estos receptores. Por tanto, son adecuados para la profilaxis y/o el tratamiento de diversos trastornos relacionados con el sistema nervioso central, el sistema inmunitario, el sistema cardiovascular, el sistema endocrino, el sistema respiratorio, el tracto gastrointestinal o con la reproducción en seres humanos y/o animales, preferiblemente en seres humanos incluyendo lactantes, niños y personas mayores.
Los hidratos reivindicados son además especialmente estables.
Por tanto, en uno de sus aspectos, la presente invención se refiere a (rac)-N-piperidinil-5-(4-clorofenil)-1-(2,4-diclorofenil)-4,5-dihidro-1H-pirazol-3-carboxamida X H2O, con X entre 0,7 y 0,3.
Especialmente preferida es la (rac)-N-piperidinil-5-(4-clorofenil)-1-(2,4-diclorofenil)-4,5-dihidro-1H-pirazol-3-carboxamida monohidratada.
En otro aspecto, la presente invención también proporciona un procedimiento para la preparación de hidratos de pirazolina sustituidos, según el cual se hace reaccionar al menos un compuesto de benzaldehído de fórmula general II
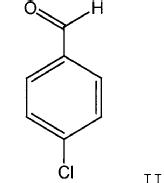
con un compuesto de piruvato de fórmula (III),
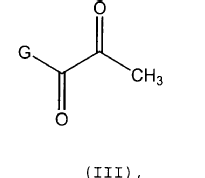
en la que G representa un grupo OR, siendo R un radical alquilo C1-6 ramificado o no ramificado o G representa un grupo O-K, siendo K un catión,
para dar un compuesto de fórmula (IV)
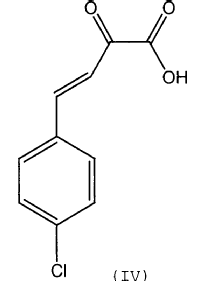
que opcionalmente se aísla y/u opcionalmente se purifica, y que se hace reaccionar con una fenilhidrazina opcionalmente sustituida de fórmula (V)
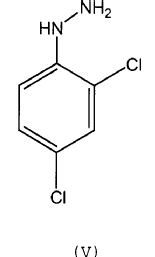
o con una sal correspondiente de la misma, bajo atmósfera inerte, para dar un compuesto de fórmula (VI)
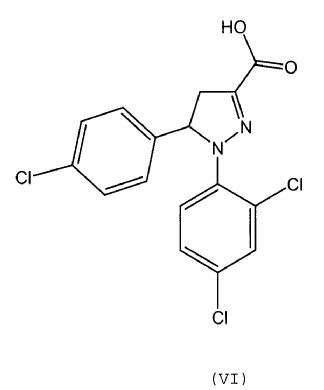
que opcionalmente se aísla y/u opcionalmente se purifica, y que se transfiere opcionalmente bajo una atmósfera inerte a un compuesto de fórmula (VII) por medio de la reacción con un agente activante,
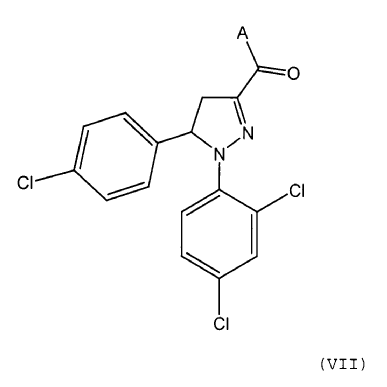
en el que A representa un grupo saliente, aislándose opcionalmente y/u purificándose opcionalmente dicho compuesto, y al menos un compuesto de formula (VII) se hace reaccionar con un compuesto de fórmula
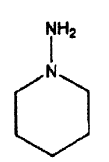
bajo atmósfera inerte para dar (rac)-N-piperidinil-5-(4-clorofenil)-1-(2,4-diclorofenil)-4,5-dihidro-1H-pirazol-3-carboxamida, que opcionalmente se aísla y/u opcionalmente se purifica,
seguido por una etapa de evaporación en la que la (rac)-N-piperidinil-5-(4-clorofenil)-1-(2,4-diclorofenil)-4,5-dihidro-1H-pirazol-3-carboxamida se disuelve en un disolvente orgánico que se evapora lentamente a temperaturas inferiores a la temperatura ambiente (25ºC), para dar (rac)-N-piperidinil-5-(4-clorofenil)-1-(2,4-diclorofenil)-4,5-dihidro-1H-pirazol-3-carboxamida X H2O.
Se prefiere que en la etapa de evaporación el disolvente orgánico se seleccione de:
acetato de etilo,
diclorometano,
1,1,1-tricloroetano
acetato de isobutilo o
acetato de etilo - agua.
Se prefiere que en la etapa de evaporación la temperatura se disminuya hasta entre +5º y -20ºC.
La reacción del compuesto de benzaldehído de fórmula II con un compuesto de piruvato de fórmula III se lleva a cabo preferiblemente en presencia de al menos una base, más preferiblemente en presencia de un hidróxido de metal alcalino, tal como hidróxido de sodio o hidróxido de potasio o un metóxido de metal alcalino, tal como metóxido de sodio, como se describe, por ejemplo, en Synthetic communications, 26(11), 2229-33, (1996). La descripción respectiva se incorpora como referencia al presente documento y forma parte de la descripción. Preferiblemente, puede utilizarse piruvato de sodio como el compuesto de piruvato. Preferiblemente, dicha reacción se lleva a cabo en un medio de reacción prótico tal como un alcohol alquílico C1-4 o mezclas de estos. También pueden utilizarse mezclas de tales alcoholes con agua, por ejemplo, etanol/agua.
La temperatura de reacción, así como la duración de la reacción, puede variar en un amplio intervalo. Las temperaturas de reacción preferidas oscilan desde -10ºC hasta el punto de ebullición del medio de reacción. Los tiempos de reacción adecuados pueden variar, por ejemplo, desde varios minutos hasta varias horas.
También se prefiere llevar a cabo la reacción del compuesto de benzaldehído de fórmula II con un compuesto de piruvato de fórmula III en condiciones catalizadas por ácido, más preferiblemente llevando a reflujo la mezcla en diclorometano en presencia de trifluorometanosulfonato de cobre (II) tal como se describe, por ejemplo, en Synlett, (1), 147-149, 2001. La descripción respectiva se incorpora como referencia al presente documento y forma parte de la descripción.
La reacción del compuesto de fórmula (IV) con una...
Reivindicaciones:
1. (rac)-N-piperidinil-5-(4-clorofenil)-1-(2,4-diclorofenil)-4,5-dihidro-1H-pirazol-3-carboxamida X H2O, con X entre 0,7 y 0,3.
2. (rac)-N-piperidinil-5-(4-clorofenil)-1-(2,4-diclorofenil)-4,5-dihidro-1H-pirazol-3-carboxamida monohidratada.
3. Procedimiento para la fabricación de los hidratos de pirazolina sustituidos según las reivindicaciones 1 ó 2, caracterizado porque se hace reaccionar un benzaldehído de fórmula II
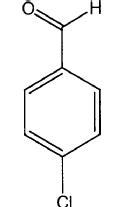
con un compuesto de piruvato de fórmula (III)
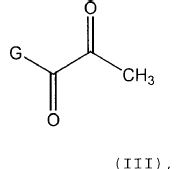
en la que G representa un grupo OR, siendo R un radical alquilo C1-6 ramificado o no ramificado o G representa un grupo O-K, siendo K un catión,
para dar un compuesto de fórmula (IV)
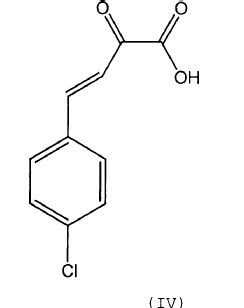
que opcionalmente se aísla y/u opcionalmente se purifica, y que se hace reaccionar con una fenilhidrazina opcionalmente sustituida de fórmula (V)
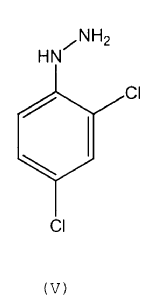
o una sal correspondiente de la misma, bajo atmósfera inerte, para dar un compuesto de fórmula (VI)
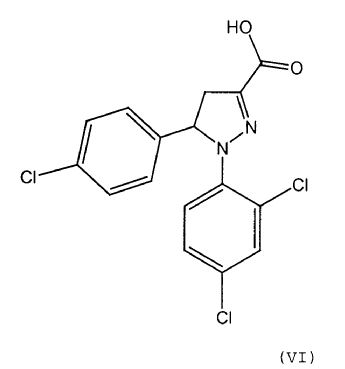
que opcionalmente se aísla y/u opcionalmente se purifica, y que se transfiere opcionalmente bajo una atmósfera inerte a un compuesto de fórmula (VII) por medio de la reacción con un agente activante
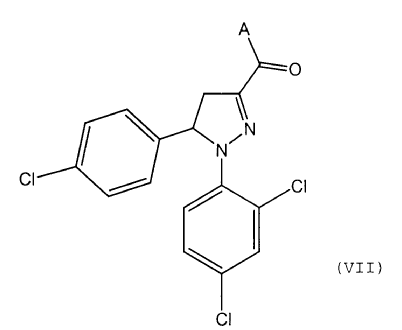
en el que A representa un grupo saliente, opcionalmente aislándose y/u opcionalmente purificándose dicho compuesto, y al menos un compuesto de formula (VII) se hace reaccionar con un compuesto de fórmula
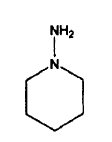
bajo atmósfera inerte para dar (rac)-N-piperidinil-5-(4-clorofenil)-1-(2,4-diclorofenil)-4,5-dihidro-1H-pirazol-3-carboxamida, que opcionalmente se aísla y/u opcionalmente se purifica,
seguido por una etapa de evaporación en la que la (rac)-N-piperidinil-5-(4-clorofenil)-1-(2,4-diclorofenil)-4,5-dihidro-1H-pirazol-3-carboxamida se disuelve en un disolvente orgánico que se evapora lentamente a temperaturas inferiores a la temperatura ambiente (25ºC), para dar (rac)-N-piperidinil-5-(4-clorofenil)-1-(2,4-diclorofenil)-4,5-dihidro-1H-pirazol-3-carboxamida X H2O.
4. Procedimiento según la reivindicación 3, caracterizado porque en la etapa de resolución el disolvente orgánico se selecciona de:
acetato de etilo,
diclorometano,
1,1,1-tricloroetano
acetato de isobutilo o
acetato de etilo-agua.
5. Procedimiento según cualquiera de las reivindicaciones 3 ó 4, caracterizado porque en la etapa de resolución la temperatura se disminuye hasta entre +5º y -20ºC.
6. Medicamento que comprende al menos un hidrato de pirazolina sustituido según la reivindicación 1 ó 2, y opcionalmente uno o más excipientes farmacéuticamente aceptables.
7. Uso del hidrato de pirazolina sustituido según una de las reivindicaciones 1 ó 2, para la preparación de un medicamento para la modulación de receptores de cannabinoides, preferiblemente los receptores de cannabinoides 1 (CB1)., para la profilaxis y/o el tratamiento de trastornos del sistema nervioso central, trastornos del sistema inmunitario, trastornos del sistema cardiovascular, trastornos del sistema endocrino, trastornos del sistema respiratorio, trastornos del tracto gastrointestinal o trastornos reproductores.
8. Uso del hidrato de pirazolina sustituido según una de las reivindicaciones 1 ó 2, para la preparación de un medicamento para la profilaxis y/o el tratamiento de trastornos de la ingestión de alimentos, preferiblemente de bulimia, anorexia, caquexia, obesidad, diabetes mellitus tipo II (diabetes no insulinodependiente), más preferiblemente de la obesidad.
9. Uso del hidrato de pirazolina sustituido según una de las reivindicaciones 1 ó 2, para la preparación de un medicamento para la profilaxis y/o el tratamiento de la psicosis.
10. Uso del hidrato de pirazolina sustituido según una de las reivindicaciones 1 ó 2, para la preparación de un medicamento para la profilaxis y/o el tratamiento del alcoholismo y/o la adicción al alcohol, abuso de nicotina y/o tabaquismo, el abuso de drogas y/o drogadicción y/o abuso de fármacos y/o farmacodependencia, preferiblemente abuso de drogas y/o drogadicción y/o abuso de nicotina y/o tabaquismo.
11. Uso del hidrato de pirazolina sustituido según una de las reivindicaciones 1 ó 2, para la preparación de un medicamento para la profilaxis y/o el tratamiento del cáncer, preferiblemente para la profilaxis y/o el tratamiento de uno o más tipos de cánceres seleccionados del grupo que consiste en cáncer cerebral, cáncer óseo, cáncer de labio, cáncer de boca, cáncer de esófago, cáncer de estómago, cáncer de hígado, cáncer de vejiga, cáncer de páncreas, cáncer de ovarios, cáncer cervical, cáncer de pulmón, cáncer de mama, cáncer de piel, cáncer de colon, cáncer intestinal y cáncer de próstata, más preferiblemente para la profilaxis y/o el tratamiento de uno o más tipos de cánceres seleccionados del grupo que consiste en cáncer de colon, cáncer intestinal y cáncer de próstata.
12. Uso del hidrato de pirazolina sustituido según una de las reivindicaciones 1 ó 2, para la preparación de un medicamento para la profilaxis y/o el tratamiento de uno o más trastornos seleccionados del grupo que consiste en trastornos óseos, preferiblemente osteoporosis (por ejemplo, osteoporosis asociada con una predisposición genética, déficit de hormonas sexuales o envejecimiento), enfermedad ósea asociada a cáncer o enfermedad ósea de Paget; esquizofrenia, ansiedad, depresión, epilepsia, trastornos neurodegenerativos, trastornos cerebelosos, trastornos espinocerebelosos, trastornos cognitivos, traumatismo craneal, traumatismo creaneoencefálico, accidente cerebrovascular, ataques de pánico, neuropatía periférica, glaucoma, migraña, enfermedad de Parkinson, enfermedad de Huntington, enfermedad de Alzheimer, enfermedad de Raynaud, temblores, trastornos compulsivos, demencia senil, trastornos tímicos, discinesia tardía, trastornos bipolares, trastornos de movimiento inducidos por medicamentos, distonía, choque endotoxémico, choque hemorrágico, hipotensión, insomnio, trastornos inmunológicos, placas escleróticas, vómitos, diarrea, asma, trastornos de la memoria, prurito, dolor, o para la potenciación del efecto analgésico de analgésicos narcóticos y no narcóticos, o para influir en el tránsito intestinal.
Patentes similares o relacionadas:
Antagonistas/agonistas inversos del receptor cannabinoide, del 13 de Noviembre de 2019, de Jenrin Discovery, Inc: Un compuesto seleccionado de los compuestos 1, 2, 3 y 4: **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo.
Compuestos de acilguanidina con actividad antiviral, del 26 de Abril de 2019, de Biotron Limited: Compuesto seleccionado del grupo que consiste en: (3-benzoil)cinamoilguanidina, 3(indan-4-il)-propenoilguanidina, 2,3-metilendioxicinamoilguanidina, y sales […]
Novedosos compuestos de aril-cianoguanidina, del 30 de Enero de 2019, de Bayer Pharma Aktiengesellschaft: Compuestos de fórmula general (I) **(Ver fórmula)** en la que R1 representa un grupo alquilo C1-C6, que está sustituido con un sustituyente seleccionado […]
Fármacos para inhibir la agregación de proteínas implicadas en enfermedades relacionadas con enfermedades neurodegenerativas y/o agregación de proteínas, del 16 de Enero de 2019, de LUDWIG-MAXIMILIANS-UNIVERSITAT MÜNCHEN: Un compuesto representado por la fórmula (E):**Fórmula** en donde: R se selecciona de hidrógeno; alquilo(C1-4); y -alquileno(C1-4)-halógeno; y […]
Derivados de pirazolona útiles en el tratamiento de esclerosis lateral amiotrófica, del 28 de Febrero de 2018, de NORTHWESTERN UNIVERSITY: Un compuesto para su uso en el tratamiento de la esclerosis lateral amiotrófica (ELA) o enfermedades neurodegenerativas caracterizadas por la […]
Compuestos heterocíclicos como plaguicidas, del 6 de Septiembre de 2017, de BAYER CROPSCIENCE AG: Uso no terapéutico de compuestos de la fórmula (I)**Fórmula** en donde A representa un radical de la serie**Fórmula** en donde […]
Derivados de arilsulfonilpirazolina carboxamidina como antagonistas de 5-HT6, del 25 de Mayo de 2016, de AbbVie Bahamas Ltd: Un compuesto de fórmula :**Fórmula** o un tautómero, estereoisómero, N-óxido o una sal farmacológicamente aceptable de cualquiera de los anteriores, donde: - R1 se […]
Compuestos de piridazina para controlar plagas de invertebrados, del 16 de Marzo de 2016, de BASF SE: Compuestos de piridazina de fórmula I y las sales y N-óxidos de los mismos, en la que A es un radical triazol, tiadiazol u oxadiazol de […]