Geles viscoelásticos como nuevos agentes de relleno.
Biomateriales que se pueden obtener mezclando
- el derivado autorreticulado de ácido hialurónico (ACP) con
- el derivado (HBC) de ácido hialurónico reticulado con 1,
4-butanodiol diglicidiléter (BDDE)
en una relación ponderal de entre 10:90 y 90:10 como nuevos agentes de relleno y/o como productos para el modelado del cuerpo.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP2010/005161.
Solicitante: FIDIA FARMACEUTICI S.P.A..
Nacionalidad solicitante: Italia.
Dirección: VIA PONTE DELLA FABBRICA 3/A 35031 ABANO TERME (PD) ITALIA.
Inventor/es: RENIER, DAVIDE, D\'ESTE,MATTEO.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61L27/26 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61L PROCEDIMIENTOS O APARATOS PARA ESTERILIZAR MATERIALES U OBJECTOS EN GENERAL; DESINFECCION, ESTERILIZACION O DESODORIZACION DEL AIRE; ASPECTOS QUIMICOS DE VENDAS, APOSITOS, COMPRESAS ABSORBENTES O ARTICULOS QUIRURGICOS; MATERIALES PARA VENDAS, APOSITOS, COMPRESAS ABSORBENTES O ARTICULOS QUIRURGICOS (conservación de cuerpos o desinfección caracterizada por los agentes empleados A01N; conservación, p. ej. esterilización de alimentos o productos alimenticios A23; preparaciones de uso medico, dental o para el aseo A61K). › A61L 27/00 Materiales para prótesis o para revestimiento de prótesis (prótesis dentales A61C 13/00; forma o estructura de las prótesis A61F 2/00; empleo de preparaciones para la fabricación de dientes artificiales A61K 6/80; riñones artificiales A61M 1/14). › Mezclas de materiales macromoleculares.
- A61L27/52 A61L 27/00 […] › Hidrogeles o hidrocoloides.
- A61L27/58 A61L 27/00 […] › Materiales al menos parcialmente reabsorbibles por el organismo.
PDF original: ES-2509225_T3.pdf
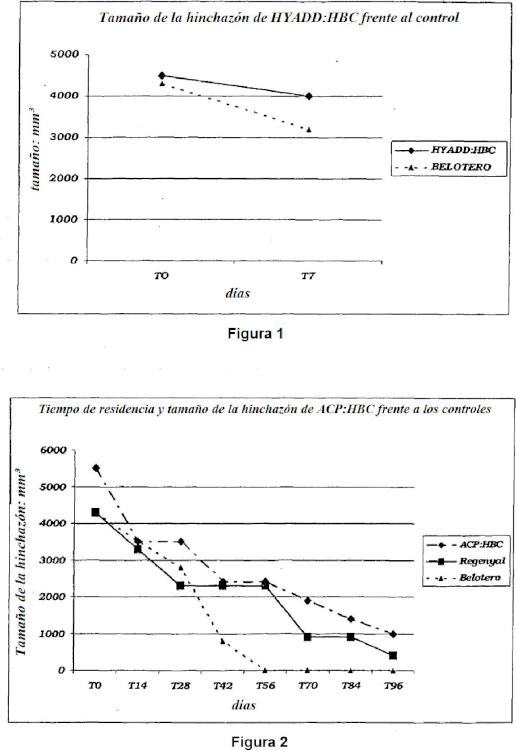
Fragmento de la descripción:
Geles viscoelásticos como nuevos agentes de relleno Objeto de la invención Geles viscoelásticos como nuevos agentes de relleno.
Campo de la invención El ácido hialurónico (AH) es un heteropolisacárido que consiste en restos alternados de ácido D-glucorónico y Nacetil-D-glucosamina.
El AH es un polímero de cadena lineal con un peso molecular que oscila entre 50.000 y 13 × 106 Dalton, dependiendo de la fuente de la que se obtenga y de los procedimientos de preparación usados.
El AH está presente en la naturaleza en geles pericelulares, en la sustancia básica del tejido conectivo de vertebrados (del que es uno de los componentes principales) , en el humor vítreo y en el cordón umbilical.
El AH desempeña un papel importante en el organismo biológico como soporte estructural y mecánico para los tejidos, y como componente activo en la fisiología celular de tejidos tales como la piel, los tendones, los músculos y el cartílago.
Es una de las moléculas principales de la matriz cartilaginosa, y también representa el principal constituyente no proteico del líquido sinovial. Puesto que es una molécula viscoelástica muy hidrófila, dota al líquido sinovial de propiedades lubricantes; por tanto el AH se ha usado en artrosis durante más de 30 años, principalmente para el tratamiento del dolor asociado.
El AH también desempeña un papel fundamental en los procedimientos de reparación tisular desde el punto de vista estructural (en la organización de la matriz extracelular y la regulación de su hidratación) , y como sustancia estimulante/reguladora de un amplio espectro de procedimientos fisiológicos en los que dicho polisacárido actúa directa y/o indirectamente (formación de coágulos, actividad fagocítica, proliferación de fibroblastos, neovascularización, reepitelización, etc.) (Weigel P. y col., J Theoretical Biol, 1986:219-234; Abatangelo G. y col., J Surg Res, 1983, 35:410-416; Goa K. y col., Drugs, 1994, 47:536-566) . Puesto que estas propiedades se conocen desde hace bastante tiempo, el AH también se ha usado para preparar apósitos para la cicatrización de heridas, úlceras y lesiones cutáneas de orígenes diferentes.
El ácido hialurónico también se usa como agente de relleno para arrugas, surcos y pequeñas depresiones de la cara, e incrementar el volumen de labios y mejillas, debido a que es inmunológicamente inerte, no tóxico, biodegradable y biorreabsorbible.
El tratamiento a base de ácido hialurónico está indicado para la corrección de:
â?¢ el volumen y el contorno de labios,
â?¢ surcos (por ejemplo, los pliegues nasolabiales)
â?¢ remodelación del contorno facial (por ejemplo, mejillas y barbilla)
â?¢ arrugas (por ejemplo, líneas glabelares y las comisuras de la boca)
â?¢ arrugas periorbitales
â?¢ cicatrices fibrosas post-acné
â?¢ cicatrices fibrosas post-traumáticas
â?¢ manchas de tejidos blandos
â?¢ cicatrices de rinoplastia.
El ácido hialurónico no es un agente de relleno permanente. Esto significa que, una vez inyectado, el producto se metaboliza y es reabsorbido gradualmente por el cuerpo en un tiempo que varía según el área tratada y el tipo de preparación usada. El efecto de relleno e incremento de volumen (o atenuación de las arrugas) es inmediato, y solo dura unas pocas semanas. Los productos principales presentes en el mercado se pueden clasificar en las siguientes categorías, en base a sus diferentes tiempos de reabsorción:
â?¢ agentes de relleno de reabsorción rápida (2-3 meses)
â?¢ agentes de relleno de duración media (5-6 meses) ,
â?¢ agentes de relleno de reabsorción lenta (1 año cerrar para tesis tal como Restylane Sub Q (QMED, documento EP0839159) .
En la dermis, el AH realiza funciones hidratantes debido a su alta capacidad para retener agua, y funciones estructurales como "andamiaje" debido a que, al unirse a otras sustancias, forma complejos macromoleculares que compactan la piel.
Por tanto, el mecanismo de acción consiste en un relleno volumétrico inmediato debido a las propiedades viscoelásticas del producto, y nueva síntesis de colágeno debido a la estimulación de los fibroblastos cutáneos.
No obstante, el AH es un polisacárido natural que es degradado rápidamente por las enzimas hialuronidasas presentes en el tejido conectivo; con el fin de obtener agentes de relleno cuyo efecto perdure durante varios meses, el AH se debe someter por tanto a procedimientos de reticulación que mejoran sus propiedades viscoelásticas e incrementan su tiempo de residencia. Los agentes de relleno así formados se reticulan, por ejemplo, mediante BDDE (1, 4-butanodiol diglicidiléter, Restylane®, BELOTERO® y Regenyal Idea) o DVS (divinil sulfona, Hylaform®) , que crean puentes entre las moléculas de polímero. Sin embargo, el incremento del grado de reticulación desnaturaliza progresivamente el AH hasta el punto de modificar profundamente sus propiedades químicas, físicas y biológicas. Las matrices de AH reticuladas en exceso se presentan en forma de sólidos particulados que ya no son reconocidos por las células (y en particular por el sistema inmunitario) como AH; por tanto, el polisacárido se percibe como un cuerpo exógeno, lo que desencadena reacciones inflamatorias con la formación de cápsulas fibróticas a su alrededor. Además, el AH excesivamente reticulado es incapaz de estimular la regeneración de tejido dérmico/cutáneo inducida, como es sabido por resultados científicos perfectamente establecidos, por fragmentos de AH (en particular aquellos con un bajo peso molecular) que tienen el efecto de estimular la síntesis de colágeno por parte de los fibroblastos cutáneos.
Los agentes de relleno también se clasifican como reabsorbibles o permanentes. El tipo reabsorbible es el más biocompatible; consisten en ácido hialurónico o colágeno, modificado o presente en su forma nativa, y en consecuencia se reabsorben en un año como máximo. El tipo permanente consiste en polímeros sintéticos tales como las poliacrilamidas, moléculas reticuladas particulares que forman un gel estable cuando se combinan con el agua. El tipo permanente siempre permanece in situ y son muy útiles para el relleno de los labios, pero su uso no está recomendado debido a que se producen inflamaciones agudas cada vez con mayor frecuencia debido a su inserción cutánea, lo que da lugar a cápsulas fibróticas en torno al agente de relleno, que es percibido como un cuerpo exógeno y por tanto tóxico.
El documento WO 2008/068297 desvela un agente de relleno que consiste en AH reticulado con BDDE y AH tal cual en una relación de 1:1 o 1:0, 05, en el que el AH libre está atrapado en la red reticulada.
El documento WO 2009/073437 describe una formulación en gel a base de polisacáridos, que incluye AH, preferentemente en forma reticulada, asociado a un inhibidor de la degradación del propio polisacárido. Entre los diversos sistemas de reticulación, también se menciona el BDDE.
El documento WO 99/24070 desvela composiciones viscoelásticas en las que el AH está esterificado y posiblemente está asociado a derivados autorreticulados del AH, y asociado adicionalmente a fármacos o sustancias biológicamente activas.
El documento WO 97/49412 describe composiciones para el tratamiento de artropatías constituidas por AH autorreticulado, opcionalmente asociado a AH tal cual.
El solicitante ha perfeccionado un nuevo tipo de biomaterial como nuevo agente de relleno y/o como nuevo producto para modelar el cuerpo, formado al mezclar dos derivados reticulados del AH de formas diferentes pero complementarias, para obtener un sustituto de piel/tejido que permite la hidratación inmediata (en consecuencia el relleno inmediato) de la piel/tejido tratados, mientras mantiene tiempos de degradación in vivo muy prolongados eliminando la necesidad de inyecciones repetidas, y reduciendo así los efectos secundarios.
Los nuevos biomateriales a los cuales se refiere la presente invención presentan características de biocompatibilidad particulares idénticas a las del ácido hialurónico tal cual, pero su biodegradabilidad es diferente; cuando se implantan in vivo, su tiempo de residencia es mucho más prolongado que el del AH sin modificar, permitiendo así la regeneración/reconstrucción inmediata del tejido dérmico/cutáneo que haya perdido su compactibilidad original.
Descripción detallada de la invención El solicitante ha perfeccionado un nuevo tipo de biomaterial como agente de relleno y/o como nuevo producto para el modelado del cuerpo basado en la mezcla de dos derivados del AH con características diferentes, pero complementarias, para obtener un nuevo producto para inyección en el tratamiento... [Seguir leyendo]
Reivindicaciones:
1. Biomateriales que se pueden obtener mezclando â el derivado autorreticulado de ácido hialurónico (ACP) con â el derivado (HBC) de ácido hialurónico reticulado con 1, 4-butanodiol diglicidiléter (BDDE)
en una relación ponderal de entre 10:90 y 90:10 como nuevos agentes de relleno y/o como productos para el modelado del cuerpo.
2. Biomateriales según la reivindicación 1, en los que la relación ponderal es de 90:10 a 50:50, como agentes de relleno biorrevitalizantes.
3. Biomateriales según la reivindicación 1, en los que la relación ponderal es de 10:90 a 50:50 con un efecto de aumento del volumen.
4. Biomateriales según la reivindicación 3, en los que la relación ponderal es de 25:75.
5. Procedimiento de mezcla de ACP con HBC preparado mediante un procedimiento que comprende las siguientes etapas:
a. disolución en solución alcalina de diepóxido de BDDE en una relación estequiométrica del 2, 5 al 25 % molar de las unidades de repetición del ácido hialurónico, seguido por
b. dispersión de ácido hialurónico (AH) en la solución mencionada en el apartado a) , a temperatura ambiente;
c. desencadenamiento de la reacción mediante la activación por calor, con la solución mencionada en el apartado b) que se calienta a una temperatura de entre 35 y 55 º C durante entre 2 y 36 horas;
d. extrusión de la masa obtenida a través de un tamiz metálico, para reducirla a partículas con un tamaño de 600 μm aproximadamente;
e. hidratación del gel obtenido diluyéndolo con agua en un factor de 3 a 20;
f. corrección del pH a neutro con una solución acuosa de HCl;
g. precipitación con un disolvente orgánico soluble en agua hasta que el producto se obtiene en forma de polvo;
h. lavado con disolventes orgánicos que contienen agua;
i. secado al vacío hasta que se hayan eliminado los disolventes residuales por debajo de 400 ppm y se obtenga un polvo de HBC; en el que el procedimiento de mezcla comprende las siguientes etapas:
j. mezcla de polvo de ACP con polvo de HBC en una relación de ACP:HBC de entre 90:10 y 10:90;
k. hidratación con solución salina o tampón fosfato, que da lugar a una concentración total de AH de entre 12 y 27 mg/ml;
l. extrusión a una temperatura de entre 25 y 65 º C a través de un tamiz con una malla de entre 50 y 500 μm;
m. llenado de la jeringa;
n. esterilización por calor con vapor de agua saturado a una temperatura de entre 120 y 124 º C durante al menos 10 min.
6. Procedimiento de mezcla de ACP con HBC preparado mediante un procedimiento que comprende las siguientes etapas:
a. disolución en solución alcalina de diepóxido de BDDE en una relación estequiométrica del 2, 5 al 25 % molar de las unidades de repetición del ácido hialurónico, seguido por
b. dispersión de AH en la solución mencionada en el apartado a) , a temperatura ambiente;
c. desencadenamiento de la reacción mediante la activación por calor, con la solución mencionada en el apartado b) que se calienta a una temperatura de entre 35 y 55 º C durante entre 2 y 36 horas;
d. corrección del pH a neutro con una solución acuosa de HCl;
e. hidratación del gel obtenido diluyéndolo con agua en un factor de 3 a 20; en el que el procedimiento de mezcla comprende las siguientes etapas:
f. mezcla de gel o polvo de ACP con HBC en forma de gel en una relación de ACP:HBC de entre 90:10 y 10:90;
g. trituración y homogeneización pasando a través de un filtro con un coeficiente de retención de material particulado de entre 25 y 150 μm;
h. llenado de la jeringa;
i. esterilización por calor con vapor saturado a una temperatura de entre 120 y 124 º C durante al menos 10 min.
7. Procedimiento según las reivindicaciones 5 o 6, en el que el AH usado para la preparación de los derivados de HBC y ACP tiene un peso molecular medio de entre 400 y 3 x 106 Da, preferentemente entre 1 x 105 Da y 1 x 106 Da, y más preferentemente entre 200.000 y 1 x 106 Da.
8. Biomateriales obtenidos según la reivindicación 6, en los que la relación ponderal de ACP:HBC es de 25:75.
9. Biomateriales según las reivindicaciones anteriores, en los que el vehículo es solución salina.
10. Biomateriales según las reivindicaciones anteriores, que contienen lidocaína.
11. Biomateriales según la reivindicación 8, que contienen lidocaína, en los que el vehículo consiste en solución salina.
12. Biomateriales según las reivindicaciones anteriores para su uso como nuevos agentes de relleno y/o como
nuevos productos para el modelado del cuerpo en el tratamiento de manchas de la piel, en dermatología, en dermocosmética y/o en cirugía estética.
Patentes similares o relacionadas:
Materiales compuestos biocompatibles anhidros, del 22 de Julio de 2020, de Kuros Biosciences B.V: Material compuesto biocompatible anhidro que comprende un material polimérico biodegradable y un material sintético granular, en donde el material polimérico […]
Material para prótesis de alta resistencia al impacto, transparente, con bajo contenido de MMA residual, del 1 de Julio de 2020, de KULZER GMBH: Material de base para prótesis bicomponente autopolimerizable, que comprende A) al menos un componente monomérico líquido, B) al menos un componente en polvo, […]
Matriz de soporte de injerto para reparación de cartílago y procedimiento de obtención de la misma, del 1 de Julio de 2020, de ETH ZURICH: Un procedimiento de proporción de una matriz de soporte de injerto para reparación de cartílagos, particularmente en un paciente humano, que comprende las etapas de: […]
Composiciones poliméricas reabsorbibles para su uso en medicina, odontología y cirugía, del 17 de Junio de 2020, de Syncera, Inc: Una composición polimérica fluida o maleable en forma esencialmente seca, que comprende: (a) un copolímero de bloques de poli(alquileno)-poli(etilen […]
Formulación de FGF-18 en hidrogeles de alginato/colágeno, del 15 de Abril de 2020, de Ares Trading SA: Un sistema de gelificación de dos componentes, en donde dicho sistema de gelificación se forma a partir de: a. un primer componente (solución 1) […]
Copolímero acrílico, hidrófobo, reticulado, a base de alcohol cinámico, para lentes intraoculares, del 8 de Abril de 2020, de Acrylian: Material polimérico acrílico, hidrófobo, es decir, que no absorbe más del 5 % de agua a 35 °C, adecuado para hacer lentes intraoculares flexibles, […]
Biomaterial conductor para mejorar la conducción in vitro e in vivo, del 1 de Abril de 2020, de UNIVERSITY HEALTH NETWORK: Un material biocompatible que comprende un polímero conductor y un componente biocompatible, en donde el polímero conductor es un polímero basado en polipirrol; el componente […]
Estructura de biomaterial para regenerar la mucosa oral, del 1 de Enero de 2020, de HISTOCELL, S.L: Método para producir una estructura de biomaterial, comprendiendo dicho método: a) proporcionar un hidrogel que comprende una red de fibrina y una red de polisacárido; […]