Formulaciones de pancreolipasa de baja potencia con recubrimiento entérico.
Una composición que contiene al menos una enzima digestiva y al menos un portador en la que:
a) la cantidad total de enzimas digestivas en la composición es entre aproximadamente 4 y aproximadamente 20% en peso, donde el portador se elige del grupo que consiste en polioles, azúcares, alcoholes de azúcar, celulosa, sales de fosfato de calcio, aminoácidos y sus mezclas; y al menos un portador de la composición tiene un tamaño de partícula mayor de 100 μm.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/IB2011/002419.
Solicitante: Aptalis Pharma Limited.
Inventor/es: BOLTRI, LUIGI, STOLLBERG,CHRISTIAN, ORTENZI,GIOVANNI, DE FRANZA,GIUSEPPE, CLEMENTI,DANILO.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K38/43 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 38/00 Preparaciones medicinales que contienen péptidos (péptidos que contienen ciclos beta-lactama A61K 31/00; dipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina 2,5-dionas, A61K 31/00; péptidos basados en la ergolina A61K 31/48; que contienen compuestos macromoleculares que tienen unidades aminoácido repartidas estadísticamente A61K 31/74; preparaciones medicinales que contienen antígenos o anticuerpos A61K 39/00; preparaciones medicinales caracterizadas por los ingredientes no activos, p. ej. péptidos como soportes de fármacos, A61K 47/00). › Enzimas; Proenzimas; Sus derivados.
- A61K9/20 A61K […] › A61K 9/00 Preparaciones medicinales caracterizadas por un aspecto particular. › Píldoras, pastillas o comprimidos.
- A61K9/28 A61K 9/00 […] › Grageas; Píldoras o comprimidos con revestimientos.
PDF original: ES-2515715_T3.pdf
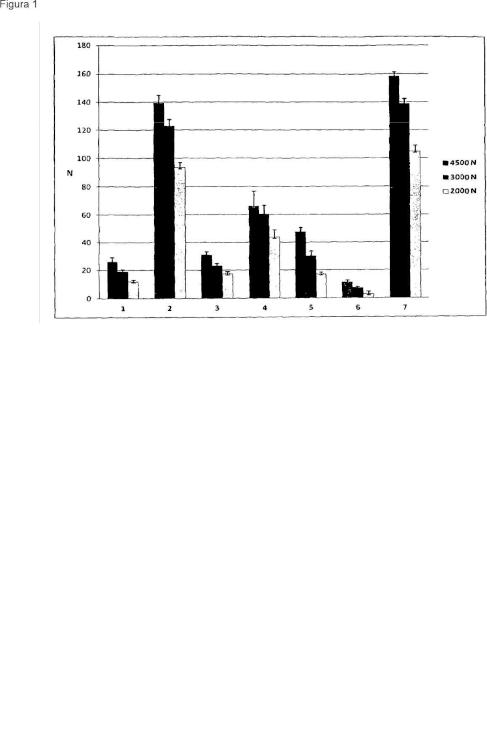
Fragmento de la descripción:
Formulaciones de pancreolipasa de baja potencia con recubrimiento entérico Campo de la invención
En diversas realizaciones, la presente invención apunta a composiciones farmacéuticas con un contenido bajo (diluido) y estable de enzimas digestivas que contienen al menos una enzima digestiva y al menos un portador, o a una forma farmacéutica de éstas. En otras realizaciones, la invención también apunta a procesos de preparación de la composición o la forma farmacéutica. En otras realizaciones, la invención apunta al tratamiento y la prevención de trastornos asociados a una deficiencia de enzimas digestivas en un paciente que lo necesita, que comprende administrar a dicho paciente una cantidad farmacéuticamente aceptable de la composición que tiene un contenido bajo y estable de enzima digestiva o una forma farmacéutica de ésta.
Antecedentes de la invención
La dosificación adecuada de medicamentos para los pacientes es un motivo de preocupación importante en el campo de la medicina. En particular, para los lactantes, los niños más pequeños o los pacientes geriátricos, y a veces también para la población adulta, la administración de medicamentos y los métodos de dosificación a menudo presentan problemas sustanciales. Es bien sabido en el área, que los medicamentos se proporcionan de muchas formas (por ej., líquida, sólida, y combinaciones de sólidos en líquidos) y se administran a los pacientes de diversas maneras (por ej., por vía oral, inyectable o transdérmica).
La FDA estima que más de 2 estadounidenses sufren de insuficiencia pancreática exocrina (IPE). La IPE implica un trastorno fisiológico en el que las personas son incapaces de digerir adecuadamente los alimentos debido a la falta de enzimas digestivas elaboradas por su páncreas. La falta de enzimas digestivas deriva en trastornos como mala digestión y mala absorción de nutrientes, que producen desnutrición y otras afecciones fisiológicas consecuentes indeseables asociadas. Estos trastornos son comunes en las personas que sufren de fibrosis quística (FQ) y otras afecciones que comprometen la función exocrina del páncreas, como el cáncer pancreático, la pancreatectomía y la pancreatitis. La desnutrición puede ser potencialmente mortal si no se trata, particularmente en el caso de lactantes y pacientes con fibrosis quística, y los trastornos pueden causar retraso del crecimiento, inmunodepresión y acortar la esperanza de vida.
Las enzimas digestivas, como la pancreolipasa y otros productos de enzimas pancreáticas (PEP), se pueden administrar para remediar al menos parcialmente la IPE. Las enzimas digestivas administradas facilitan que los pacientes puedan digerir más eficazmente los alimentos. El tratamiento con enzimas es un aspecto fundamental del manejo clínico de la nutrición y la digestión en la población con FQ. Pautas infantiles publicadas recientemente recomiendan la iniciación inmediata de TREP (terapia de reemplazo con enzima pancreática) en los recién nacidos con FQ que tienen insuficiencia pancreática sintomática o confirmada. En este contexto se debe identificar un régimen de dosificación óptimo. Se cree que el uso de terapia de reemplazo con enzima pancreática en los lactantes puede mejorar el crecimiento a corto y a largo plazo y los resultados nutricionales y en consecuencia incrementar la función pulmonar y en última instancia la supervivencia.
Las enzimas pancreáticas que se han utilizado en el tratamiento de IPE para compensar la pérdida de la función digestiva, se han utilizado por más de 6 años. Su uso hasta hace poco no estaba sujeto a las directrices reglamentarias que rigen las aprobaciones de fármacos basadas en la seguridad y la eficacia y los controles durante la fabricación. Recientemente, las terapias de reemplazo con enzimas pancreáticas se han convertido en el tema de las iniciativas de las autoridades reguladoras estadounidenses y europeas que exigen que los productos de enzimas pancreáticas comercializados pasen por el proceso actual de aprobación de fármacos para permanecer en el comercio. Zenpep®, Creon® y Pancreaze® son tres productos que atravesaron con éxito el proceso establecido por la FDA y están aprobados para su comercialización en los Estados Unidos. En otros territorios o países donde iniciativas similares aún están en curso o aún no han sido implementadas, todavía se dispone de diversos productos de enzimas pancreáticas.
Se han desarrollado cápsulas que contienen enzimas digestivas como pancreolipasa para la administración oral. Sin embargo, si un paciente no puede tragar las cápsulas, cada cápsula se puede abrir y el contenido espolvorear sobre una pequeña cantidad de alimento, generalmente un alimento blando, ácido (como puré de manzana comercial) y administrar por vía oral al paciente con una cuchara. Alternativamente, dichos medicamentos se pueden administrar por vía oral a lactantes y niños utilizando una jeringa que contenga el contenido suspendido en un medio adecuado para su administración.
En la rotulación de los productos de pancreolipasa se indica generalmente que contienen tres clases de enzimas: lipasa, amilasa y proteasa, y las concentraciones o la potencia de éstas. Estas enzimas catalizan la hidrólisis de las grasas a glicerol y ácidos grasos, el almidón a dextrina y azúcares, y las proteínas a aminoácidos y sustancias
derivadas. La digestión es, sin embargo, un proceso complejo en el que participan muchas otras enzimas y sustratos que contribuyen al funcionamiento digestivo correcto y a la producción de toda la gama de productos digestivos. Otras enzimas contenidas en la pancreolipasa incluyen tripsina, carboxipeptidasas, elastasas, fosfolipasas y colesterolasas entre otras, y varios cofactores y coenzimas. Estas sustancias se producen naturalmente en el páncreas y también contribuyen al correcto funcionamiento digestivo.
La pancreolipasa se prepara habitualmente a partir de glándulas pancreáticas porcinas, aunque también se pueden utilizar otras fuentes, por ejemplo los que se describen en U.S. 6,51,22, U.S. 24/57944, 21/46493 y WO 2644529, cada una de las cuales se incorpora por referencia en su totalidad a todos los efectos.
Las enzimas pancreáticas tienen una actividad óptima en condiciones próximas a las neutras y ligeramente alcalinas. En condiciones gástricas, las enzimas pancreáticas pueden ser inactivadas con la pérdida de actividad biológica resultante. Por consiguiente, las enzimas administradas de manera exógena están generalmente protegidas de la inactivación gástrica y permanecen intactas durante su tránsito a través del estómago y al duodeno. Por lo tanto, es deseable recubrir las enzimas pancreáticas. Las lipasas pancreáticas son las más sensibles a la inactivación gástrica y constituyen la clase más importante de enzimas en el tratamiento de la mala absorción. Habitualmente se controla la actividad de la lipasa para determinar la estabilidad de una composición enzimática que contenga lipasa.
Todo el contenido de U.S. 7,658,918 expedida a Ortenzi et al. está expresamente incorporado en este documento, por referencia, en su totalidad a todos los efectos. U.S. 7,658,918 describe composiciones de enzimas digestivas estables y explica que ciertos medicamentos particulados, para administración oral, se diseñan para que pasen a través del estómago del paciente y posteriormente se liberen en los intestinos; la cantidad total de pancreolipasa (en peso) en los núcleos de las partículas contenidas en las composiciones o formas farmacéuticas orales dadas a conocer en dicha patente es de 68 a 9%.
Aptalis Pharma comercializa al menos algunos medicamentos multiparticulados de perlas de enzima pancreolipasa con recubrimiento entérico. Por ejemplo, Aptalis Pharma comercializa cápsulas de liberación retardada para el tratamiento de la insuficiencia pancreática exocrina (IPE) en pacientes, con la designación EUR-18 y la marca registrada Zenpep®. Cada cápsula de Zenpep® para administración oral contiene perlas con recubrimiento entérico de alto contenido de pancreolipasa (1.8 a 1.9 mm para 3, 5 unidades USP de lipasa, 2.2 a 2.5 mm para 1 , 15 , 2 y 25 unidades USP de lipasa).
Todos los productos de pancreolipasa comercializados tienen un contenido de pancreolipasa muy alto.
Algunas composiciones de enzimas digestivas disponibles en el comercio tienen una pérdida de actividad de lipasa en el tiempo de hasta 35% o más. Para compensar la pérdida de actividad enzimática durante el almacenamiento y para asegurar que el producto proporcione la potencia declarada en la rotulación al final de la vida útil, generalmente los fabricantes llenan en exceso las formas farmacéuticas entre un 5% y un 6% y las especificaciones de la USP para las cápsulas... [Seguir leyendo]
Reivindicaciones:
1. Una composición que contiene al menos una enzima digestiva y al menos un portador en la que:
a) la cantidad total de enzimas digestivas en la composición es entre aproximadamente 4 y aproximadamente 2% en peso, donde el portador se elige del grupo que consiste en polioles, azúcares, alcoholes de azúcar, celulosa, sales de fosfato de calcio, aminoácidos y sus mezclas; y al menos un portador de la composición tiene un tamaño de partícula mayor de 1 pm.
2. La composición de la reivindicación 1, en la que la cantidad total de enzimas digestivas en la composición es entre aproximadamente 4 y aproximadamente 2% en peso, y al menos un portador es celulosa microcristalina.
3. La composición de la reivindicación 1 o la reivindicación 2, en la que las enzimas digestivas están en forma de perlas de pancreolipasa con recubrimiento entérico.
4. La composición de la reivindicación 3, en la que las perlas con recubrimiento entérico contienen: entre aproximadamente 4 y aproximadamente 2% en peso de pancreolipasa, y entre aproximadamente 7 y aproximadamente 96% en peso de al menos un portador, donde cada porcentaje en peso se basa en el peso total de las perlas sin recubrir.
5. La composición de la reivindicación 3, en la que las perlas con recubrimiento entérico contienen aproximadamente 15% en peso de pancreolipasa, aproximadamente 8% del portador y aproximadamente 5% de otros excipientes, donde cada % en peso se basa en el peso total de las perlas sin recubrir.
6. La composición de la reivindicación 1, en la que el portador se elige del grupo que consiste en celulosa microcristalina, trehalosa, inositol, L-prolina en forma anhidra, fosfato dibásico de calcio anhidro, lactosa anhidra, lactosa monohidratada, isomalt, manitol, o sus mezclas.
7. La composición de la reivindicación 6, en la que el portador es celulosa microcristalina con un contenido de humedad menor de 5%, un tamaño medio nominal de partícula de aproximadamente 16 pm, tamaño de malla 38: cantidad retenida á 1.%, tamaño de malla 94: cantidad retenida < 5.%, tamaño de malla 3: cantidad retenida <
7.%.
8. La composición de la reivindicación 6, en la que el portador es celulosa microcristalina con un contenido de humedad menor o igual de 5%, un tamaño medio nominal de partícula de aproximadamente 18 pm, tamaño de malla 6: cantidad retenida £ 1,%, tamaño de malla 1: cantidad retenida £ 5.%.
9. Una forma farmacéutica que contiene la composición de las reivindicaciones 1 a 8.
1. La forma farmacéutica de la reivindicación 9, donde dicha forma farmacéutica es una cápsula.
11. La forma farmacéutica de la reivindicación 1, en la que la actividad de lipasa de la forma farmacéutica es entre aproximadamente 5 y aproximadamente 5 unidades USP.
12. La forma farmacéutica de la reivindicación 11, en la que la actividad de lipasa de la forma farmacéutica es entre aproximadamente 675 y aproximadamente 825 unidades USP.
13. La forma farmacéutica de la reivindicación 12, en la que la actividad de lipasa de la forma farmacéutica es entre aproximadamente 675 y aproximadamente 825 unidades USP, la actividad de proteasa es entre 125 y 385 unidades USP y la actividad de amilasa entre 16 y 6575 unidades USP
14. Un envase que contiene un recipiente sellado, en el que el recipiente sellado está compuesto por un material resistente la humedad, un desecante, y al menos una forma farmacéutica de las reivindicaciones 9 a 13, en el que el desecante y al menos una forma farmacéutica están dentro del recipiente sellado.
15. El envase de la reivindicación 14, en el que el material resistente a la humedad se elige del grupo que consiste en metal, vidrio, plástico y plástico recubierto de metal.
16. Un proceso para la preparación de la composición de las reivindicaciones 1 a 8, que comprende los pasos siguientes: a) mezclar la pancreolipasa y el al menos un portador, y opcionalmente otros excipientes; b) comprimir la mezcla en forma de perlas; c) recubrir las perlas con un polímero entérico; donde los pasos se llevan a cabo en un ambiente de baja humedad y la humedad del portador o los portadores es menor o igual de 5%.
17. Un proceso para la preparación de la forma farmacéutica de las reivindicaciones 9 a 13 que consiste en preparar
la forma farmacéutica de la composición de las reivindicaciones 1 a 8, donde los pasos se llevan a cabo en un ambiente de baja humedad y la humedad del portador o los portadores es menor o igual de 5%.
18. El proceso de la reivindicación 17, en el que la forma farmacéutica es una cápsula que tiene un contenido de 5 humedad residual inferior a 5%.
19. El proceso de la reivindicación 17, en el que la forma farmacéutica es una cápsula que tiene un contenido de humedad residual inferior a 2%.
2. La composición o la forma farmacéutica de las reivindicaciones 1 a 13, para usar en un método para tratar o
prevenir un trastorno o una afección asociados a deficiencia de enzimas digestivas en un paciente que lo necesita.
21. La composición o la forma farmacéutica de las reivindicaciones 1 a 13 para usar en un procedimiento de terapia de reemplazo de enzima pancreática (TREP) en un recién nacido o lactante con fibrosis quística que tiene
insuficiencia pancreática exocrina sintomática o confirmada.
22. La composición o la forma farmacéutica de las reivindicaciones 1 a 13, para usar en un método de mejora a corto o largo plazo del crecimiento y los resultados nutrlclonales de un recién nacido o un lactante con insuficiencia pancreática sintomática o confirmada.
Patentes similares o relacionadas:
Compuestos para el tratamiento de Trastornos Neuropsiquiátricos, del 24 de Junio de 2020, de Curemark LLC: Una composición que comprende enzimas digestivas para uso en el tratamiento del Trastorno Esquizofreniforme, en donde las enzimas digestivas comprenden amilasa, lipasa […]
Procedimientos para el tratamiento dietético del síndrome del intestino irritable y la malabsorción de carbohidratos, del 3 de Junio de 2020, de GANEDEN BIOTECH, INC.: Uso de esporas de Bacillus coagulans Hammer en la fabricación de un medicamento para reducir los síntomas del síndrome del intestino irritable (SII) […]
Antígenos de coagulasa estafilocócica y métodos para su uso, del 13 de Mayo de 2020, de UNIVERSITY OF CHICAGO: Una composición inmunógena que comprende al menos dos dominios 1-2 de coagulasa estafilocócica diferentes, en donde cada uno de los al menos dos dominios […]
Ceramidasa y diferenciación celular, del 22 de Abril de 2020, de MOUNT SINAI SCHOOL OF MEDICINE: Un método in vitro para mejorar el fenotipo de una población de condrocitos, dicho método comprende: seleccionar una población de condrocitos de mamífero que […]
Composiciones para tratar MPSI, del 22 de Abril de 2020, de THE TRUSTEES OF THE UNIVERSITY OF PENNSYLVANIA: Un vector que lleva un casete de expresión que comprende un gen de la alfa-L-iduronidasa humana (hIDUA) que tiene la secuencia de nucleótidos de SEQ ID NO: […]
Nanopartículas de sílice huecas con ingredientes bioactivos encapsulados, procedimiento de preparación y aplicaciones de las mismas, del 11 de Marzo de 2020, de National Taiwan University (50.0%): Nanopartícula de sílice, que comprende cubiertas de sílice con múltiples capas, en las que cada capa tiene mesoporos y encierra un espacio hueco cerrado, […]
Composición de enzimas digestivos adecuada para la administración entérica, del 19 de Febrero de 2020, de Allergan Pharmaceuticals International Limited: Composición de enzimas digestivos que comprende: a) un producto de enzimas digestivos recubierto entéricamente, en el que el producto digestivo […]
Composición, del 16 de Octubre de 2019, de Optibiotix Limited: Una composición que comprende una cepa de Lactobacilli que tiene una elevada actividad de hidrolasa de sales biliares y un agente modificador […]