Método para el enriquecimiento de espermatozoides sin rotura de la cadena de ADN y reducción de los riesgos de anomalías y/o aneuploidía.
Método para producir una muestra enriquecida de espermatozoides sin roturas de la cadena de ADN,
que comprende las siguientes etapas
(a) disponer un fluido seminal que comprende al menos 15% de oligo-, al menos 32% de asteno- y/o al menos 4% de terato-zoospermia, basado en la cantidad total de los espermatozoides en el fluido seminal en una primera cámara de un dispositivo de selección;
(b) llenar una segunda cámara del dispositivo de selección con un medio para recibir espermatozoides sin rotura de la cadena de ADN; y
(c) conectar ambas cámaras mediante un elemento de puente de tal manera que se forma un puente de fluido entre la primera y la segunda cámara que permite que los espermatozoides sin rotura de la cadena de ADN pasen de la primera a la segunda cámara.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP2011/065665.
Solicitante: ZECH, JOSEF.
Nacionalidad solicitante: Austria.
Dirección: Brennerstrasse 15 6020 Innsbruck AUSTRIA.
Inventor/es: ZECH, JOSEF.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61B17/43 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61B DIAGNOSTICO; CIRUGIA; IDENTIFICACION (análisis de material biológico G01N, p.ej. G01N 33/48). › A61B 17/00 Instrumentos, dispositivos o procedimientos quirúrgicos, p. ej. torniquetes (A61B 18/00 tiene prioridad; dispositivos anticonceptivos, pesarios, dispositivos para su introducción A61F 6/00; cirugía ocular A61F 9/007; cirugía otorrina A61F 11/00). › para la inseminación artificial.
- C12M3/00 QUIMICA; METALURGIA. › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12M EQUIPOS PARA ENZIMOLOGIA O MICROBIOLOGIA (instalaciones para la fermentación de estiércoles A01C 3/02; conservación de partes vivas de cuerpos humanos o animales A01N 1/02; aparatos de cervecería C12C; equipos para la fermentación del vino C12G; aparatos para preparar el vinagre C12J 1/10). › Equipos para el cultivo de tejidos, de células humanas, animales o vegetales, o de virus.
- C12N5/076 C12 […] › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 5/00 Células no diferenciadas humanas, animales o vegetales, p. ej. líneas celulares; Tejidos; Su cultivo o conservación; Medios de cultivo para este fin (reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00). › Células espermáticas; Espermatogonias.
PDF original: ES-2543041_T3.pdf
Fragmento de la descripción:
Método para el enriquecimiento de espermatozoides sin rotura de la cadena de ADN y reducción de los riesgos de anomalías y/o aneuploidía La presente invención se refiere a un método para producir una muestra enriquecida de espermatozoides sin rotura de la cadena de ADN o, en particular, una muestra enriquecida de espermatozoides sin rotura de la cadena de ADN humano, que se puede utilizar adicionalmente en la tecnología de reproducción artificial (es decir, fertilización in vitro (FIV) , inseminación) o métodos de diagnóstico. Por consiguiente, la presente invención se refiere a un método para producir una o más muestras enriquecidas de espermatozoides sin rotura de la cadena de ADN, p. ej., fluido seminal (incluyendo pero no limitado a muestras de esperma/fluido seminal de una calidad deficiente) . Dicho método emplea un dispositivo de selección que comprende dos cámaras y un elemento puente tal como se proporciona en esta memoria. En particular, un método de este tipo puede comprender las siguientes etapas: (a) disponer un fluido seminal (por ejemplo una muestra de fluido seminal deficiente que comprende al menos 15% de oligo-, al menos 32% de asteno-y/o al menos 4% de terato-zoospermia, basado en la cantidad total de los espermatozoides en el fluido seminal) en la primera cámara del dispositivo de selección; (b) llenar la segunda cámara del dispositivo de selección con un medio para recibir espermatozoides sin rotura de la cadena de ADN; y (c) conectar ambas cámaras mediante el elemento de puente de manera que se produce un puente de fluido entre la primera y la segunda cámara. Esta técnica permite que los espermatozoides sin rotura de la cadena de ADN pasen de la primera a la segunda cámara. La muestra de espermatozoides sin rotura de la cadena de ADN obtenida es de alta calidad y se puede utilizar en diversas aplicaciones. De acuerdo con la presente invención, se encontró, en particular, que el método tal como se proporciona en esta memoria, conduce a métodos de reproducción tales como fertilizaciones in vitro, a una tasa sorprendentemente baja de anomalías y/o aneuploidías en la descendencia, en particular en la descendencia de padres que se caracterizan por su baja calidad del esperma. Por lo tanto, la presente invención se refiere a medios y métodos para la reducción del riesgo de anomalías congénitas o aneuploidías en tecnologías reproductivas artificiales, comprendiendo dichos medios y métodos la selección y/o el enriquecimiento de los espermatozoides de acuerdo con esta invención. En este contexto, también se describen medios y métodos para la selección y/o el enriquecimiento de espermatozoides que tienen un riesgo reducido de inducir o conducir a anomalías congénitas o aneuploidías después de y en el curso de las tecnologías de reproducción artificial tales como fertilizaciones in vitro.
Un número relativamente alto de pacientes no logra quedar embarazado a pesar de la ausencia evidente de factor masculino o femenino de la infertilidad. Es probable que muchas de estas parejas posean en realidad factor masculino genómico, incluyendo alteraciones meióticas, aneuploidía o daños del ADN de espermatozoides. La fragmentación del ADN de espermatozoides aumenta en muestras de semen de calidad deficiente y se correlaciona con la fertilización fallida, desarrollo defectuoso de pre-implantación, resultado del embarazo reducido y, en particular, tasa elevada de malformaciones de la descendencia (Zini, A., et al, 2008, "Sperm DNA damage is associated with an increased risk of pregnancy loss after IVF and ICSI:systemic review and meta-analysis Hum. Reprod. 23, 2663-2668) .
En los últimos años, se han establecido varios ensayos para el análisis de la fragmentación del ADN de espermatozoides. Entre otros, marcaje de extremos mellados con dUTP mediado por TdT (TUNEL) , ensayo cometa, ensayo de la estructura de la cromatina espermática (SCSA) , así como el ensayo de dispersión de la cromatina espermática (SCD) son los enfoques más comúnmente utilizados en los laboratorios de fecundación in vitro. Estos ensayos se pueden subdividir en dos categorías, los que detectan directamente el daño del ADN (p. ej., TUNEL) y los que miden la fragmentación del ADN después de un proceso de desnaturalización más bien suave (p. ej., SCSA, SCD) .
Se cree que muchos factores inducen una fragmentación del ADN, tales como apoptosis, radicales oxígeno, radioterapia y quimioterapia o agentes tóxicos medioambientales, etc.
El daño en el ADN del espermatozoide puede producirse durante la producción y/o el transporte de los gametos masculinos.
Durante la espermatogénesis los mecanismos de selección en las células de Sertoli son los responsables de la inducción de la apoptosis mediante el marcaje de espermatozoides individuales con marcadores apoptóticos que provocan la fagocitosis de estas células (Billig et al, 1 996, "Gondal cell apoptosis: hormone-regulated cell dermis", Hum. Reprod. Update 2, 103-117) . La actividad de nucleasa endógena testicular requerida para facilitar la protaminación aumenta adicionalmente el porcentaje de espermatozoides dañados en el ADN (McPherson et al,
1993, "Chromatin structure-function alternations during mammalian spermatogenesis: DNA nicking and repair in elongating spermatides", Eur. J. Histochem. 37, 109-128) .
Se está especulando que la fragmentación de ADN post-testicular que surge durante el transporte de espermatozoides a través del epidídimo es incluso más frecuente, ya que los espermatozoides testiculares muestran un menor nivel de daños en el ADN que los del epidídimo o los eyaculados.
Además, se sabe que los espermatozoides inmaduros (p. ej., que muestran retenciones citoplasmáticas) producen altos niveles de especies reactivas de oxígeno (ROS) y, dado que los espermatozoides están altamente empaquetados en el epidídimo, es muy probable que se produzca un daño de ADN asociado con ROS (ya sea directamente o a través de la activación de las caspasas) . Por término medio, se encontró que un incremento del 25% en el nivel de ROS seminal se correlacionaba con un incremento del 10% en la fragmentación del ADN.
Sin embargo, si los mecanismos testiculares y del epidídimo para la separación de espermatozoides genómicamente defectuosos no funcionan correctamente, un determinado porcentaje de las células germinales defectuosos terminará en la eyaculación presentando roturas de la cadena de ADN. La influencia de este tipo de problemas en el resultado reproductor sólo puede estimarse, ya que no se sabe en qué medida el ovocito puede compensar un factor paterno e incluso si un alto porcentaje de espermatozoides en el eyaculado puede tener ADN fragmentado, podría elegirse un espermatozoide no afectado para la inseminación artificial. Esta zona gris podría ser una de las razones para la discusión convencional sobre el posible efecto de roturas de la cadena de ADN de espermatozoides sobre un resultado adicional.
Un aspecto importante con respecto a la fragmentación de ADN de espermatozoides es la cuestión de si las roturas de la cadena de ADN son sencillas o dobles, ya que los defectos individuales son adecuadamente más fáciles de reparar en comparación con roturas del ADN de doble cadena. A este respecto debe tenerse en cuenta que el tratamiento de los espermatozoides tales como, p. ej., la centrifugación en gradiente de densidad, también podría provocar un incremento aparente de las roturas de la cadena de ADN, por lo tanto, es sumamente importante la técnica de procesamiento de espermatozoides aplicada para separar espermatozoides dañados en el ADN.
Se han desarrollado varios métodos para enriquecer espermatozoides sin rotura de la cadena de ADN, por ejemplo: la clasificación celular magnética utilizando microperlas de anexina-V puede separar efectivamente espermatozoides apoptóticos y no apoptóticos (Said et al, 2005, "Advantage of combining magnetic cell separation with sperm preparation techniques ", Reprod.
Biomed Online 10, 740-746) . Otro reducido porcentaje de espermatozoides con roturas de la cadena de ADN, ya sea la selección basada en la madurez, p. ej., según la evaluación de los sitios de unión de ácido hialurónico en la cabeza del espermatozoide (Parmegiani et al, 2010, "Physiologic ICSI: hyaluronic acid (HA) favors selection of spermatozoa without DNA fragmentation and with normal nucleus, resulting in improvement of embr y o quality, Fertil. Steril. 93, 598-604) o en un aumento mayor (Bartoov et al, 2003, "Pregnancy rates higher with intracytoplasmic morphologically selected sperm injection than with conventional intracytoplasmic injection" Fertil. Steril. 80, 14131419; Itzkan et al., 2007, "Confocal light adsorption and scattering spectroscopic microscopic monitors... [Seguir leyendo]
Reivindicaciones:
1. Método para producir una muestra enriquecida de espermatozoides sin roturas de la cadena de ADN, que comprende las siguientes etapas
(a) disponer un fluido seminal que comprende al menos 15% de oligo-, al menos 32% de asteno-y/o al menos 4% de terato-zoospermia, basado en la cantidad total de los espermatozoides en el fluido seminal en una primera cámara de un dispositivo de selección;
(b) llenar una segunda cámara del dispositivo de selección con un medio para recibir espermatozoides sin rotura de la cadena de ADN; y
(c) conectar ambas cámaras mediante un elemento de puente de tal manera que se forma un puente de fluido entre la primera y la segunda cámara que permite que los espermatozoides sin rotura de la cadena de ADN pasen de la primera a la segunda cámara.
2. El método de acuerdo con la reivindicación 1, caracterizado por que el fluido seminal comprende 5 a 95% de espermatozoides con rotura de la cadena de ADN, basado en la cantidad total de espermatozoides en el fluido seminal y determinado mediante el ensayo de SCD.
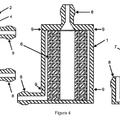
3. El método de acuerdo con las reivindicaciones 1 ó 2, caracterizado por que el fluido seminal de la primera cámara y el medio de la segunda cámara están separados por al menos una pared de las cámaras que tiene un borde superior, y en el que el elemento de puente que conecta ambas cámaras encierra el borde superior y una parte superior de dicha pared.
4. El método de acuerdo con una cualquiera de las reivindicaciones precedentes, caracterizado por que el puente de fluido entre las dos cámaras se genera mediante fuerzas capilares, de modo que el elemento de puente queda completamente saturado o se produce un contacto parcial con el fluido seminal de la primera cámara y el medio de la segunda cámara.
5. El método de acuerdo con una cualquiera de las reivindicaciones precedentes, caracterizado por que el elemento de puente tiene al menos un canal formado por paredes limitadoras que se extienden desde la primera cámara a la segunda cámara del dispositivo de selección.
6. El método de acuerdo con una cualquiera de las reivindicaciones precedentes, caracterizado por que la distancia entre las paredes limitadoras opuestas que forman un canal, o partes de dichas paredes limitadoras, se pre-definen de modo que las fuerzas capilares actúan sobre el medio con el que se llena el canal, de modo que el canal queda completamente saturado de manera independiente o se produce un contacto parcial con el medio.
7. El método de acuerdo con una cualquiera de las reivindicaciones precedentes, caracterizado por que la primera cámara es de forma anular y encierra a la segunda cámara.
8. El método de acuerdo con una cualquiera de las reivindicaciones precedentes, caracterizado por que el método se lleva a cabo en un período de tiempo de 20 a 120 minutos.
Patentes similares o relacionadas:
BIORREACTOR Y PROCEDIMIENTO DE PRODUCCIÓN DE CULTIVOS CELULARES ADHERENTES QUE EMPLEA EL BIORREACTOR, del 9 de Julio de 2020, de BIOTECH FOODS S.L: Biorreactor y procedimiento de producción de cultivos celulares adherentes que emplea el biorreactor. El biorreactor comprende un recipiente […]
Métodos para la recopilación, estabilización y conservación de muestras, del 8 de Julio de 2020, de Drawbridge Health, Inc: Un método para estabilizar uno o más componentes biológicos de una muestra biológica de un sujeto, comprendiendo el método obtener un […]
Dispositivo para la detección de analitos, del 1 de Julio de 2020, de TECHLAB, INC.: Un dispositivo para detectar por lo menos una sustancia de interés en una muestra líquida, comprendiendo el dispositivo: (a) una unidad que […]
Evaluación de embriones, del 27 de Mayo de 2020, de UNISENSE FERTILITECH A/S: Un método implementado por ordenador para clasificar embriones de FIV para predecir su potencial de desarrollo después de la transferencia; […]
Métodos para la transducción y el procesamiento de células, del 27 de Mayo de 2020, de Juno Therapeutics, Inc: Un método de transducción, que comprende incubar, en una cavidad interna de una cámara de centrífuga, una composición de entrada que comprende células y partículas […]
Un aparato para la incubación y vitrificación combinadas de un material biológico, del 6 de Mayo de 2020, de Esco Medical UAB: Un aparato para la incubación y vitrificación combinadas de un material biológico viable; dicho aparato comprende: una carcasa que tiene una extensión […]
Método y conjunto de electrodo para tratar células adherentes, del 29 de Abril de 2020, de Lonza Cologne GmbH: Procedimiento para someter células adherentes que se adhieren al fondo de un espacio de reacción, a por lo menos un campo eléctrico, en […]
 Biorreactor compuesto por cámara hermética al agua y matriz interna para la generación de implantes médicos con células, del 25 de Marzo de 2020, de Association for the Advancement of Tissue Engineering and Cell Based Technologies & Therapies (A4TEC) - Associação: Biorreactor para la generación de implantes médicos con células caracterizado porque comprende una cámara externa hermética al agua unicompartimentada […]
Biorreactor compuesto por cámara hermética al agua y matriz interna para la generación de implantes médicos con células, del 25 de Marzo de 2020, de Association for the Advancement of Tissue Engineering and Cell Based Technologies & Therapies (A4TEC) - Associação: Biorreactor para la generación de implantes médicos con células caracterizado porque comprende una cámara externa hermética al agua unicompartimentada […]