Dispositivo intraluminal implantable y procedimiento de uso del mismo en el tratamiento de aneurismas.
Un dispositivo intraluminal (2) que comprende:
un cuerpo tubular de malla que incluye una pluralidad de filamentos (3),
teniendo el cuerpo tubular de malla una configuración contraída de manera que el cuerpo tubular de malla es capaz de ser manipulado a través de una arteria (22) de un paciente, y una configuración expandida de manera que el cuerpo tubular de malla pueda ser colocado en contacto con una superficie interior de una arteria (22),
en el que dicha pluralidad de filamentos (3) definen una pluralidad de aberturas (7), teniendo cada una de dicha pluralidad de aberturas (7) una longitud de 50 a 400 μm en la configuración expandida, y
en el que cada uno de dicha pluralidad de filamentos (3) son de sección transversal circular y tienen un diámetro inferior a 60 μm.
Tipo: Patente Europea. Resumen de patente/invención. Número de Solicitud: E11185045.
Solicitante: STRYKER CORPORATION.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 2825 AIRVIEW BOULEVARD KALAMAZOO, MI 49002 ESTADOS UNIDOS DE AMERICA.
Inventor/es: YODFAT,OFER, LIEBER,BARUCH, GRAD,YGAEL, NISHRI,BOAZ.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61F2/06 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61F FILTROS IMPLANTABLES EN LOS VASOS SANGUINEOS; PROTESIS; DISPOSITIVOS QUE MANTIENEN LA LUZ O QUE EVITAN EL COLAPSO DE ESTRUCTURAS TUBULARES, p. ej. STENTS; DISPOSITIVOS DE ORTOPEDIA, CURA O PARA LA CONTRACEPCION; FOMENTACION; TRATAMIENTO O PROTECCION DE OJOS Y OIDOS; VENDAJES, APOSITOS O COMPRESAS ABSORBENTES; BOTIQUINES DE PRIMEROS AUXILIOS (prótesis dentales A61C). › A61F 2/00 Filtros implantables en los vasos sanguíneos; Prótesis, es decir, elementos de sustitución o de reemplazo para partes del cuerpo; Dispositivos para unirlas al cuerpo; Dispositivos para proporcionar permeabilidad o para evitar que colapsen las estructuras tubulares del cuerpo, p. ej. stents (como artículos cosméticos, ver las subclases apropiadas, p. ej. pelucas o postizos, A41G 3/00, A41G 5/00, uñas artificiales A45D 31/00; prótesis dentales A61C 13/00; materiales para prótesis A61L 27/00; riñones artificiales A61M 1/14; corazones artificiales A61M 60/00). › Vasos sanguíneos.
- A61F2/07 A61F 2/00 […] › Injertos stent.
- A61F2/82 A61F 2/00 […] › Dispositivos para mantener la luz o para evitar que se colapsen las estructuras tubulares del cuerpo, p. ej. stents (injertos stent para estructuras tubulares del cuerpo distintas de los vasos sanguíneos A61F 2/04; injertos stent para vasos sanguíneos A61F 2/07; instrumentos especialmente adaptados para la colocación o eliminación de stents o injertos stent A61F 2/95; para cerrar las heridas o para mantener las heridas cerradas A61B 17/03; dilatadores A61M 29/00).
- A61F2/90 A61F 2/00 […] › caracterizados por una estructura en forma de red o malla.
PDF original: ES-2530873_T3.pdf
Fragmento de la descripción:
Dispositivo intraluminal implantable y procedimiento de uso del mismo en el tratamiento de aneurismas Campo de la invención
La presente invención se refiere a dispositivos intraluminales implantables en un vaso sanguíneo para el tratamiento de aneurismas cerebrales.
Antecedentes de la invención
Una serie de publicaciones se enumeran al final de esta memoria para la información de fondo y están numéricamente referenciadas en el texto siguiente:
Los aneurismas intracraneales son la principal causa de hemorragias subaracnoideas no traumáticas y son responsables de alrededor del 25% de todas las muertes relacionadas con eventos cerebrovasculares. Los estudios de autopsias muestran que la frecuencia global de aneurismas intracraneales en la población general es de aproximadamente un 5 por ciento y sugieren que de 10 a 15 millones de personas en los Estados Unidos tienen o tendrán aneurismas intracraneales [1]. En aproximadamente 15.000 casos (6 casos por cada 100.000 personas por año), los aneurismas intracraneales se rompen cada año en América del Norte [2], La rotura de los aneurismas intracraneales conduce a una hemorragia subaracnoidea aneurismática (HSA), que tiene una tasa de mortalidad a 30 días del 45%, y resulta en aproximadamente en que la mitad de los supervivientes sufren un daño irreversible en el cerebro [1, 2],
El objetivo principal de los tratamientos para el aneurisma intracraneal es la prevención de la rotura de los aneurismas, evitando de este modo el sangrado o el resangrado. En la actualidad, existen tres métodos generales de tratamiento. Estos pueden ser agrupados de acuerdo a su enfoque: extravascular, endovascular y extra- endovascular.
El método extravascular implica la cirugía o microcirugía del aneurisma. Un procedimiento quirúrgico es la aplicación de un clip metálico o de una ligadura de sutura a través de la arteria que alimenta el aneurisma (cuello), permitiendo así que el aneurisma se coagule y que probablemente se encoja. Otro procedimiento quirúrgico es a "reconstrución quirúrgica" de la porción aneurismática de la arteria, mediante el recorte quirúrgico del aneurisma y la reparación del vaso mediante el uso de un injerto de vaso sintético o natural. Ambos de estos procedimientos quirúrgicos requieren típicamente anestesia general, craneotomla, retracción del cerebro y disección del aracnoide alrededor del cuello del aneurisma.
El tratamiento quirúrgico de aneurisma Intracraneal vascular se acompaña de una tasa de mortalidad del 3,8% y una tasa de morbilidad del 10,9% [3], Debido a las altas tasas de mortalidad y de morbilidad, y porque la condición de muchos pacientes no les permite someterse a una operación abierta, el procedimiento quirúrgico a menudo se retrasa o no se practica. Por esta razón, la técnica anterior ha buscado medios alternativos de tratamiento.
El desarrollo de microcatéteres ha hecho posible el uso de procedimientos endovasculares (basados en catéteres). La principal ventaja de los procedimientos endovasculares es que no requieren el uso de cirugía abierta. Por lo general, son más beneficiosos y tienen unas tasas de mortalidad y de morbilidad mucho más bajas que los procedimientos extravasculares.
Existen muchas variaciones de los procedimientos endovasculares, y algunos de los más importantes son los siguientes:
1. Colocación de material embólico, tal como microespiras metálicas o cuentas esféricas, en el interior del saco del aneurisma para formar una masa dentro de este saco que reducirá el flujo sanguíneo y generalmente fomentará que el aneurisma se coagule y se encoja. Para llevar a cabo este procedimiento, un microcatéter se guía a través de las arterias cerebrales hasta alcanzar el sitio del aneurisma. La punta distal del microcatéter se coloca a continuación dentro del saco del aneurisma, y el material embólico se inyecta en el saco del aneurisma. Microcatéteres típicos adecuados para este procedimiento se divulgan en las patentes US Nos. 5.853.418; 6.066.133; 6.165.198 y 6.168.592.
La experiencia generalizada y larga con esta técnica ha demostrado varios riesgos y limitaciones. El método tiene un 4% de tasa de morbilidad y un 1% de tasa de mortalidad y logra la oclusión completa del aneurisma en sólo un 52% a un 78% de los casos en los que se emplea. La tasa de éxito relativamente baja se debe a limitaciones técnicas (por ejemplo, flexibilidad, forma y dimensiones de la espira) que impiden el empaquetado hermético del saco del aneurisma, especialmente aneurismas con cuellos anchos [3], Otras dificultades están asociadas con la presencia de trombos preexistentes dentro de la cavidad del aneurisma, lo que puede ser cortado en el tronco principal, provocando la oclusión de la arteria principal. También puede producirse la perforación del aneurisma durante la colocación de las espiras en el aneurisma. Además, la aparición de movimiento de la espira y la compactaclón pueden favorecer a la revascularización o al crecimiento del aneurisma.
2. Otra técnica endovascular para el tratamiento de aneurismas implica la Inserción de un globo amovible en el saco del aneurisma usando un microcatéter. El globo amovible se infla a continuación utilizando material embólico, tal como un material de polímero liquido o microespiras. El globo se separa a continuación del microcatéter y se deja dentro del saco del aneurisma en un intento de llenar el saco y formar una masa trombótica en el interior del aneurisma.
Una de las desventajas de este método es que los globos amovibles, cuando se inflan, típicamente no se ajustan a la configuración interior del saco aneurlsmátlco. En su lugar, el saco del aneurisma se ve obligado a conformarse a la superficie exterior del globo amovible. Por lo tanto, existe un riesgo mayor de que el balón amovible rompa el saco del aneurisma.
3. Tecnología de stents se ha aplicado a la vasculatura intracraneal. El uso de esta tecnología ha sido limitada hasta hace poco por la falta de stents disponibles y sistemas de suministro de stents capaces de una navegación segura y eficaz a través de los vasos intercraneales. Ejemplos de stents conocidos se describen en los documentos US-A-4.655.771 y WO 99/02092 A, asi como en el documento WO 03/006097 A, que es una citación solamente para novedad a tenor del articulo 54 (3) CPE. El uso de tales stents es particularmente difícil respecto a aneurismas en los vasos sanguíneos de la cabeza debido al número de vasos perforantes en estos vasos sanguíneos, y con ello, el aumento del peligro de que uno o más vasos perforantes puedan estar en la proximidad de dicho aneurisma. Lo mismo es cierto respecto a las bifurcaciones de una división de vasos sanguíneos en uno o más vasos ramificados, que también pueden estar en la proximidad de un aneurisma. Cuando el suministro de sangre hacia un aneurisma se reduce, es critico que el suministro de sangre a estos vasos perforantes o vasos ramificados, en la proximidad del aneurisma no se reduzca de forma excesiva hasta el grado de causar daños a los tejidos Irrigados con sangre mediante tales vasos perforantes o ramificados.
Por lo tanto, existe un serio peligro de que la colocación de un stent endovascular convencional dentro de la arteria principal a través del cuello del aneurisma reduzca el flujo sanguíneo al aneurisma, para promover estatis en la estasis y trombosis [4,5],
Stents que tienen porciones de diferentes permeabilidades se describen, por ejemplo, en la patente US 5.951.599 de McCrory, la patente US 6.093.199 de Brown y otros, la patente US 4.954.126 de Wallsten, la patente US 6.258.115 de Dubrul, y la publicación Internacional N° WO 03/006097.
La patente de McCrory describe un stent trenzado que tiene una primera porción con un Indice de porosidad relativamente alto para ser muy permeable al flujo sanguíneo, y una segunda porción de menor Indice de porosidad para que sea menos permeable al flujo sanguíneo. Cuando el stent se despliega, la porción de baja permeabilidad está situada para recubrir el cuello del aneurisma, y la porción de alta permeabilidad está separada del cuello del aneurisma. Una construcción de stent trenzado con diferentes porosidades también se divulga en la patente de Dubrul.
Brown y otros, por otra parte, divulga un dispositivo ¡ntraluminal o stent que comprende un desviador, en forma de una almohadilla de espuma de baja permeabilidad, para recubrir el cuello del aneurisma, a horcajadas en sus lados opuestos mediante un par de elementos de espira de alta permeabilidad para el anclaje del dispositivo en el vaso
sanguíneo.
La patente US 4.954.126 de Wallsten divulga un dispositivo ¡ntraluminal tubular trenzado para su uso en varias aplicaciones, una de cuyas aplicaciones es... [Seguir leyendo]
Reivindicaciones:
1. Un dispositivo intraluminal (2) que comprende:
un cuerpo tubular de malla que incluye una pluralidad de filamentos (3), teniendo el cuerpo tubular de malla una configuración contraída de manera que el cuerpo tubular de malla es capaz de ser manipulado a través de una arteria (22) de un paciente, y una configuración expandida de manera que el cuerpo tubular de malla pueda ser colocado en contacto con una superficie interior de una arteria (22), en el que dicha pluralidad de filamentos (3) definen una pluralidad de aberturas (7), teniendo cada una de dicha pluralidad de aberturas (7) una longitud de 50 a 400 pm en la configuración expandida,
y
en el que cada uno de dicha pluralidad de filamentos (3) son de sección transversal circular y tienen un diámetro inferior a 60 pm.
2.-. El dispositivo intraluminal (2) de la reivindicación 1,
en el que la pluralidad de filamentos (3) se extienden hellcoldalmente de una manera entrelazada en direcciones opuestas para formar un tubo trenzado.
3.- El dispositivo intraluminal (2) de la reivindicación 1 o 2,
en el que cada una de dicha pluralidad de aberturas (7) tiene una longitud de 80 a 300 pm en la configuración expandida y/o cuando es desplegado dentro de la arteria (22) de tamaño apropiado.
4.- El dispositivo intraluminal (2) de cualquiera de las reivindicaciones anteriores,
en el que el dispositivo intraluminal (2) incluye múltiples cuerpos tubulares de malla en una formación a modo de capas
5.- El dispositivo intraluminal (2) de cualquiera de las reivindicaciones anteriores,
en el que al menos algunos de dichos filamentos (3) incluyen una rugosidad a microescala configurada para controlar el crecimiento neointimal.
6. El dispositivo intraluminal (2) de las reivindicaciones 1 o 2,
en el que cada uno de dicha pluralidad de aberturas (7) tiene un diámetro inscrito de 30 a 480 pm en la configuración expandida y/o cuando es desplegado dentro de la arteria (22) de tamaño apropiado.
7. El dispositivo intraluminal (2) de las reivindicaciones 1 o 2,
en el que cada una de dicha pluralidad de aberturas (7) tiene un diámetro inscrito de 50 a 320 pm en la configuración expandida y/o cuando es desplegado dentro de la arteria (22) de tamaño apropiado.
8. El dispositivo intraluminal (2) de las reivindicaciones 1 o 2, en el que dicho cuerpo tubular de malla está formado trenzando de 24 a 144 filamentos (3) o de 62 a 120 filamentos (3).
9. El dispositivo intraluminal (2) de la reivindicaciones 1 o 2,
en el que dicho cuerpo tubular de malla tiene una longitud de 5 a 60 mm cuando es desplegado dentro de la arteria (22) de tamaño apropiado.
10. El dispositivo intraluminal (2) de las reivindicaciones 1 o 2,
en el que al menos la mayoría de dichos filamentos (3) son de sección transversal circular y tienen un diámetro de 10 a 60 pm o de 20 a 40 pm.
11. El dispositivo intraluminal (2) de las reivindicaciones 1 o 2,
en el que al menos una primera porción de dicha pluralidad de filamentos (3) comprende un primer material biocompatible y una segunda porción de dicha pluralidad de filamentos (3) comprende un segundo material biocompatible diferente de dicho primer material biocompatible.
12. El dispositivo intraluminal (2) de las reivindicaciones 1 o 2,
en el que al menos una porción de dicha pluralidad de filamentos (3) es radio-opaca.
13. El dispositivo intraluminal (2) de las reivindicaciones 1 o 2,
en el que dicha pluralidad de filamentos (3) comprende un material biocompatible seleccionado a partir del grupo que consiste en: acero inoxidable, tantalio, cobalto, Nitinol y polímeros.
14. El dispositivo intraluminal (2) de las reivindicaciones 1 o 2,
en el que al menos un filamento de dicha pluralidad de filamentos (3) incluye una combinación de varios materiales biocompatibles.
15. El dispositivo intraluminal (2) de las reivindicaciones 1 o 2,
en el que al menos una primera porción de dicha pluralidad de filamentos (3) es de sección transversal circular y dicha primera porción de dicha pluralidad de filamentos (3) tiene un primer diámetro, y una segunda porción de dicha
pluralidad de filamentos (3) es de sección transversal circular y dicha segunda porción de dicha pluralidad de filamentos (3) tiene un segundo diámetro diferente de dicho primer diámetro.
Patentes similares o relacionadas:
 Procedimiento y dispositivo para producir un objeto multicelular tridimensional, del 29 de Julio de 2020, de TECHNISCHE UNIVERSITAT BERLIN: Procedimiento para producir un objeto multicelular tridimensional, con los pasos siguientes:
a) introducción de un primer líquido fotopolimerizable […]
Procedimiento y dispositivo para producir un objeto multicelular tridimensional, del 29 de Julio de 2020, de TECHNISCHE UNIVERSITAT BERLIN: Procedimiento para producir un objeto multicelular tridimensional, con los pasos siguientes:
a) introducción de un primer líquido fotopolimerizable […]
Tapón de catéter extraíble y aplicaciones del mismo, del 3 de Junio de 2020, de Pristine Access Technologies Ltd: Tapón de catéter extraíble , que comprende: un cuerpo de tapón configurado para […]
Dispositivos de cierre automático, del 29 de Abril de 2020, de Solinas Medical Inc: Un puerto de acceso que se puede unir a una superficie dentro del cuerpo de un paciente, que comprende: un cuerpo del puerto que comprende un material […]
Dispositivo para el tratamiento del aneurisma de aorta, del 21 de Abril de 2020, de SERVICIO ANDALUZ DE SALUD: Dispositivo para el tratamiento del aneurisma de aorta. La invención describe un dispositivo para el tratamiento del aneurisma de aorta que comprende: un estent exterior […]
Endoprótesis y dispositivo de colocación para implantar tal endoprótesis, del 15 de Abril de 2020, de Kardiozis: Stent vascular o stent cardiaco que comprende al menos una parte de cuerpo, en el que están dispuestos elementos trombogénicos al menos […]
Dispositivos para tratar la vasculatura de la extremidad inferior, del 12 de Febrero de 2020, de LimFlow GmbH: Un sistema de prótesis implantable para tratar una oclusión en un primer vaso, el sistema de prótesis comprende: un estent (100, 134, 140, 150, 160, 200, 220, […]
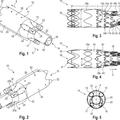 Prótesis vascular autoexpandible, del 29 de Enero de 2020, de JOTEC GMBH: Prótesis vascular autoexpandible para la implantación en un vaso sanguíneo de un paciente, con un cuerpo de base cilíndrico hueco , así […]
Prótesis vascular autoexpandible, del 29 de Enero de 2020, de JOTEC GMBH: Prótesis vascular autoexpandible para la implantación en un vaso sanguíneo de un paciente, con un cuerpo de base cilíndrico hueco , así […]
Dispositivo de protección de microválvula, del 22 de Enero de 2020, de Surefire Medical, Inc: Un dispositivo endovascular para reducir el reflujo de un agente de embolización en un vaso durante un procedimiento de terapia de embolización, comprendiendo […]