Procedimiento para la preparación de dióxido de titanio que tiene dimensiones nanométricas y forma controlada.
Procedimiento para la preparación de partículas de TiO2 nanocristalinas de forma controlada,
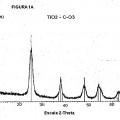
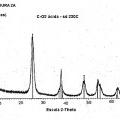
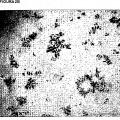
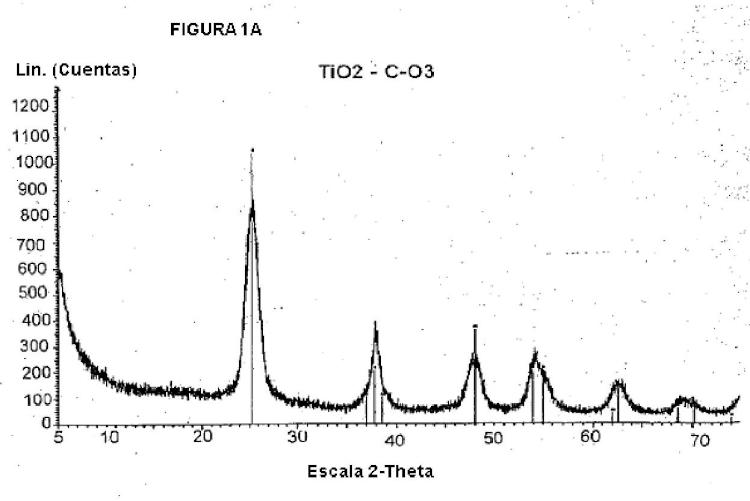
principalmente en forma de anatasa, en el que al menos el 50% en peso de dichas partículas de TiO2 tienen forma de nanovarilla o nanocubo, que comprende la reacción de un precursor de dióxido de titanio con un éster, agua y opcionalmente un alcohol, en el que el precursor es tetraisopropóxido de titanio, el éster es acetato de butilo, en el que el butilo es lineal o ramificado, o acetato de bencilo, y el alcohol, cuando está presente, es alcohol bencílico.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP2010/004316.
Solicitante: Daunia Solar Cell S.r.l.
Nacionalidad solicitante: Italia.
Dirección: Strada Statale, 16, S.S. 16 Zona Industriale Incoronata 71100 Foggia ITALIA.
Inventor/es: MATTEUCCI,FRANCESCO, CICCARELLA,GIUSEPPE, ZAMA,ISABELLA, MARTELLI,CHRISTIAN.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- B82Y30/00 TECNICAS INDUSTRIALES DIVERSAS; TRANSPORTES. › B82 NANOTECNOLOGIA. › B82Y USOS O APLICACIONES ESPECIFICOS DE NANOESTRUCTURAS; MEDIDA O ANALISIS DE NANOESTRUCTURAS; FABRICACION O TRATAMIENTO DE NANOESTRUCTURAS. › Nano tecnología para materiales o ciencia superficial, p.ej. nano compuestos.
- C01G23/047 QUIMICA; METALURGIA. › C01 QUIMICA INORGANICA. › C01G COMPUESTOS QUE CONTIENEN METALES NO CUBIERTOS POR LAS SUBCLASES C01D O C01F (hidruros metálicos C01B 6/00; sales de oxácidos de halógenos C01B 11/00; peróxidos, sales de los perácidos C01B 15/00; tiosulfatos, ditionitos, politionatos C01B 17/64; compuestos que contienen selenio o teluro C01B 19/00; compuestos binarios del nitrógeno con metales C01B 21/06; azidas C01B 21/08; amidas metálicas C01B 21/092; nitritos C01B 21/50; fosfuros C01B 25/08; sales de los oxácidos del fósforo C01B 25/16; carburos C01B 32/90; compuestos que contienen silicio C01B 33/00; compuestos que contienen boro C01B 35/00; compuestos que tienen propiedades de tamices moleculares pero que no tienen propiedades de cambiadores de base C01B 37/00; compuestos que tienen propiedades de tamices moleculares y de cambiadores de base, p. ej. zeolitas cristalinas, C01B 39/00; cianuros C01C 3/08; sales del ácido ciánico C01C 3/14; sales de cianamida C01C 3/16; tiocianatos C01C 3/20; procesos de fermentación o procesos que utilizan enzimas para la preparación de elementos o de compuestos inorgánicos excepto anhídrido carbónico C12P 3/00; obtención a partir de mezclas, p. ej. a partir de minerales, de compuestos metálicos que son los compuestos intermedios de un proceso metalúrgico para la obtención de un metal libre C21B, C22B; producción de elementos no metálicos o de compuestos inorgánicos por electrólisis o electroforesis C25B). › C01G 23/00 Compuestos de titanio. › Dióxido de titanio.
- C25B1/00 C […] › C25 PROCESOS ELECTROLITICOS O ELECTROFORETICOS; SUS APARATOS. › C25B PROCESOS ELECTROLITICOS O ELECTROFORETICOS PARA LA PRODUCCION DE COMPUESTOS ORGANICOS O INORGANICOS, O DE NO METALES; SUS APARATOS (protección anódica o catódica C23F 13/00; crecimiento de monocristales C30B). › Producción electrolítica de compuestos inorgánicos o no metales.
PDF original: ES-2552699_T3.pdf

Patentes similares o relacionadas:
Método de producción de grafeno mediante erosión electroquímica de electrodos de grafito, del 29 de Julio de 2020, de CAMBRIDGE ENTERPRISE LIMITED: Un método de producción de láminas de grafeno que comprende las etapas de: (a) formar un polvo carbonoso mediante erosión electroquímica de un electrodo […]
Un proceso para producir CO a partir de CO2 en una célula de electrolisis de óxido sólido, del 22 de Julio de 2020, de HALDOR TOPS E A/S: Un proceso para producir monóxido de carbono (CO) a partir de dióxido de carbono (CO2) en una pila de células de electrolisis de óxido sólido (SOEC), en el que se conduce […]
Generador de gas antiexplosión para uso sanitario, del 24 de Junio de 2020, de Lin, Hsin-Yung: Un generador de gas antiexplosión para uso sanitario que comprende un dispositivo de electrólisis para electrolizar agua para producir un gas que comprende hidrógeno, […]
Un proceso para la producción segura de fosgeno, del 27 de Mayo de 2020, de HALDOR TOPS E A/S: Un proceso para la producción de fosgeno (COCl2) a partir de monóxido de carbono y cloro según el esquema de reacción CO (g) + Cl2 (g) → COCl2 (g) […]
Producción de combustible usando energía solar, del 13 de Mayo de 2020, de Sunthetics AB: Un método para producir un producto de combustible, que comprende: suministrar electricidad, generada en una disposición de células fotovoltaicas y un motor de […]
Dispositivo y procedimiento de producción de gas de síntesis, del 6 de Mayo de 2020, de Engie: Dispositivo de producción de gas natural sintético, caracterizado por que comprende: - un medio de coelectrólisis a alta temperatura […]
Dispositivo y procedimiento de producción de gas de síntesis, del 29 de Abril de 2020, de Engie: Dispositivo de producción de gas de síntesis, caracterizado por que comprende: - un medio de electrólisis de agua para producir dioxígeno […]
Procedimiento y sistema de electrólisis para el aprovechamiento de dióxido de carbono, del 1 de Abril de 2020, de SIEMENS AKTIENGESELLSCHAFT: Procedimiento para el aprovechamiento de dioxido de carbono por medio de un sistema de electrolisis, - en el que un electrolito y dioxido de carbono (CO2) se conducen por […]