Métodos para el tratamiento de tumores sólidos.
Un compuesto de fórmula I ópticamente activo**Fórmula**
una sal farmacéuticamente aceptable del mismo,
o una composición farmacéutica que comprende un compuesto ópticamente activo de fórmula I o una sal farmacéuticamente aceptable del mismo; para uso en un método de tratamiento de un tumor sólido en un sujeto.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2010/031794.
Solicitante: Gilead Calistoga LLC.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 333 Lakeside Drive Foster City. CA 94404 ESTADOS UNIDOS DE AMERICA.
Inventor/es: GIESE, NEILL A., PURI,KAMAL D, EVARTS,JERRY B, LANNUTTI,BRIAN.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K31/517 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › condensadas en orto o en peri con sistemas carbocíclicos, p. ej. quinazolina, perimidina.
- A61K31/519 A61K 31/00 […] › condensadas en orto o en peri con heterociclos.
- A61P35/00 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › Agentes antineoplásicos.
- A61P37/00 A61P […] › Medicamentos para el tratamiento de problemas inmunológicos o alérgicos.
PDF original: ES-2548253_T3.pdf


Fragmento de la descripción:
Métodos para el tratamiento de tumores sólidos Referencia cruzada a solicitudes relacionadas
Esta solicitud reivindica la prioridad de la solicitud de patente provisional en Estados Unidos N° 61/171.047 presentada el 20 de abril de 2009.
Campo técnico
La invención se sitúa en el campo de los agentes terapéuticos y la química médica. En particular, la invención concierne a métodos para el tratamiento de determinados tumores sólidos que incluyen la administración de determinados derivados de quinazolinona.
Técnica anterior
La señalización celular por medio de fosfoinositidas 3-fosforiladas se ha implicado en varios procesos celulares, por ejemplo, la transformación maligna, la señalización del factor de crecimiento, la inflamación, y la inmunidad. La enzima responsable de generar estos productos de señalización fosforilados, la fosfatidilinositol 3-quinasa (PI3- quinasa; PI3K), se identificó originalmente como una actividad asociada a oncoproteínas virales y a tirosina quinasas receptoras del factor de crecimiento que fosforila el fosfatidilinositol (Pl) y sus derivados fosforilados en el 3-hidroxilo del anillo de inositol.
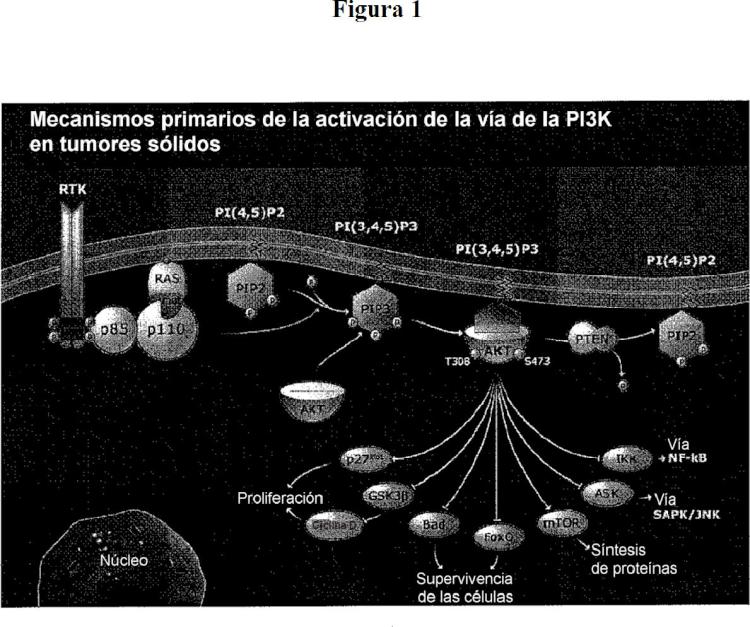
La activación de la PI3-quinasa, se cree que está implicada en una serie de respuestas celulares que incluyen el crecimiento, la diferenciación y la apóptosis celular. La Figura 1 muestra algunas vías celulares mediante las cuales la PI3K (representada por p110 y p5) participa en la activación de los tumores sólidos.
La purificación inicial y la clonación molecular de la PI3-quinasa revelaron que era un heterodímero que consiste en las subunidades p85 y p110. Se han identificado cuatro PI3K de Clase I distintas, designadas como PI3K a, (3, ó, y y, consistiendo cada una en una subunidad catalítica p110 distinta y una subunidad reguladora. Más específicamente, tres de las subunidades catalíticas, es decir, la p110a, la p110(3 y la p1105, interactúan cada una con la misma subunidad reguladora, la p85; mientras que la p110y interactúa con una subunidad reguladora distinta, la p101. Los patrones de expresión de cada una de estas PI3K en células y tejidos humanos son también distintos.
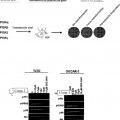
La identificación de la isoforma p110ó de la PI3-quinasa se describe en Chantry et al., J. Biol. Chem., 272:19236-41 (1997). Se observó que la isoforma p110ó humana se expresa en un modo restringido al tejido. Se expresa a elevados niveles en linfocitos y tejidos linfoides, sugiriendo que la proteína podría desempeñar un papel en la señalización mediada por la PI3-quinasa en el sistema inmune. La isoforma p110(3 de la PI3K puede desempeñar un papel en la señalización mediada por la PI3K en ciertos cánceres. La Figura 2 ilustra las cantidades relativas de estas isoformas de la p110 en una serie de diferentes líneas celulares cancerosas. Algunos tumores sólidos exhiben muy poco o nada de la p110a, y muchos tienen bajos niveles de la p110ó, pero todos los ensayados mostraban niveles significativos de la p110p.
Existe la necesidad de un tratamiento de los trastornos mediados por la PI3K relacionados con cánceres, enfermedades inflamatorias, y enfermedades autoinmunes. Se han descrito compuestos de quinazolinona como generalmente útiles para el tratamiento de cánceres principalmente hematológicos que expresan niveles relativamente elevados de la p110ó, ya que las quinazolinonas son más activas como inhibidores de la p1105. Otros inhibidores de la PI3K están en desarrollo para el tratamiento de tumores sólidos, pero parece que son inhibidores no selectivos de varias isoformas de la p110, o inhibidores principalmente de la p110a. Por ejemplo, el XL-147 inhibe la p110a y la p110ó y la p110y con similares CI50 de acuerdo con Exelixis, y tiene un actividad 10 veces menor sobre la p110(3; el BEZ235 se describe como un inhibidor de la pan-PI3K que también actúa sobre la mTOR; y el GDC-0941 se describe como un inhibidor de la p110a. Los inhibidores con menor selectividad, o con mayores niveles de actividad p110a, cabría esperar que tuvieran actividades inespecíficas; la p110a, por ejemplo, está implicada en la regulación de la glucosa y los niveles de insulina. La presente invención proporciona un isómero específico de un compuesto de quinazolinona que es particularmente útil para el tratamiento de tumores sólidos. Aunque es más activo sobre la p110ó que sobre las otras isoformas de la PI3K, la capacidad de este compuesto para tratar tumores sólidos se cree que se debe a su actividad relativamente elevada como inhibidor de la p110p combinada con un alto nivel de biodisponibilidad oral, y exhibe niveles relativamente bajos de actividad funcional frente a la p110a.
Sumario
La invención proporciona un compuesto de fórmula (I) para su uso en nuevos métodos para tratar determinados tumores sólidos. En un aspecto, la invención proporciona un compuesto de fórmula I ópticamente activo para su uso en un método para el tratamiento del cáncer en un sujeto que comprende administrar a dicho sujeto un compuesto
de fórmula I ópticamente activo:
**(Ver fórmula)**o una sal farmacéuticamente aceptable del mismo. El compuesto ópticamente activo es predominantemente el isómero S mostrado en el presente documento, si bien puede contener como componente minoritario cierta proporción del enantiómero R. Preferentemente el compuesto para su uso en los métodos de la invención consiste fundamentalmente en el isómero S como se discutirá más adelante en el presente documento.
El compuesto para su uso en los métodos de la invención se puede administrar mediante diversas vías de administración, si bien, preferentemente, el compuesto se administra por vía oral.
El sujeto puede ser cualquier mamífero; en realizaciones preferidas el sujeto es un humano.
Sin desear quedar ligado a teoría alguna, la actividad antitumoral de este compuesto se cree que resulta de su inhibición de la p110(5 más que de la inhibición de la p1105 o la p110a. Exhibió actividad en varias líneas celulares cancerosas que expresaban muy poco la p1105, y algunas que no expresaban cantidades significativas de la p110a; pero todas las líneas celulares ensayadas expresaban la p110f>.
Asimismo, el Compuesto I exhibió una actividad funcional comparativamente baja sobre la p110a en un sistema de transformación celular diseñado para medir la actividad funcional de estas quinasas, si bien es un potente inhibidor tanto de la p110p como de la p1105 en ese ensayo. Véase el ejemplo 1. Se ha comunicado que este sistema de transformación de fibroblastos de embrión de pollo (FEP) es un modo útil para evaluar la actividad funcional de la vía de señalización de la PI3K. Denley, et al., "Oncogenic signaling of class I PI3K isoforms," Oncogene, vol. 27(18), 2561-74 (2008). La transformación de las células FEP en el ensayo depende de la actividad quinasa funcional. Kang, et al., Proc. Nafl Acad. Sci. EE.UU., vol. 103(5), 1289-94 (2006). Análogamente en otros ensayos funcionales basados en células, el Compuesto I es el más activo sobre la p1105 y la p110p, con una actividad relativamente menor frente a la p110a.
Tal y como ilustra la Figura 4, el Compuesto I a una concentración 10 micromolar inhibe la fosforilación de la Akt, que es un mediador corriente abajo de la activación de la PI3K (Véase la Figura 1), en dos líneas celulares cancerosas, la T47D (cáncer de mama) y la OVCAR-3 (cáncer de ovario). Es significativo también que la T47D tiene una mutación que activa la p110a, aunque no reduce significativamente el efecto del Compuesto I frente a esta línea celular, sugiriendo además que la actividad antitumoral de este compuesto debe residir en su efecto sobre otras isoformas más que sobre la p110a. Esto distingue al Compuesto I de otros inhibidores conocidos de la PI3K en desarrollo para el tratamiento de tumores sólidos, que se cree actúa fundamentalmente sobre la isoforma p110a o sobre la p110a más otras isoformas, o incluso sobre todas las PI3K más la mTOR.
El Compuesto I es útil para tratar determinados cánceres. En algunas realizaciones el cáncer es un cáncer no hematopoyético. En algunas realizaciones, el cáncer es un tumor sólido seleccionado de entre el cáncer pancreático; el cáncer de vejiga; el cáncer colorrectal; el cáncer de mama; el cáncer de próstata; el cáncer renal; el cáncer hepatocelular; el cáncer de pulmón; el cáncer de ovario; el cáncer de cuello uterino; el cáncer gástrico; el cáncer de esófago; el cáncer de cabeza y cuello; el melanoma; cánceres neuroendocrinos; cánceres del SNC; tumores cerebrales; el cáncer óseo; y el sarcoma de los tejidos blandos. En algunas realizaciones es el cáncer de pulmón (el carcinoma no microcítico de pulmón, el carcinoma microcítico de pulmón),... [Seguir leyendo]
Reivindicaciones:
1. Un compuesto de fórmula I ópticamente activo
**(Ver fórmula)**una sal farmacéuticamente aceptable del mismo, o una composición farmacéutica que comprende un compuesto ópticamente activo de fórmula I o una sal farmacéuticamente aceptable del mismo; para uso en un método de tratamiento de un tumor sólido en un sujeto.
2. El compuesto para uso de la reivindicación 1, en donde el tumor sólido se selecciona de entre el grupo que consiste en cáncer pancreático; cáncer de vejiga; cáncer colorrectal; cáncer de mama; cáncer de próstata; cáncer renal; cáncer hepatocelular; cáncer de pulmón; cáncer de ovario; cáncer de cuello uterino; cáncer gástrico; cáncer de esófago; cáncer de cabeza y cuello; melanoma; cánceres neuroendocrinos; cánceres del SNC; tumores cerebrales; cáncer óseo; y sarcoma de los tejidos blandos, o en donde el tumor sólido se selecciona de entre cáncer no microcítico de pulmón, cáncer microcítico de pulmón, cáncer de colon, cáncer del SNC, melanoma, cáncer de ovario, cáncer renal, cáncer de próstata y cáncer de mama.
3. El compuesto para uso de la reivindicación 1, en el que el enantiómero S predomina sobre el enantiómero R en una relación de al menos aproximadamente 9:1 y preferentemente en el que el enantiómero S predomina sobre el enantiómero R en una relación de al menos aproximadamente 19:1.
4. El compuesto para uso de cualquiera de las reivindicaciones 1-3, en donde el compuesto es para administración al sujeto por vía oral, por vía intravenosa o mediante inhalación, y preferentemente en donde el compuesto es para administración al sujeto en forma sólida.
5. El compuesto para uso de la reivindicación 4, en el que la forma sólida comprende el compuesto de fórmula I ópticamente activo mezclado con al menos un excipiente farmacéuticamente aceptable.
6. El compuesto para uso de la reivindicación 5, en donde el tumor sólido es cáncer de ovario, renal, de mama, de pulmón, de colon o de próstata.
7. El compuesto para uso de cualquiera de las reivindicaciones 1-3, en dondeel sujeto no responde al tratamiento de quimioterapia o sufre una recaída tras el tratamiento de quimioterapia.
8. El compuesto para uso de cualquiera de las reivindicaciones 1-3, en donde el compuesto de fórmula I es para su administración a una dosis de 20-500 mg/día, o preferentemente a una dosis de 50-250 mg/día, o más preferentemente a una dosis de 50-150 mg dos veces al día.
9. El compuesto para uso de cualquiera de las reivindicaciones 1-3, en donde un compuesto de fórmula I es para administración al menos dos veces al día.
10. El compuesto para uso de cualquiera de las reivindicaciones 1-3, en donde el sujeto es un sujeto humano.
11. El compuesto para uso de la reivindicación 10, en donde la concentración del compuesto en la sangre es entre 40-3000 ng/ml durante un periodo de 12 horas desde el momento de la administración.
12. El compuesto para uso de la reivindicación 10, en donde la concentración del compuesto en la sangre es entre aproximadamente 100 nM y 2000 nM en el sujeto tratado.
13. El compuesto para uso de cualquiera de las reivindicaciones 1-3, en donde el método de tratamiento comprende adicionalmente administrar además de un compuesto de fórmula I a dicho sujeto una cantidad terapéuticamente eficaz de al menos un agente terapéutico y/o un procedimiento terapéutico seleccionado para tratar dicho cáncer en dicho paciente, y en donde dicho agente terapéutico se selecciona preferentemente de entre el grupo siguiente que
consiste en docetaxel, mitoxantrona, prednisona, estramustina, antraciclinas, (doxorubicina (Adriamycin), epirubicina (Ellence), y doxorubicina liposómica (Doxil), taxanos (docetaxel (Taxotere), paclitaxel (Taxol), y paclitaxel unido a proteínas (Abraxane), ciclofosfamida (Cytoxan), capecitabina (Xeloda) y 5 fluorouracilo (5 FU), gemcitabina (Gemzar), metotrexato, vinorelbina (Navelbine), un inhibidor del RFCE tal como erlotinib, trastuzumab, Herceptin, Avastin, platinos (cisplatino, carboplatino), temazolamida, interferón alfa, e IL-2, o en donde dicho agente terapéutico se selecciona de entre el grupo que consiste en un inhibidor del RFCE, un inhibidor de la mTOR, un platino y un taxano.
14. El compuesto para uso de la reivindicación 13, en donde dicho procedimiento terapéutico se selecciona de entre el grupo que consiste en trasplante de células madre de sangre periférica, trasplante autólogo de células madre hematopoyéticas, trasplante autólogo de médula ósea, terapia con anticuerpos, terapia biológica, terapia con inhibidores de enzimas, irradiación total del cuerpo, infusión de células madre, ablación de médula ósea con apoyo de células madre, trasplante de células madre de sangre periférica tratadas in vitro, trasplante de sangre de cordón umbilical, técnica inmunoenzimática, compuesto de tinción inmunohistoquímica, estudio farmacológico, terapia de rayos gamma con cobalto 60 de baja TLE, bleomicina, cirugía convencional, radioterapia, quimioterapia de dosis alta y trasplante alogénico no mieloablativo de células madre hematopoyéticas.
15. El compuesto para uso de cualquiera de las reivindicaciones 1-3, que comprende además obtener una muestra biológica de dicho sujeto; y analizar dicha muestra biológica con un procedimiento analítico seleccionado de entre el grupo que consiste en análisis químico de la sangre, análisis de translocaciones cromosómicas, biopsia con aguja, hibridación fluorescente in situ, análisis con biomarcadores de laboratorio, compuesto de tinción inmunohistoquímica, citometría de flujo o una combinación de los mismos, en donde el compuesto es preferentemente para su administración a dicho sujeto dos veces al día durante aproximadamente 28 días y después se deja de administrar durante al menos 7 días.
Patentes similares o relacionadas:
Formas cristalinas de 6-((6,7-dimetoxiquinazolin-4-il)oxi)-N,2-dimetilbenzofuran-3-carboxamida, del 29 de Julio de 2020, de Hutchison Medipharma Limited: Forma I de 6-((6,7-dimetoxiquinazolin-4-il)oxi)-N,2-dimetilbenzofuran-3-carboxamida, en donde el difractograma de rayos X de polvo de la Forma […]
Compuestos y procedimientos de uso, del 29 de Julio de 2020, de Medivation Technologies LLC: Un compuesto de fórmula (Aa-1): **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en la que: A representa H, halógeno, amino, […]
Complejos de agentes terapéuticos de base vírica y poli(beta-amino-ésteres) modificados, del 29 de Julio de 2020, de Sagetis Biotech, SL: Un complejo de un agente terapéutico de base vírica con un polímero de fórmula I: **(Ver fórmula)** donde cada L1 y L2 están seleccionados […]
Compuestos de alquinilbenceno heterocíclicos, y composiciones médicas y usos de los mismos, del 29 de Julio de 2020, de Guangzhou Healthquest Pharma Co., Ltd: Un compuesto de alquinilbenceno heterocíclico que tiene la fórmula (I) y una sal farmacéuticamente aceptable, o estereoisómero del mismo, **(Ver […]
 Composiciones y métodos para el tratamiento de trastornos de células plasmáticas y trastornos prolinfocíticos de células b, del 29 de Julio de 2020, de Knopp Biosciences LLC: Una composición que comprende una cantidad terapéuticamente eficaz de dexpramipexol para su uso en el tratamiento de un trastorno de células B caracterizado por niveles elevados […]
Composiciones y métodos para el tratamiento de trastornos de células plasmáticas y trastornos prolinfocíticos de células b, del 29 de Julio de 2020, de Knopp Biosciences LLC: Una composición que comprende una cantidad terapéuticamente eficaz de dexpramipexol para su uso en el tratamiento de un trastorno de células B caracterizado por niveles elevados […]
Derivados de piperidina 1,4 sustituidos, del 29 de Julio de 2020, de 89Bio Ltd: Un compuesto de acuerdo con la Fórmula I: **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en donde: A se selecciona de […]
Profármacos de gemcitabina, del 29 de Julio de 2020, de NuCana plc: Una formulación farmacéutica que comprende gemcitabina-[fenil-benzoxi-L-alaninil)]-(S)-fosfato 3: **(Ver fórmula)** o una sal o solvato […]
Formas sólidas de un compuesto modulador de quinasas, del 22 de Julio de 2020, de PLEXXIKON, INC: Una forma cristalina del Compuesto I: **(Ver fórmula)** que es la Forma C del Compuesto I caracterizado por un difractograma de rayos […]