Compuestos morfinanos.
Un compuesto de formula I:**Fórmula**
o una sal del mismo farmacéuticamente aceptable,
en la que:
R1 es CD3; y
R2 es CD3,
o una sal del mismo farmacéuticamente aceptable, en el que el factor de enriquecimiento isotópico para cada átomo de deuterio designado es de al menos 6000.
Tipo: Patente Europea. Resumen de patente/invención. Número de Solicitud: E12176476.
Solicitante: CONCERT PHARMACEUTICALS, INC.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 99 HAYDEN AVENUE, SUITE 100 LEXINGTON, MA 02421 ESTADOS UNIDOS DE AMERICA.
Inventor/es: TUNG,ROBERT.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K31/439 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › formando parte el ciclo de un sistema cíclico puenteado, p. ej. quinuclidina (aza-8-biciclo[3.2.1]octanos A61K 31/46).
- A61P11/14 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › A61P 11/00 Medicamentos para el tratamiento de trastornos del aparato respiratorio. › Agentes antitusígenos.
- C07B59/00 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07B PROCESOS GENERALES DE QUIMICA ORGANICA; SUS APARATOS (preparación de ésteres de ácidos carboxílicos por telomerización C07C 67/47; procesos para la preparación de compuestos macromoleculares, p.ej. telomerzación C08F, C08G). › Introducción de isótopos de elementos en los compuestos orgánicos.
- C07D471/08 C07 […] › C07D COMPUESTOS HETEROCICLICOS (Compuestos macromoleculares C08). › C07D 471/00 Compuestos heterocíclicos que contienen átomos de nitrógeno como únicos heteroátomos del sistema condensado, teniendo al menos un ciclo de seis miembros con un átomo de nitrógeno, no previstos en los grupos C07D 451/00 - C07D 463/00. › Sistemas puenteados.
PDF original: ES-2523286_T3.pdf






Fragmento de la descripción:
Compuestos morfinanos Antecedentes La presente divulgación se refiere a nuevos compuestos morfinanos y sus derivados, sales farmacéuticamente aceptables, solvatos e hidratos de los mismos. La presente divulgación también proporciona composiciones que comprenden un compuesto de la presente divulgación y el uso de tales composiciones en procedimientos para el tratamiento de enfermedades y afecciones que se tratan de manera beneficiosa mediante la administración de un agonista del receptor σ1 que también tiene actividad antagonista NMDA.
En la actualidad el dextrometoríano es uno de los antitusivos más ampliamente usado. También conocido por el nombre químico (+) -3-metoxi-17-metil- (9α, 13α, 14α) -morfinano, el dextrometoríano se comercializa como Zenvia® y Neurodex® en forma de un producto que comprende hidrobromuro de dextrometoríano y sulfato de quinidina.
Además de la actividad fisiológica indicada anteriormente, el dextrometoríano también es un agonista del receptor σ2, un antagonista del N-metil-D-aspartato (NDMA) y un antagonista del receptor nicotínico α3β4. El dextrometoríano inhibe a neurotransmisores, tales como el glutamato, de que activen receptores en el cerebro. También se inhibe la captación de la dopamina y de la serotonina.
El dextrometoríano está aprobado para su uso en productos inhibidores de la tos sin prescripción médica. En la actualidad se encuentra en ensayos clínicos en Fase I para tratamiento de individuos con espasmos en la voz y en estudios clínicos en Fase III para tratamiento del Síndrome de Rett (http: //www.clinicaltrials.gov) . El dextrometoríano se está estudiando con otros fármacos en un ensayo clínico en Fase II para caracterizar los mecanismos de procesamiento del dolor en individuos con síndrome de intestino irritable (http://www.clinicaltrials.gov/) . El dextrometoríano también está en ensayos clínicos en Fase I para el tratamiento de la hiperalgesia en individuos mantenidos con metadona (http://www.clinicaltrials.gov/) .
Además, una combinación de hidrobromuro de dextrometoríano y sulfato de quinidina se encuentra actualmente en ensayos clínicos en Fase III para el tratamiento del dolor en la neuropatía diabética. (http://www.clinicaltrials.gov) . Esta combinación de fármacos también se encuentra en ensayos clínicos en Fase III para el tratamiento del Desorden de Expresión Emocional Involuntaria (IEED) , también conocido como afectación pseudobulbar, en individuos que sufren el mal de Alzheimer, apoplejía, enfermedad de Parkinson y lesión traumática cerebral (http://www.clinical-trials.gov) .
El dextrometoríano se metaboliza en el hígado. La degradación comienza con una O-y N-desmetilación para formar los metabolitos primarios dextroríano y 3-metoxi-morfinano, los cuales son adicional y respectivamente N-y Odesmetilados en 3-hidroxi-morfinano. Se cree que estos tres metabolitos son terapéuticamente activos. Un catalizador metabólico importante es la enzima 2D6 del citocromo P450 (CPY2D6) , que la es responsable de las reacciones de O-desmetilación del dextrometoríano y del 3-metoximorfinano. La N-desmetilación del dextrometoríano y del dextroríano se cataliza por medio de enzimas de la familia relacionada con CPY3A. Se pueden detectar conjugados del dextroríano y de 3-hidroximorfinano en plasma y en orina humanos a las pocas horas de su ingestión.
El abuso de dextrometoríano se ha relacionado con su metabolito activo, el dextroríano. Los efectos de tipo PCP atribuidos al dextrometoríano se producen con mayor seguridad por el dextroríano y de esta manera se puede atribuir el potencial de abuso en seres humanos al metabolismo del dextrometoríano en dextroríano. (Miller, SC et al., Addict Biol, 2005, 10 (4) : 325-7., Nicholson, KL et al., Psychopharmacology (Berl) , 1999 Sep 1, 146 (1) : 49-59., Pender, ES et al., Pediatr Emerg Care, 1991, 7: 163-7) . Un estudio de los efectos psicotrópicos del dextrometoríano descubrió que los metabolizadores extensivos (EM) informaron de un mayor potencial de abuso en comparación con los metabolizadores lentos (PM) proporcionando la evidencia de que el dextroríano contribuye al potencial de abuso de dextrometoríano (Zawertailo LA, et al., J Clin Psychopharmacol, 1998 Aug, 18 (4) : 332-7) .
Una fracción significativa de la población tiene una deficiencia funcional en la enzima CYP2D6. De esta manera, ya que la vía metabólica principal para el dextrometoríano requiere CYP2D6, la disminución de la actividad da como resultado una duración de la acción mucho mayor y un mayor efecto del fármaco en individuos con déficit de CYP2D6. Además de la deficiencia funcional intrínseca, determinadas medicaciones, tales como antidepresivos, son potentes inhibidores de la enzima CYP2D6. Con su bajo nivel de metabolismo en determinadas personas, el dextrometoríano, especialmente en combinación con otra u otras medicaciones, puede producir efectos adversos graves.
Una duración del fármaco en el organismo mayor de la recomendada puede proporcionar efectos beneficiosos duraderos, pero también puede crear o prolongar efectos secundarios no deseados. Los efectos secundarios no deseados para las dosis recomendadas en la terapia de dextrometoríano incluyen nauseas, pérdida de apetito, diarrea, somnolencia, mareo e impotencia.
Por consiguiente, es deseable proporcionar un compuesto que tenga las actividades beneficiosas del dextrometoríano y que también pueda tener otros beneficios, por ejemplo, la reducción de los efectos secundarios adversos, con una disminución de las desventajas metabólicas, la extensión de forma adicional de su vida farmacológica eficaz, la mejora de la conformidad del individuo y, potencialmente, la disminución de la variabilidad farmacocinética en la población y/o la disminución de su potencial de interacciones peligrosas fármaco-fármaco o la disminución de la probabilidad del abuso de dextrometoríano debido a la formación de metabolitos tales como el dextroríano.
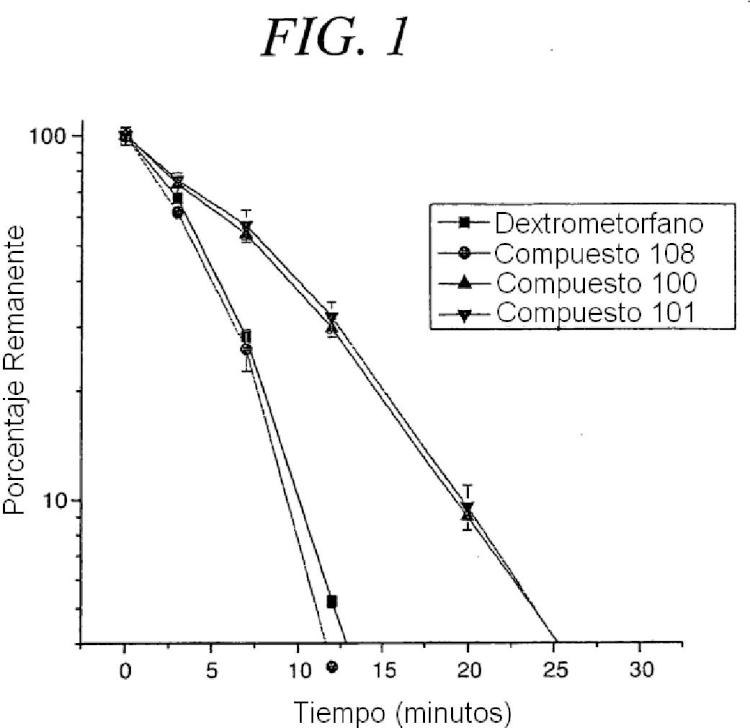
Breve descripción de las figuras La Figura 1 representa la estabilidad frente al tiempo de diversos compuestos de la presente divulgación en microsomas hepáticos de mono cinomolgus.
La Figura 2 representa la estabilidad frente al tiempo de diversos compuestos de la presente divulgación en microsomas hepáticos humanos.
La Figura 3 representa la estabilidad frente al tiempo de diversos compuestos de la presente divulgación en Supersomes 2D6TM .
La Figura 4 representa los niveles en plasma del compuesto 101, del dextrometoríano, así como de los isotopólogos deuterados de dextroríano y del propio dextroríano, en monos con ausencia de codosificación de quinidina.
La Figura 5 representa los niveles en plasma del compuesto 101, del dextrometoríano, así como de los isotopólogos deuterados de dextroríano y del propio dextroríano, en monos codosificados con quinidina.
La Figura 6 representa los niveles en orina del compuesto 101, del dextrometoríano, así como de los isotopólogos deuterados de dextroríano y del propio dextroríano, en función de la concentración de quinidina en monos.
Descripción detallada Definiciones Los términos "aliviar" y "tratar" se usan indistintamente e incluyen el tratamiento terapéutico y/o profiláctico. Ambos términos significan descenso, supresión, atenuación, disminución, detención, o estabilización del desarrollo o progreso de una enfermedad (por ejemplo, una enfermedad o trastorno descrito en el presente documento) .
"Enfermedad" significa cualquier afección o trastorno que daña o interfiere la función normal de una célula, tejido u órgano.
Se podrá reconocer que tienen lugar algunas variaciones de la abundancia isotópica natural en los compuestos sintetizados que dependen del origen de los materiales químicos usados en la síntesis. De esta manera, una preparación de dextrometoríano podrá contener de manera inherente pequeñas cantidades de isotopólogos deuterados y/o que contengan 13C. La concentración de los isótopos de hidrógeno y carbono estables abundantes de forma natural, a pesar de esta variación, es pequeña e irrelevante si se compara con el grado de sustitución isotópica estable de los compuestos de la presente divulgación. Véase, por ejemplo, Wada E et al, Seikagaku 1994, 66:15; Ganes LZ et al, Comp Biochem Physiol A Mol Integr Physiol 1998, 119:725. En un compuesto de la presente divulgación, cuando se designa que una determinada posición contiene deuterio, se entiende que la abundancia del deuterio en dicha posición es considerablemente mayor que la abundancia natural del deuterio, que es del 0, 015 %. Una posición designada para contener deuterio presenta generalmente un factor de enriquecimiento... [Seguir leyendo]
Reivindicaciones:
1. Un compuesto de formula I:
5
o una sal del mismo farmacéuticamente aceptable, en la que:
R1 es CD3; y 10 R2 es CD3,
o una sal del mismo farmacéuticamente aceptable, en el que el factor de enriquecimiento isotópico para cada átomo de deuterio designado es de al menos 6000.
2. El compuesto de la reivindicación 1, en el que el factor de enriquecimiento isotópico para cada átomo de deuterio 15 designado es de al menos 6333, 3.
3. El compuesto de la reivindicación 1, en el que el factor de enriquecimiento isotópico para cada átomo de deuterio designado es de al menos 6466, 7.
4. El compuesto o una sal farmacéuticamente aceptable del mismo de cualquiera de las reivindicaciones anteriores, en el que cualquier átomo no designado como deuterio está presente en su abundancia isotópica natural.
5. Una composición libre de pirógenos que comprende el compuesto o una sal farmacéuticamente aceptable del
mismo de cualquiera de las reivindicaciones anteriores y un vehículo aceptable. 25
6. La composición de la reivindicación 5 formulada para administración farmacéutica y en la que el vehículo es un vehículo farmacéuticamente aceptable.
7. Un compuesto, una sal farmacéuticamente aceptable del mismo o una composición de acuerdo con cualquiera de 30 las reivindicaciones anteriores, para su uso en un método de tratamiento del cuerpo humano o animal.
8. Un compuesto, una sal farmacéuticamente aceptable del mismo o una composición de acuerdo con la reivindicación 7, para su uso en el tratamiento de una enfermedad o de una afección seleccionadas entre: labilidad emocional; afectación pseudobulbar; autismo; trastornos neurológicos; enfermedades neurodegenerativas; lesión 35 cerebral; alteraciones de trastornos de la consciencia; enfermedades cardiovasculares; glaucoma; discinesia tardía; neuropatía diabética; enfermedades retinopáticas; enfermedades o trastornos causados por apoptosis inducida por homocisteína; enfermedades o trastornos causados por niveles elevados de homocisteína; dolor crónico; dolor intratable; dolor neuropático; dolor mediado por el sistema nervioso simpático; dolor asociado a disfunción gastrointestinal; ataques epilépticos; acúfenos; disfunción sexual; tos intratable; dermatitis; trastornos de adicción;
síndrome de Rett (RTT) ; trastornos de la voz debidos a espasmos musculares laríngeos incontrolados; neurotoxicidad del metotrexato; y fatiga causada por cáncer.
9. Un compuesto, una sal farmacéuticamente aceptable del mismo o una composición de acuerdo con la reivindicación 8, para su uso en el tratamiento del dolor neuropático o de la afectación pseudobulbar. 45
10. Un compuesto, una sal farmacéuticamente aceptable del mismo o una composición de acuerdo con la reivindicación 9, para su uso en el tratamiento de la afectación pseudobulbar.
11. La composición de las reivindicaciones 5 o 6, o de las reivindicaciones 7-10 cuando dependen de las
reivindicaciones 5 o 6, que comprende adicionalmente un segundo agente terapéutico útil en el tratamiento o la prevención de una enfermedad o de una afección seleccionadas entre labilidad emocional; afectación pseudobulbar; autismo; trastornos neurológicos; enfermedades neurodegenerativas; lesión cerebral; alteraciones de trastornos de la consciencia; enfermedades cardiovasculares; glaucoma; discinesia tardía; neuropatía diabética; enfermedades retinopáticas; enfermedades o trastornos causados por apoptosis inducida por homocisteína; enfermedades o 55 trastornos causados por niveles elevados de homocisteína; dolor crónico; dolor intratable; dolor neuropático; dolor mediado por el sistema nervioso simpático; dolor asociado a disfunción gastrointestinal; ataques epilépticos;
acúfenos; disfunción sexual; tos intratable; dermatitis; trastornos de adicción; síndrome de Rett (RTT) ; trastornos de la voz debidos a espasmos musculares laríngeos incontrolados; neurotoxicidad del metotrexato; y fatiga causada por el cáncer.
12. La composición de la reivindicación 11, en la que el segundo agente terapéutico se selecciona entre quinidina, sulfato de quinidina, oxicodona y gabapentina.
13. Formas de dosificación por separado de:
(i) un compuesto, una sal farmacéuticamente aceptable del mismo o una composición de acuerdo con cualquiera de las reivindicaciones 1-6; y
(ii) un segundo agente terapéutico útil en el tratamiento o la prevención de una enfermedad o de una afección seleccionadas entre labilidad emocional; afectación pseudobulbar; autismo; trastornos neurológicos; enfermedades neurodegenerativas; lesión cerebral; alteraciones de trastornos de la consciencia; enfermedades cardiovasculares; glaucoma; discinesia tardía; neuropatía diabética; enfermedades retinopáticas; enfermedades o trastornos causados por apoptosis inducida por homocisteína; enfermedades o trastornos causados por niveles elevados de homocisteína; dolor crónico; dolor intratable; dolor neuropático; dolor mediado por el sistema nervioso simpático; dolor asociado a disfunción gastrointestinal; ataques epilépticos; acúfenos; disfunción sexual; tos intratable; dermatitis; trastornos de adicción; síndrome de Rett (RTT) ; trastornos de la voz debidos a espasmos musculares laríngeos incontrolados, neurotoxicidad del metotrexato; y fatiga causada por el cáncer, en donde dicho compuesto, sal farmacéuticamente aceptable del mismo o composición y el segundo agente terapéutico se asocian el uno con el otro.
14. Formas de dosificación por separado de acuerdo con la reivindicación 13, en las que dicho segundo agente 25 terapéutico se selecciona entre quinidina, sulfato de quinidina, oxicodona y gabapentina.
15. Una presentación que comprende formas de dosificación por separado de acuerdo con las reivindicaciones 13 o 14.
16. Formas de dosificación por separado o una presentación de acuerdo con cualquiera de las reivindicaciones 1315, en las que dicho segundo agente es para administración simultánea.
17. Formas de dosificación por separado o una presentación de acuerdo con cualquiera de las reivindicaciones 13
15, en las que dicho segundo agente es para administración por separado. 35
18. La composición, las formas de dosificación por separado o la presentación de acuerdo con cualquiera de las reivindicaciones 11-17, que comprenden 10-60 mg del compuesto de Fórmula I o una sal farmacéuticamente aceptable del mismo, y 2, 5-30 mg de quinidina.
19. El uso de un compuesto, una sal farmacéuticamente aceptable del mismo o una composición de acuerdo con cualquiera de las reivindicaciones 1-6 en la fabricación de un medicamento para el tratamiento de una enfermedad o de una afección seleccionadas entre labilidad emocional; afectación pseudobulbar; autismo; trastornos neurológicos; enfermedades neurodegenerativas; lesión cerebral; alteraciones de trastornos de la consciencia; enfermedades cardiovasculares; glaucoma; discinesia tardía; neuropatía diabética; enfermedades retinopáticas; enfermedades o 45 trastornos causados por apoptosis inducida por homocisteína; enfermedades o trastornos causados por niveles elevados de homocisteína; dolor crónico; dolor intratable; dolor neuropático; dolor mediado por el sistema nervioso simpático; dolor asociado a disfunción gastrointestinal; ataques epilépticos; acúfenos; disfunción sexual; tos intratable; dermatitis; trastornos de adicción; síndrome de Rett (RTT) ; trastornos de la voz debidos a espasmos musculares laríngeos incontrolados; neurotoxicidad del metotrexato; y fatiga causada por el cáncer.
20. El uso de acuerdo con la reivindicación 19, en el que la enfermedad o la afección son dolor neuropático o afectación pseudobulbar.
21. El uso de acuerdo con la reivindicación 20, en el que la enfermedad o la afección es afectación pseudobulbar. 55
22. El uso de cualquiera de las reivindicaciones 19-21, junto con un segundo agente terapéutico útil en el tratamiento o en la prevención de una enfermedad o de una afección seleccionadas entre labilidad emocional; afectación pseudobulbar; autismo; trastornos neurológicos; enfermedades neurodegenerativas; lesión cerebral; alteraciones de trastornos de la consciencia; enfermedades cardiovasculares; glaucoma; discinesia tardía; neuropatía diabética; 60 enfermedades retinopáticas; enfermedades o trastornos causados por apoptosis inducida por homocisteína; enfermedades o trastornos causados por niveles elevados de homocisteína; dolor crónico; dolor intratable; dolor neuropático; dolor mediado por el sistema nervioso simpático; dolor asociado a disfunción gastrointestinal; ataques epilépticos; acúfenos; disfunción sexual; tos intratable; dermatitis; trastornos de adicción; síndrome de Rett (RTT) ; trastornos de la voz debidos a espasmos musculares laríngeos incontrolados; neurotoxicidad del metotrexato; y
fatiga causada por el cáncer.
23. El uso de la reivindicación 22, en el que el segundo agente terapéutico se selecciona entre quinidina, sulfato de quinidina, oxicodona y gabapentina.
24. El uso de las reivindicaciones 22 o 23, en el que el segundo agente es quinidina, y en el que la cantidad de dosificación del compuesto de Fórmula I o de una sal farmacéuticamente aceptable del mismo es de 10-60 mg, y la cantidad de dosificación de la quinidina es de 2, 5-30 mg.
Patentes similares o relacionadas:
NANOPARTÍCULAS TERAPÉUTICAS QUE ENCAPSULAN TERPENOIDES Y/O CANNABINOIDES, del 14 de Mayo de 2020, de GBS GLOBAL BIOPHARMA: En el presente documento se proporcionan nanopartículas de PEGA que encapsulan terpenoides y cannabinoides y composiciones farmacéuticas que comprenden […]
Compuestos o-quinónicos como agentes neutralizantes del óxido nítrico, del 29 de Abril de 2020, de INSTITUT DES SUBSTANCES VEGETALES: Compuesto de fórmula (I) **(Ver fórmula)** en la que R1 se selecciona entre el grupo que constituido por: • -CH=CH-COOR2 […]
Composición para el tratamiento de la cavidad de la garganta/orofaringe, del 25 de Marzo de 2020, de MARIA CLEMENTINE MARTIN KLOSTERFRAU VERTRIEBSGESELLSCHAFT MBH: Composición en forma de una dosificación líquida para su utilización en el tratamiento profiláctico o terapéutico de enfermedades inflamatorias de la cavidad oral y/o […]
Composición basada en plantas para su utilización en el tratamiento de la tos, del 3 de Julio de 2019, de ABOCA S.P.A. SOCIETA'' AGRICOLA: Composición para su utilización en el tratamiento de la tos que consiste en: azúcar de caña, miel, agua desionizada, zumo de limón, extracto de Plantago […]
Orvepitant para el tratamiento de la tos crónica, del 26 de Junio de 2019, de NeRRe Therapeutics Limited: El ácido 2-(R)-(4-fluoro-2-metil-fenil)-4-(S)-((8aS)-6-oxo-hexahidro-pirrolo[1,2-α]-pirazin-2-il)-piperidin-1- carboxílico [1-(R)-(3,5-bis-trifluorometil-fenil)-etil]-metilamida…
DROPROPIZINA EN COMBINACIÓN CON AMBROXOL EN LA FORMA FARMACÉUTICA DE JARABE Y TABLETAS, del 23 de Mayo de 2019, de PRODUCTOS FARMACÉUTICOS, S.A. DE C.V: La presente invención se refiere a una combinación farmacéutica de ambroxol o una sal farmacéuticamente aceptable del mismo y dropropizina. Asimismo, se refiere a una […]
Composición farmacéutica que contiene flurbiprofeno, del 15 de Mayo de 2019, de Reckitt Benckiser Healthcare International Limited: Un AINE o una sal farmacéuticamente aceptable del mismo para su uso en el tratamiento tópico de la tos en la membrana mucosa de la garganta de una persona que necesita tratamiento […]
Compuestos de quinina e isómeros ópticos, procedimiento de preparación y uso médico de los mismos, del 27 de Febrero de 2019, de Beijing Shuobai Pharmaceutical Co., Ltd: Compuesto de fórmula I:**Fórmula** o una sal, solvato o isómero óptico de la misma farmacéuticamente aceptables, en donde en la fórmula I: n se selecciona entre […]