Compuestos de 4-oxadiazolil-piperidina y uso de los mismos.
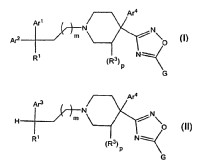
Compuesto de fórmula (I):
o una sal farmacéuticamente aceptable del mismo,
en donde:
Ar1 es fenilo no sustituido o sustituido con uno o más grupos R2
; Ar2 es fenilo no sustituido o sustituido con uno, dos, o tres grupos R2;
Ar4 es fenilo no sustituido o sustituido con uno, dos, o tres grupos R2;
G es -H, -C(O)(CH2)nCO2R4, -C(O)(CH2)nR4, -(alquileno C1-C5)C(O)OR4,3 ó -(alquileno C1-C5)R5;
R1 = -H, -C(O)NH2, -C(O)NHOH, -CO2R4, -CHO, -CN, -(alquilo C1-C4), -C(O)NH(alquilo C1-C4), -C(O)N(alquilo C1-C4)2, -CF3, -CHF2, -CH2F,
R2 y R3 son cada uno independientemente -halógeno, alquilo -C1-C3, -O(alquilo C1-C3), -NH(alquilo C1-C3), - N(alquilo C1-C3)2, -CF3, u -OCF3;
R4 = -H, -alquilo -C1-C10, -CH2O(alquilo C1-C4), -CH2N(alquilo C1-C4)2, ó -CH2NH(alquilo C1-C4);
R5 = -NH2, -NHSO2R4, -C(O)NH2, -C(O)NHOH, -SO2NH2, -C(O)NH(alquilo C1-C4), -C(O)N(alquilo C1-C4)2, - SO2NH(alquilo C1-C4), -SO2N(alquilo C1-C4)2, -H, -OH, -CN, -C3-C8 cicloalquilo, fenilo, naftilo, antrilo, fenantrilo, o heteroarilo (5 a 7 miembros), no estando sustituido o estando sustituido con uno o más grupos R2 cada C3-C8 cicloalquilo, fenilo, naftilo, antrilo, fenantrilo, o heteroarilo (5 a 7 miembros);
m = un entero que va de 0 a 4;
n = un entero que va de 1 a 4;
p = 0 ó 1; y
q = un entero que va de 1 a 6.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP2006/011150.
Solicitante: PURDUE PHARMA LP.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: ONE STAMFORD FORUM 201 TRESSER BOULEVARD STAMFORD CT 06901 ESTADOS UNIDOS DE AMERICA.
Inventor/es: TAFESSE,LAYKEA.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K31/454 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › conteniendo un ciclo de cinco eslabones con el nitrógeno como heteroátomo del ciclo, p. ej. pimozida, domperidona.
- A61P25/00 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › Medicamentos para el tratamiento de trastornos del sistema nervioso.
- C07D413/04 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07D COMPUESTOS HETEROCICLICOS (Compuestos macromoleculares C08). › C07D 413/00 Compuestos heterocíclicos que contienen dos o más heterociclos, teniendo al menos un ciclo átomos de nitrógeno y oxígeno como únicos heteroátomos del ciclo. › unidos directamente por un enlace entre dos miembros cíclicos.
- C07D413/14 C07D 413/00 […] › que contienen tres o más heterociclos.
PDF original: ES-2382712_T3.pdf
Fragmento de la descripción:
Compuestos de 4-oxadiazolil-piperidina y uso de los mismos
1. Campo de la invención
La presente invención se refiere a Compuestos de 4-oxadiazolil-piperidina, a composiciones que comprenden un Compuesto de 4-oxadiazolil-piperidina y a su uso para prevenir o tratar dolor o diarrea en un animal, que comprende administrar una cantidad eficaz de un Compuesto de 4-oxadiazolil-piperidina a un animal que necesite dicha prevención
o tratamiento.
2. Antecedentes de la invención
El dolor es el síntoma más común para el cual los pacientes buscan consejo y tratamiento médicos. El dolor puede ser agudo o crónico. Mientras que el dolor agudo es habitualmente autolimitado, el dolor crónico puede persistir durante 3 meses o más tiempo y puede conducir a cambios significativos en la personalidad, el estilo de vida, la capacidad funcional o la calidad de vida global de un paciente (K.M. Foley, Pain, en Cecil Textbook of Medicine 100107, eds. J. C. Bennett y F. Plum, ed. 20ª 1996) .
El dolor se ha tratado tradicionalmente administrando un analgésico no opioide, tal como ácido acetilsalicílico, trisalicilato de colina y magnesio, acetaminofeno, ibuprofeno, fenoprofeno, diflusinal y naproxeno; o un analgésico opioide, tal como morfina, hidromorfona, metadona, levoríanol, fentanilo, oxicodona y oximorfona. Id.
La patente de Estados Unidos n.º 6.576.650 B1, la patente de Estados Unidos 6.166.039, y la patente de Estados Unidos n.º 5.849.761, concedidas a Yaksh, y la patente de Estados Unidos n.º 6.573.282, concedida a Yaksh et al., describen derivados de piperidina 1, 4-sustituidos útiles supuestamente como opiáceos antihiperalgésicos periféricamente activos.
La patente de Estados Unidos n.º 6.362.203 B1 concedida a Mogi et al. describe derivados de 4-hidroxi–4– fenilpiperidina que se supone que presentan una acción analgésica periférica.
La publicación de patente canadiense n.º 949560 de Carron et al. describe derivados de piperidina que portan sustituyentes en las posiciones 1 y 4, que se supone que son útiles como analgésicos.
La publicación internacional n.º WO 02/38185 A2 de Dunn et al. describe compuestos de piperidina 1, 4 sustituidos que supuestamente son útiles como opiáceos antihiperalgésicos.
El resumen de la publicación internacional n.º WO 01/70689 A1 da a conocer también derivados de piperidina que portan sustituyentes en las posiciones 1 y 4 y que supuestamente son útiles como agonistas de los receptores opioides
El documento WO 2004/046 132 describe compuestos de 4-tetrazolil piperidina con la misma actividad.
Los analgésicos opioides tradicionales ejercen su actividad farmacológica una vez que han pasado a través de la barrera hematoencefálica. No obstante, este paso a través de la barrera hematoencefálica puede derivar en efectos secundarios no deseables mediados por el sistema nervioso central, tales como depresión respiratoria, aumento de la tolerancia a los fármacos, aumento de la farmacodependencia, estreñimiento y una euforia no deseada.
Sigue existiendo una necesidad evidente de fármacos nuevos que resulten útiles para tratar o prevenir el dolor o la diarrea y que reduzcan o eviten uno o más de los efectos secundarios asociados a la terapia tradicional para el tratamiento del dolor o la diarrea.
3. Resumen de la invención [0012] La presente invención abarca compuestos que presentan la fórmula (I) :
y sales farmacéuticamente aceptables de los mismos, en donde:
Ar1 es fenilo, que no está sustituido o está sustituido con uno, dos, o tres grupos R2;
[0014] Ar2 es fenilo, que no está sustituido o está sustituido con uno, dos, o tres grupos R2; [0015] Ar4 es fenilo, que no está sustituido o está sustituido con uno, dos, o tres grupos R2; [0016] G es -H, -C (O) (CH2) nCO2R4, -C (O) (CH2) nR5, - (alquileno C1-C5) CO2R4, ó - (alquileno C1-C5) R5;
R1 = -H, -C (O) NH2, -C (O) NHOH, -CO2R4, -CHO, -CN, - (alquilo C1-C4) , -C (O) NH (alquilo C1-C4) , -C (O) N (alquilo C1C4) 2, -CF3, -CHF2, -CH2F,
ó
R2 y R3 son cada uno independientemente -halógeno, alquilo -C1-C3, -O (alquilo C1-C3) , -NH (alquilo C1-C3) , N (alquilo C1-C3) 2, -CF3, u -OCF3; 15 [0019] R4 = -H, -alquilo -C1-C10, -CH2O (alquilo C1-C4) , -CH2N (alquilo C1-C4) 2, ó -CH2NH (alquilo C1-C4) ;
R5 = -NH2, -NHSO2R4, -C (O) NH2, -C (O) NHOH, -SO2NH2, -C (O) NH (alquilo C1-C4) , -C (O) N (alquilo C1-C4) 2, SO2NH (alquilo C1-C4) , -SO2N (alquilo C1-C4) 2, -H, -OH, -CN, ó -C3-C8 cicloalquilo, fenilo, naftilo, antrilo, fenantrilo, 20 heteroarilo (5 a 7 miembros) , no estando sustituido o estando sustituido con uno o más grupos R2 cada C3-C8 cicloalquilo, fenilo, naftilo, antrilo, fenantrilo, heteroarilo (5 a 7 miembros) ;
m = un entero que vade 0 a 4; n = un entero que va de 1 a 4; 25 p = 0 ó 1; y q = un entero que va de 1 a 6.
La presente invención abarca también compuestos que presentan la fórmula (II) :
y sales farmacéuticamente aceptables de los mismos, en donde:
Ar3 es fenilo, que no está sustituido o está sustituido con uno, dos, o tres grupos R2; [0023] Ar4 es fenilo, que no está sustituido o está sustituido con uno, dos, o tres grupos R2;
[0024] G = H, -C (O) (CH2) nC (O) OR4, -C (O) (CH2) nR5, - (alquileno C1-C5) COOR4, ó - (alquileno C1-C5) R5; [0025] R1 = -H, -C (O) NH2, -C (O) NHOH, -CO2R4, -CHO, -CN, - (alquilo C1-C4) , -C (O) NH (alquilo C1-C4) , -C (O) N (alquilo C1-C4) , -CF3, -CHF2, -CH2F,
ó
R2 y R3 son cada uno independientemente -halógeno, alquilo -C1-C3, -O (alquilo C1-C3) , -NH (alquilo C1-C3) , N (alquilo C1-C3) 2, -CF3, ó -OCF3;
R4 = -H, -alquilo -C1-C10, -CH2O (alquilo C1-C4) , -CH2N (alquilo C1-C4) 2, ó -CH2NH (alquilo C1-C4) ;
R5 = -NH2, -NHSO2R4, -C (O) NH2, -C (O) NHOH, -SO2NH2, -C (O) NH (alquilo C1-C4) , -C (O) N (alquilo C1-C4) 2, SO2NH (alquilo C1-C4) , -SO2N (alquilo C1-C4) 2, -H, -OH, -CN, ó -C3-C8 cicloalquilo, fenilo, naftilo, antrilo, fenantrilo, heteroarilo (5 a 7 miembros) , no estando sustituido o estando sustituido con uno o más grupos R2 cada C3-C8 cicloalquilo, fenilo, naftilo, antrilo, fenantrilo, heteroarilo (5 a 7 miembros) ;
m = un entero que vade 0 a 4;
n = un entero que va de 1 a 4;
p = 0 ó 1; y
q = un entero que va de 1 a 6.
Un compuesto de fórmula (I) o (II) o una sal del mismo farmacéuticamente aceptable (siendo cada uno de ellos un “Compuesto de 4–oxadiazolil–piperidina”) es útil para tratar o prevenir el dolor o la diarrea en un animal.
La invención se refiere también a composiciones que comprenden un Compuesto de 4–oxadiazolil–piperidina y un vehículo o excipiente farmacéuticamente aceptable. Las presentes composiciones son útiles para tratar o prevenir el dolor o la diarrea en un animal.
La invención se refiere también a kits que comprenden un envase que contiene una cantidad eficaz de un Compuesto de 4–oxadiazolil–piperidina e instrucciones para usarlo con vistas a tratar o prevenir el dolor o la diarrea.
La invención se refiere además a un Compuesto de 4-oxadiazolil-piperidina para su uso en la prevención del dolor o la diarrea en un animal, que comprende administrar una cantidad eficaz de un Compuesto de 4-oxadiazolilpiperidina a un animal que lo necesite. En otros aspectos de esta realización, estos usos para prevenir el dolor o la diarrea en un animal comprenden además administrar una cantidad eficaz de un analgésico opioide, un analgésico no opioide, un agente anti-emético, o una combinación de los mismos.
La invención se refiere además a un Compuesto de 4-oxadiazolil-piperidina para su uso en el tratamiento del dolor o la diarrea en un animal, que comprende administrar una cantidad eficaz de un Compuesto de 4-oxadiazolilpiperidina a un animal que lo necesite. En otros aspectos de esta realización, estos usos para tratar el dolor o la diarrea en un animal comprenden además administrar una cantidad eficaz de un analgésico opioide, un analgésico no opioide, un agente anti-emético, o una combinación de los mismos.
La invención se refiere también... [Seguir leyendo]
Reivindicaciones:
1. Compuesto de fórmula (I) :
o una sal farmacéuticamente aceptable del mismo, en donde: 5 Ar1 es fenilo no sustituido o sustituido con uno o más grupos R2; Ar2 es fenilo no sustituido o sustituido con uno, dos, o tres grupos R2; Ar4 es fenilo no sustituido o sustituido con uno, dos, o tres grupos R2; G es -H, -C (O) (CH2) nCO2R4, -C (O) (CH2) nR5, - (alquileno C1-C5) C (O) OR4, ó - (alquileno C1-C5) R5; R1 = -H, -C (O) NH2, -C (O) NHOH, -CO2R4, -CHO, -CN, - (alquilo C1-C4) , -C (O) NH (alquilo C1-C4) , -C (O) N (alquilo 10 C1-C4) 2, -CF3, -CHF2, -CH2F, ó R2 y R3 son cada uno independientemente -halógeno, alquilo -C1-C3, -O (alquilo C1-C3) , -NH (alquilo C1-C3) , N (alquilo C1-C3) 2, -CF3, u -OCF3; R4 = -H, -alquilo -C1-C10, -CH2O (alquilo C1-C4) , -CH2N (alquilo C1-C4) 2, ó -CH2NH (alquilo C1-C4) ; R5 = -NH2, -NHSO2R4, -C (O) NH2, -C (O) NHOH, -SO2NH2, -C (O) NH (alquilo C1-C4) , -C (O) N (alquilo C1-C4) 2, 15 SO2NH (alquilo C1-C4) , -SO2N (alquilo C1-C4) 2, -H, -OH, -CN, -C3-C8 cicloalquilo, fenilo, naftilo, antrilo, fenantrilo, o heteroarilo (5 a 7 miembros) , no estando sustituido o estando sustituido con uno o más grupos R2 cada C3-C8 cicloalquilo, fenilo, naftilo, antrilo, fenantrilo, o heteroarilo (5 a 7 miembros) ; m = un entero que va de 0 a 4; n = un entero que va de 1 a 4; 20 p = 0 ó 1; y q = un entero que va de 1 a 6. 2. Compuesto de fórmula (II) :o una sal farmacéuticamente aceptable del mismo, en donde:
Ar3 es fenilo no sustituido o sustituido con uno, dos, o tres grupos R2; Ar4 es fenilo no sustituido o sustituido con uno, dos, o tres grupos R2; G = H, -C (O) (CH2) nC (O) OR4, -C (O) (CH2) nR5, - (alquileno C1-C5) C (O) OR4, ó - (alquileno C1-C5) R5; R1 = -H, -C (O) NH2, -C (O) NHOH, -CO2R4, -CHO, -CN, - (alquilo C1-C4) , -C (O) NH (alquilo C1-C4) , -C (O) N (alquilo
30 C1-C4) 2, -CF3, -CHF2, -CH2F, R2 y R3 son cada uno independientemente -halógeno, alquilo -C1-C3, -O (alquilo C1-C3) , -NH (alquilo C1-C3) , N (alquilo C1-C3) 2, -CF3, u -OCF3; R4 = -H, -alquilo -C1-C10, -CH2O (alquilo C1-C4) , -CH2N (alquilo C1-C4) 2, ó -CH2NH (alquilo C1-C4) ; R5 = -NH2, -NHSO2R4, -C (O) NH2, -C (O) NHOH, -SO2NH2, -C (O) NH (alquilo C1-C4) , -C (O) N (alquilo C1-C4) 2,
SO2NH (alquilo C1-C4) , -SO2N (alquilo C1-C4) 2, -H, -OH, -CN, -C3-C8 cicloalquilo, fenilo, naftilo, antrilo, fenantrilo, o heteroarilo (5 a 7 miembros) , no estando sustituido o estando sustituido con uno, dos o tres grupos R2 cada C3-C8 cicloalquilo, fenilo, naftilo, antrilo, fenantrilo, o heteroarilo (5 a 7 miembros) ; m = un entero que vade 0 a 4; n = un entero que va de 1 a 4; p = 0 ó 1; y q = un entero que va de 1 a 6.
3. Compuesto de la reivindicación 1 ó 2, en el que m = 1 y G = H.
4. Compuesto de la reivindicación 1 ó 2, en el que R1 es -C (O) NH2, -C (O) NH (alquilo C1-C4) , ó -C (O) N (alquilo C1-C4) (alquilo C1-C4) .
5. Compuesto de la reivindicación 1 ó 2, en el que R1 es -CN.
6. Compuesto de la reivindicación 1 ó 2, en el que m = 1, p = 0 y q = 3.
7. Compuesto de la reivindicación 1 ó 2, en el que G = - (CH2) 2NHSO2H.
8. Compuesto de la reivindicación 1 ó 2, en el que G = -CH2C (O) NH2, -CH2C (O) NH (alquilo C1-C4) ó 25 CH2C (O) N (alquilo C1-C4) (alquilo C1-C4) , preferentemente -CH2C (O) NH2.
9. Compuesto de la reivindicación 1 ó 2, en el que G = -CH2C (O) OCH2CH3.
10. Compuesto de la reivindicación 8 ó 9, en el que R1 = -C (O) N (CH3) 2.
11. Compuesto de la reivindicación 8 ó 9, en el que R1 es
12. Compuesto de la reivindicación 1 ó 2, en el que G = - (CH2) 2C (O) OCH2CH3.
13. Compuesto de la reivindicación 1 ó 2, en el que G = - (CH2) 4C (O) OCH2CH3. 35
14. Compuesto de la reivindicación 1 ó 2, en el que p = 1.
15. Composición que comprende un compuesto de la reivindicación 1 ó 2 y un vehículo o excipiente farmacéuticamente aceptable.
16. Composición de la reivindicación 15, que comprende además por lo menos un compuesto seleccionado del grupo consistente en un analgésico opioide, un analgésico no opioide, y un agente antiemético.
17. Método para preparar una composición, comprendiendo el método mezclar un compuesto de la reivindicación 1 ó 45 2 y un vehículo o excipiente farmacéuticamente aceptable.
18. Kit que comprende un envase que contiene la composición de la reivindicación 15, preferentemente que comprende además un agente antidiarreico.
19. Uso de un compuesto de la reivindicación 1 ó 2 ó una sal farmacéuticamente aceptable del mismo, en la preparación de un medicamento en el tratamiento o prevención del dolor o la diarrea.
20. Uso según la reivindicación 19, que comprende además administrar una cantidad eficaz de por lo menos un compuesto seleccionado del grupo consistente en un analgésico opioide, un analgésico no opioide, y un agente antiemético.
21. Compuesto de la reivindicación 1, descrito por la siguiente fórmula
o una sal farmacéutica del mismo.
22. Compuesto de la reivindicación 1, descrito por la siguiente fórmula
o una sal farmacéutica del mismo.
23. Compuesto de la reivindicación 1, descrito por la siguiente fórmula
o una sal farmacéutica del mismo.
24. Compuesto de la reivindicación 1, descrito por la siguiente fórmula
o una sal farmacéutica del mismo.
25. Uso de un compuesto de la reivindicación 1 ó 2 ó una sal farmacéuticamente aceptable del mismo, como 5 medicamento.
26. Uso de un compuesto para la reivindicación 1 ó 2 ó una sal farmacéuticamente aceptable del mismo, en la preparación de un medicamento para estimular la función de los receptores opioides en una célula, que comprende hacer entrar en contacto una célula capaz de expresar un receptor opioide con una cantidad eficaz del
compuesto de la reivindicación 1 ó 2 ó una sal farmacéuticamente aceptable del mismo, para el tratamiento del dolor o la diarrea.
27. Uso según la reivindicación 26, en el que el receptor se selecciona del grupo consistente en un receptor opioide κ,
un receptor opioide μ, un receptor opioide δ o un receptor ORL-1 para el tratamiento del dolor o la diarrea. 15
28. Compuesto según la reivindicación 1 ó 2 ó una sal farmacéuticamente aceptable del mismo, para el tratamiento del dolor o la diarrea.
29. Compuesto según la reivindicación 1 ó 2 ó una sal farmacéuticamente aceptable del mismo, para la estimulación 20 de una función de los receptores opioides en una célula, para el tratamiento del dolor o la diarrea.
Patentes similares o relacionadas:
Preparación sólida que contiene colorante, del 29 de Julio de 2020, de DAIICHI SANKYO COMPANY, LIMITED: Preparación farmacéutica sólida que comprende monobencenosulfonato de ácido [(1R,5S,6S)-6-(aminometil)-3- etilbiciclo[3.2.0]hept-3-en-6-il]acético […]
Derivados de 8-amino-2-oxo-1,3-diazaespiro-[4.5]-decano, del 29 de Julio de 2020, de GRUNENTHAL GMBH: Un compuesto según la fórmula general (I) **(Ver fórmula) donde R1 y R2 significan independientemente -H; -alquilo C1-C6, lineal o ramificado, […]
Derivados de bencimidazol como inhibidores Nav 1.7 (subunidad alfa del canal de sodio, dependiente del voltaje, tipo IX (SCN9A)) para tratar el dolor, la disuria y la esclerosis múltiple, del 22 de Julio de 2020, de Sumitomo Dainippon Pharma Co., Ltd: Un compuesto de fórmula (I): **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, donde R1a, R1b, R1c, y R1d son independientemente hidrógeno, […]
Nuevos moduladores de receptores de fosfato de esfingosina, del 15 de Julio de 2020, de THE SCRIPPS RESEARCH INSTITUTE: Una composicion farmaceutica que comprende un compuesto de formula 265: **(Ver fórmula)** o una sal, estereoisomero, hidrato o solvato farmaceuticamente aceptable […]
Derivado de 5-etiol-4-metil-pirazol-3-carboxamida que tiene actividad como agonista de TAAR, del 15 de Julio de 2020, de F. HOFFMANN-LA ROCHE AG: Un compuesto de fórmula I: **(Ver fórmula)** que es 5-etil-4-metil-N-[4-[(2S) morfolin-2-il]fenil]-1H-pirazol-3-carboxamida, o una sal de adición de ácido farmacéuticamente […]
Composición que comprende cinamaldehído y cinc, del 8 de Julio de 2020, de SOCIETE DES PRODUITS NESTLE S.A.: Composición que comprende cinamaldehído y cinc para la utilización en la mejora de uno o más de rendimiento cognitivo, cognición, humor o memoria en un […]
Cápsulas blandas entéricas de liberación controlada de ésteres de fumarato, del 1 de Julio de 2020, de Banner Life Sciences LLC: Una composición farmacéutica oral que comprende una cápsula blanda entérica que encapsula fumarato de monometilo suspendido en una matriz líquida […]
Síntesis y formas de sal novedosas de (R)-5-((E)-2-pirrolidin-3-ilvinil)pirimidina, del 1 de Julio de 2020, de Oyster Point Pharma, Inc: Un procedimiento para la fabricación de (R)-5-((E)-2-pirrolidin-3-ilvinil)pirimidina que comprende: (a) tratar el compuesto 1 con cloruro de metanosulfonilo para […]