COMPOSICIÓN FARMACÉUTICA QUE COMPRENDE ANASTROZOL.
Una formulación de liberación prolongada, que comprende; (i) un polímero de polilactida o copolímero de poli(lactida-co-glicolida) que tiene un peso molecular medio de entre 5.
000 Daltons y 50.000 Daltons; (ii) una relación molar de lactida a glicolida de entre 100:0 y 50:50; y (iii) de aproximadamente 10 a 55% en peso de anastrozol en base al peso total de la formulación; en donde la formulación de liberación prolongada libera de manera continua anastrozol a lo largo de un periodo de al menos 10 días cuando se pone en un entorno acuso de tipo fisiológico
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/GB2006/003199.
Solicitante: ASTRAZENECA AB.
Nacionalidad solicitante: Suecia.
Dirección: 151 85 SÖDERTÄLJE SUECIA.
Inventor/es: GELLERT,PAUL RICHARD, MATHARU,Balvinder,Singh.
Fecha de Publicación: .
Fecha Solicitud PCT: 29 de Agosto de 2006.
Clasificación Internacional de Patentes:
- A61K9/00M5D
- A61K9/16H6D4
Clasificación PCT:
- A61K9/00 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › Preparaciones medicinales caracterizadas por un aspecto particular.
- A61K9/16 A61K […] › A61K 9/00 Preparaciones medicinales caracterizadas por un aspecto particular. › Aglomerados; Granulados; Microbolitas.
- A61K9/50 A61K 9/00 […] › Microcápsulas (A61K 9/52 tiene prioridad).
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Eslovenia, Finlandia, Rumania, Chipre, Lituania, Letonia.
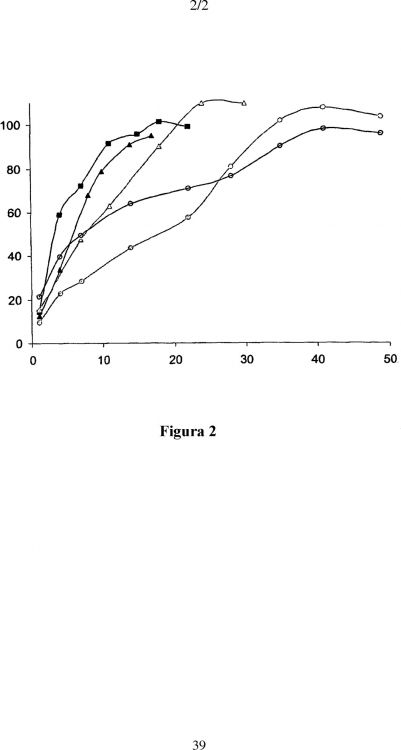
Fragmento de la descripción:
La presente invención se refiere a formulaciones de anastrozol de liberación lenta, más particularmente a polímeros biodegradables, típicamente polímeros de polilactida y copolímeros de poli(lactida-co-glicolida), en los que se incorpora anastrozol, que incluyen formulaciones de micropartículas y formulaciones de 5 implantes monolíticos. La invención también se refiere a dichas formulaciones para el uso en métodos de tratamiento, particularmente para el uso en métodos para el tratamiento del cáncer de mama.
El anastrozol (Arimidex™) es un inhibidor de la aromatasa, los inhibidores de la aromatasa son una clase de compuestos que actúan para inhibir la síntesis de 10 estrógenos en los tejidos. Estos compuestos impiden la biosíntesis de estrógenos inhibiendo la enzima aromatasa, que cataliza la conversión de andrógenos adrenales (androstenodiona y testosterona) a estrógenos (estrógeno y estradiol). El anastrozol es un inhibidor de la aromatasa no esteroideo que es altamente selectivo, bien tolerado, y es eficaz en el tratamiento del cáncer de mama avanzado (Buzdar et al 1995, 5 The 15 Breast 4(3): 256-257 Abs 104; Jonat et al 1995, European Journal of Cancer 32A(3): 404-412; Plourde et al 1995, Journal of Steroid Biochemistry 53:175-179). (Se puede encontrar información adicional sobre la experiencia clínica con Arimidex en la hoja de información prescriptiva para el Arimidex). El anastrozol se describe en la patente de EE.UU. RE 366717. 20
Se conocen varias formulaciones de liberación prolongada que usan polilactida y copolímeros de poli(lactida-co-glicolida). Por ejemplo, la patente europea EP 058 481 describe implantes monolíticos que comprenden un copolímero de poli(lactida-co-glicolida) biodegradable y un agonista de LH-RH.
El anastrozol se administra en la actualidad como un comprimido oral diario de 25 1 mg de liberación inmediata. Es importante que los pacientes tomen anastrozol diariamente para que reciban el beneficio terapéutico óptimo. El cumplimiento por parte del paciente de tal régimen de dosificación diario es, sin embargo, difícil de asegurar, especialmente cuando el curso de la terapia es largo o de duración intermedia o para toda la vida. Por tanto, hay una necesidad de una formulación de 30 anastrozol de liberación prolongada para mejorar el cumplimiento/conveniencia del paciente y dar a los pacientes un beneficio terapéutico óptimo. Formular compuestos en formas de dosificación de liberación prolongada, tales como implantes monolíticos y formulaciones de micropartículas, también proporciona otros beneficios. Por ejemplo, una dosificación menos frecuente de fármacos en la forma de formulaciones de 35
liberación prolongada suaviza de manera eficaz las fluctuaciones en el perfil de concentración en plasma-tiempo. Tal suavización de los perfiles en plasma tiene el potencial de no sólo mejorar el efecto terapéutico del fármaco, sino también de reducir cualesquiera efectos secundarios no deseados. Una ventaja adicional de una formulación de liberación prolongada, particularmente importante para indicaciones de 5 oncología, es la mejora en la “calidad de vida” que da al suprimir el recordatorio diario de la enfermedad.
Con el fin de ganar la aceptación del paciente de tal implante o formulación de micropartículas sobre el tratamiento oral convencional, es importante que la formulación cause la mínima incomodidad en la inyección. Por tanto, sería sumamente 10 ventajoso administrar la dosis en una cantidad de formulación tan pequeña como sea posible, es decir, un bajo volumen de inyección de micropartículas o un pequeño tamaño del implante. Con el fin de conseguir esto a la dosis oral de 1 mg/día, se necesitaría que la formulación contuviera un alto porcentaje en peso de anastrozol. Sin embargo, el anastrozol tiene un peso molecular de 293,4 Daltons y una solubilidad en 15 agua de 0,53 mg/ml a 25ºC. Los compuestos de bajo peso molecular con tal solubilidad no se ajustan de manera ideal a la formación de formulaciones de liberación prolongada. Esto es debido a que se esperan típicamente niveles bajos de entrega de fármaco in vivo con grandes descargas de fármaco iniciales y periodos sólo cortos de liberación de fármaco para formulaciones de micropartículas o implantes que 20 comprenden tales compuestos. El efecto es potenciado cuando las formulaciones contienen altos niveles de fármaco y bajos niveles de polímero modificador de la velocidad. Además, muchos de los procedimientos de fabricación más establecidos que se usan para preparar formulaciones de micropartículas de liberación prolongada emplean disolventes acuosos. Para estos procedimientos, los compuestos solubles en 25 agua de bajo peso molecular, tales como el anastrozol, tienden a repartirse en estas fases acuosas durante el proceso de encapsulación, lo que conduce a eficacias de encapsulación deficientes y a cargas de fármaco bajas.
Los autores de la invención han encontrado, sorprendentemente, que es posible producir formulaciones de liberación prolongada de anastrozol usando 30 polilactida y copolímeros de poli(lactida-co-glicolida), que liberan anastrozol a lo largo de periodos de al menos 10 días, cuando se ponen en un entorno acuso de tipo fisiológico.
Según un primer aspecto de la presente invención, se proporciona una formulación de liberación prolongada que comprende: 35
(i) un polímero de polilactida o copolímero de poli(lactida-co-glicolida) que tiene un peso molecular medio de entre 5.000 Daltons y 50.000 Daltons;
(ii) una relación molar de lactida a glicolida de entre 100:0 y 50:50; y
(iii) de aproximadamente 10 a 55% en peso de anastrozol en base al peso total de la formulación, 5
en donde la formulación de liberación prolongada libera de manera continua anastrozol a lo largo de un periodo de al menos 10 días cuando se pone en un entorno acuso de tipo fisiológico.
Según un aspecto adicional de la presente invención, se proporciona una formulación de liberación prolongada que comprende: 10
(i) un polímero de polilactida o copolímero de poli(lactida-co-glicolida) que tiene un peso molecular medio de entre 5.000 Daltons y 50.000 Daltons;
(ii) una relación de lactida a glicolida de entre 100:0 y 50:50; y
(iii) de aproximadamente 10 a 55% en peso de anastrozol en base al peso total de la formulación; 15
en donde
(i) para cargas de anastrozol a las relaciones de lactida a glicolida dadas en la tabla que se muestra a continuación, el peso molecular medio del polímero está por encima de la cifra dada en la tabla:
Lactida/Glicolida
Carga
Peso molecular medio
50:50 - 65:35
>=10%
>15.000
50:50 - 65:35
>20%
>25.000
65:35
>30%
>45.000
66:34 - 75:25
>20%
>15.000
66:34 - 75:25
>30%
>40.000
76:24 - 85:15
>20%
>10.000
76:24 - 85:15
>30%
>30.000
85:15
>40%
>45.000
86:14 - 95:5
>20%
>10.000
86:14 - 95:5
>30%
>15.000
86:14 - 95:5
>35%
>30.000
86:14 - 95:5
>40%
>40.000
96:4 - 100/0
>30%
>17.000
96:4 - 100/0
>40 %
>35.000
20
y
(ii) para cargas de anastrozol por encima de 30% la relación lactida/glicolida es 65:35 o superior, y para cargas de anastrozol por encima de 40% la relación lactida/glicolida es 85:15 o superior.
Según un aspecto adicional de la presente invención, se proporciona una 5 formulación de liberación prolongada que comprende:
(i) un polímero de polilactida o copolímero de poli(lactida-co-glicolida) que tiene un peso molecular medio de entre 5.000 Daltons y 50.000 Daltons;
(ii)...
Reivindicaciones:
1. Una formulación de liberación prolongada, que comprende;
(i) un polímero de polilactida o copolímero de poli(lactida-co-glicolida) que tiene un peso molecular medio de entre 5.000 Daltons y 50.000 Daltons; 5
(ii) una relación molar de lactida a glicolida de entre 100:0 y 50:50; y
(iii) de aproximadamente 10 a 55% en peso de anastrozol en base al peso total de la formulación;
en donde la formulación de liberación prolongada libera de manera continua anastrozol a lo largo de un periodo de al menos 10 días cuando se pone en un 10 entorno acuso de tipo fisiológico.
2. Una formulación de liberación prolongada según la reivindicación 1, en donde la formulación de liberación prolongada es un implante monolítico.
15
3. Una formulación de liberación prolongada según la reivindicación 1, en donde la formulación de liberación prolongada es una formulación de micropartículas.
4. Una formulación de implante monolítico de liberación prolongada, que comprende:
(i) un polímero de polilactida o copolímero de poli(lactida-co-glicolida) que tiene un 20 peso molecular medio de entre 5.000 Daltons y 50.000 Daltons;
(ii) una relación molar de lactida a glicolida de entre 100:0 y 50:50;
(iii) de aproximadamente 10 a 65% en peso de anastrozol en base al peso total de la formulación;
en donde la formulación de liberación prolongada es un implante monolítico, y en 25 donde el peso molecular medio mínimo del polímero se puede calcular a partir de la ecuación que se muestra a continuación:
en la que
fA es la fracción de anastrozol, en donde 1,0 es 100%, es decir, 5% se 30 expresaría como 0,05; y
fG es la fracción de glicolida, en donde 1,0 es 100%, es decir, 50% se expresaría como 0,50.
5. Una formulación de micropartículas de liberación prolongada, que comprende:
(i) un polímero de polilactida o copolímero de poli(lactida-co-glicolida) que tiene un peso molecular medio de entre 5.000 Daltons y 50.000 Daltons;
(ii) una relación molar de lactida a glicolida de entre 100:0 y 50:50; y 5
(iii) de aproximadamente 10 a 55% en peso de anastrozol en base al peso total de la formulación
en donde la formulación de liberación prolongada es una formulación de micropartículas, y en donde el peso molecular medio mínimo del polímero se puede calcular a partir de la ecuación que se muestra a continuación: 10
en la que
fA es la fracción de anastrozol, en donde 1,0 es 100%, es decir, 5% se expresaría como 0,05; y
fG es la fracción de glicolida, en donde 1,0 es 100%, es decir, 50% se 15 expresaría como 0,50.
6. Una formulación de liberación prolongada según una cualquiera de las reivindicaciones precedentes, en la que la relación molar de lactida a glicolida está entre 100:0 y 95:5. 20
7. Una formulación de liberación prolongada según una cualquiera de las reivindicaciones precedentes, en la que el polímero de polilactida o el copolímero de poli(lactida-co-glicolida) tiene un peso molecular medio ponderal de entre 8.000 Daltons y 45.000 Daltons. 25
8. Una formulación de implante monolítico de liberación prolongada según la reivindicación 2 o la reivindicación 4, en la que el polímero de polilactida o el copolímero de poli(lactida-co-glicolida) tiene un peso molecular medio ponderal de entre 15.000 Daltons y 30.000 Daltons y la relación molar de lactida a glicolida 30 está entre 100:0 y 95:5.
9. Una formulación de implante monolítico de liberación prolongada según la reivindicación 8 cuando es dependiente de la reivindicación 4, en donde la
formulación comprende de aproximadamente 10 a 60% en peso, en base al peso total de la formulación, de anastrozol.
10. Una formulación de micropartículas de liberación prolongada según la reivindicación 3 o la reivindicación 5, en la que el polímero de polilactida o el 5 copolímero de poli(lactida-co-glicolida) tiene un peso molecular medio ponderal de entre 10.000 Daltons y 35.000 Daltons y la relación molar de lactida a glicolida está entre 100:0 y 95::5.
11. Una formulación de micropartículas de liberación prolongada según la 10 reivindicación 10, en donde la formulación comprende de aproximadamente 10 a 30% en peso, en base al peso total de la formulación, de anastrozol.
12. El uso de una formulación de liberación prolongada según una cualquiera de las reivindicaciones 1 a 11 en la fabricación de un medicamento para el tratamiento de 15 una dolencia, preferiblemente cáncer de mama, tratable por anastrozol en un animal de sangre caliente.
13. Un procedimiento para la preparación de una formulación de implante monolítico según una cualquiera de las reivindcaciones 2 ó 4, que comprende las etapas: 20
(i) preparar una disolución o dispersión de anastrozol en una disolución que comprende el polímero de polilactida o poli(lactida-co-glicolida) y un disolvente orgánico adecuado;
(ii) retirar sustancialmente todo el disolvente orgánico de la disolución o dispersión formada en la etapa (i); y 25
(iii) conformar el producto de la etapa (ii) en un implante monolítico de las dimensiones requeridas.
14. Un procedimiento para la preparación de una formulación de implante monolítico según la reivindicación 2, que comprende las etapas: 30
(i) preparar una mezcla de anastrozol y el polímero de polilactida o poli(lactida-co-glicolida);
(ii) conformar la mezcla en un implante monolítico de las dimensiones requeridas.
15. Un procedimiento para la preparación de una formulación de micropartículas según la reivindicación 3, que comprende las etapas:
(i) preparar una disolución o dispersión de anastrozol en una disolución que comprende el polímero de polilactida o poli(lactida-co-glicolida) y un disolvente orgánico adecuado; 5
(ii) dispersar la disolución preparada en (i) en un medio de proceso acuoso para formar una emulsión aceite en agua;
(iii) retirar sustancialmente todo el disolvente orgánico de la emulsión formada en la etapa (ii) para formar micropartículas; y
(iv) lavar y secar las micropartículas. 10
Patentes similares o relacionadas:
FORMULACIONES DE LIBERACIÓN PROLONGADA DE ILOPERIDONA Y POLÍMERO EN FORMA DE ESTRELLA, del 10 de Mayo de 2011, de NOVARTIS AG: Una formulación de liberación prolongada que comprende iloperidona y un polímero biodegradable, biocompatible que es un polímero de poli(d,l-lactida-co-glicolida) […]
COMPOSICIONES POLIHIDROXIALCANOATO QUE TIENEN TASAS DE DEGRADACIÓN CONTROLADAS, del 7 de Abril de 2011, de METABOLIX, INC.: Un stent que comprende un copolímero poli(4-hidroxibutirato) o un copolímero poli(butirato-cohidroalcanoato) del mismo, donde el hidroxialcanota […]
 PROCEDIMIENTO PARA LA PREPARACIÓN DE PARTÍCULAS A PARTIR DE UNA EMULSIÓN EN CO2 SUPERCRÍTICO O LÍQUIDO, del 26 de Enero de 2011, de INSTITUT NATIONAL DE LA SANTE ET DE LA RECHERCHE MEDICALE (INSERM): Procedimiento para la preparación de partículas que comprende las etapas que consisten en: i) preparar una emulsión que contiene: - como fase continua, CO2 líquido o supercrítico, […]
PROCEDIMIENTO PARA LA PREPARACIÓN DE PARTÍCULAS A PARTIR DE UNA EMULSIÓN EN CO2 SUPERCRÍTICO O LÍQUIDO, del 26 de Enero de 2011, de INSTITUT NATIONAL DE LA SANTE ET DE LA RECHERCHE MEDICALE (INSERM): Procedimiento para la preparación de partículas que comprende las etapas que consisten en: i) preparar una emulsión que contiene: - como fase continua, CO2 líquido o supercrítico, […]
PREPARACION DE LIBERACION SOSTENIDA DE UN COMPUESTO MACROLIDO COMO TACROLIMUS, del 27 de Julio de 2010, de FUJISAWA PHARMACEUTICAL CO., LTD.: Formulación de liberación sostenida de un compuesto macrólido, en la que el tiempo (T63,2%) requerido para que se disuelva el 63,2% de la cantidad máxima […]
MICROPARTICULAS QUE COMPRENDEN ANALOGOS DE SOMATOSTATINA, del 14 de Mayo de 2010, de NOVARTIS AG NOVARTIS PHARMA GMBH: Micropartículas que comprenden ciclo[{4-(NH2-C2H4-NH-CO-O-)Pro}-Phg-DTrp-Lys-Tyr(4-Bzl)-Phe] en forma libre, en forma de sal o en forma protegida, embebido en una matriz de […]
 IMPLANTES SUBCUTANEOS QUE LIBERAN UN PRINCIPIO ACTIVO DURANTE UN PERIODO DE TIEMPO PROLONGADO, del 23 de Abril de 2010, de MEDIOLANUM PHARMACEUTICALS LIMITED: Implantes subcutáneos obtenidos mediante extrusión, que contienen: micropartículas que contienen un ingrediente activo dispersado en una matriz de […]
IMPLANTES SUBCUTANEOS QUE LIBERAN UN PRINCIPIO ACTIVO DURANTE UN PERIODO DE TIEMPO PROLONGADO, del 23 de Abril de 2010, de MEDIOLANUM PHARMACEUTICALS LIMITED: Implantes subcutáneos obtenidos mediante extrusión, que contienen: micropartículas que contienen un ingrediente activo dispersado en una matriz de […]
 COMPOSICION FARMACEUTICA DE MICROESFERAS PARA PREVENIR LA AMPUTACION DE PIE DIABETICO, del 14 de Diciembre de 2009, de CENTRO DE INGENIERIA GENETICA Y BIOTECNOLOGIA: Una composición farmacéutica que contiene microesferas cargadas con Factor de Crecimiento Epidérmico para ser administrada por viaparenteral […]
COMPOSICION FARMACEUTICA DE MICROESFERAS PARA PREVENIR LA AMPUTACION DE PIE DIABETICO, del 14 de Diciembre de 2009, de CENTRO DE INGENIERIA GENETICA Y BIOTECNOLOGIA: Una composición farmacéutica que contiene microesferas cargadas con Factor de Crecimiento Epidérmico para ser administrada por viaparenteral […]
AGENTES PARA EL TRATAMIENTO DE LA RETINOPATÍA GLAUCOMATOSA Y DE LA NEUROPATÍA ÓPTICA, del 30 de Diciembre de 2011, de NOVARTIS AG: Composición para el tratamiento de la retinopatía glaucomatosa o de la neuropatía óptica en un sujeto en la que la composición proporciona una concentración […]