COMPOSICION FARMACEUTICA DE LIBERACION SOSTENIDA DE SOMATOSTATINA O UN ANALOGO SUYO.
Composición farmacéutica de liberación sostenida de somatostatina o un análogo suyo.
Composición farmacéutica de somatostatina, o un análogo de somatostatina, de liberación sostenida para su uso en el tratamiento y/o prevención de la diarrea y su uso en la preparación de un medicamento para el tratamiento y/o prevención de la diarrea
Tipo: Patente de Invención. Resumen de patente/invención. Número de Solicitud: P200703103.
Solicitante: GP PHARM S.A.
Nacionalidad solicitante: España.
Provincia: BARCELONA.
Inventor/es: GARCES GARCES, JOSEP, PARENTE DUEA,ANTONIO, MIS VIZCAINO, RICARD, SAVULSKY,CLAUDIO.
Fecha de Solicitud: 23 de Noviembre de 2007.
Fecha de Publicación: .
Fecha de Concesión: 4 de Mayo de 2010.
Clasificación Internacional de Patentes:
- A61K38/31 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 38/00 Preparaciones medicinales que contienen péptidos (péptidos que contienen ciclos beta-lactama A61K 31/00; dipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina 2,5-dionas, A61K 31/00; péptidos basados en la ergolina A61K 31/48; que contienen compuestos macromoleculares que tienen unidades aminoácido repartidas estadísticamente A61K 31/74; preparaciones medicinales que contienen antígenos o anticuerpos A61K 39/00; preparaciones medicinales caracterizadas por los ingredientes no activos, p. ej. péptidos como soportes de fármacos, A61K 47/00). › Somatostatinas.
- A61K9/50 A61K […] › A61K 9/00 Preparaciones medicinales caracterizadas por un aspecto particular. › Microcápsulas (A61K 9/52 tiene prioridad).
Clasificación PCT:
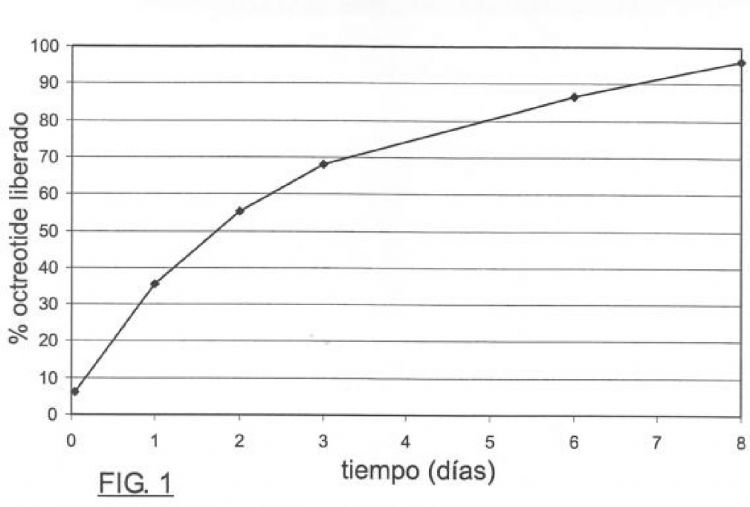
Fragmento de la descripción:
Composición farmacéutica de liberación sostenida de somatostatina o un análogo suyo.
Campo de la invención
La presente invención se encuadra en general dentro del campo de la biomedicina y en particular, se refiere al uso de una composición farmacéutica de somatostatina, o un análogo suyo, de liberación sostenida durante una semana aproximadamente.
Antecedentes de la invención
Se sabe desde hace tiempo que la diarrea es uno de los efectos secundarios asociados a la quimioterapia y a la radioterapia abdominal y/o pélvica en el tratamiento del cáncer y que este efecto secundario conlleva en numerosos casos la hospitalización del paciente y la reducción de la dosis del tratamiento e incluso a la interrupción del tratamiento si supone un peligro para la vida del paciente debido a la deshidratación y pérdida de electrolitos (Journal of Clinical Oncology, 2004, 22(14), 2918-26).
Más de la mitad de los enfermos tratados con 5-fluorouracilo, cisplatino, irinotecan, capecitabina, leucovorina, tegafur, ciclofosfamida o metotrexato, entre otros agentes quimioterapéuticos, o sometidos a radioterapia abdominal y/o pélvica padecen de diarrea (Annals of Oncology, 2001, 12(2), 227-9), y en particular de diarrea severa en grado 3-4 (según National Cancer Institute Common Toxicity Criteria) a partir de las 8 horas posteriores a la administración de los agentes quimioterapéuticos o de la aplicación de la radioterapia.
Una vez iniciado el tratamiento de la diarrea severa asociada a la quimioterapia o a la radioterapia abdominal y/o pélvica, su duración, en la mayoría de los casos, no se extiende más allá de una semana.
Se conoce en el estado de la técnica que la administración de derivados de somatostatina previa, simultánea o posterior a la administración de agentes quimioterapéuticos o radioterapia pélvica sirve para parar o reducir la intensidad de la diarrea asociada a estos agentes o a la radioterapia (International Journal of Radiation Oncology, Biology, Physics, 2002, 54(1), 195-202). Así por ejemplo los documentos US 6395708 B1 y US 6159935 B1 se refieren a un método de prevención de la diarrea causada por la administración de irinotecan que comprende la administración de octreotide. De acuerdo con la descripción, el acetato de octreotide se administra en la forma de la composición de liberación lenta de octreotide Sandostatin LAR® (liberación depot de 1 mes).
En particular, el documento US 6214792 B1 describe un método de tratamiento de la diarrea aguda y severa que comprende la administración de octreotide en una cantidad suficiente para aliviar la diarrea sin provocar bradicardia. Según la descripción el octreotide se administra parenteralmente cada 12 horas conjuntamente con un agente anticolinérgico.
El documento WO 02/074042 A2 describe una preparación que comprende una epotilona para el tratamiento de tumores sólidos y un agente antidiarreico para el tratamiento de la diarrea asociada a la administración de epotilonas. Entre los agentes antidiarreicos se menciona el octreotide, administrado bien como una composición de liberación inmediata o bien como la composición de liberación lenta de octreotide Sandostatin LAR® (liberación depot de 1 mes).
Además, los documentos WO 2005/117830 A1 y WO 2006/075124 A1 describen una preformulación de liberación lenta, no polimérica, que comprende octreotide, diacil glicerol, fosfatidilcolina y un disolvente orgánico. Esta formulación puede utilizarse para el tratamiento de la diarrea inducido por la quimioterapia y se administra cada 20-90 días. Si bien, excepcionalmente, la preformulación con octreotide se puede administrar cada 2-8 semanas en el tratamiento de tumores avanzados.
Asimismo, existen otros documentos que mencionan la administración de octreotide junto con otros principios activos para el tratamiento de la diarrea. Así por ejemplo, el documento WO 2005/105080 A1 se refiere a un método de tratamiento de la diarrea en un paciente con cáncer que comprende la administración de una amida del ácido 3-[4-bromo-2,6-difluorobenziloxi)-5-(3-(4-pirrolidin-1-il-butil)-ureidoj-isotiazol-4-carboxílico conjuntamente con octreotide, entre otros agentes antidiarreicos. Según ese documento, la administración de octreotide puede realizarse mediante una composición de liberación sostenida oral, cápsulas orales, polvos y soluciones orales, o bien mediante inyección parenteral como solución, suspensión o emulsión.
Por otro lado, el documento EP 1040829 A2 describe una composición farmacéutica que comprende octreotide y un inhibidor de la fosfodiesterasa PDE-4 para tratar o prevenir la estasis resultado de la hipomotilidad en el estómago causada por un agente terapéutico que produce hipomotilidad gástrica o desórdenes gastrointestinales.
El documento WO 99/11277 A1 describe un método de aliviar un desorden gastrointestinal, entre los que se encuentran la diarrea y la diarrea aguda, y que comprende la supresión de la secreción gástrica y adicionalmente el tratamiento con un agente antidiarreico como es ef octreotide, donde éste se administra en una formulación de liberación inmediata. Igualmente, el documento WO 2004/006902 A1 describe una composición para prevenir o tratar un desorden gastrointestinal que comprende un amino-éter y/o amino-éster y un inhibidor de la secreción gástrica, entre los que se menciona el octreotide, administrado bien como una composición de liberación inmediata o bien como la composición de liberación lenta de octreotide Sandostatin LAR® (liberación depot de 1 mes).
Finalmente, se conocen en el estado de la técnica el uso de octreotide para aliviar y/o eliminar la diarrea asociada a otras patologías y/o trastornos. Así por ejemplo los documentos US 5789411 A, US 5919760 A y WO 99/63935 A2 se refieren a la administración de octreotide para suprimir o aliviar la diarrea asociada a un método de desintoxicación de narcóticos, y donde la administración de octreotide se realiza cada 12 horas.
Por otro lado se sabe del uso de octreotide para aliviar y/o eliminar la diarrea en grado 3-4 como uno de los síntomas del SIDA (AIDS, 1991, 5(6), 765-7; Scandinavian Journal of Infectious Diseases, 1994, 26(1), 55-7), de la diarrea en grado 3-4 asociada a la enfermedad del injerto contra el huésped gastrointestinal aguda (Journal of Pediatric Hematology/Oncology, 2000, 22(4), 344-50), o de la diarrea asociada a otros desórdenes gastrointestinales como colitis ulcerosa, colitis colagenosa, colitis microscópica, colitis linfocítica, enfermedad de Crohn o diarreas de origen infeccioso vírico o bacteriano.
Las composiciones mencionadas anteriormente de octreotide de liberación inmediata y de liberación lenta son composiciones comerciales. Entre las composiciones de liberación inmediata destaca la comercializa bajo la marca Sandostatin®, que se obtiene como se describe en el documento GB 2208200 A, esto es, una composición farmacéutica de liberación inmediata que comprende un tampón de ácido láctico y un análogo de somatostatina como es el octreotide. Entre las composiciones de liberación lenta, destaca la composición comercializada bajo la marca Sandostatin LAR®, se obtiene y administra como se describe en el documento GB 2265311 A, esto es, una composición de liberación lenta de octreotide en un soporte polimérico biodegradable y biocompatible. Según se afirma en ese documento, la biodeg-radación del- polímero alcanza desde varias semanas a uno o dos meses, lo que hace la composición adecuada para una formulación de liberación a lo largo de un mes. En todos los ejemplos de dicho documento se observa que se midieron niveles de octreotide en plasma de 0,5 ng/ml como mínimo durante 21 días, llegando incluso hasta 42 días según otros ejemplos.
Además, el documento WO 2007/071395 A1 describe composiciones de liberación sostenida de octreotide con dos o más polímeros poliláctico-co-glicólico (PLGA), donde la liberación de principio activo se extiende un período de más de 3 meses, preferiblemente entre 3 y 6 meses.
Tal como se ha mencionado anteriormente, la diarrea severa en grado 3-4 asociada a la quimioterapia tiene una duración de aproximadamente una semana en la mayoría de los casos. Sin embargo, no se había planteado la necesidad de composiciones farmacéuticas de octreotide de liberación únicamente durante una semana aproximadamente. Es por esto que las composiciones farmacéuticas de octreotide conocidas en el estado de...
Reivindicaciones:
1. Composición de microcápsulas de copolímero láctico-co-glicólico (PLGA) o copolímero láctico-co-glicólico y polietilenglicol (PLGA-PEG) comprendiendo somatostatina, o un análogo de somatostatina, para uso en el tratamiento y/o prevención de la diarrea, caracterizado porque las microcápsulas de PLGA o PLGA-PEG liberan sostenidamente una cantidad terapéuticamente eficaz de somatostatina, o un análogo de somatostatina, durante un período de entre 3 y 10 días desde su administración.
2. Composición de microcápsulas de copolímero láctico-co-glicólico (PLGA) o copolímero láctico-co-glicólico y polietilenglicol (PLGA-PEG) comprendiendo somatostatina, o un análogo de somatostatina, para uso en el tratamiento y/o prevención de la diarrea según la reivindicación 1, donde la diarrea se selecciona del grupo formado por diarrea asociada a la quimioterapia o asociada a la radioterapia abdominal- y/o pélvica en el tratamiento del cáncer, diarrea como uno de los síntomas del SIDA, diarrea asociada a la enfermedad del injerto contra el huésped gastrointestinal aguda, diarrea asociada a colitis ulcerosa, colitis colagenosa, colitis microscópica, colitis linfocítica, enfermedad de Crohn, diarreas de origen infeccioso vírico y diarreas de origen bacteriano.
3. Composición de microcápsulas de copolímero láctico-co-glicólico (PLGA) o copolímero láctico-co-glicólico y polietilenglicol (PLGA-PEG) comprendiendo somatostatina, o un análogo de somatostatina, para uso en el tratamiento y/o prevención de la diarrea según la reivindicación 2, donde la diarrea se selecciona del grupo formado por diarrea en grado 3-4 asociada a la quimioterapia o asociada a la radioterapia abdominal y/o pélvica en el tratamiento del cáncer, diarrea en grado 3-4 como uno de los síntomas del SIDA y diarrea en grado 3-4 asociada a la enfermedad del injerto contra el huésped gastrointestinal aguda.
4. Composición de microcápsulas de copolímero láctico-co-glicólico (PLGA) o copolímero láctico-co-glicólico y polietilenglicol (PLGA-PEG) comprendiendo somatostatina, o un análogo de somatostatina, para uso en el tratamiento y/o prevención de la diarrea según cualquiera de las reivindicaciones anteriores, donde las microcápsulas de PLGA-PEG comprenden copolímeros diblock PLGA-PEG o triblock con las estructuras PLGA-PEG-PLGA o PEG-PLGA-PEG.
5. Composición de microcápsulas de copolímero láctico-co-glicólico (PLGA) o copolímero láctico-co-glicólico y polietilenglicol (PLGA-PEG) comprendiendo somatostatina, o un análogo de somatostatina, para uso en el tratamiento y/o prevención de la diarrea según cualquiera de las reivindicaciones anteriores, donde las microcápsulas de PLGA-PEG comprenden entre un 1% y un 50% en peso de polietilenglicol.
6. Composición de microcápsulas de copolímero láctico-co-glicólico (PLGA) o copolímero láctico-co-glicólico y polietilenglicol (PLGA-PEG) comprendiendo somatostatina, o un análogo de somatostatina, para uso en el tratamiento y/o prevención de la diarrea según cualquiera de las reivindicaciones anteriores, donde en las microcápsulas de PLGA o PLGA-PEG el ratio entre las unidades de lactato y glicolato está comprendido entre un 25% de lactato y 25% de glicolato.
7. Composición de microcápsulas de copolímero láctico-co-glicólico (PLGA) o copolímero láctico-co-glicólico y polietilenglicol (PLGA-PEG) comprendiendo somatostatina, o un análogo de somatostatina, para uso en el tratamiento y/o prevención de la diarrea según cualquiera de las reivindicaciones anteriores, donde las microcápsulas de PLGA o PLGA-PEG tienen un peso molecular inferior a 100.000 Daltons.
8. Composición de microcápsulas de copolímero láctico-co-glicólico (PLGA) o copolímero láctico-co-glicólico y polietilenglicol (PLGA-PEG) comprendiendo somatostatina, o un análogo de somatostatina, para uso en el tratamiento y/o prevención de la diarrea según cualquiera de las reivindicaciones anteriores, donde las microcápsulas de PLGA o PLGA-PEG incorporan de un 0,1% a un 25% en peso de ésteres del ácido cítrico.
9. Composición de microcápsulas de copolímero láctico-co-glicólico (PLGA) o copolímero láctico-co-glicólico y polietilenglicol (PLGA-PEG) comprendiendo somatostatina, o un análogo de somatostatina, para uso en el tratamiento y/o prevención de la diarrea según la reivindicación 8, donde el éster del ácido cítrico se selecciona del grupo formado por trietil citrato, acetil trietil citrato, tributil citrato, acetil tributil citrato, trimetil citrato, trihexil citrato, acetil trihexil citrato, trioctil citrato, acetil trioctil citrato o sus mezclas.
10. Composición de microcápsulas de copolímero láctico-co-glicólico (PLGA) o copolímero láctico-co-glicólico y polietilenglicol (PLGA-PEG) comprendiendo somatostatina, o un análogo de somatostatina, para uso en el tratamiento y/o prevención de la diarrea según cualquiera de las reivindicaciones anteriores, donde la somatostatina, o un análogo de somatostatina, se selecciona del grupo formado por octreotide, vapreotide, lanreotida, somatostatina, seglitide, cortistatina, pasireotida o una o varias de las sales farmacéuticamente aceptables de estos compuestos.
11. Composición de microcápsulas de copolímero láctico-co-glicólico (PLGA) o copolímero láctico-co-glicólico y polietilenglicol (PLGA-PEG) comprendiendo somatostatina, o un análogo de somatostatina, para uso en el tratamiento y/o prevención de la diarrea según la reivindicación 10, donde la somatostatina, o un análogo de somatostatina, se selecciona del grupo formado por acetato de octreotide, acetato de somatostatina o acetato de lanreotida.
12. Composición de microcápsulas de copolimero láctico-co-glicólico (PLGA) o copolímero láctico-co-glicólico y polietilenglicol (PLGA-PEG) comprendiendo somatostatina, o un análogo de somatostatina, para uso en el tratamiento y/o prevención de la diarrea según cualquiera de las reivindicaciones anteriores, donde la cantidad terapéuticamente eficaz de somatostatina, o un análogo de somatostatina, está comprendida entre un 0,05% y un 70% en peso de polímero de PLGA o PLGA-PEG.
13. Composición de microcápsulas de copolímero láctico-co-glicólico (PLGA) o copolímero láctico-co-glicólico y polietilenglicol (PLGA-PEG) comprendiendo somatostatina, o un análogo de somatostatina, para uso en el tratamiento y/o prevención de la diarrea según cualquiera de las reivindicaciones anteriores, donde la somatostatina, o un análogo de somatostatina, se administra en una dosis equivalente a entre 0,10 y 12 mg de octreotide.
14. Composición de microcápsulas de copolimero láctico-co-glicólico (PLGA) o copolímero láctico-co-glicólico y polietilenglicol (PLGA-PEG) comprendiendo somatostatina, o un análogo de somatostatina, para uso en el tratamiento y/o prevención de la diarrea según cualquiera de las reivindicaciones 1 a 12, donde la somatostatina, o un análogo de somatostatina, se administra en una dosis equivalente a entre 0,10 y 80 mg de somatostatina.
15. Composición de microcápsulas de copolímero láctico-co-glicólico (PLGA) o copolímero láctico-co-glicólico y polietilenglicol (PLGA-PEG) comprendiendo somatostatina, o un análogo de somatostatina, para uso en el tratamiento y/o prevención de la diarrea según cualquiera de las reivindicaciones 1 a 12, donde la somatostatina, o un análogo de somatostatina, se administra en una dosis equivalente a entre 0,10 y 50 mg de lanreotida.
16. Composición de microcápsulas de copolímero láctico-co-glicólico (PLGA) o copolímero láctico-co-glicólico y polietilenglicol (PLGA-PEG) comprendiendo somatostatina, o un análogo de somatostatina, para uso en el tratamiento y/o prevención de la diarrea según cualquiera de las reivindicaciones anteriores, donde la liberación sostenida de somatostatina, o un análogo de somatostatina, dura un período de entre 5 a 8 días desde su administración.
17. Composición de microcápsulas de copolímero láctico-co-glicólico (PLGA) o copolímero láctico-co-glicólico y polietilenglicol (PLGA-PEG) comprendiendo somatostatina, o un análogo de somatostatina, para uso en el tratamiento y/o prevención de la diarrea según cualquiera de las reivindicaciones anteriores, donde la composición comprende al menos un agente auxiliar farmacéuticamente aceptable.
18. Composición de microcápsulas de copolímero láctico-co-glicólico (PLGA) o copolímero láctico-co-glicólico y polietilenglicol (PLGA-PEG) comprendiendo somatostatina, o un análogo de somatostatina, para uso en el tratamiento y/o prevención de la diarrea según la reivindicación 17, donde el agente auxiliar farmacéuticamente aceptable se selecciona del grupo formado por excipientes, espesantes, diluyentes, disolventes, dispersantes, agentes mejoradores de la liofilización o adyuvantes.
19. Composición de microcápsulas de copolímero láctico-co-glicólico (PLGA) o copolímero láctico-co-glicólico y polietilenglicol (PLGA-PEG) comprendiendo somatostatina, o un análogo de somatostatina, para uso en el tratamiento y/o prevención de la diarrea según cualquiera de las reivindicaciones anteriores, que comprende al menos un agente seleccionado del grupo formado por agentes anticolinérgicos, agentes antidiarreicos y agentes antieméticos.
20. Composición de microcápsulas de copolímero láctico-co-glicólico (PLGA) o copolímero láctico-co-glicólico y polietilenglicol (PLGA-PEG) comprendiendo somatostatina, o un análogo de somatostatina, para uso en el tratamiento y/o prevención de la diarrea según cualquiera de las reivindicaciones anteriores, donde la composición se administra en forma de suspensión o disolución estéril por vía parenteral subcutánea, intramuscular o intravenosa.
21. Composición de microcápsulas de copolímero láctico-co-glicólico (PLGA) o copolímero láctico-co-glicólico y polietilenglicol (PLGA-PEG) comprendiendo somatostatina, o un análogo de somatostatina, para uso en el tratamiento y/o prevención de la diarrea según cualquiera de las reivindicaciones anteriores, donde la composición se presenta en forma de dosis unitaria.
22. Composición de microcápsulas de copolímero láctico-co-glicólico (PLGA) o copolímero láctico-co-glicólico y polietilenglicol (PLGA-PEG) comprendiendo somatostatina, o un análogo de somatostatina, para uso en el tratamiento y/o prevención de la diarrea según la reivindicación 21, donde la composición de dosis unitaria se presenta en forma de polvo liofilizado que se reconstituye antes de su administración.
23. Composición de microcápsulas de copolímero láctico-co-glicólico (PLGA) o copolímero láctico-co-glicólico y polietilenglicol (PLGA-PEG) comprendiendo somatostatina, o un análogo de somatostatina, para uso en el tratamiento y/o prevención de la diarrea según la reivindicación 21, donde la composición de dosis unitaria se presenta como una suspensión o disolución estéril que forma in situ un implante sólido biodegradable y biocompatible.
24. Uso de una composición de microcápsulas de copolímero láctico-co-glicólico (PLGA) o copolímero láctico-co-glicólico y polietilenglicol (PLGA-PEG) comprendiendo somatostatina, o un análogo de somatostatina, en la preparación de un medicamento para el tratamiento y/o prevención de la diarrea, caracterizado porque las microcápsulas de PLGA o PLGA-PEG liberan sostenidamente una cantidad terapéuticamente eficaz de somatostatina, o un análogo de somatostatina, durante un período de entre 3 y 10 días desde la administración del medicamento.
25. Uso de una composición de microcápsulas de copolímero láctico-co-glicólico (PLGA) o copolímero láctico-co-glicólico y polietilenglicol (PLGA-PEG) comprendiendo somatostatina, o un análogo de somatostatina, en la preparación de un medicamento para el tratamiento y/o prevención de la diarrea según la reivindicación 24, donde la diarrea se selecciona del grupo formado por diarrea asociada a la quimioterapia o asociada a la radioterapia abdominal y/o pélvica en el tratamiento del cáncer, diarrea como uno de los síntomas del SIDA, diarrea asociada a la enfermedad del injerto contra el huésped gastrointestinal aguda, diarrea asociada a colitis ulcerosa, colitis colagenosa, colitis microscópica, colitis linfocítica, enfermedad de Crohn, diarreas de origen infeccioso vírico y diarreas de origen bacteriano.
26. Uso de una composición de microcápsulas de copolímero láctico-co-glicólico (PLGA) o copolímero láctico-co-glicólico y polietilenglicol (PLGA-PEG) comprendiendo somatostatina, o un análogo de somatostatina, en la preparación de un medicamento para el tratamiento y/o prevención de la diarrea según la reivindicación 25, donde la diarrea se selecciona del grupo formado por diarrea en grado 3-4 asociada a la quimioterapia o asociada a la radioterapia abdominal y/o pélvica en el tratamiento del cáncer, diarrea en grado 3-4 como uno de los síntomas del SIDA y diarrea en grado 3-4 asociada a la enfermedad del injerto contra el huésped gastrointestinal aguda.
27. Uso de una composición de microcápsulas de copolímero láctico-co-glicólico (PLGA) o copolímero láctico-co-glicólico y polietilenglicol (PLGA-PEG), comprendiendo somatostatina, o un análogo de somatostatina, en la preparación de un medicamento para el tratamiento y/o prevención de la diarrea según cualquiera de las reivindicaciones 24 a 26, donde las microcápsulas de PLGA-PEG comprenden copolímeros diblock PLGA-PEG o triblock con las estructuras PLGA-PEG-PLGA o PEG-PLGA-PEG.
28. Uso de una composición de microcápsulas de copolímero láctico-co-glicólico (PLGA) o copolímero láctico-co-glicólico y polietilenglicol (PLGA-PEG) comprendiendo somatostatina, o un análogo de somatostatina, en la preparación de un medicamento para el tratamiento y/o prevención de la diarrea según cualquiera de las reivindicaciones 24 a 27, donde las microcápsulas de PLGA-PEG comprenden entre un 1% y un 50% en peso de polietilenglicol.
29. Uso de una composición de microcápsulas de copolímero láctico-co-glicólico (PLGA) o copolímero láctico-co-glicólico y polietilenglicol (PLGA-PEG) comprendiendo somatostatina, o un análogo de somatostatina, en la preparación de un medicamento para el tratamiento y/o prevención de la diarrea según cualquiera de las reivindicaciones 24 a 28, donde en las microcápsulas de PLGA o PLGA-PEG el ratio entre las unidades de lactato y glicolato está comprendido entre un 25% de lactato y 25% de glicolato.
30. Uso de una composición de microcápsulas de copolímero láctico-co-glicólico (PLGA) o copolímero láctico-co-glicólico y polietilenglicol (PLGA-PEG) comprendiendo somatostatina, o un análogo de somatostatina, en la preparación de un medicamento para el tratamiento y/o prevención de la diarrea según cualquiera de las reivindicaciones 24 a 29, donde las microcápsulas de PLGA o PLGA-PEG tienen un peso molecular inferior a 100.000 Daltons.
31. Uso de una composición de microcápsulas de copolímero láctico-co-glicólico (PLGA) o copolímero láctico-co-glicólico y polietilenglicol (PLGA-PEG) comprendiendo somatostatina, o un análogo de somatostatina, en la preparación de un medicamento para el tratamiento y/o prevención de la diarrea según cualquiera de las reivindicaciones 24 a 30, donde las microcápsulas de PLGA o PLGA-PEG incorporan de un 0,1% a un 25% en peso de ésteres del ácido cítrico.
32. Uso de una composición de microcápsulas de copolímero láctico-co-glicólico (PLGA) o copolímero láctico-co-glicólico y polietilenglicol (PLGA-PEG) comprendiendo somatostatina, o un análogo de somatostatina, en la preparación de un medicamento para el tratamiento y/o prevención de la diarrea según la reivindicación,31 donde el éster del ácido cítrico se selecciona del grupo formado por trietil citrato, acetil trietil citrato, tributil citrato, acetil tributil citrato, trimetil citrato, trihexil citrato, acetil trihexil citrato, trioctil citrato, acetil trioctil citrato o sus mezclas.
33. Uso de una composición de microcápsulas de copolímero láctico-co-glicólico (PLGA) o copolímero láctico-co-glicólico y polietilenglicol (PLGA-PEG) comprendiendo somatostatina, o un análogo de somatostatina, en la preparación de un medicamento para el tratamiento y/o prevención de la diarrea según cualquiera de las reivindicaciones 24 a 32, donde la somatostatina, o un análogo de somatostatina, se selecciona del grupo formado por octreotide, vapreotide, lanreotida, somatostatina, seglitide, cortistatina, pasireotida o una o varias de las sales farmacéuticamente aceptables de estos compuestos.
34. Uso de una composición de microcápsulas de copolímero láctico-co-glicólico (PLGA) o copolímero láctico-co-glicólico y polietilenglicol (PLGA-PEG) comprendiendo somatostatina, o un análogo de somatostatina, en la preparación de un medicamento para el tratamiento y/o prevención de la diarrea según la reivindicación 33, donde la somatostatina, o un análogo de somatostatina, se selecciona del grupo formado por acetato de octreotide, acetato de somatostatina o acetato de lanreotida.
35. Uso de una composición de microcápsulas de copolímero láctico-co-glicólico (PLGA) o copolímero láctico-co-glicólico y polietilenglicol (PLGA-PEG) comprendiendo somatostatina, o un análogo de somatostatina, en la preparación de un medicamento para el tratamiento y/o prevención de la diarrea según cualquiera de las reivindicaciones 24 a 34, donde la cantidad terapéuticamente eficaz de somatostatina, o un análogo de somatostatina, está comprendida entre un 0,05% y un 70% en peso de polímero de PLGA o PLGA-PEG.
36. Uso de una composición de microcápsulas de copolímero láctico-co-glicólico (PLGA) o copolímero láctico-co-glicólico y polietilenglicol (PLGA-PEG) comprendiendo somatostatina, o un análogo de somatostatina, en la preparación de un medicamento para el tratamiento y/o prevención de la diarrea según cualquiera de las reivindicaciones 24 a 35, donde la somatostatina, o un análogo de somatostatina, se administra en una dosis equivalente a entre 0,10 y 12 mg de octreotide.
37. Uso de una composición de microcápsulas de copolímero láctico-co-glicólico (PLGA) o copolímero láctico-co-glicólico y polietilenglicol (PLGA-PEG) comprendiendo somatostatina, o un análogo de somatostatina, en la preparación de un medicamento para el tratamiento y/o prevención de la diarrea según cualquiera de las reivindicaciones 24 a 35, donde la somatostatina, o un análogo de somatostatina, se administra en una dosis equivalente a entre 0,10 y 80 mg de somatostatina.
38. Uso de una composición de microcápsulas de copolímero láctico-co-glicólico (PLGA) o copolímero láctico-co-glicólico y polietilenglicol (PLGA-PEG) comprendiendo somatostatina, o un análogo de somatostatina, en la preparación de un medicamento para el tratamiento y/o prevención de la diarrea según cualquiera de las reivindicaciones 24 a 35, donde la somatostatina, o un análogo de somatostatina, se administra en una dosis equivalente a entre 0,10 y 50 mg de lanreotida.
39. Uso de una composición de microcápsulas de copolímero láctico-co-glicólico (PLGA) o copolímero láctico-co-glicólico y polietilenglicol (PLGA-PEG) comprendiendo somatostatina, o un análogo de somatostatina, en la preparación de un medicamento para el tratamiento y/o prevención de la diarrea según cualquiera de las reivindicaciones 24 a 38, donde la liberación sostenida de somatostatina, o un análogo de somatostatina, dura un período de entre 5 a 8 días desde la administración del medicamento.
40. Uso de una composición de microcápsulas de copolímero láctico-co-glicólico (PLGA) o copolímero láctico-co-glicólico y polietilenglicol (PLGA-PEG) comprendiendo somatostatina, o un análogo de somatostatina, en la preparación de un medicamento para el tratamiento y/o prevención de la diarrea según cualquiera de las reivindicaciones 24 a 39, donde la composición comprende al menos un agente auxiliar farmacéuticamente aceptable.
41. Uso de una composición de microcápsulas de copolímero láctico-co-glicólico (PLGA) o copolímero láctico-co-glicólico y polietilenglicol (PLGA-PEG) comprendiendo somatostatina, o un análogo de somatostatina, en la preparación de un medicamento para el tratamiento y/o prevención de la diarrea según la reivindicación 40, donde el agente auxiliar farmacéuticamente aceptable se selecciona del grupo formado por excipientes, espesantes, diluyentes, disolventes, dispersantes, agentes mejoradores de la liofilización o adyuvantes.
42. Uso de una composición de microcápsulas de copolímero láctico-co-glicólico (PLGA) o copolímero láctico-co-glicólico y polietilenglicol (PLGA-PEG) comprendiendo somatostatina, o un análogo de somatostatina, en la preparación de un medicamento para el tratamiento y/o prevención de la diarrea según cualquiera de las reivindicaciones 24 a 41, que comprende al menos un agente seleccionado del grupo formado por agentes anticolinérgicos, agentes antidiarreicos y agentes antieméticos.
43. Uso de una composición de microcápsulas de copolímero láctico-co-glicólico (PLGA) o copolímero láctico-co-glicólico y polietilenglicol (PLGA-PEG) comprendiendo somatostatina, o un análogo de somatostatina, en la preparación de un medicamento para el tratamiento y/o prevención de la diarrea según cualquiera de las reivindicaciones 24 a 42, donde el medicamento se administra en forma de suspensión o disolución estéril por vía parenteral subcutánea, intramuscular o intravenosa.
44. Uso de una composición de microcápsulas de copolímero láctico-co-glicólico (PLGA) o copolímero láctico-co-glicólico y polietilenglicol (PLGA-PEG) comprendiendo somatostatina, o un análogo de somatostatina, en la preparación de un medicamento para el tratamiento y/o prevención de la diarrea según cualquiera de las reivindicaciones 24 a 43, donde el medicamento se presenta en forma de dosis unitaria.
45. Uso de una composición de microcápsulas de copolímero láctico-co-glicólico (PLGA) o copolímero láctico-co-glicólico y polietilenglicol (PLGA-PEG) comprendiendo somatostatina, o un análogo de somatostatina, en la preparación de un medicamento para el tratamiento y/o prevención de la diarrea según la reivindicación 44, donde la composición de dosis unitaria se presenta en forma de polvo liofilizado que se reconstituye antes de su administración.
46. Uso de una composición de microcápsulas de copolímero láctico-co-glicólico (PLGA) o copolímero láctico-co-glicólico y polietilenglicol (PLGA-PEG) comprendiendo somatostatina, o un análogo de somatostatina, en la preparación de un medicamento para el tratamiento y/o prevención de la diarrea según la reivindicación 45, donde la composición de dosis unitaria se presenta como una suspensión o disolución estéril que forma in situ un implante sólido biodegradable y biocompatible.
Patentes similares o relacionadas:
Composición que comprende hidrocortisona, del 22 de Julio de 2020, de Diurnal Limited: Una composición farmacéutica adaptada para administración oral que comprende: i) un portador que consiste esencialmente en partículas de celulosa microcristalina […]
Microesferas o micropartículas biodegradables o bioerosionables de liberación con el tiempo en suspensión en una formulación de fármaco inyectable de formación de depósito solidificante, del 8 de Julio de 2020, de ALLERGAN, INC.: Material compuesto para la administración de fármacos, que comprende: una pluralidad de micropartículas dispersas en una composición de medios; en el que las micropartículas […]
MATERIAL QUE INCORPORA VITAMINA D PARA SU POSTERIOR LIBERACIÓN Y MÉTODO PARA OBTENER DICHO MATERIAL, del 2 de Julio de 2020, de UNIVERSIDAD DE SANTIAGO DE CHILE: La presente invención se relaciona al campo de los materiales, más en específico al tratamiento de materiales para la liberación de compuestos activos […]
Composiciones y métodos no hormonales para la anticoncepción masculina que comprenden (R)-Silodosina, del 1 de Julio de 2020, de Laboratoires Major: Composición para su uso en un método anticonceptivo no hormonal para un sujeto masculino, en la que dicha composición es una formulación de liberación prolongada […]
Sales de butirato para uso en enfermedades inflamatorias, del 17 de Junio de 2020, de Birrbeheer B.V: Una preparación que comprende una sal de butirato para uso en el tratamiento de un sujeto que padece una enfermedad que está asociada con inflamación sistémica, […]
Composiciones de polifenol, del 3 de Junio de 2020, de Nugerontix Limited: Enoteína B para uso en terapia para tratar, prevenir o retrasar la aparición de disfunción endotelial donde el tratamiento, prevención o retraso comprende […]
Formulaciones de ganaxolona y procedimientos para la preparación y uso de las mismas, del 3 de Junio de 2020, de Marinus Pharmaceuticals, Inc: Una composición que comprende partículas que comprenden ganaxolona; un polímero hidrófilo; un agente humectante; y un agente complejante, en la que el diámetro medio ponderado […]
Sistema para dirigir agentes hacia dentro de un ojo, del 3 de Junio de 2020, de UNIVERSITY OF MARYLAND: Un sistema para dirigir un agente hacia el interior o a traves de un tejido, que comprende: (a) un agente que es magnetico o magnetizable o que responde magneticamente; […]